Введение
Хотя старение является индивидуальным процессом, а его начало и развитие у разных людей сильно варьируются, ООН определяет возраст 60 лет как границу перехода в группу пожилых. В медицинской литературе чаще говорят о пожилом возрасте начиная с 65 лет. Число людей 60 лет и старше в мире неуклонно растет. За последние 30 лет оно удвоилось (759 млн в 2010 г. против 378 млн в 1980-м) и предположительно к 2050 г. возрастет еще более существенно, составив впечатляющую популяцию – 2 млрд человек (данные официального сайта ООН: http://social. un.org). В то же время стремительно возрастает и число больных сахарным диабетом (СД), которое в возрастной группе 60 лет и старше уже в 2010 г. превысило 100 млн человек [1]. В американской популяции распространенность СД в группе лиц 65 лет и старше в 2006 г. составляла 31,49 % [2].
Таким образом, проблема СД у пожилых, его лечения с учетом возрастных особенностей, характеристик эффективности и безопасности фармакотерапии, установленных в соответствии с требованиями доказательной медицины, приобретает всевозрастающую значимость.
Несмотря на обширность группы пожилых больных СД (разумеется, она представлена преимущественно СД 2 типа [СД2]), особенности этой категории пациентов и рекомендации по их лечению пока недостаточно освещены в медицинской литературе.
Это связано прежде всего с существенной гетерогенностью группы, которая определяется не только длительностью СД, выраженностью его осложнений, но и общим состоянием здоровья, более всего – наличием коморбидных заболеваний. Возраст обусловливает своего рода “накопительный эффект” различных проблем со здоровьем. Часть пожилых больных СД по разным причинам ослаблены, имеют серьезные ограничения в физических и когнитивных функциях. В то же время другие активны и их состояние здоровья вполне может быть расценено как хорошее. Это затруднят создание простого и универсального терапевтического алгоритма для СД, т. к. учесть особенности всех пациентов весьма сложно.
Благодаря подробному анализу результатов исследований UKPDS (с последующим 10-летним наблюдением), ACCORD, ADVANCE, VADT и ряда др. в последние годы стало складываться представление о необходимости индивидуализации терапии СД в зависимости от возраста и сопряженных с ним состояний, прежде всего сопутствующей сердечно-сосудистой патологии. В настоящее время представляется, что чрезмерное стремление к нормогликемии у пожилых пациентов с СД, имеющих распространенное поражение артерий, может принести больше вреда, чем пользы.
С другой стороны, невозможно пренебречь большей уязвимостью пожилых пациентов в отношении развития выраженных стадий осложнений СД – слепоты, почечной недостаточности, хронических язв, ампутаций нижних конечностей и т. п. [3, 4]. Пожилые люди также часто ослаблены и больше страдают от симптомов гипергликемии, таких как полиурия, слабость, кожные инфекции. Выраженная гипергликемия может стать причиной угрожающих жизни явлений: дегидратации, незаживающих ран, наконец коматозных состояний.
Договоренность относительно конкретных терапевтических целей для гликемии и уровня гликированного гемоглобина (HbA1c) у пожилых пациентов в эндокринологическом сообществе пока не достигнута. В частности, “возрастные” цели не оговариваются Американской диабетической ассоциацией и Европейской ассоциацией по изучению диабета [5]. Отечественный проект Консенсуса совета экспертов Российской ассоциации эндокринологов по инициации и интенсификации сахароснижающей терапии СД2 предлагает при определении гликемических терапевтических целей руководствоваться не столько возрастом, сколько понятием “ожидаемая продолжительность жизни”, а также наличием осложнений, сердечнососудистых заболеваний и риском гипогликемий [6] (рис. 1). Это отражает реально существующую сложную ситуацию, обусловленную гетерогенностью популяции больных СД2, в т. ч. пожилых.
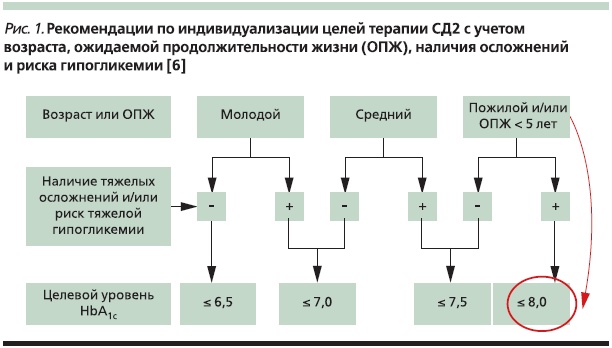
Однако и пациентам пожилого возраста (или с ожидаемой продолжительностью жизни < 5 лет) при наличии тяжелых осложнений и/или высоком риске тяжелых гипогликемий как отечественный проект Консенсуса, так и Американское гериатрическое общество (American Geriatric Society) рекомендуют целевой уровень HbA1c не выше 8 % [6, 7]. Но, как показывает опыт, даже эти “щадящие” цели в условиях рутинной практики не так просто достижимы.
Гликемический контроль у пожилых больных СД
СД является фактором риска прогрессирования гериатрических синдромов, к которым относят депрессию, полипрагмазию, когнитивную дисфункцию, недержание мочи, падения, приводящие к травматизации, персистирующий болевой синдром, саркопению и др. [3, 8]. Некоторые из них напрямую связаны с гликемическим контролем.
Так, результаты ряда исследований показали, что гипергликемия ассоциирована с ухудшением когнитивной функции, а улучшение состояния углеводного обмена ведет к ее частичному восстановлению [9–11].
Обусловленная гипергликемией глюкозурия, даже несмотря на тенденцию к повышению почечного порога в пожилом возрасте, может вызывать полиурию, учащенное мочеиспускание и вносить вклад в формирование синдрома недержания мочи. Болевой синдром усугубляется нейропатией, – прямым следствием декомпенсации углеводного обмена.
Говоря о таком важном показателе при СД, как масса тела, следует отметить, что пожилые пациенты имеют высокий риск развития как ожирения, так и дефицита питания [3]. Возможно, что недостаточное питание и сопряженная с ним саркопения даже более опасны. Старение в целом ассоциировано с существенным сокращением потребления пищи и со снижением веса [12]. В популяции 70 лет и старше масса тела уже не является предиктором сердечно-сосудистой и общей смертности [13]. Более того, снижение веса в возрасте между 60 и 70 годами ассоциируется с повышенной смертностью в последующие 10 лет, причем при СД ассоциация наиболее выражена [14]. Вероятно, это в большой степени связано с возрастной тенденцией к развитию саркопении (потере мышечной массы), которая особенно характерна для пациентов с СД [15]. Не требует специальных доказательств тот факт, что в патологическое снижение массы тела вносит вклад, прежде всего декомпенсация углеводного обмена.
Склонность к падениям, характерная для многих пожилых людей, усиливается при СД, особенно при его длительном течении. К доказанным факторам риска падений относятся женский пол, нарушенная подвижность, ортостатическая гипотензия, высокий индекс массы тела и неудовлетворительный гликемический контроль [16, 17]. Низкий уровень HbA1c (≤ 6 %) ассоциируется с возрастанием числа падений пациентов на инсулинотерапии, но не на пероральных сахароснижающих препаратах (ПССП) [18].
Осложнения СД (снижение функций периферических нервов, почек и ухудшение зрения) также увеличивают риск падений. Предполагается, что фактором риска падений пожилых больных СД также могут быть деформации стоп и полипрагмазия (в связи с побочными эффектами и взаимодействием препаратов различных групп [8].
Итак, несмотря на хорошо осознаваемый в настоящее время риск чрезмерно строгого гликемического контроля больных СД старшего возраста, нельзя игнорировать и большую важность поддержания компенсации в удовлетворительных пределах.
К позитивным эффектам хорошего гликемического контроля можно отнести:
• благоприятное воздействие на симптомы, являющиеся очевидным следствием глюкозурии (слабость, полиурия и др.), и когнитивную дисфункцию, что часто недооценивается;
• поддержание статуса нормального питания: купирование глюкозурии – прекращение потери калорий, а в случаях, когда компенсация достигается применением инсулина, и его прямой анаболический эффект [8];
• профилактика гериатрических синдромов, что способствует нормальному процессу старения.
Без сомнения основным барьером на пути к хорошему гликемическому контролю, особенно у пожилых больных, являются гипогликемии.
Риск, ассоциированный с гипогликемиями, рассматривается прежде всего в аспекте контррегуляторного ответа, ведущего к удлинению интервала QT с возможной последующей желудочковой аритмией. Для пожилых пациентов с распространенным поражением сосудов и автономной нейропатией последствия могут быть критическими. Тяжелые гипогликемии обнаруживают взаимосвязь с развитием деменции (три эпизода удваивают риск в сравнении с больными без тяжелых гипогликемий) [19], увеличивают частоту обращений за экстренной медицинской помощью и госпитализаций [20].
Следует понимать, что оценки уровня HbA1c может быть недостаточно для выявления этой проблемы. Так, в исследовании M.N. Munshi и соавт. (2011) с помощью длительного мониторирования гликемии была выявлена неожиданно высокая частота гипогликемий у пожилых больных СД с неудовлетворительным гликемическим контролем [21]. В выборке, состоявшей из 40 пациентов (из них 28 с СД2, 37 – на инсулинотерапии) с уровнем HbA1c ≥ 8 %, у 26 (65 %) зарегистрирован по крайней мере 1 эпизод гипогликемии (гликемия < 2,77 ммоль/л) в течение 3 дней мониторирования. Таким образом, простое повышение целевых уровней HbA1c не решает проблемы профилактики гипогликемий полностью – необходима систематическая целенаправленная работа в этом направлении, включающая обучение, самоконтроль и в ряде случаев применение систем длительного мониторирования гликемии.
Подходы к терапии СД у пожилых больных
Немедикаментозные методы лечения
Как уже обсуждалось, пожилые пациенты имеют риск развития как ожирения, так и дефицита питания. При избыточном весе может быть рекомендовано ограничение калорийности, но не более чем на 5 % от актуального веса [3]. Фактически в лечении пожилых больных СД вес, даже если сохраняется его избыток, перестает быть основной целью терапевтических вмешательств: внимание должно быть уделено более значимым с точки зрения возраста аспектам (сердечнососудистым заболеваниям, гериатрическим синдромам). Нередко пожилые пациенты продолжают придерживаться ранее полученных рекомендаций, ориентированных в основном на снижение веса, что может способствовать недостаточному питанию и саркопении. Широко распространенные стоматологические проблемы усугубляют ситуацию [8].
Значение физической активности в пожилом возрасте трудно переоценить. Малоподвижный образ жизни наряду с СД и ожирением способствует прогрессированию инсулинорезистентности, в то время как у пожилых физически активных людей не отмечается возрастного снижения чувствительности к инсулину и упражнения вносят потенциальный вклад в продление жизни [22].
Разумеется, именно у пожилых людей имеется много ограничений в отношении выполнения физических упражнений и при физических нагрузках требуется большая осторожность. Пациентам должны быть предоставлены адекватные, адаптированные к возрасту рекомендации по питанию и физическим нагрузкам, не следует забывать, что обучающие подходы эффективны и для пациентов старше 65 лет [23].
Медикаментозная сахароснижающая терапия
Назначение сахароснижающих лекарств пожилым больным СД осуществляется по тем же принципам, что и более молодым пациентам, однако возможность выбора, как правило, сужена в связи с многочисленными противопоказаниями. Среди них: нарушения функции почек, печени, сердечная недостаточность и др. А поскольку монотерапия таблетированными препаратами далеко не всегда позволяет достигать хотя бы минимальных терапевтических целей, риск побочных эффектов усугубляется полипрагмазией.
В пожилом возрасте широко применяется метформин, который практически не вызывает гипогликемий, но его применение существенно ограничивается нарушением почечной функции. Патология почек, в т. ч. недиабетического происхождения, – распространенное среди пожилых людей явление, которое часто не диагностируется. В американской популяции пожилых больных СД2 сниженный клиренс эндогенного креатинина (< 60 мл/мин) был отмечен в 77 % случаев, повышение уровня креатинина сыворотки крови – в 43 % [24]. Метформин также противопоказан при любых состояниях, способных вызывать тканевую гипоксию; следует избегать его применения среди ослабленных пациентов с недостатком питания и сниженным аппетитом, что не является редкостью для пожилых людей [3].
Препараты сульфонилмочевины в связи с механизмом действия, стимулирующим секрецию инсулина, более всего ассоциируются с риском гипогликемий, особенно при большой продолжительности действия. Риск усиливается у лиц со сниженной функцией почек, параллельным применением инсулиновых сенситайзеров, препаратов инсулина. Другие факторы риска: возраст более 60 лет, недавняя выписка из стационара, злоупотребление алкоголем, недостаточное питание, множественные медикоментозные назначения [3].
Меглитиниды обладают явными преимуществами в лечении пожилых пациентов в связи с кратковременной продолжительностью действия и преобладающей метаболизацией в печени. Благодаря этим особенностям возможно эффективное воздействие на постпрандиальную гипергликемию, которая характерна для пожилых [25], а также применение у пациентов с ограниченной функцией почек. Доказано меньшее число гипогликемий у пожилых пациентов при применении репаглинида по сравнению с глибенкламидом [26].
Применение глитазонов (тиазолидиндионов) пожилыми пациентами весьма ограничено в связи с риском задержки натрия и воды и развития (прогрессирования) сердечной недостаточности. Риск усугубляется с возрастом, почечной недостаточностью и предшествовавшими сердечнососудистыми событиями. Кроме того, эти препараты ассоциированы с риском остеопороза и переломов у пожилых женщин [8], поэтому их применение обсуждаемым контингентом особенно проблематично.
Препараты инкретинового ряда (агонисты глюкагоноподобного пептида 1 и ингибиторы дипептидилпептидазы-4) являются очень перспективными для лечения пожилых больных СД, прежде всего в связи с отсутствием риска гипогликемий, однако пока не накоплено достаточного числа исследований по оценке их эффективности и безопасности для этой категории пациентов.
Несмотря на связанный с применением инсулина риск гипогликемий, большое число больных СД2 со временем требуют его назначения по разным причинам. Чаще, чем молодым пациентам, инсулин показан пожилым в связи с множеством противопоказаний к ПССП (почечная, сердечная недостаточность), прогрессивным снижением функции β-клеток и необходимостью достижения пусть даже не очень строгих терапевтических целей [8, 27].
При назначении инсулина больным старшего возраста следует иметь в виду возможную сниженную потребность в инсулине по ряду причин: наличие почечной недостаточности (замедление деградации инсулина), снижение массы тела (повышение чувствительности к инсулину) [8]. Кроме того, у пожилых пациентов нередко снижен аппетит и они меньше едят. Надо проявлять осторожность и при распределении дозы в течение суток – есть данные, что пожилые люди склонны есть больше утром, чем вечером [28].
Часто ссылаются на негативное отношение пожилых пациентов к инсулинотерапии, их неспособность справляться со сложным режимом. Возможно, это не соответствует истине, т. к. есть исследования, свидетельствующие об обратном [29, 30].
Успех и безопасность инсулинотерапии четко зависят от рациональности назначенного режима, тщательного врачебного наблюдения, особенно на начальном этапе лечения, а также обучения пациента и родственников. Врачу необходимо убедиться в способности пациента осуществлять инсулинотерапию, оценивать остроту его зрения, точность движений пальцев, когнитивное функционирование, что возможно, только если больной выполнит инъекцию под контролем. При больших затруднениях всем аспектам инсулинотерапии должны быть обучены родственники.
При лечении пожилых пациентов разумно применять медленное (начиная с небольших доз и минимального количества инъекций), поэтапное введение инсулинотерапии. Большое значение имеет простота терапевтического режима.
Одна или две инъекции базального инсулина в качестве дополнения к терапии ПССП – наиболее распространенный вариант инициации инсулинотерапии пожилых больных СД2. Преимущества длительно действующих аналогов гларгина и детемира перед НПХ-инсулином в качестве начального варианта терапии заключаются прежде всего в достоверно меньшем количестве гипогликемий [31–33], что крайне важно для пожилых больных.
Пациентам с существенной постпрандиальной гипергликемией, а таковых среди пожилых больных 50–70 % [25], необходимо введение инсулина короткого действия перед едой. У этого контингента ультракороткие аналоги (лизпро, аспарт, глулизин) также имеют преимущество: их фармакокинетический профиль минимизирует риск гипогликемий в постпрандиальном периоде; они не требуют паузы между инъекцией и едой (что важно для людей со сниженной памятью), их можно вводить и после еды, например если у пациента неустойчивый аппетит или имеются затруднения в планировании приема углеводов [27].
Наконец многими выгодными свойствами с точки зрения применения лицами старшего возраста обладают готовые инсулиновые смеси. Это простой режим дозирования – как правило, 2 инъекции перед утренним и вечерним приемами пищи; “самодостаточность” –отсутствие необходимости комбинирования с ПССП, т. к. эти инсулиновые препараты обеспечивают как поддержание базального уровня гликемии, так и его прандиальную регуляцию.
Хотя небольшое сравнительное исследование (130 больных, продолжительность –24 недели) режима инсулин гларгин в сочетании с ПССП против готовой смеси (человеческий инсулин регуляр и НПХ 30/70) у пожилых пациентов продемонстрировало большее число гипогликемий на смешанном инсулине при близком итоговом уровне HbA1c [34], появление аналоговых инсулиновых смесей существенно повысило безопасность инсулинотерапии у обсуждаемого контингента больных. Сравнение того же гларгина + ПССП с двухфазным лизпро микс 25 (222 против 258 пациентов 65 лет и старше) показало более низкий уровень HbA1c и равное количество ночных гипогликемий при несколько большем их общем количестве на инсулиновой смеси; число тяжелых гипогликемий при сравниваемых режимах не различалось [35].
Кроме того, абсолютным преимуществом инсулиновых смесей как монотерапии является отсутствие проблемы противопоказаний и побочных явлений, характерных для таблетированных противодиабетических препаратов.
Впечатляющие результаты получены в крупном 6-месячном проспективном многоцентровом исследовании PRESENT (Physicians’ Routin Evaluation of Safety and Efficacy of NovoMix 30 Therapy Korea Study) с участием 174 центров для оценки эффективности, безопасности и удовлетворенности лечением при использовании двухфазного инсулина аспарт 30 (НовоМикс 30) больными СД2 с неудовлетворительным гликемическим контролем [36]. В исследование были включены 5828 пациентов с СД2, из них 1720 – в возрасте 65 лет и старше. Эффективность применения инсулина НовоМикс 30 была высокой: зарегистрировано снижение среднего уровня HbA1c на 1,2 % (с 9,1 до 7,9 %) за 6 месяцев в условиях обычной клинической практики (рис. 2).
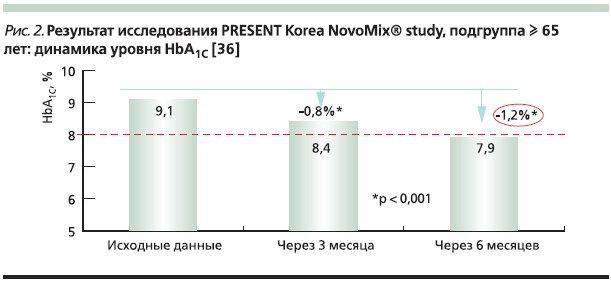
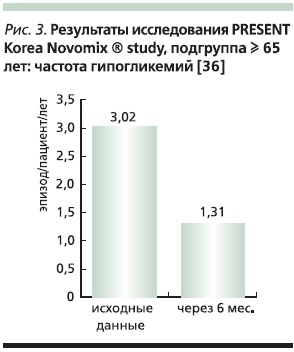
Число гипогликемий сократилось с 3,02 до 1,31 эпизода/пациенто-лет (на 56,6 %), что особенно важно в связи с тем, что исходно многие больные уже были на инсулинотерапии в различных режимах. Авторы связывают этот эффект главным образом с ультракороткой составляющей смеси, которая действует более физиологично в ответ на прием пищи в сравнении с терапией человеческим инсулином.
Другой нежелательный эффект инсулинотерапии, ограничивающий достижение терапевтических целей, – прибавка массы тела, в исследовании был минимальным: 0,3 кг за 6 месяцев.
Удовлетворенность лечением, вопреки распространенному мнению о негативной позиции пожилых больных СД в отношении инсулинотерапии, в данном исследовании возросла при сравнении с предшествовавшим вариантом лечения большинства пациентов (84 % пожилых больных ответили “удовлетворен” или “чрезвычайно удовлетворен” терапией НовоМикс 30). Не исключено, по мнению авторов, что этот факт хотя бы отчасти можно отнести за счет удобства использования одноразовых шприцев-ручек ФлексПен; ранее было показано, что эти устройства воспринимались пожилыми пациентами весьма адекватно [37].
В целом эффективность и безопасность применения инсулина НовоМикс 30 оказались сопоставимыми с таковыми у более молодых пациентов, и, по мнению авторов, пациенты старшего возраста при данном режиме лечения не требуют большего внимания, чем молодые.
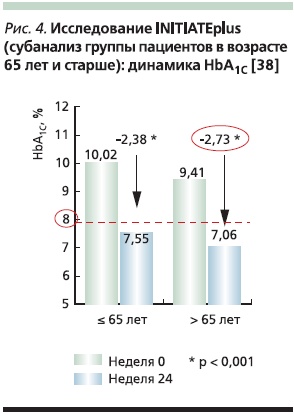
Уже в этом году опубликованы результаты масштабного исследования INITIATEplus (The Initiation of insulin to reach A1c Target), подтвердившие высокую эффективность и хорошую переносимость двухфазного инсулина НовоМикс 30 пожилыми больными СД2 [38]. В исследование были включены 3492 пациента моложе 65 лет и 716 – 65 лет и старше, не имевших компенсации при применении ПССП. Пациенты самостоятельно осуществляли титрацию дозы инсулина согласно алгоритму, которому их обучали перед началом инсулинотерапии. На обучающей сессии продолжительностью 1 час обсуждались и вопросы самоконтроля, техники инъекций, базовые принципы питания, риск гипогликемии. Наблюдение продолжалось 24 недели.
По окончании исследования уровень HbA1c снизился более значительно у пациентов 65 лет и старше (на 2,73 против 2,38 % в группе более молодых; p < 0,0001; рис. 3). Кроме того, большее число больных в старшей группе достигли установленного в исследовании целевого уровня HbA1c ≤ 7 % (55 % против 39 %). Гликемия натощак была несколько выше в группе старшего возраста: 91,2 мг/дл против 85,2 мг/дл (p < 0,004).
О легких гипогликемиях сообщили 7,7 % и 9,7 % пациентов старше и моложе 65 лет соответственно (p < 0,01). Тяжелые гипогликемии зарегистрированы среди 3,1 % (больные 65 лет и старше) и 1,5 % (пациенты до 65 лет) (p < 0,01).
Таким образом, исследование INITIATEplus доказало, что применение двухфазного инсулина НовоМикс 30 с самостоятельной титрацией дозы эффективно и безопасно для пациентов 65 лет и старше, так же как и для больных более молодого возраста. Уровни HbA1c и гликемии натощак снизились в группе старшего возраста даже более значительно, а число легких и тяжелых гипогликемий в обеих возрастных группах было ниже показателя 0,5 эпизода на пациента в год.
Одно из самых крупномасштабных к настоящему моменту исследований по изучению эффективности и безопасности терапии инсулином НовоМикс 30 пожилых пациентов – IMPROVETM [39]. Всего в исследование IMPROVETM были включены 52 419 пациентов с СД2, которым в условиях рутинной клинической практики лечащим врачом была назначена терапия инсулином НовоМикс 30 в виде либо старта инсулинотерапии, либо перевода с лечения другими сахароснижающими препаратами, в т. ч. инсулином. Подгруппа пожилых пациентов включала 11 988 человек в возрасте 65 лет и старше. Продолжительность IMPROVETM, как и исследования INITIATEplus, составила 6 месяцев. Выбор дозы и частоты введения инсулина НовоМикс 30 осуществлялся лечащим врачом, данная информация регистрировалась при стартовом визите и через 26 недель терапии.
Средний уровень HbA1c снизился достоверно (-2,1 ±1,9 %; р < 0,0001) по всей когорте пожилых пациентов после 26 недель терапии инсулином НовоМикс 30, достигнув 7,1 ±1,1 % (см. таблицу). Достоверное снижение уровня HbA1c наблюдалось во всех группах предшествующей терапии с максимальным улучшением в группе пациентов, предварительно не получавших медикаментозного лечения.
Таблица.Эффективность терапии инсулином НовоМикс 30 пожилых пациентов в исследовании IMPROVETM.
Средние уровни гликемии натощак и постпрандиальной гликемии после всех основных приемов пищи достоверно улучшились во всей когорте пожилых пациентов.
Частота тяжелых гипогликемических эпизодов снизилась значительно в общей когорте пожилых пациентов и в группах предшествовашей терапии ПССП и инсулином ±ПССП (рис. 4). Наибольшее снижение числа гипогликемических эпизодов отмечено в группе предшествовавшей терапии инсулином ±ПССП.
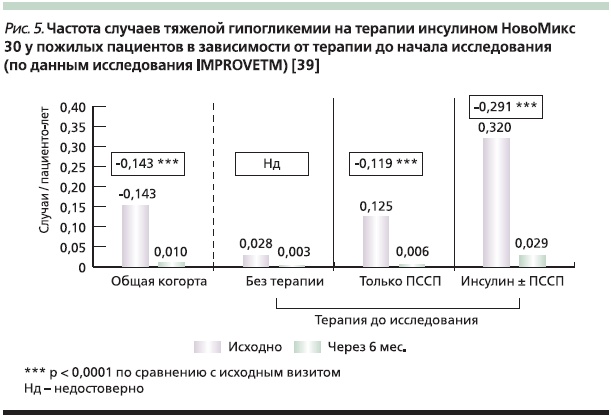
Количество эпизодов легкой гипогликемии среди пожилых пациентов снизилось на 20 % (с 3,84 до 3,06 эпизода/пациенто-лет от исходного к финальному визиту; р < 0,0001). По сравнению с исходными характеристиками к финальному визиту вес пациентов достоверно не изменился.
Таким образом, исследование IMPROVETM показало, что применение инсулина НовоМикс 30 – это выбор эффективной, безопасной и простой терапии для пожилых пациентов. При использовании данного двухфазного инсулинового аналога возможен как простой старт инсулинотерапии, так и эффективная интенсификация с применением только одного типа инсулина.
Заключение
Завершая обсуждение подходов к эффективной и безопасной терапии больных СД пожилого возраста, можно резюмировать, что существует ряд состояний, характерных для этой категории пациентов, на которые следует обращать особое внимание.
Необходимо тщательно выявлять осложнения СД и коморбидные заболевания (сердечную, почечную недостаточность и т. п.), которые у пожилых пациентов часто не диагностируются, а также менее известные эндокринологам гериатрические синдромы. Последние ухудшают качество жизни больных в степени, сопоставимой с осложнениями СД и гипогликемиями [40]. Следует также оценивать пищевые стереотипы и уровень физической активности, т. к. эти важнейшие составляющие образа жизни существенно влияют на результаты терапии.
Необходимо обучать пациентов и при необходимости членов их семей основным принципам рационального питания, физических нагрузок, профилактике гипогликемий. Полезно использовать любые приемы и устройства для преодоления характерной для пожилых людей забывчивости (дневники диабета, специальные боксы для таблеток, таймеры).
Наконец именно в пожилом возрасте особую важность приобретает адекватный выбор медикаментозной сахароснижающей терапии, подразумевающий учет всех особенностей этого контингента больных.
Готовые инсулиновые смеси, в особенности аналоговые, например НовоМикс 30, – оптимальный выбор для пожилых пациентов, не достигших приемлемого гликемического контроля на ПССП и/или инсулине продленного действия или имеющих противопоказаний к ПССП.
Информация об авторе:
Суркова Елена Викторовна – доктор медицинских наук, ведущий научный сотрудник федерального государственного учреждения“Эндокринологический научный центр” Минздравсоцразвития Российской Федерации.
Тел. (499) 124 35 00, e-mail: elenasurkova@mail.ru



