Актуальность
Достижение и удержание целевых значений гликемического контроля у пациентов с сахарным диабетом 2 типа (СД2) безусловно служат основой терапевтических мероприятий [1], направленных на снижение риска развития осложнений СД. Зачастую при неэффективности пероральной сахароснижающей терапии (ССТ) и терапии инъекциями препаратов инкретинового ряда возникает необходимость назначения препаратов инсулина.
В ряде исследований интенсификация ССТ инсулином больных СД2 оказалась важнейшим фактором повышенного риска развития гипогликемии, в т.ч. тяжелой [2, 3]. В исследовании ACCORD в группе интенсивного лечения инсулином частота тяжелой гипогликемии была более чем в 3 раза выше по сравнению с таковой в группе контроля, что ассоциировалось с повышением общей и сердечно-сосудистой летальности на 22 и 35% соответственно [3]. Выявлено несколько механизмов влияния гипогликемии у пожилых пациентов с СД2 и сердечно-сосудистой патологией на риск развития инсульта, инфаркта миокарда и аритмий как основных причин смерти [4, 5]. Гипогликемия является фактором стимуляции симпатико-адреналовой системы с активацией прокоагулянтных и проаритмогенных факторов. Опосредованным механизмом влияния гипогликемии является активация факторов воспаления, которые не только способствуют прогрессированию атеросклероза артерий, но и приводят к дестабилизации атеросклеротической бляшки, тромбозам и тромбоэмболиям артерий различной локализации [4, 5]. В исследовании DEVOTE продемонстрирована связь между вариабельностью гликемии натощак и риском гипогликемий [6, 7]. В связи с этим особенно актуален вопрос снижения вариабельности действия базальных инсулинов на уровень гликемии [8, 9].
Инсулин деглудек (Тресиба®) является аналогом базального инсулина с продолжительностью действия более 42 часов. Деглудек характеризуется высокой эффективностью в отношении гликемического контроля, низкой вариабельностью гликемии, подтвержденной безопасностью в отношении сердечно-сосудистой системы и гибкостью режима дозирования, что отличает его от других базальных инсулинов [8–11]. Основным показателем оценки гликемического контроля СД2 является уровень гликированного гемоглобина (HbA1c), который отражает среднюю гликемию за последние 2–3 месяца. Однако даже при удовлетворительных значениях HbA1c могут отмечаться значительные колебания уровня гликемии в течение суток (высокая вариабельность), что диктует необходимость использования непрерывного мониторинга гликемии на этапе коррекции терапии. Время гликемии в целевом диапазоне 3,9–10,0 ммоль/л более 70% ниже целевого диапазона (<3,9 ммоль/л) менее 4%, коэффициент вариабельности уровня глюкозы менее 36% рассматриваются как не менее важные терапевтические цели лечения пациентов СД2 [12].
В представленном ниже клиническом случае показана эффективность и безопасность интенсификации терапии СД2 инсулином деглудек.
Клинический случай
Пациент Б. 60 лет предъявлял жалобы на постоянную сухость во рту, учащенное мочеиспускание, слабость, частые головокружения, снижение памяти, онемение нижних конечностей на уровне стопы.
Анамнез заболевания: СД2 в течение 10 лет был выявлен на фоне ожирения 1-й степени и артериальной гипертензии. С момента диагностики заболевания пациент принимал метформин 2000 мг в комбинации с вилдаглиптином 100 мг/сут. С 2015 г. вилдаглиптин был заменен на лираглутид, с 2021 г. к терапии добавлен канаглифлозин 300 мг. Уровень гликированного гемоглобина (HbA1c) от 29.04.2022 составил 6,4%. После перенесенной новой короновирусной инфекции в феврале 2023 г. пациент отметил нарастание симптомов гипергликемии, уровень HbA1c от 22.04.2023 – 9,5%. Лираглутид был заменен на семаглутид в дозе 1 мг 1 раз в неделю. Значительного улучшения гликемического контроля отмечено не было. Гликемия натощак составляла 10–12 ммоль/л, постпрандиально до 17 ммоль/л, по данным самоконтроля и флеш-мониторирования глюкозы (система FreeStyle Libra), гипогликемических состояний зарегистрировано не было, уровень HbA1c от 22.09.2023 составил 10,4%.
Осложнения СД: диабетическая микроангиопатия: диабетическая нефропатия – ХБП С3 А2, альбуминурия 2-й ст. с 2022 г. диабетическая невропатия, сенсомоторная форма по периферическому типу с 2020 г.; диабетическая макроангиопатия: цереброваскулярная болезнь: атеросклероз общей сонной артерии со стенозом до 25% с обеих сторон с 2020 г.; атеросклероз артерий нижних конечностей: стеноз общей бедренной артерии справа – 35%, слева – 25%, подколенной артерии справа – 15%, слева – 15%, хроническая артериальная недостаточность 1-й ст. с 2020 г.
Сопутствующие заболевания: Гипертоническая болезнь 3 ст. Контролируемая АГ. Риск 4. Гипер-липидемия 2 b. Гиперурикемия. Нару-шение ритма сердца. Персистирующая форма фибрилляции предсердий (постоянно принимает амиодарон 200 мг). Неалкогольная жировая болезнь печени. ХСН I ФК 2.
Общий осмотр: рост – 181 см, масса тела – 100 кг, индекс массы тела – 31,2 кг/м2, окружность талии – 108 см. Кожные покровы чистые, периферических отеков не выявлено. Слизистые оболочки полости рта суховатые, чистые, язык сухой, умеренно обложен белым налетом. Щитовидная железа 0-й степени. В легких дыхание везикулярное, частота дыхания – 16/мин, хрипов нет. Тоны сердца приглушены, ритмичные, частота сердечных сокращений – 72 уд/мин, пульс – 72 уд/мин, артериальное давление – 130/90 мм рт.ст. При осмотре живот без патологии, при пальпации патологических изменений не выявлено.
Результаты исследований: HbA1c – 10,4%, уровень креатинина – 83,2 мкмоль/л, скорость клубочковой фильтрации – 88 мл/мин/1,73 м2, мочевая кислота – 340 мкмоль/л, NT-proBNP – 100 пг/мл, липопротеиды низкой плотности – 1,1 ммоль/л, триглицериды – 1,3 ммоль/л, аланинаминотрансфераза – 31,9 ЕД/л, аспартатаминотрансфераза – 25,7 ЕД/л, билирубин – 30 мкмоль/л.
Для контроля уровня глюкозы пациент использует флэш-мониторинг. По данным флэш-мониторинга глюкозы, в целевом диапазоне зарегистрировано 14% измерений (норма – более 70%), в гипогликемическом диапазоне – 0%, в гипергликемическом диапазоне – 85%, вариабельность уровня глюкозы (коэффициент вариабельности) – 11,1% (рис. 1, 2).
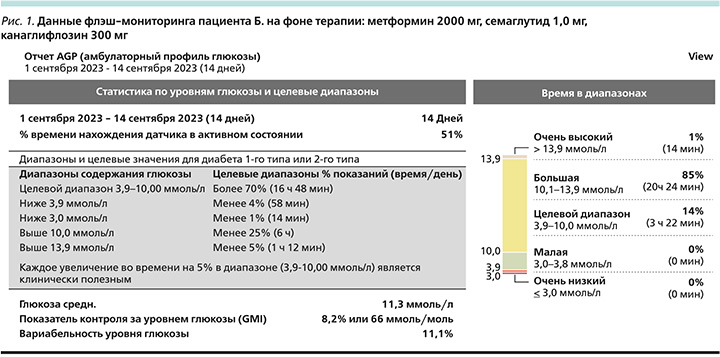
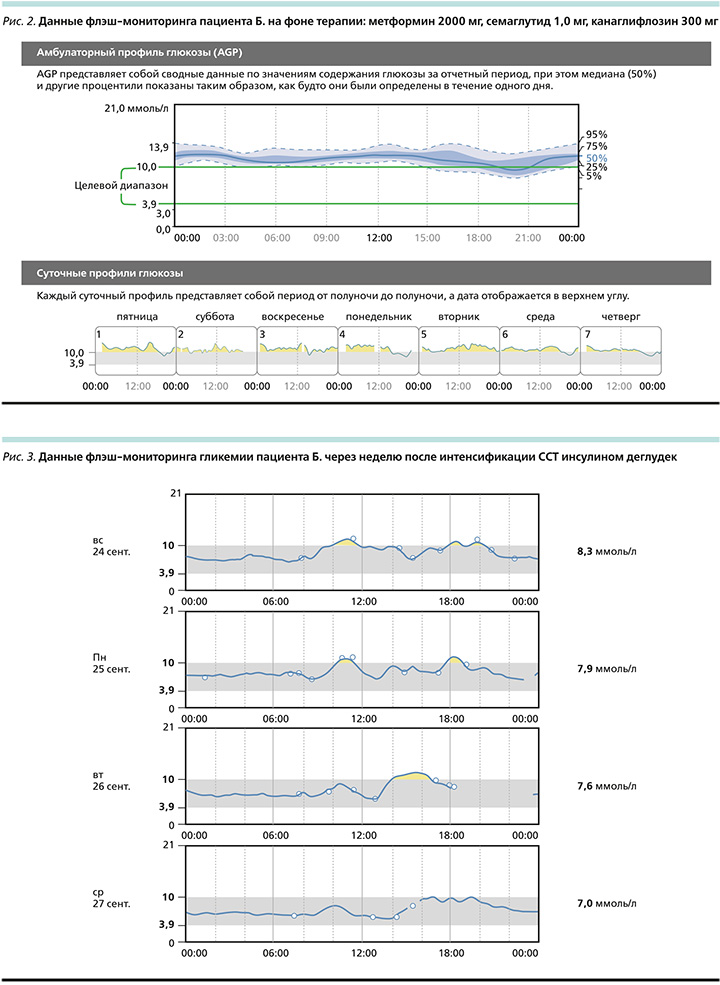
Представленные данные указывают на наличие гипергликемии в течение суток без выраженных колебаний гликемии после приема пищи. Выявлена гипергликемия как в ночное время, так повышение уровня глюкозы в утренние часы. Данные флэш-мониторинга свидетельствуют о неэффективности проводимой ССТ.
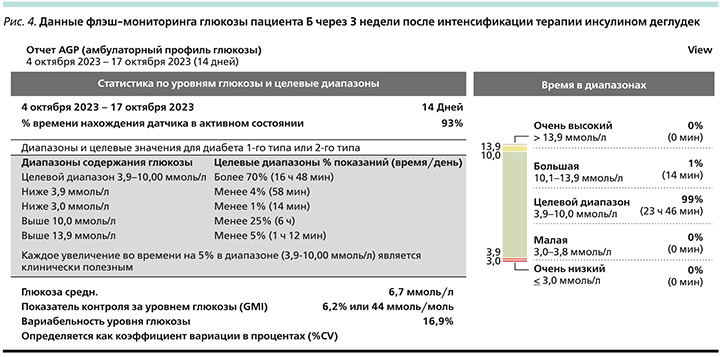
С учетом низкого коэффициента вариабельности гипергликемии натощак и постпрандиально в качестве метода интенсификации для данного пациента выбрана терапия базальным инсулиновым аналогом с минимальным риском гипогликемических состояний – инсулином деглудек. Стартовая доза инсулина деглудек составила 20 ЕД 1 раз в сутки в 21.00 (0,2 ЕД на 1 кг массы тела). Через 4 дня после старта терапии инсулином проводили титрацию дозы на основании среднего значения двух предшествующих измерений глюкозы плазмы натощак. Целевой уровень гликемии натощак для данного пациента определен менее 7,0 ммоль/л. Через неделю после назначения инсулина достигнуто улучшение показателей гликемии. Гликемия натощак составила 5,59–5,43 ммоль/л, постпрандиальная гликемия – до 10,4 ммоль/л. Гипогликемических состояний зарегистрировано не было. Пациент отметил значительное улучшение самочувствия, отсутствие симптомов гипергликемии. Доза инсулина деглудек составила 22 ЕД (рис. 3), предшествовавшая ССТ была изменена (семаглутид отменен).
Через 3 недели с момента интенсификации ССТ инсулином деглудек доза инсулина увеличена до 30 ЕД в сутки. По данным самоконтроля глюкозы по глюкометру, гликемия натощак составляла 5,4–5,6 ммоль/л, через 2 часа после приема пищи – 6,4–8,0 ммоль/л, симптомов гипогликемии зарегистрировано не было. При оценке показателей флэш-мониторинга выявлена низкая вариабельность уровня глюкозы: коэффициент вариабельности составил 16,9%. В целевом диапазоне (3,9–10,0 ммоль/л) показатели глюкозы пациента находились 99% времени, гипогликемических состояний зарегистрировано не было (рис. 4, 5).
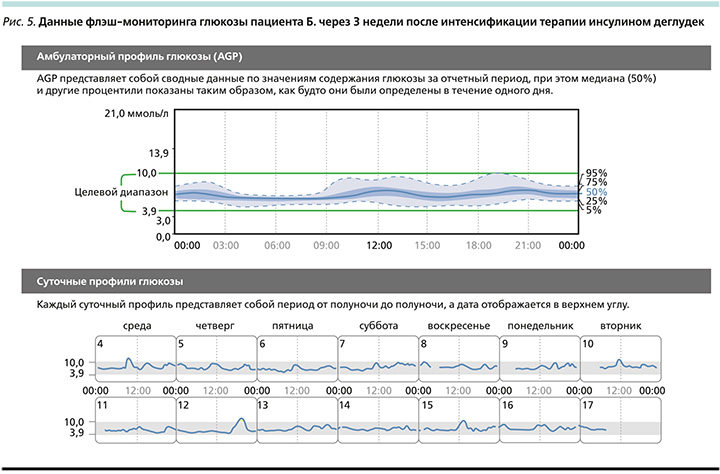
Как видно из представленных рисунков, благодаря проведенной терапии достигнута нормализация показателей уровня глюкозы как натощак, так и постпрандиально, без гипогликемических состояний. После нормализации показателей гликемического контроля пациент был проинформирован о возможности изменять время введения инсулина деглудек (гибкость введения) в пределах суток с учетом 8-ми часового минимального и 40-часового максимального интервала введения.
Обсуждение
Недостижение целевых значений НbА1с и гликемического контроля на фоне трехкомпонентной ССТ у пациента Б. послужило основанием для интенсификации терапии. С учетом данных флэш-мониторинга глюкозы: гипергликемии натощак и постпрандиально (85% времени уровень глюкозы у пациента находился выше целевого диапазона), невысокого показателя вариабельности гликемии в течение суток, в качестве препарата выбора назначен базальный инсулиновый аналог – деглудек. Применение данного препарата обеспечило достижение нормогликемии у пациента без гипогликемических состояний, что сопровождалось улучшением его самочувствия.
Заключение
Таким образом, интенсификация ССТ СД2 инсулином деглудек в условиях реальной клинической практики продемонстрировала высокую эффективность в достижении целей гликемического контроля, низкую вариабельность уровня глюкозы и низкий риск гипогликемий. Также можно отметить простоту применения и возможность гибкого введения инсулина в течение суток. Применение базального инсулинового аналога – инсулина деглудек, позволяет добиваться целевых показателей контроля гликемии даже у коморбидных пациентов с длительным анамнезом СД.
Финансирование. Написание статьи выполнено по инициативе авторов без привлечения финансирования.


