Плеоморфные ксантоастроцитомы относятся к редким опухолям глиального ряда. Они составляют менее 1% от астроцитом головного мозга. Плеоморфные ксантоастроцитомы – это глиальные опухоли низкой степени злокачественности, 2-й степени злокачественности по классификации Всемирной организации здравоохранения. Чаще всего выявляются у детей и лиц молодого возраста (2/3 всех пациентов в возрасте до 19 лет), локализуются в коре и прилежащем белом веществе и прорастают в мягкую мозговую оболочку; 98% плеоморфных ксантоастроцитом локализуются супратенториально, чаще всего в височной доле головного мозга [3, 4]. Большинство таких опухолей содержит крупные кисты. Ввиду наличия макроскопически четких границ и связи с мозговыми оболочками плеоморфная ксантоастроцитома в ходе нейрохирургической операции иногда интерпретируется как менингиома. Под микроскопом новообразование характеризуется резко выраженным полиморфизмом ядер с наличием гигантских многоядерных клеток-монстров. Помимо этого в ткани опухоли выявляются очаги липоидоза в виде ретикулярных структур, содержащих скопления ксантомных клеток с пенистой цитоплазмой. Встречаются и отдельные клетки, содержащие в цитоплазме эоэинофильные зернистые включения. В плеоморфных ксантоастроцитомах всегда имеется масса сосудов без пролиферации эндотелия. Опухолевые клетки обнаруживают тесную связь с сосудистыми стенками. Несмотря на выраженный клеточно-ядерный полиморфизм, плеоморфная ксантоастроцитома расценивается как биологически доброкачественная опухоль с медленным темпом роста. Индекс пролиферации Ki-67 обычно менее 1% [3].
Плеоморфная ксантоастроцитома подразделяется на три гистологические разновидности: типичную, пролиферирующую и злокачественную.
К характерным признакам злокачественной трансформации плеоморфной ксантоастроцитомы относятся эпителиоидно-клеточные скопления, состоящие из округлых элементов с обильной цитоплазмой и пузырьковидным ядром. В этих скоплениях отмечается высокая митотическая активность [3, 8].
Чаще всего плеоморфная ксантоастроцитома имеет длительный анамнез и проявляется эпилептическими припадками. Компьютерная томография и магнитно-резонансная томография (МРТ) являются ведущими в диагностике плеоморфных ксантоастроцитом мозга, при этом обычно определяются опухолевая масса и/или опухолевые кисты. Перифокальный отек чаще всего минимальный, что связано с медленным ростом опухоли [3].
Основным методом лечения плеоморфных ксантоастроцитом является хирургический. Цель операции – тотальное удаление опухоли, что часто достижимо. При неполной резекции необходимо длительное наблюдение за пациентом, поскольку опухоль может расти очень медленно – в течение многих лет, прежде чем она вновь потребует лечения. В этом случае возможно проведение повторной операции [2].
Прогноз при плеоморфной ксантоастроцитоме в большинстве случаев благоприятный. Опубликованы данные исследований об отдаленных результатах лечения в группах больных плеоморфной ксантоастроцитомой: 5- и 10-летняя выживаемость без прогрессирования болезни составила 72 и 61% соответственно. По данным другого исследования, 5-летняя общая выживаемость составила 81, 10-летняя – 70% [3].
Возможность полного хирургического удаления опухоли служит основным прогностическим фактором [2]. Независимым прогностическим фактором является повышенная (более 5 митозов в поле высокого увеличения) митотическая активность, наличие участков некроза в опухоли. Большинство опухолей с агрессивным течением характеризуется этим показателем. Опухоли с этими характеристиками относят к анапластическим плеоморфным ксантоастроцитомам. Они характеризуются более агрессивным течением, частыми рецидивами [7, 8]. В этих случаях течение болезни аналогично глиомам головного мозга высокой степени злокачественности (анапластическая астроцитома или глиобластома).
В 30–40% при анапластических плеоморфных ксантоастроцитомах определяется мутация BRAF V600. Описаны клинические случаи достижения ремиссий при лечении ингибиторами BRAF анапластических плеоморфных ксантоастроцитом у детей [1, 5, 6].
Приводим пример клинического случая успешного лечения больного анапластической плеоморфной ксантоастроцитомой с мутацией B-raf.
В январе 2012 г. пациент М. 26 лет обратился с жалобами на головные боли. При обследовании по данным МРТ головного мозга с контрастным усилением выявлена опухоль левой теменно-затылочной области головного мозга. Тотальное удаление опухоли головного мозга выполнено 12.01.2012. При морфологическом исследовании установлен диагноз «плеоморфная ксантоастроцитома c явлениями анаплазии» (G III–IV, Ki-67 до 15%). С февраля по апрель 2012 г. проведен курс лучевой терапии на область первичной опухоли головного мозга (РОД=2, СОД=60 Гр).
При обследовании в сентябре 2014 г. выявлен рецидив опухоли головного мозга. Повторное удаление опухоли левой теменно-затылочной области головного мозга выполнено 23.09.2014. При морфологическом исследовании: анапластическая плеоморфная ксантоастроцитома, G IV, Ki-67>20%. При генетическом исследовании не выявлено метилирования гена MGMT, не выявлено делеции генов 1р и 19q в опухоли. Выявлена мутация BRAF V600E в опухоли.
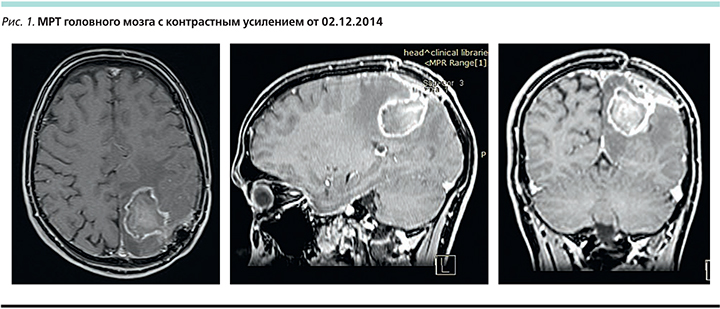
В декабре 2014 г. отмечено прогрессирование болезни в виде продолженного роста опухоли головного мозга. Размеры опухолевого узла, по данным МРТ головного мозга с контрастным усилением от 02.12.2014, составили 4,0×3,0 см (рис. 1).
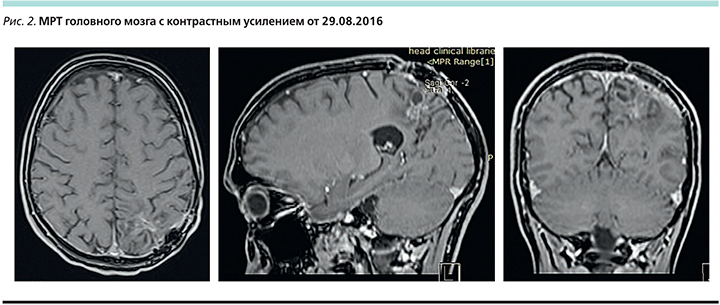
С декабря 2014 г. начата таргетная терапия ингибитором BRAF препаратом вемурафениб 960 мг 2 раза в сутки внутрь постоянно. Отмечен выраженный частичный регресс опухоли головного мозга. По данным МРТ головного мозга с контрастным усилением от 29.08.2016, опухоль головного мозга практически перестала определяться (рис. 2). Переносимость лечения удовлетворительная. Отмечена умеренная сыпь 1-й степени на коже.
Дополнительно была выполнена позитронно-эмиссионная томография головного мозга с метионином 15.06.2016. Отмечена низкая метаболическая активность в зоне остаточной опухоли головного мозга, SUV=1,36.
В настоящее время пациент продолжает прием вемурафениба и находится под динамическим наблюдением в РОНЦ им. Н.Н. Блохина.
Таким образом, данный клинический случай демонстрирует возможность достижения длительных ремиссий при использовании ингибиторов BRAF, в т.ч. вемурафениба, в терапии пациентов с рецидивами анапластических плеоморфных ксантоастроцитом и с мутацией BRAF V600E в опухоли. Необходимо проведение клинических исследований по изучению ингибиторов BRAF на больных анапластической плеоморфной ксантоастроцитомой с наличием мутаций BRAF V600.


