Синдром раздраженного кишечника (СРК) является одним из наиболее распространенных желудочно-кишечных расстройств, которым страдают 10–15 % населения в развитых странах [1, 2]. Считается, что функциональное расстройство кишечника характеризуется болью или эквивалентным ей дискомфортом, связанным с дефекацией или изменением стула.
Согласно современным представлениям, СРК – это биопсихосоциальное заболевание, в основе развития которого лежит взаимодействие двух основных патологических механизмов: повышенного (в некоторых случаях негативного) психосоциального воздействия и рецепторно-двигательной дисфункции (нарушения висцеральной чувствительности и моторной активности кишечника). Следует отметить, что развитие висцеральной гиперчувствительности необходимо рассматривать как основу формирования всей функциональной патологии желудочно-кишечного тракта (ЖКТ). Еще недавно СРК относили к функциональным заболеваниям, при которых патогенез развития симптомов не может быть объяснен органическими причинами. За последние годы удалось установить, что в основе висцеральной чувствительности и аллодинии (снижение порога восприятия боли) лежит развитие воспалительной реакции в стенке кишечника больных СРК [3]. В связи с этим становится понятно, что наличие только спазмолитического эффекта от препаратов, используемых при лечении больных СРК, способно оказывать необходимое позитивное воздействие на двигательную дисфункцию, но не влияет на восстановление висцеральной чувствительности. Отсюда закономерно следует вывод: при сохраненной гиперчувствительности моторные нарушения будут существовать длительное время, а значит, необходимо и длительное использование спазмолитических препаратов. Следовательно, должны использоваться препараты с доказанной эффективностью и безопасностью. Национальный институт здравоохранения и клинического мастерства Великобритании (NICE) выпустил новые рекомендации по диагностике и лечению СРК в первичной помощи. На основании тщательного анализа клинических данных было сделано заключение: «...спазмолитические средства, такие как Бускопан®, содержащий хорошо известную активную субстанцию гиосцина бутилбромид, являются препаратами первой линии в диагностике и управлении общими симптомами пациентов с СРК. Испытания с использованием Бускопана проявили эффективность в уменьшении симптомов боли, связанных с СРК» [3]. Однако продолжительность первичного курса лечения составляет не менее 6–8 недель, базовой терапии – 1–3 месяца.
Попытка использовать ненаркотические анальгетики (производные пиразолона, пара-аминофенола, индолуксусной кислоты и др.), которые не влияют на тканевую воспалительную реакцию слизистой оболочки кишечника, а следовательно, и не изменяют висцеральной чувствительности, не имела успеха, поскольку оказывался только временный обезболивающий эффект. У пациентов с СРК было выявлено достоверное увеличение NF-kB-зависимой протеолитической активности биоптата слизистой оболочки толстой кишки по сравнению с пациентами группы контроля. Введение ингибитора NF-kB приводило к нормализации протеолитической активности. Введение супернатантов биопсии кишечника от больных СРК вызвало явление гипералгезии (повышенное болевое реагирование) и аллодинии (уменьшение болевого порога) у мышей, которые купировались применением ингибиторов сериновых протеаз и ингибитором NF kB [4]. С этим связана попытка (имевшая определенный положительный результат) использовать в лечении больных СРК кетотифен длительными курсами [5, 6]. Однако логичнее было избрать тактику устранения причины данной воспалительной реакции – дисбиоза кишечника [7]. В данном контексте себя нашли как комбинация рифаксимина с пребиотиками, так и использование только пребиотических препаратов [8, 9].
Однако в основу нормализации дисбиотических нарушений кишечника должен быть положен принцип нивелирования моторных и секреторных нарушений ЖКТ. Безусловно в данном контексте будут представлять интерес препараты, обладающие комплексным воздействием на органы ЖКТ. Таким представителем можно считать гиосцина бутилбромид, обладающий помимо вышеописанного спазмолитического эффекта еще и секретолитической активностью. Наличие MAP-киназной активности у М3-холиновых рецепторов обусловило необходимость изучения воздействия холинолитических препаратов на пролиферативную активность эпителия. Первоначально была выявлена повышенная экспрессия мускариновых М1- и М3-рецепторов на эпителиальных и гладкомышечных клетках дыхательных путей больных хронической обструктивной болезнью легких [10, 11]. Активация М3-рецепторов не только приводила к констрикции бронхов, но и оказывала пролиферативное воздействие на эпителий бронхов. Эффект был опосредован Gq-белками М3-мускариновых рецепторов, которые активируют фосфатидилинозитол-3-киназу (PI3K), и ингибирующим фосфорилированием гликогенсинтазы киназы-3 (GSK-3). Холинергическая стимуляция мускариновых рецепторов усиливала экспрессию генов провоспалительных агентов (IL-6, -8, циклооксигеназы (ЦОГ) -1 и -2 и урокиназы активатора плазминогена) в гладких мышцах и клетках эпителия. В дальнейшем удалось установить протеинкиназа С-зависимое увеличение нуклеарного фактора NF-kB, оказывающее пролиферативный эффект. На фоне провоспалительного эффекта стимуляция мускариновых рецепторов приводила к митогенному эффекту, сопровождавшемуся снижением дифференцировки клеток. Закономерным следствием длительной блокады М3-рецепторов были не только достижение спазмолитического эффекта, но и предупреждение ремоделирования бронхиальных путей, противовоспалительный эффект [12].
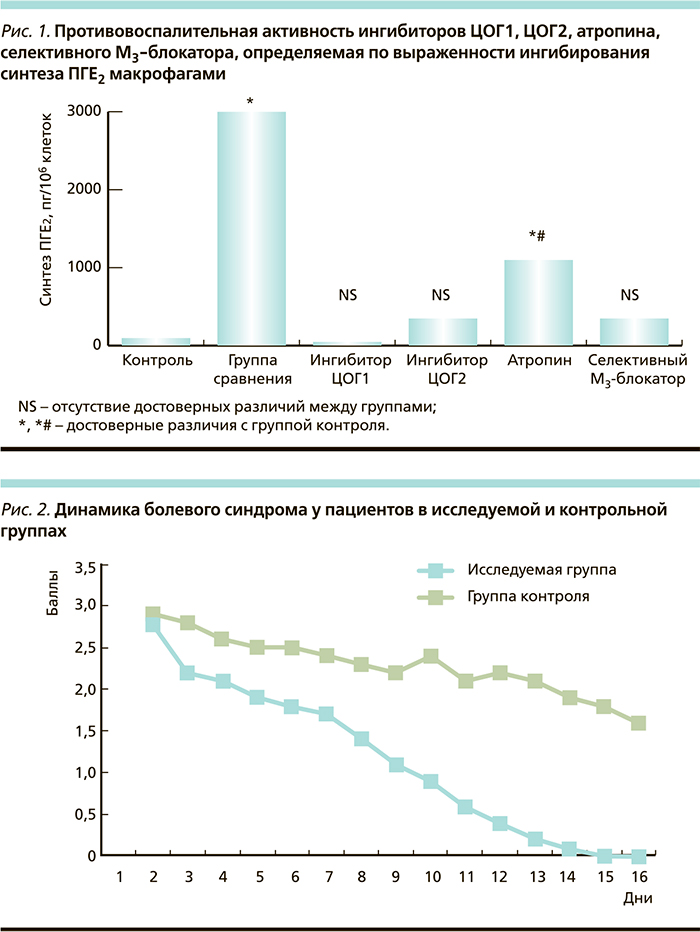
В случае когда пациенты наблюдались с постинфекционной формой СРК, данные изменения рассматривались как остаточные воспалительные. В то же время у группы пациентов отсутствовала связь в анамнезе с кишечной инфекцией. Для данной категории пациентов была установлена связь психотравмирующих факторов с провоспалительной активностью супернатантов, а также увеличение экспрессии М3-ацетилхолиновых рецепторов [13]. Использование селективных М3-холинолитиков позволяло не только устранять болевой синдром за счет спазмолитического эффекта, но и добиваться снижения провоспалительной активности, а также гиперчувствительности кишечной стенки [14]. При этом в эксперименте была подтверждена противовоспалительная активность селективных М3-блокаторов, для эпителиальных тканей сопоставимая с селективными ингибиторами ЦОГ-2 (рис. 1) [15].
В основу собственного исследования было положено наблюдение за 132 пациентами с СРК; средний возраст больных составил 34,9±4,6 года (мужчины – 32,1 ± 4,1 года, женщины – 36,6 ± 3,3). Пациенты были разделены на две группы в зависимости от проводимой терапии. Основная группа представлена 98 больными, в комплексной терапии которых использовался гиосцина бутилбромид (Бускопан®) в суточной дозировке 60 мг, длительность терапии составила 6 недель.
В контрольной группе 34 пациента получали дротаверин в суточной дозировке 120 мг.
Все больные проходили стационарное обследование и лечение в клинике 2-й кафедры (терапии усовершенствования врачей) Военно-медицинской академии, Санкт-Петербург.
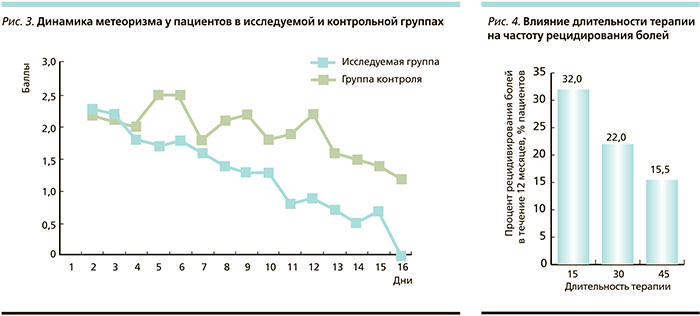
Использование гиосцина бутилбромида данной категорией пациентов позволило в течение двух недель достичь купирования болевого абдоминального синдрома и метеоризма (рис. 2, 3) в отличие от группы контроля.
Следует отметить: состояние гиперсенситивности у пациентов с СРК сохраняется еще в течение 3–4 недель после купирования клинической симптоматики. Для дальнейшего исследования зависимости висцеральной гиперчувствительности от длительности лечения пациенты основной группы были разделены по срокам лечения на 3 подгруппы: 34 пациента со сроком лечения 2 недели и по 32 пациента со сроками лечения 4 и 6 недель. По результатам исследования установлено, что на фоне использования гиосцина бутилбромида только к концу 6-й недели пациентам удалось значительно снизить гиперчувствительность.
В клиническом эквиваленте это нашло отражение в частоте рецидивирования у пациентов исследуемых групп. Так, у пациентов со сроками лечения 2 недели частота рецидивирования достигала 32 %, со сроками лечения 4 недели снижалась до 22 %, а при сроках лечения 6 недель составила 15,5 %.
Таким образом, использование гиосцина бутилбромида в течение 6 недель позволило снизить частоту рецидивирования в течение года в 2 раза по сравнению с группой, лечившейся 2 недели.
Таким образом, полученные результаты позволяют заключить, что гиосцина бутилбромид (Бускопан®) обладает физиологическим воздействием на секреторную и моторную функции ЖКТ, способен эффективно устранять их нарушения. Обнаруженные ранее противовоспалительные и пролиферативные эффекты селективных М3-холиноблокаторов открывают новые горизонты длительного использования данной группы препаратов с целью восстановления процессов репарации и дифференцировки.
Не проникая через гематоэнцефалический барьер и в результате не оказывая влияния на центральную нервную систему, имея абсолютную биодоступность менее 1 % и одновременно высокую аффинность к мускариновым и никотиновым рецепторам, Бускопан® распределяется главным образом в гладкомышечных клетках органов брюшной полости и малого таза, а также в интрамуральных ганглиях органов брюшной полости [16]. За счет таких фармакокинетических свойств он реализует свой спазмолитический эффект, практически не вызывая побочных реакций, частота возникновения которых сопоставима с плацебо [17, 18, 19], что позволяет назначать препарат Бускопан® для длительного курсового лечения и последующего приема по требованию. По данным обзора Титгат [16], где также были представлены данные по безопасному применению Бускопана® в течение 90 дней, компания Бёрингер Ингельхайм, производитель препарата Бускопан®, регулярно подает отчет Periodic Safety Update Report по безопасности применения Бускопана® в мире.
С 1992 года было подано 3 отчета, где было зафиксировано 194 миллиона эпизодов приема таблетированного Бускопана®, и только в 48 случаях (т. е. 0,00000025 %) были зафиксированы п/э антихолинергической при-роды, которые могли быть связаны с приемом этого лекарственного средства.
Длительное использование гиосцина бутилбромида в составе комплексной терапии больных СРК не только безопасно, но и прогностически оправданно для данной категории пациентов, поскольку способствует восстановлению висцеральной чувствительности и достоверно снижает частоту рецидивирования заболевания.


