Синдром раздраженного кишечника (СРК) – это хроническое заболевание кишечника достаточно высокой распространенности, которая составляет в среднем от 5 до 10% в популяции. В западных странах заболевание встречается чаще (до 20% общей численности населения) [7, 8], однако отмечается рост числа случаев СРК в странах Азии. Данных о распространенности СРК в Южной Америке и Африке мало [11]. Среди пациентов врачей-гастроэнтерологов больные СРК составляют около 20%. При этом 2/3 лиц не обращаются к врачам [8]. Из тех, кто обращается, 40–70% имеют характерный психоэмоциональный статус (наличие тревоги, неуверенности, страха, депрессии, навязчивых состояний). Пик заболеваемости отмечается в возрасте 24–40 лет. Соотношение мужчины:женщины составляет 1:1, 1:2. Женщины больше склонны к запорам, мужчины – к поносам. У сельских жителей СРК встречается значительно реже, чем у городских [2].
В процессе изучения функциональных расстройств патогенез их развития был сформирован как биопсихосоциальная модель, в которой четко определено место большинства факторов, влияющих на возникновение и развитие заболеваний этой группы [5].
Факторы, влияющие на развитие СРК:
- тип личности (влияние генетики или среды);
- психосоциальные факторы – нервно-психические воздействия (хронический и острый стресс, отношение больного к психотравме);
- генетическая предрасположенность;
- низкий уровень интерлейкина-10 (ИЛ-10) в слизистой оболочке кишечника, полиморфизм ферментов обратного захвата серотонина, увеличение адренергических нейросекреторных гранул в энтеральной нервной системе;
- нарушение моторики: гиперсегментарный гиперкинез, дистонический гипо- и акинез, антиперистальтический гиперкинез.
Влияние психосоциальных факторов, типа личности и среды имеет большое значение на возникновение СРК и подверглось тщательному изучению [1]. В связи с этим важнейшую роль в помощи таким пациентам играют психотерапевтические методики и взаимопонимание врача и пациента.
К сожалению, в проведенных исследованиях было показано, что часть врачей отрицают само существование функциональных расстройств желудочно-кишечного тракта (ЖКТ), другие выражают пренебрежительное или негативное отношение к пациентам, некоторые врачи склонны проводить ненужные диагностические исследования.

Симптомы функциональных расстройств кишечника связаны с комбинацией нескольких известных физиологических факторов:
- усиление двигательной активности;
- увеличение висцеральной гиперчувствительности;
- изменение иммунной и воспалительной функций слизистой оболочки (включая изменение микрофлоры);
- изменение регуляции центральной нервной системы (ЦНС)–энтерической нервной системы (ЭНС).
Роль мигрирующего моторного комплекса
В состоянии натощак моторика желудка и кишечника демонстрирует циклические изменения, получившие название мигрирующего моторного комплекса (ММК). Он состоит из четырех фаз. Сокращения начинаются в области нижнего сфинктера пищевода и желудка, а затем в 12-перстной кишке, откуда распространяются вниз по всей тонкой кишке. Первая фаза характеризуется относительным отсутствием сокращений. Во второй фазе отмечается нарастающая, нерегулярная сократительная активность, но сокращения достаточно редкие. Третья фаза – это высокоамплитудные, сильные, регулярные сокращения, которые начинаются в антральном отделе желудка или проксимальном отделе тонкого кишечника и распространяются на всю тонкую кишку. Четвертая фаза – короткий переходный период к очередному периоду покоя первой фазы. ММК у человека составляет 100–130 минут и прерывается приемом пищи. Важную роль в инициации ММК играет мотилин, локализующийся преимущественно в стенке 12-перстной кишки или проксимальных отделах тощей кишки. Серотонин и сомастатин ингибируют сокращения третьей фазы в желудке, сокращения возникают в 12-перстной кишке. Обсуждается влияние грелина на третью фазу, однако подробные исследования отсутствуют.
Моторика ЖКТ у пациентов с СРК по сравнению со здоровыми людьми имеет некоторые отличия. В исследованиях было установлено несколько фактов. Так, во время бодрствования у пациентов с СРК продолжительность постпрандиальной моторной активности была меньше по сравнению со здоровыми. У пациентов с преобладанием диареи интервалы между двумя последовательными ММК были короче, чем у пациентов с запорами. Кроме того, была выявлена значительно более активная моторика 12-перстной кишки во время второй и третьей фаз у пациентов с СРК с диареей. У пациентов с СРК с запорами показатели моторики тощей кишки во время второй фазы и показатели моторики 12-перстной и тощей кишки во время третьей фазы были значительно выше по сравнению со здоровыми добровольцами. Симрен и соавт. показали, что у пациентов с СРК вне зависимости от частоты опорожнения кишечника уровень мотилина в плазме в дневное время выше, чем у здоровых. Таким образом, данные исследования демонстрируют изменения в ММК у больных СРК.
Роль висцеральной болевой чувствительности в формировании боли
Большинство ученых считают, что висцеральная гиперчувствительность приводит как к нарушениям моторики, так и к возникновению болей в животе при СРК. У пациентов отмечается снижение болевого порога при растяжении кишечника или повышенная чувствительность даже к нормальной кишечной функции.
Воспаление
Около трети пациентов связывают начало симптомов с перенесенной острой кишечной инфекцией [6]. Кроме того, в слизистой оболочке таких лиц обычно повышено число воспалительных клеток и провоспалительных цитокинов. Не исключена вероятность того, что эти факторы имеют значение в развитии висцеральной гиперчувствительности.
Бактериальная микрофлора
Есть работы по изучению влияния Bifidobakterium infantis на купирование симптомов СРК, которые сопровождались изменением соотношения ИЛ-10/ИЛ-12. Но это требует дальнейшего изучения.
Нервная регуляция кишечника (ЦНС–ЭНС)
Пищеварительная нервная система иннервируется специализированной сетью нервных клеток, формирующих ЭНС, которая контролирует сократительную способность ЖКТ. ЭНС связана с ЦНС (головным мозгом) посредством автономной нервной системы. Нарушение регуляции этих двух систем при СРК может приводить к изменению восприятия, сократительной способности и иммунной функции [10]. Дисфункция нервной регуляции кишечника, вероятно, обусловлена нейропептидами и рецепторами, присутствующими в ЭНС и ЦНС. Среди предполагаемых веществ – 5-НТ (5-гидрокситриптамин) и его представители, энкефалины и агонисты опиоидов, субстанция Р, кальцитонин-генсвязанный полипептид, холецистокинин, рецептор нейрокинина и антагонисты кортикотропин-релизинг гормона. В настоящее время проходит исследование препаратов с применением веществ, действующих на эти рецепторные области. Есть надежда, что данные препараты будут купировать разнообразные симптомы: боль, дисфункцию кишечника и психологический дистресс.
Римский консенсус-III в 2006 г. определил СРК как функциональное кишечное расстройство, при котором абдоминальная боль или дискомфорт связаны с нарушением акта дефекации и изменением ритма опорожнения кишечника [4, 5]. Стоит обратить внимание, что ведущим симптомом при СРК является боль, связанная с ритмом опорожнения кишечника (запор, диарея). Именно боль отличает СРК от других функциональных расстройств: функциональной диареи, характеризующейся разжижением стула и отсутствием боли, или функционального запора, при котором также не должно быть болевого синдрома. Каждое состояние отличается диагностическими и лечебными подходами.
В Римской классификации-III функциональных желудочно-кишечных расстройств кишечным расстройствам посвящен раздел С, в котором выделено 5 нозологических форм.
С. Функциональные кишечные расстройства:
С. 1. Синдром раздраженного кишечника.
С. 2. Функциональное вздутие живота.
С. 3. Функциональный запор.
С. 4. Функциональная диарея.
С. 5. Неспецифические функциональные расстройства кишечника.
К диагностическим критериям СРК относятся рецидивирующая боль в животе или дискомфорт по крайне мере 3 дня в месяц за последние 3 месяца, связанные с двумя или более признаками из следующих:
- улучшение после дефекации;
- начало, связанное с изменением частоты стула;
- начало, связанное с изменением формы (внешнего вида) стула.
Дополнительные симптомы:
патологическая частота стула (менее 3 раз в неделю и более 3 раз в сутки);
- патологическая форма стула;
- натуживание при дефекации;
- императивный позыв или чувство неполного опорожнения, выделение слизи, вздутие.
Подтверждающие критерии:
- ненормальная частота стула (3 и менее испражнений в неделю, более 3 испражнений в сутки);
- ненормальная форма стула (шероховатый/твердый стул или расслабленный/водянистый стул);
- натуживание при дефекации;
- безотлагательность или чувство неполного опорожнения;
- выделение слизи и вздутие.
Дополнительные симптомы:
- патологическая частота стула (менее 3 раз в неделю и более 3 раз в сутки);
- патологическая форма стула;
- натуживание при дефекации;
- императивный позыв или чувство неполного опорожнения, выделение слизи, вздутие.
Для того чтобы выявить симптомы, которые входят в диагностические критерии функциональных расстройств, необходимо правильно построить беседу с больным, должны быть точно заданы вопросы, ответы на которые помогут поставить диагноз.
Вопросы, которые обязательно должен задать врач для того, чтобы заподозрить функциональное кишечное расстройство:
- Есть ли у Вас нарушения стула?
- Что изменилось – частота, форма стула?
- Сопровождается ли нарушение стула болью?
- Становится ли легче после стула?
- Как давно беспокоят Вас эти симптомы (короткий анамнез не в пользу СРК)?
- Есть или нет примесь крови в стуле (очень опасный симптом – срочно обследовать)?
- Повышалась или нет температура (при коротком анамнезе исключаем инфекцию, воспалительные заболевания кишечника, онкологию)?
- Вы похудели или нет? Если да, то на сколько и за какой период (снижение массы тела не характерно для функциональных расстройств)?
- Беспокоит ли что-нибудь еще: слабость, боли в суставах – эти симптомы не в пользу функциональных расстройств?
- Как Вы считаете, с чем связано Ваше заболевание?
- Был ли стресс?
- Как Вы спите?
- Все ли в порядке в семье, на работе?
- Не связаны ли жалобы с перенесенной ранее кишечной инфекцией?
Задав эти вопросы, врач может заподозрить органическую патологию: воспалительное или инфекционное заболевание кишечника, онкологическую патологию, либо будет склонен считать это заболевание функциональным и, исходя из этих предположений, строить план обследования.
Лечебные подходы к пациентам с СРК строятся, исходя из представлений о патогенезе данной патологии.
Прежде всего необходимо достигнуть понимания и доверия между врачом и пациентом. В России до настоящего времени практически отсутствует возможность обращения таких пациентов к психотерапевтам, которые могли бы проводить им когнитивно-поведенческую терапию, релаксацию, гипноз, комбинированное лечение, что позволяет снижать уровень тревожности, поощрять здоровый образ жизни, повышать ответственность пациента за лечение, улучшать переносимость боли. Поэтому на терапевта или гастроэнтеролога ложится основная нагрузка по психологической работе с больными СРК.
Думаю, специалистам могут быть полезны рекомендации, данные Дугласом А. Дросманом для достижения терапевтического контакта между врачом и пациентом [5]:
- Собирайте анамнез внимательно, обстоятельно, глубоко интересуясь пациентом.
- Проводите обследование тщательно, учитывайте его стоимость.
- Установите, насколько хорошо пациент знаком с причинами своего заболевания. Проведите исчерпывающее объяснение причин.
- Объясните, какого улучшения надо ожидать в процессе лечения.
- Если возможно, оцените связь факторов стресса с симптомами.
- Установите твердые ограничения в назначении обезболивающих средств.
- Вовлекайте больного в процесс лечения.
- Дайте рекомендации, согласующиеся с интересами больного («антидепрессанты могут быть использованы для лечения депрессии, но в малых дозах эти лекарства могут применяться и для лечения боли»).
- Устанавливайте прочную длительную связь с семейным (участковым) врачом.
Основной подход к лечению
СРК – симптоматический. Римский консенсус-III дал рекомендации по лечению трех основных симптомов СРК: понос, запор, боль (табл. 1) [9].
Крайне важным остается умение врача использовать антидепрессанты в лечении пациентов с СРК. Именно антидепрессанты оказывают основное регулирующее влияние на висцеральную болевую чувствительность больных этой категории. Трициклические антидепрессанты (амитриптиллин) и более современные ингибиторы обратного захвата серотонина-норадреналина (дулоксетин) контролируют боль через центральную анальгезию, а также путем облегчения сопутствующих симптомов депрессии. Селективные ингибиторы обратного захвата серотонина (флуоксетин, пароксетин) менее эффективны в подавлении боли, но могут уменьшать уровень тревоги и депрессии. Применение антидепрессантов стоит рассматривать для всех пациентов с хронической болью, даже в отсутствие симптомов депрессии. Лечение надо назначать не менее чем на месяц и продолжать до года с постепенной отменой препарата.
Нарушения ММК, которые установлены у пациентов с СРК, дают все основания для назначения спазмолитиков, рекомендованных Международным консенсусом в Риме в 2006 г. Необходимо отметить их влияние не только на двигательные нарушения кишечника, но и на болевой синдром, связанный с ними [3].
Классификация спазмолитиков:
Нейротропные спазмолититки (холинолитики, М-холиноблокаторы):
Неселективные:
- атропинового ряда (атропин, платифиллин) (М2);
- гастроцепинового ряда (гастроцепин) (М1).
Селективные:
- гиосцина бутилбромид (М3, М2).
2. Миотропные спазмолитики:
Неселективные:
- папаверин;
- дротаверин.
Селективные:
- мебеверин;
- пиноверия бромид;
- отилония бромид.
3. Регуляторы сокращения мышечного волокна:
- тримебутин.
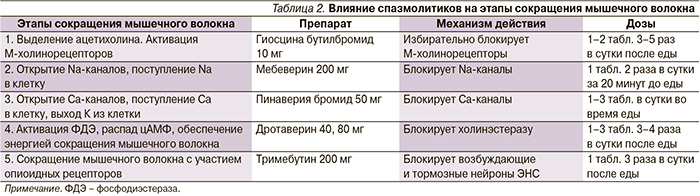
При выборе спазмолитиков для лечения функциональных расстройств необходимо помнить, на какие этапы сокращения мышечного волокна влияет каждый из них (табл. 2).
Поскольку гиосцина бутилбромид блокирует самые ранние механизмы спазма, его стоит назначать в случаях выраженного болевого синдрома, когда необходимо получить быстрый эффект. Кроме того, данный препарат показал свою эффективность при преобладании диарейного синдрома. Анализ исследований эффективности спазмолитиков Американской коллегии гастроэнтерологов в 2009 г. и Кокрейновский систематический обзор 2011 г. подтвердили положительное влияние селективных блокаторов кальциевых каналов на абдоминальную боль и дискомфорт. С учетом вышеприведенных данных стоит отдавать предпочтение этим препаратам (в настоящий момент в России используется только пиноверия бромид). В случае если боль умеренная либо слабая, что довольно характерно для СРК, оправданно использование селективных миотропных спазмолитиков, т.к. действие дротаверина менее эффективно.
Агонист периферических опиоидных рецепторов тримебутин служит препаратом, который позволяет нормализовать кишечную дисфункцию – как спазм, так и гипотонию, кроме того, он влияет и на опиатные рецепторы, находящиеся в ганглионарных клетках энтерального нервного сплетения, что позволяет уменьшать нарушения висцеральной болевой чувствительности. Он показал и эффективность при сочетании болевого и диарейного синдромов.
В случае выраженного диарейного синдрома необходимо рекомендовать применение лоперамида (оказывает влияние на опиоидные рецепторы), но его применение может быть только кратковременным (по требованию).

Значительно шире выбор препаратов для лечения запоров. Псиллиум, лактулоза, полиэтиленликоль характеризуются как высокой эффективностью, так и безопасностью для больных. Но не стоит забывать о необходимости рекомендовать пациентам правильный рацион питания с содержанием большого количества клетчатки. До сих пор остается актуальной рекомендация по приему отрубей и продуктов, их содержащих.
К сожалению, в практическом здравоохранении современные рекомендации выполняются не всегда, это зависит от уровня подготовленности врача, как правило, профильные специалисты значительно лучше ориентируются как в диагностике, так и в лечении функциональных заболеваний. Это показало исследование результатов лечения пациентов СРК разными специалистами.
Цель работы: провести оценку клинической эффективности лечения больных СРК врачами-терапевтами и гастроэнтерологами в поликлинике.
Материал и методы
Проведен анализ 5-летнего амбулаторного наблюдения 52 больных СРК в возрасте от 21 до 72 лет, которые были разделены на 2 группы: группа 1 – 32 больных находились под наблюдением гастроэнтеролога поликлиники; группа 2 – 20 больных наблюдались участковыми терапевтами. Клиническая характеристика больных представлена в табл. 3.
Использовались общеклинические методы обследования, для оценки качества жизни (КЖ) больных СРК был применен международный опросник IBSQOL (Irritablу Bowel Syndrom Quality of Life).
В исследование были включены только те больные, у которых диагноз СРК был подтвержден, отсутствовали органическая патология кишечника и изменения со стороны других органов пищеварительной системы.
Оценивали следующие показатели: адекватность проводимого лечения, частоту рецидивирования, частоту обращаемости в поликлинику, длительность пребывания на больничном листе, частоту госпитализаций. Достоверность различий показателей между группами оценивали по критерию достоверности Фишера и по t-критерию Стьюдента.
Результаты и обсуждение
Данные сравнительного анализа лечения больных СРК разными специалистами представлены табл. 4.
Можно отметить, что гастроэнтеролог достоверно чаще назначал спазмолитики, пищевые волокна и психотропные средства, при этом из спазмолитиков преимущественно использовались селективные блокаторы кальциевых каналов гладких мышц ЖКТ: мебеверин, пиноверия бромид, что отражено в табл. 5. Терапевты отдавали предпочтение слабительным средствам, прокинетикам 1-го поколения, в основном использовали миотропные спазмолитики: дротаверин, папаверин, применялось сочетание спазмолитиков и прокинетиков, что является нерациональным.

При назначении слабительных гастроэнтеролог чаще использовал гидрофильные коллоиды (псиллиум, макрогол, лактулоза), терапевты – препараты других механизмов действия (сенна, Сенаде, бисакодил, кора крушины, Гутталакс). Соотношение групп назначаемых слабительных представлено в табл. 6. Особое внимание обращает на себя отсутствие использования пищевых волокон в терапевтических кабинетах.
Больные СРК, как правило, нуждаются в амбулаторном обследовании и лечении. В стационар гастроэнтеролог направлял больных в случае технических трудностей, при подготовке больного к инвазивным методам обследования, что составило 8%. Госпитализация больных терапевтами проводилась достоверно чаще (71%), без наличия соответствующих показаний, что является экономически нецелесообразным. Таким образом, показатели эффективности составили 92% в группе гастроэнтеролога и 29% в группе терапевта, что составило в расчете на одного больного 0,92 и 0,29 соответственно.
За время наблюдения средняя длительность пребывания больных СРК на больничном листе составила 5 дней у гастроэнтеролога и 17 дней в терапевтическом кабинете. Экономическая эффективность составляет 13 дней нетрудоспособности на одного больного в год. Средняя длительность временной нетрудоспособности в двух анализируемых группах составила 8 дней.
В группе гастроэнтеролога – 5, в группе терапевта – 11 дней. Коэффициент нетрудоспособности составил 1,6 в группе гастроэнтеролога и 0,73 у терапевта.
Частота обострений для СРК не определялась, т.к. данное заболевание, как правило, четко очерченных обострений не имеет.
Таким образом, гастроэнтерологи применяют медикаментозную и немедикаментозную психотерапию для подавляющего большинства больных. Терапевты крайне редко при лечении функциональных расстройств назначают современные спазмолитические препараты (селективные блокаторы Са-каналов, регуляторы сокращения мышечного волокна), современные слабительные средства (лактулозу, гидрофильные коллоиды, псиллиум). Совсем не используются пищевые волокна (гастроэнтеролог назначает их 86% больных). Длительность временной нетрудоспособности в терапевтическом кабинете выше на 64 дня больничного листа на одного больного за 5 лет наблюдения. Из терапевтических кабинетов на госпитализацию больных направлялись в 9 раз чаще.
Для оценки КЖ больных СРК был применен международный опросник IBSQOL (Irritablу Bowel Syndrom Quality of Life). Полученные данные представлены в табл. 7.
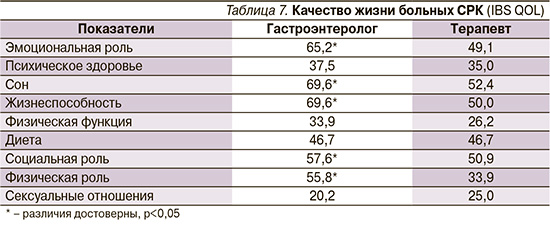
Исследования показали, что все критерии КЖ у больных СРК, наблюдаемых терапевтом, имеют четкую тенденцию к снижению по сравнению с гастроэнтерологом. При этом достоверные отличия касаются 5 критериев: Эмоциональная роль, Жизнеспособность, Сон, Социальная и Физическая роли. Больные СРК из терапевтического кабинета считали, что эмоциональные проблемы, связанные со здоровьем, значительно больше влияли на их повседневную деятельность, чем больные гастроэнтеролога. У них было больше проблем, связанных с нарушением сна, что и отражено в показателе сон. У больных СРК, наблюдавшихся терапевтами, было больше ограничений повседневной деятельности, связанных с физическими проблемами, что отражено в показателе «физическая функция». Такой показатель, как жизнеспособность, показывающий, как респондент оценивает свой жизненный тонус, у больных из терапевтического кабинета также оказался более низким. Социальная активность больных СРК (показывающая ограничения во взаимоотношениях с родственниками, друзьями, коллегами по работе), получающих лечение у терапевта, также имела тенденцию к более низкому уровню по сравнению с группой контроля. Величина других показателей не имела статистически достоверных отличий, однако общая тенденция была прежней. У пациентов терапевта было больше ограничений при выполнении работ, связанных с физической нагрузкой, их физическая активность была ниже, что отражено в показателе физическая роль. Свое настроение, ограничения в питании больные СРК обеих групп оценивали одинаково. Показатель сексуальных отношений был ниже у больных, наблюдавшихся в гастроэнтерологическом кабинете, т.к. средний возраст респондентов был более высоким и большинство из них указали на отсутствие половой жизни.
Таким образом, КЖ больных СРК, наблюдавшихся у терапевтов, по сравнению с больными гастроэнтеролога было ниже по всем основным показателям, что обусловлено комплексом физических, социальных и эмоциональных факторов, которые определяют жизнеспособность больных и в конечном итоге отражают качество их лечения.
Выводы
Врачи-специалисты (гастроэнтерологи) по сравнению с терапевтами проводят патогенетически обоснованное лечение больных в соответствии с современными международными рекомендациями.
Неполноценное лечение больных СРК терапевтами приводит к необходимости стационарного лечения в 71% случаев и увеличению длительности временной нетрудоспособности на 11 дней на одного больного в год.
Показатели КЖ пациентов с СРК значительно лучше на фоне четкого использования современных схем лечения.
Данное исследование показывает необходимость регулярного обучения врачей-терапевтов лечению функциональных расстройств кишечника.



