Согласно классическому определению, эндометриоз является гормонально- и иммунозависимым, генетически обусловленным заболеванием, характеризующимся доброкачественным разрастанием ткани, по морфологическому строению сходной с эндометрием, но находящейся за пределами полости матки [1]. Наружный генитальный эндометриоз (НГЭ) – широко распространенное заболевание, которое встречается среди 50–60 % девушек-подростков с тазовыми болями, 35–50 % женщин с бесплодием и 70–80 % пациенток с хроническими тазовыми болями. Эндометриоз характеризуется хроническим прогрессирующим и рецидивирующим течением.
В настоящее время методы, позволяющие радикально излечивать генитальный эндометриоз, отсутствуют.
Основные цели лечения:
• устранение или снижение выраженности болевого синдрома;
• yуменьшение степени распространенности эндометриоза;
• cохранение или восстановление репродуктивной функции;
• предотвращение или максимальная отсрочка рецидива заболевания;
• улучшение качества жизни.
Несомненно, универсального и стандартизированного подхода к лечению эндометриоза, который был бы идеальным для всех пациентов, не существует. В связи с этим целесообразно планировать терапию в зависимости от потребностей и предпочтений пациенток [2].
Задачи индивидуализированной терапии включают устранение жалоб и симптомов (боль, бесплодие, нарушения менструального цикла), оптимизацию соотношения профилей эффективности, безопасности и переносимости, а также повышение приверженности проводимому лечению. Наиболее рациональным подходом к лечению НГЭ является комбинированное воздействие, включающее хирургическое вмешательство с максимальным удалением эндометриоидных очагов, последующую гормональную и иммуномодулирующую терапию [3]. Известно, что эндометриоз характеризуется абсолютной или относительной гиперэстрогенемией, поэтому применяемая в настоящее время патогенетически обоснованная гормономодулирующая терапия направлена на уменьшение секреции эстрадиола яичниками вследствие временного угнетения их циклической функции, результатом чего является регресс эндометриоидных очагов. Выбор гормонального препарата, дозы и длительности лечения определяется многими факторами: возрастом больной, клиническими проявлениями заболевания, локализацией и распространенностью эндометриоза, состоянием органов-мишеней (молочных желез, эндометрия, костной ткани), а также переносимостью и наличием побочных эффектов препаратов. Кроме того, лечебная тактика зависит от репродуктивных планов женщины, особенностей хирургического лечения, состояния внутренних органов, свертывающей системы крови, центральной нервной системы. Несомненно, к важным аспектам выбора метода гормональной терапии относится ее эффективность [3].
В настоящее время для лечения эндометриоза применяются следующие группы гормональных препаратов:
1. Агонисты гонадотропин-рилизинг гормона (ГнРГ).
2. Антагонисты люлиберинов.
3. Антигонадотропины.
4. Прогестагены.
5. Андроген с антипрогестероновым и антиэстрогенным эффектами (гестринон).
6. Комбинированные эстрогенпрогестагенные контрацептивы.
7. Ингибиторы ароматазы.
8. Антиэстрогены.
9. Селективные модуляторы прогестероновых рецепторов.
Несмотря на большое разнообразие применяемых гормональных препаратов лечения генитального эндометриоза, только три группы лекарственных средств можно отнести к т. н. специфической терапии данного заболевания. К ним относятся агонисты ГнРГ, антигонадотропины (даназол) и единственный препарат группы прогестагенов – диеногест, опыт применения которого в России в настоящее время не столь значителен.
Согласно современным представлениям, эндометриоз следует рассматривать как хроническое заболевание, требующее планового лечения в течение всей жизни, цель которого – добиться максимально эффективного использования медикаментозной терапии и избежать повторных хирургических вмешательств [4].
Применение даназола и агонистов ГнРГ ассоциируется с выраженными побочными эффектами, в связи с чем данные препараты не подходят для долгосрочной терапии эндометриоза [5]. Согласно рекомендациям ESHRE, гестагены можно рассматривать в качестве терапии первого выбора лечения эндометриоза, т. к. они так же эффективны в отношении уменьшения тяжести заболевания по лапароскопической шкале оценки и борьбы с болевым синдромом, как даназол и агонисты ГнРГ, более дешевы и характеризуются более низкой частотой побочных эффектов [6].
Поэтому с учетом хорошей переносимости прогестагенов, минимальных метаболических эффектов и низкой стоимости они могут рассматриваться как препараты выбора [7].
Целью исследования явилась оценка эффективности и переносимости больными НГЭ диеногеста в дозе 2 мг.
Материал и методы
Представлены результаты наблюдения за 176 больными НГЭ, которые получали терапию диеногестом в течение 6 месяцев. Всем больным диагноз НГЭ был установлен на основании лапароскопии и подтвержден результатами гистологического исследования. Определение уровня антимюллеровского гормона (АМГ) выполнялось иммуноферментным методом с использованием коммерческих наборов “DRG Diagnostics” (Германия).
Оценка минеральной плотности костной ткани (МПК) осуществлялась в регионе L1–L4, шейке бедра и в общем показателе проксимального отдела бедренной кости. Остеоденситометрическое исследование проведено с помощью рентгеновского костного денситометра “Prodigy” (СE Lunar Corporation, USA).
Результаты и обсуждение
Согласно пересмотренной классификации Американского общества фертильности (R-AFS), I степень распространенности заболевания отмечена у 16 (9,1 %), II – у 44 (25 %), III – у 56 (31,8 %) и IV степень у – 60 (34,1 %) женщин. Таким образом, 66 % больных НГЭ, включенных в исследование, страдали распространенным эндометриозом. Эндометриоидные кисты яичников (эндометриомы) наблюдались cреди 118 (67,1 %) женщин. Иссечение позадишеечного эндометриоидного инфильтрата методом “shaving” было проведено 49 (27,8 %) больным. Экстрагенитальный эндометриоз (аппендикс, толстая кишка, мочевой пузырь, диафрагма) наблюдался cреди 13 (7,4 %) больных. НГЭ был впервые выявлен у 70 (39,8 %) больных; заболевание 106 (60,2 %) женщин носило рецидивирующий характер.
Известно, что эндометриоз яичников и последующая хирургическая операция, в особенности с бесконтрольным использованием хирургических энергий, нарушают функцию яичников и снижают т. н. овариальный резерв [8]. Кроме того, массивная электрокоагуляция ложа кисты яичника приводит к нарушению его сосудистой системы. При этом удаление части нормальной ткани яичника вместе со стенкой эндометриомы неизбежно происходит при применении любой хирургической техники. Таким образом, потенциальное влияние многих обычных хирургических процедур на овариальный резерв значимо. Среди больных с рецидивирующим характером течения эндометриоза терапия агонистами ГнРГ в анамнезе отмечена у 73 (68,9 %) пациенток. На основании определения уровня АМГ сниженный овариальный резерв имел место у 125 (71 %) женщин с НГЭ. Средний уровень АМГ составил 0,62 ± 0,39 нг/мл.
НГЭ сочетался с другими гиперпластическими процессами органов репродуктивной системы: c аденомиозом – в 27,8 % случаев, с простой гиперплазией эндометрия без атипии – в 26,1 % (из них у 45,7 % пациенток выявлена железисто-кистозная гиперплазия эндометрия, у 54,3 % – железистая гиперплазия эндометрия), миома матки наблюдалась у 21,6 % больных. Симультанная миомэктомия при лапароскопии была выполнена всем женщинам с миомой матки, максимальный размер удаленного узла составил 15, минимальный – 1,2 см.
На основании результатов двухэнергетической рентгеновской абсорбциометрии поясничного отдела позвоночника и проксимального отдела бедренной кости у 48 (27,3 %) больных НГЭ был выявлен остеопенический синдром.
Диеногест является прогестагеном 4-го поколения и объединяет фармакологические свойства группы прогестерона и прогестероноподобных соединений, а также производных 19-нортестостерона. Таким образом, диеногест характеризуется хорошей переносимостью, обладает антиандрогенным и антипролиферативным эффектами, относительно умеренным ингибирующим действием на секрецию гонадотропинов, а также сильным прогестагенным влиянием на эндометрий и высокой биодоступностью при приеме внутрь (> 90 %) [9, 10]. Диеногест в дозе 2 мг был специально разработан для комплексного лечения эндометриоза и изучен в специальной программе исследований [11].
Известно, что болевой синдром характерен для генитального эндометриоза. До начала терапии диеногестом дисменорея наблюдалась нами среди 71,6 % больных НГЭ, диспареуния отмечена у 34,1 % женщин, жалобы на тазовые боли, не связанные с менструальным циклом, предъявили 46 % пациенток.
Известными и ожидаемыми побочными эффектами применения прогестагенов являются нарушения менструального цикла, проявляющиеся нерегулярными, различными по длительности и обильности кровянистыми выделениями. На фоне применения диеногеста регулярный менструальный цикл сохранился у 41 (23,3 %) больной, однако менструации стали значительно более скудными. В данной группе больных наблюдалась достаточно высокая частота аменореи – у 63 (35,8 %) пациенток. Нарушения менструального цикла по типу “межменструальных” кровянистых выделений отмечены у 69 (39,2 %) женщин, “прорывные кровотечения” – только у 3 (1,7 %). Для повышения приверженности терапии с больными до начала применения диеногеста 2 мг была проведена беседа относительно возможных изменений характера кровотечений. Отмечено, что после начала использования диеногеста менструальный цикл стал менее регулярным, однако частота и интенсивность “межменструальных” кровянистых выделений уменьшались при увеличении длительности терапии.
На фоне шестимесячного курса применения диеногеста наблюдалось достоверное уменьшение болевого синдрома. Так, выраженность дисменореи снизилась в 3,8 раза, тазовой боли – в 2,2 и диспареунии – в 1,9 раза (см. рисунок).
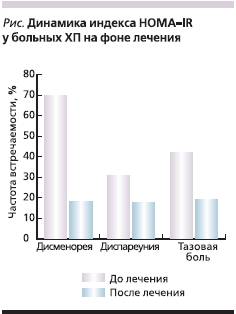
На фоне лечения наблюдались следующие побочные эффекты: наиболее часто отмечены изменения настроения – 16 (9,1 %), мастодиния – 9 (5,1 %), аcne vulgaris – 7 (4 %) пациенток. Кроме того, увеличение массы тела наблюдалось у 11 (6,3 %) больных, причем максимальная прибавка составила 2,5 кг, жалобы на головную боль предъявили 5 (2,8 %) больных. Вышеперечисленные побочные эффекты были легкими и/или умеренно выраженными и не потребовали досрочного окончания лечения.
Таким образом, шестимесячный курс лечения диеногестом в дозе 2 мг получила группа больных с лапароскопически и гистологически подтвержденным эндометриозом, преимущественно III–IV степени. Рецидивирующий характер заболевания наблюдался у 60,2 % женщин. В связи с тем что диеногест обладает умеренно выраженным действием на уровень гонадотропинов, его применение оправданно в отношении больных со сниженным овариальным резервом, отмеченным у 71 % обследованных. На основании результатов остеоденситометрического обследования наличие остеопенического синдрома диагностировано среди 27,3 % больных НГЭ, что несомненно следует учитывать при выборе гормональной терапии. Известно, что ряд препаратов лечения эндометриоза (агонисты ГнРГ, антилюлиберины, ингибиторы ароматазы и депо-формы медроксипрогестерона ацетата) может приводить к снижению МПК. Согласно проведенным исследованиям, применение диеногеста не сопровождалось снижением костной массы [12], а также не способствовало значимому изменению маркеров костного метаболизма (пиридинолина, дезоксипиридинолина и перекрестно-связанного N-телопептида коллагена 1-го типа в моче) [12, 13].
У ряда больных, получивших лечение диеногестом, НГЭ сочетался с другими гиперпластическими процессами в органах репродуктивной системы (аденомиозом, миомой матки и гиперплазией эндометрия). На фоне шестимесячного курса терапии ни у одной из 46 больных простой гиперплазией эндометрия без атипии в анамнезе (железисто-кистозной или железистой гиперплазией эндометрия) при ультразвуковом исследовании органов малого таза толщина М-эхо не превышала 4 мм.
В группе обследованных больных НГЭ миома матки обнаруживалась практически у каждой пятой пациентки. Вопрос о выборе терапии женщин с миомой матки дискуссионный, т. к. известно, что на рост узлов могут оказывать влияние не только эстрогены, но и прогестагены. Следует отметить, что у 38 пациенток, находившхся под наблюдением, при сочетании НГЭ с миомой матки не было отмечено рецидива или роста миоматозных узлов на фоне шестимесячного курса применения диеногеста. Однако вопрос об эффективности данной терапии больных миомой матки несомненно требует дальнейшего изучения и увеличения как числа больных, так и длительности лечения.
Аналогичные данные получены при сочетании НГЭ с аденомиозом (49 больных). За время шестимесячного курса лечения диеногестом 2 мг увеличения размера матки не было отмечено ни в одном случае.
Заключение
Диеногест в дозе 2 мг является препаратом специфической терапии эндометриоза, позволяющим достоверно снижать выраженность болевого синдрома, может применяться длительно и рассматривается как препарат выбора для больных с рецидивами заболевания.


