По экспертным оценкам Международной диабетической федерации (IDF), в мире насчитывается около 366 млн больных сахарным диабетом (СД), что составляет 8,3 % от населения в возрасте 20–79 лет [1]. По прогнозам специалистов, к 2030 г. общая распространенность СД составит 552 млн больных (9,9 % той же возрастной популяции). При этом количество недиагностированных случаев заболевания, включая ранние его стадии, может в 2–3 раза превышать количество зарегистрированных. В развитых странах СД страдают около 4–5 % населения, а в некоторых развивающихся странах таких больных может быть 20 % и более. В России в настоящее время насчитывается около 3,4 млн зарегистрированных больных СД.
В ноябре 2011 г. были опубликованы новые Алгоритмы специализированной медицинской помощи больным сахарным диабетом [2]. Это уже 5-й выпуск руководства, которое фактически является национальным стандартом диагностики и лечения СД, а также его осложнений. Первый выпуск вышел
в свет в 2002 г. [3], предыдущий – в 2009-м [4]. В новом выпуске произошли существенные изменения, прежде всего касающиеся лечения СД 2 типа (СД2). Ранее, в январе 2011 г., в журнале “Сахарный диабет” был опубликован для обсуждения проект “Консенсус совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии (ССТ) СД2” [5]. Была получена масса отзывов и предложений, многие из которых учтены и нашли отражение в последних алгоритмах. Ниже представлены основные изменения по главам.
Определение сд и его классификация
В этой главе никаких изменений не произошло. По-прежнему используется классификация Всемирной
организации здравоохранения (ВОЗ), предложенная в 1999 г., с небольшими добавлениями, сделанными ранее и касающимися других специфических типов СД [6].
• СД 1 типа (СД1; иммуноопосредованный, идиопатический);
• СД2 (с преимущественной инсулинорезистентностью [ИР] и относительной инсулиновой недостаточностью или преимущественным нарушением секреции инсулина с ИР или без нее);
• другие специфические типы СД (генетические дефекты функции β-клеток, генетические дефекты
действия инсулина, заболевания экзокринной части поджелудочной железы и др.);
• гестационный СД (возникает во время беременности, включает нарушенную толерантность к глюкозе и СД).
Диагностика сд
По-прежнему используются критерии диагностики СД и других нарушений гликемии, предложенные ВОЗ в 1999 г. [6] и подтвержденные в 2006 г. [7]. Оставлены диагностические критерии только для венозной плазмы и цельной капиллярной крови (табл. 1). Требования к подтверждению диагноза у людей, имеющих выраженную клиническую картину СД, отличаются от таковых у пациентов без симптомов. При наличии клинической картины СД для установления диагноза достаточно при однократном измерении получить повышенный уровень глюкозы, соответствующий СД. В отсутствие
симптомов на основании однократного получения значения глюкозы в крови, превышающего норму, диагноз не ставят. В этом случае для установления диагноза СД необходимо повторно выявить гликемию в диабетическом диапазоне натощак, при случайном измерении или в ходе перорального
глюкозотолерантного теста (ПГТТ) в последующие дни.
Таблица 1. Диагностические критерии СД и других нарушений гликемии.
Впервые появилась возможность в целях диагностики СД использовать определение гликированного гемоглобина (HbA1c), утвержденного ВОЗ в 2011 г. [8]. В качестве диагностического критерия СД выбран уровень HbA1c ≥ 6,5 %. При этом диагностический тест должен быть выполнен с использованием метода определения HbA1c, сертифицированного в соответствии с National Glycohemoglobin Standardization Program (NGSP) и стандартизованного в соответствии с референсными значениями, принятыми в Diabetes Control and Complications Trial (DCCT), т. е. нормальным считается уровень до 6 %.
Терапевтические цели при СД1 и СД2
Этот раздел претерпел весьма существенные изменения. Напомню, что в алгоритмах 2009 г. [4] показатели контроля углеводного обмена выглядели следующим образом (табл. 2).
Таблица 2. Показатели контроля углеводного обмена (2009).
Естественно, что никто не оспаривает утверждения о том, что содержание глюкозы в крови у больного СД должно быть максимально (насколько это возможно) приближено к нормальным показателям. В то же время следует помнить о безопасном уровне гликемии. Поэтому индивидуальный
подход к больному с определением индивидуального целевого уровня гликемического контроля должен являться основой выбора стратегии ССТ. Недавно завершившиеся рандомизированные исследования ACCORD [9], ADVANCE [10] и VADT [11] убедительно продемонстрировали важность выбора индивидуальных целей гликемического контроля для каждого пациента в зависимости от возраста, длительности СД, наличия сердечно-сосудистых осложнений. Согласно новым алгоритмам, выбор индивидуальных целей лечения во многом зависит от возраста пациента, ожидаемой продолжительности жизни (ОПЖ), наличия тяжелых осложнений и риска тяжелой гипогликемии (табл. 3).
Таблица 3. Алгоритм индивидуализированного выбора целей терапии по HbA1c.
Данным целевым уровням HbA1c будут соответствовать следующие целевые значения пре- и постпрандиального уровня глюкозы плазмы (табл. 4).
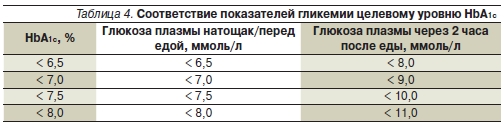
В связи с введением индивидуализированных целей лечения понятия “компенсация”, “субкомпенсация”, “декомпенсация” у взрослых пациентов не будут использоваться. При этом после формулировки диагноза необходимо указать целевой уровень гликемического контроля.
Целевые параметры лечения СД в отношении липидного обмена и артериального давления (АД) не претерпели изменений. В частности, целевой уровень систолического АД составляет ≤ 130, диастолического ≤ 80 мм рт. ст.
Требования к формулировке диагноза при сд
Понятие тяжести СД, которое существовало ранее [4], было отменено. Оно в основном отражало наличие ССТ и стадию осложнений, которые и так будут в дальнейшей формулировке клинического диагноза. Фактически следует признать, что понятие тяжести не имело медицинского смысла, а существовало для медико-социальной экспертизы. В связи с тем что понятия компенсации также отменены, формулировка диагноза СД выглядит следующим образом:
• Сахарный диабет 1 типа (2 типа) или
• Сахарный диабет вследствие (указать причину).
• Диабетические микроангиопатии:
ретинопатия (указать стадию на левом глазу, на правом глазу);
• состояние после лазерокоагуляции сетчатки или оперативного лечения (если проводились) от года;
• нефропатия (указать стадию).
• Диабетическая нейропатия (указать форму).
• Синдром диабетической стопы (указать форму).
• Диабетическая остеоартропатия (указать фазу).
• Диабетические макроангиопатии: ИБС (указать форму); сердечная недостаточность (ука-
зать функциональный класс по NYHA);цереброваскулярные заболевания (указать, какие);
хроническое облитерирующее заболевание артерий нижних конечностей (указать стадию).
• Артериальная гипертензия (указать степень).
• Дислипидемия.
• Сопутствующие заболевания.
сахарный диабет 1 типа
При СД1, возникновение которого связано с гибелью β-клеток и инсулиновой недостаточностью, основной метод лечения – заместительная инсулинотерапия. Питание (количество углеводов) и физические нагрузки больной должен лишь учитывать для выбора правильной дозы инсулина. Никаких изменений эта часть не претерпела. Мониторинг основных показателей у больных СД1 подвергся небольшим изменениям (в частности, появилось непрерывное мониторирование уровня глюкозы).
Сахарный диабет 2 типа
Этот раздел претерпел самые существенные изменения.
Подчеркнуто, что диетотерапия – необходимая составная часть лечения СД2 при любом варианте медикаментозной ССТ. Среди пациентов с СД2 может быть выделено несколько категорий, например по наличию или отсутствию избыточной массы тела, артериальной гипертензии, виду ССТ и др. Рекомендации по питанию для них различаются. В целом принципы диетотерапии не изменились. В новых алгоритмах нет ранее дававшегося соотношения пищевых нутриентов (не более 30 % жиров, 50–55 % углеводов, 15–20 % белков), количества холестерина (200 мг/сут), поскольку точное выполнение таких рекомендаций нереалистично.
Рекомендации по физической активности не изменились. Если изменением образа жизни не удается
достичь контроля углеводного обмена у больных СД2, назначают сахароснижающие препараты (ССП) [12]. В новых алгоритмах указано, что препараты росиглитазона запрещены для применения в Европе, ограничена их продажа и в США.
Алгоритм лечения СД2
Алгоритм назначения ССП изменился в соответствии с Консенсусом совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии СД2 [5]. За основу была взята модель совместного алгоритма Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологии (ААСЕ/АСЕ) [13].
Общие положения Консенсуса РАЭ по инициации и интенсификации ССТ СД2:
1. Определение индивидуального целевого значения контроля гликемии по уровню НbА1с.
2. Стратификация терапевтической тактики в зависимости от исходного уровня HbA1c.
Изменение образа жизни (снижение массы тела при ее избытке, ограничение легкоусвояемых углеводов и насыщенных жиров, активизация физических нагрузок) является основой терапии СД2 при любом исходном уровне метаболического контроля.
При исходном HbA1c 6,5–7,5 % достижения целевых значений гликемии возможно при использовании
монотерапии ССП (рис. 1). Приоритет должен быть отдан средствам с минимальным риском гипогликемий, таким как метформин (Мет), ингибиторы дипептидилпептидазы-4 (иДДП-4),
агонисты рецепторов глюкагоноподобного пептида-1 (аГПП-1); при наличии ожирения и артериальной гипертензии аГПП-1 предпочтительны в связи с эффективным снижением массы тела и уровня систолического АД. При непереносимости или противопоказаниях к препаратам первого ряда рекомендуется старт терапии с других классов ССП: сульфонилмочевины (СМ), тиазолидиндио-
нов (ТЗД), в частности пиоглитазона (Пио). Эффективным считается темп снижения НbA1c ≥ 0,5 % за 6 месяцев наблюдения. Если при монотерапии достичь поставленных целей не удается, в последующем возможно применение комбинированного лечения (2 или 3 препаратами).
Рисунок 1. Старт и интенсификация лечения СД2 при исходном HbA1c 6,5 - 7,5%.
При исходном HbA1c 7,6–9,0 % следует сразу начинать с комбинированной терапии (рис. 2). В данной
ситуации начинать лечение рекомендуется с комбинации двух ССП, воздействующих на разные механизмы развития заболевания. К наиболее рациональным комбинациям относятся сочетания Мет (базового препарата, снижающего ИР) и препаратов, стимулирующих секрецию инсулина: иДПП-4, аГПП-1, СМ или глинидов. Эффективным считается темп снижения НbA1c ≥ 1,0 % за 6 месяцев наблюдения. При неэффективности возможно сочетание трех ССП или начало инсулинотерапии.
Рисунок 2. Старт и интенсификация лечения СД2 при исходном HbA1c 7,6 - 9,0%.
Рисунок 3. Старт и интенсификация лечения СД2 при исходном HbA1c > 9,0%.
При исходном HbA1c ≥ 9,0 % следует назначить инсулинотерапию (рис. 3). Данная ситуация характеризуется наличием выраженной глюкозотоксичности, для снятия которой необходимо начинать инсулинотерапию (изолированную или в комбинации с ССП). В редких случаях, когда в
дебюте заболевания определяется уровень HbA1c ≥ 9 %, но при этом отсутствуют выраженные клинические симптомы декомпенсации (прогрессирующая потеря массы тела, жажда, полиурия), можно начать лечение с альтернативного варианта – комбинации двух или трех ССП. Основой такой комбинации должны стать препараты СМ как средства с максимальной инсулинсекреторной способностью. В дальнейшем в случае достижения целевых показателей метаболического контроля пациент может быть переведен на комбинированное лечение без инсулина.
На рис. 4 показаны наиболее рациональные комбинации сахароснижающих средств.
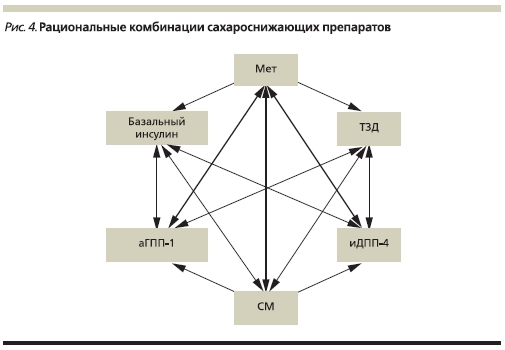
Мониторинг эффективности ССТ по уровню НbА1с рекомендуется осуществлять каждые 3 месяца. Титрация дозы назначенных ССП до максимально эффективной (переносимой) осуществляется по данным самоконтроля гликемии. Изменение (интенсификация) ССТ при ее неэффективности (т. е. в отсутствие достижения индивидуальных целей НbА1с) должно быть выполнено не позднее чем через
6 месяцев. В случае ухудшения самочувствия или в отсутствие признаков эффективности лечения решение об интенсификации может быть принято раньше.
Инсулинотерапия
Этот раздел алгоритмов также подвергся изменениям, связанным с изменением в выборе целевых параметров лечения. За основу были взяты Российские клинические рекомендации по оптимизации и интенсификации инсулинотерапии при СД2, опубликованные в 2010 г. [14].
Показания к переводу на инсулинотерапию:
• для лиц с впервые выявленным СД2 – уровень HbA1c > 9 % и наличие выраженной клинической симптоматики декомпенсации;
• для лиц с анамнезом СД2 – отсутствие достижения индивидуальных целей гликемического контроля на комбинированной терапии максимально переносимыми дозами других ССП;
• наличие противопоказаний к назначению или непереносимость других ССП;
• кетоацидоз;
• необходимость оперативного вмешательства, острые интеркуррентные и обострения хронических
заболеваний, сопровождающихся декомпенсацией углеводного обмена (возможен временный перевод на инсулинотерапию).
Показания к интенсификации инсулинотерапии при СД2:
• отсутствие достижения индивидуальных целей терапии на предшествующем режиме инсулинотерапии в течение 3–6 месяцев;
• дальнейшее титрование дозы в одной инъекции ограничена из-за большой однократной дозы (увеличения риска развития гипогликемии);
• режим питания предполагает необходимость интенсификации инсулинотерапии.
Общая схема рекомендаций по началу, оптимизации и интенсификации инсулинотерапии при СД2 представлена на рис. 5.
Рисунок 5. Рекомендации по началу, оптимизации и интенсификации инсулинотерапии при СД2.
Мониторинг основных показателей у больных СД2 подвергся небольшим изменениям и выглядит следующим образом (табл. 5).
Таблица 5. Мониторинг больных СД2 без осложнений.
Диабетические микроангиопатии
Диабетическая ретинопатия
Классификация диабетической ретинопатии несколько изменилась (удалена стадия регресса после лазерокоагуляции по поводу пролиферативной диабетической ретинопатии). Основой профилактики и лечения диабетической ретинопатии остается компенсация углеводного обмена. К специфическим методам лечения относятся лазерная коагуляция сетчатки, витрэктомия; впервые появилось интравитреальное введение ранибизумаба (Луцентис). Последний зарегистрирован для лечения диабетического макулярного отека.
Диабетическая нефропатия
Введена в действие классификация диабетической нефропатии в соответствии с классификацией хронической болезни почек (ХБП) [16]. При формулировке диагноза вначале ставится стадия микроальбуминурии или протеинурии (табл. 6), а затем указывается стадия ХБП в соответствии со скоростью клубочковой фильтрации (СКФ; табл. 7).
Таблица 6. Диагностические показатели альбуминурии.
Таким образом, при выявлении у больного СД микроальбуминурии или протеинурии диагноз будет выглядеть следующим образом:
• Диабетическая нефропатия, стадия микроальбуминурии, ХБП 1, 2, 3 или 4.
• Диабетическая нефропатия, стадия протеингурии, ХБП 1, 2, 3 или 4.
• Диабетическая нефропатия, ХБП 5.
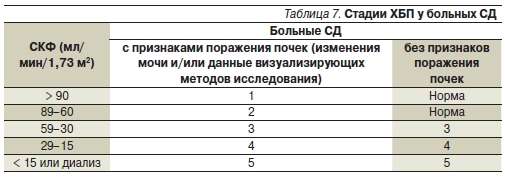
При выявлении у больного СД снижения СКФ < 60 мл/мин/1,73 м2 в отсутствие других признаков поражения почек (микроальбуминурии, протеинурии) будет ставиться диагноз: “ХБП 3, 4 или 5”.
Принципиальных изменений в лечении диабетической нефропатии не произошло. В табл. 8 представлены данные о допустимости применения различных ССП на разных стадиях ХБП.
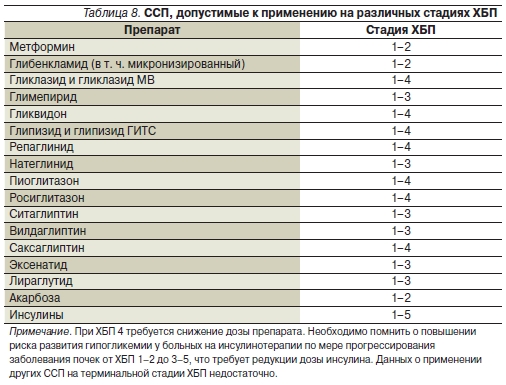
Диабетические макроангиопатии
Существенных изменений в главе не произошло. Более четко представлены алгоритмы диагностики и лечения острого коронарного синдрома. Дана рекомендация о том, что ТЗД и бигуаниды при развитии последнего должны быть немедленно отменены.
Диабетическая полиневропатия
Принципиальных изменений не произошло. Основой профилактики и лечения диабетической невропатии является компенсация углеводного обмена. Другие методы лечения имеют симптоматический характер и используются в основном при болевой форме дистальной невропатии. В представленном алгоритме лечения болевой невропатии отсутствуют препараты тиоктовой кислоты и витамины как не имеющие достаточной доказательной базы (табл. 9).
Таблица 9. Лечение болевой формы диабетической невропатии.
Диабетическая нейроостеоартропатия
Выделена в отдельную главу. Даны клинические стадии, этапы диагностики и лечения этого осложнения. Подчеркнуто, что единственным эффективным методом лечения острой стадии диабетической остеоартропатии является разгрузка пораженного сустава с помощью индивидуальной
разгрузочной повязки Total Contact Cast, которая должна быть наложена пациенту сразу после установления диагноза. В качестве дополнительного по отношению к разгрузке пораженного сустава методом лечения острой стадии может стать назначение препаратов группы бисфосфонатов (алендронат, памидронат).
СД у детей и подростков
Изменены целевые значения показателей углеводного обмена в соответствии с принятым в 2010 г. российским консенсусом [17]. Они индивидуализированы по возрасту (табл. 10). В отличие от взрослых пациентов сохранены понятия “компенсация”, “субкомпенсация” и “декомпенсация”.
Таблица 10. Целевые значения показателей углеводного обмена у детей и подростков.
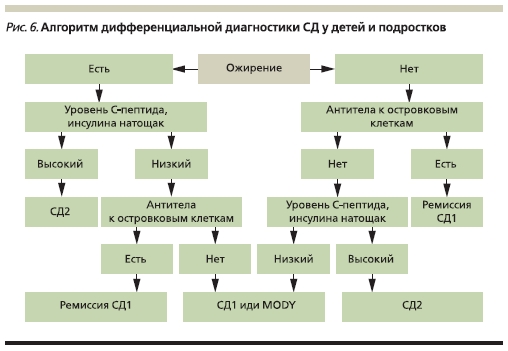
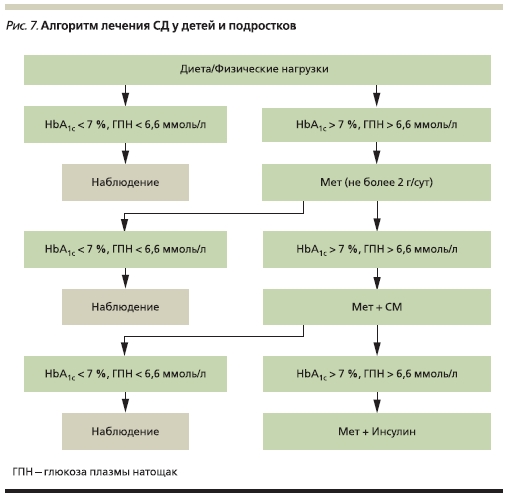
В главе представлен алгоритм дифференциальной диагностики СД у детей и подростков, уточнен алгоритм лечения СД2 у этой категории больных (рис. 6, 7). Представлена подробная характеристика наиболее часто встречающихся генетических синдромов, связанных с СД.
Другие разделы алгоритмов
В остальные разделы новых алгоритмов внесены относительно небольшие изменения.
Так, в главу об обучении больных СД добавлены конкретные обязательные разделы обучающих программ [15].
Не претерпела принципиальных изменений и глава об острых осложнениях СД. Здесь в определении гипогликемии зафиксировано, что мероприятия по ее купированию у больных СД следует начинать при уровне глюкозы плазмы < 3,9 ммоль/л. В главе, посвященной СД и артериальной гипертензии, в раздел медикаментозного лечения были добавлены прямые ингибиторы ренина (алискирен).
Предложены более строгие цели лечения СД во время ведения беременности: глюкоза плазмы натощак/перед едой – до 5,5 ммоль/л; глюкоза плазмы через час после еды – до 7,2 ммоль/л; HbA1c –
≤ 6 %. В факторах риска гестационного СД граница индекса массы тела изменена с 30 на 25 кг/м2. Критерии диагностики оставлены прежними, рекомендованными ВОЗ.
В рекомендации о контрацепции при СД добавлены оральные контрацептивы с динамическим режимом дозирования (Клайра). Также добавлен фрагмент, касающийся контрацепции в период лактации.
Для пожилых пациентов с СД2, лиц с этим заболеванием и ожидаемой продолжительностью жизни менее 5 лет изменены критерии оптимальной компенсации в соответствии с принятой индивидуализацией целей лечения. Целевой уровень HbА1c у таких больных в отсутствие ослож-
нений и риска тяжелой гипогликемии должен быть < 7,5 %, а при наличии тяжелых осложнений и/или риска тяжелой гипогликемии < 8,0.
Произошли небольшие изменения в списке инсулинов и других ССП.
В заключение следует отметить, что в 2011 г. опубликовано 2-томное руководство “Сахарный диабет” под редакцией И.И. Дедова, М.В. Шестаковой: 1-й том посвящен вопросам диагностики, лечения и профилактики СД [18], 2-й – острым и хроническим осложнениям СД [19]. В этом руководстве подробно представлена информация, изложенная в новых алгоритмах.



