Введение
Сахарный диабет (СД) на сегодняшний день представляет серьезную проблему, масштабы которой в течение последних лет приобрели глобальный характер. Так, по данным Международной федерации диабета (International Diabetes Federation), в 2015 г. количество людей с СД составило 415 млн случаев, по прогнозам экспертов в 2040 г. с ним столкнутся уже 642 млн людей [1] и речь идет прежде всего о СД 2 типа [СД2]).
Тактика ведения пациентов с СД2 включает рекомендации по изменению образа жизни, а также назначение таблетированной и/или инъекционной сахароснижающей терапии.
У большинства больных СД2 лечение начинают с моно- или комбинированной таблетированной терапии, однако со временем для поддержания уровня глюкозы плазмы в пределах целевого диапазона этого зачастую бывает недостаточно, что связано с прогрессированием дисфункции β-клеток. Согласно различным клиническим рекомендациям, как отечественным, так и международным [2, 3], когда речь идет о глюкозотоксичности, неэффективности или наличии противопоказаний к другим сахароснижающим препаратам, а также при снижении секреторной функции β-клеток поджелудочной железы, следует перейти к инсулинотерапии, которая выступает наиболее эффективным способом контроля гликемии.
Как правило, у пациентов с СД2 лечение начинают с назначения базального инсулина. К сожалению, существующие режимы инсулинотерапии имеют ограничения. Трудности в подборе оптимальных доз инсулина обусловлены вариабельностью фармакокинетического профиля препаратов, что способствует развитию гипогликемии – наиболее распространенного побочного эффекта инсулинотерапии.
Внедрение в практику аналогов базального инсулина с большей продолжительностью действия, а также обладающих более плавным профилем, стало логичным шагом на пути к уменьшению количества гипогликемических событий и улучшению показателей углеводного обмена. На сегодняшний день в России зарегистрирован и доступен для применения новый аналог инсулина длительного действия гларгин 300 МЕ/мл (Туджео СолоСтар®). Увеличение концентрации гларгина в единице объема с формированием подкожного депо меньшего объема привело к изменению фармакокинетических свойств препарата: гларгин 300 МЕ/мл по сравнению с гларгином 100 МЕ/мл (Лантус СолоСтар®) более медленно, а следовательно, более длительно высвобождается из подкожно-жирового депо, что приводит к формированию более ровного и длительного профиля действия.
Основные клинические характеристики препарата были сформулированы на основании результатов серии крупных рандомизированных клинических исследований (РКИ) III фазы под общим названием EDITON [4–6]. Ее результаты продемонстрировали неменьшую эффективность инсулина гларгин 300 МЕ/мл по сравнению с инсулином гларгин 100 МЕ/мл в отношении гликемического контроля с меньшим риском гипогликемий и динамикой массы тела.
Безусловно, РКИ представляют собой мощный инструмент получения надежных научных доказательств безопасности и эффективности медицинских продуктов. Однако РКИ проводятся в жестких условиях с установленными критериями включения/исключения участников, согласно протоколу исследования, направленного на получение достоверных данных, позволяющих сделать выводы о предусмотренных конечных точках. Вместе с тем выборка пациентов, включаемых в РКИ, может существенно отличаться от тех, которые встречаются в реальной клинической практике. По этим причинам в течение последних нескольких лет наблюдается тенденция в виде увеличения интереса к исследованиям реальной клинической практики (РКП). Эти исследования отличаются от РКИ более широкими критериями включения/исключения, позволяя получить данные об эффективности и безопасности применения недавно вышедших на рынок препаратов в реальной жизни [7].
Так, после проведения серии контролируемых испытаний EDITION возник интерес к результатам применения гларгина 300 МЕ/мл в рутинной практике, что послужило поводом для проведения нескольких исследований РКП, анализу которых и посвящен настоящий обзор.
 Применение инсулина гларгин 300 ЕД/мл в условиях РКП для инициации инсулинотерапии у пациентов с СД2
Применение инсулина гларгин 300 ЕД/мл в условиях РКП для инициации инсулинотерапии у пациентов с СД2
Безусловно, высокий интерес вызывает сравнение в РКП различных клинических показателей на фоне применения инсулинов гларгин 100 ЕД/мл и гларгин 300 ЕД/мл у пациентов с СД2, ранее не получавших инсулинотерапию. Изучение этого вопроса стало целью ретроспективного исследования, проведенного Н. Wang и соавт. [8]. Авторами были проанализированы данные опроса врачей, записи медицинских карт пациентов с СД2, которым впервые был назначен инсулин, а именно гларгин 300 МЕ/мл или гларгин 100 МЕ/мл. Специалисты, принимавшие участие в исследовании, должны были иметь сертификат по эндокринологии, опыт работы 3–5 лет, по крайней мере 60% рабочего времени посвящать клинической работе, вести как минимум 10 пациентов с СД2 в месяц, лечить как минимум четырех пациентов гларгином 300 МЕ/мл и одного больного гларгином 100 МЕ/мл в течение последнего полугода. Врачи on-line заполняли медицинские карты, а также опросники. Целью анализа было проведение оценки уровня гликированного гемоглобина (HbA1c), а также частоты гипогликемических событий до назначения и на фоне применения гларгина 300 МЕ/мл и гларгина 100 МЕ/мл.
Всего в статистический анализ были включены 298 пациентов, получавших гларгин 300 МЕ/мл, и 92 пациента – гларгин 100 МЕ/мл. Группы были сопоставимыми по среднему возрасту (53,8±12,14 года) и среднему уровню HbA1c на момент включения в исследование (8,6±1,25%).
Согласно результатам этого исследования, было выявлено значимое снижение уровня HbA1c как в группе гларгин 300 МЕ/мл, так и в группе гларгин 100 МЕ/мл (-1,21%; p<0,001 и -1,12%; p<0,001 соответственно). Однако существенных различий в снижении HbA1c между группами получено не было (p=0,62), что свидетельствовало о сопоставимой эффективности препаратов.
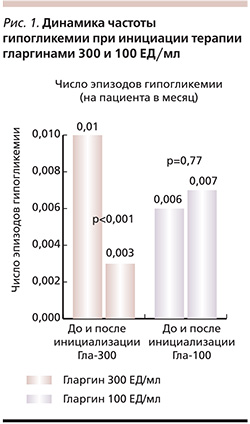
Помимо этого, было установлено, что на фоне применения инсулина гларгин 300 МЕ/мл количество гипогликемий на одного пациента в месяц было достоверно ниже, чем перед его назначением (p<0,001), в то время как в группе гларгина 100 МЕ/мл подобных изменений получено не было (p=0,77). Применение гларгина 300 МЕ/мл было ассоциировано с достоверно меньшим числом гипогликемических событий, чем применение гларгина 100 МЕ/мл (относительный риск [ОР] гипогликемий в месяц – 0,31; 95% доверительный интервал [ДИ] – 0,12–0,81;p=0,018; рис. 1).
Начальная доза гларгина 300 МЕ/мл (0,331 ЕД/кг) была сходной с таковой в группе гларгина 100 МЕ/мл (0,339 ЕД/кг; p=0,86). При дальнейшей титрации инсулина до индивидуальных целевых показателей гликемии существенных различий в дозах препаратов между группами получено не было (0,428 ЕД/кг для гларгина 300 МЕ/мл и 0,441 ЕД/кг для гларгина 100 МЕ/мл; p=0,77). Кроме того, в обеих группах пациенты после титрации получали инсулин в значимо большей дозе, чем при инициации терапии.
Таким образом, в реальной клинической практике терапия ранее не получавших инсулинотерапию пациентов с СД2 инсулином гларгин 300 МЕ/мл оказалась не менее эффективной, чем терапия инсулином гларгин 100 МЕ/мл, приводя к значимому снижению уровня HbA1c. Вместе с тем применение гларгина 300 МЕ/мл было ассоциировано с меньшим количеством гипогликемий, чем применение гларгина 100 МЕ/мл.
Клинические исходы у пациентов с СД2 при переводе на инсулин гларгин 300 МЕ/мл
В ретроспективном анализе L. Tong и соавт. [9] была проведена оценка риска гипогликемических событий и клинических исходов у пациентов с СД2, получавших инсулинотерапию базальным инсулином и переведенных на гларгин 300 МЕ/мл. Критерии включения для специалистов здравоохранения и методы сбора данных (из медицинских карт и полученные из опроса врачей) были идентичными таковым в вышеописанном исследовании Н. Wang и соавт. Были проанализированы демографические данные, анамнез заболевания, уровень HbA1c, частота гипогликемических событий, а также причина перевода на гларгин 300 МЕ/мл. Временной промежуток перед переводом на гларгин 300 МЕ/мл (исходный период) составил 6 месяцев. Период после перехода на гларгин 300 МЕ/мл был определен как ≥30 дней.
 Всего были проанализированы данные 184 пациентов с СД2, переведенных на инсулин гларгин 300 МЕ/мл. Средний возраст участников исследования составил 56,2±10,5 лет, средний индекс массы тела – 33,7±6,6 кг/м2. Среди причин перевода на гларгин 300 МЕ/мл лидирующую позицию занимала недостаточная, по мнению лечащего врача, эффективность получаемого препарата, другими распространенными поводами для перевода на гларгин 300 МЕ/мл были приверженность пациентов лечению, приемлемое дозирование, осведомленность о препарате, а также обеспокоенность по поводу гипогликемий.
Всего были проанализированы данные 184 пациентов с СД2, переведенных на инсулин гларгин 300 МЕ/мл. Средний возраст участников исследования составил 56,2±10,5 лет, средний индекс массы тела – 33,7±6,6 кг/м2. Среди причин перевода на гларгин 300 МЕ/мл лидирующую позицию занимала недостаточная, по мнению лечащего врача, эффективность получаемого препарата, другими распространенными поводами для перевода на гларгин 300 МЕ/мл были приверженность пациентов лечению, приемлемое дозирование, осведомленность о препарате, а также обеспокоенность по поводу гипогликемий.
Период после перевода на гларгин 300 МЕ/мл составил 30–329 дней (примерно 1–11 месяцев), средняя длительность лечения гларгином 300 МЕ/мл была 4 месяца.
Важно отметить, что после перевода на гларгин 300 ЕД/мл зарегистрировано статистически значимое снижение уровня HbA1c по сравнению с предшествовавшей терапией (разница составила 0,96%, 95% ДИ от -1,14 до -0,77; p<0,0001).
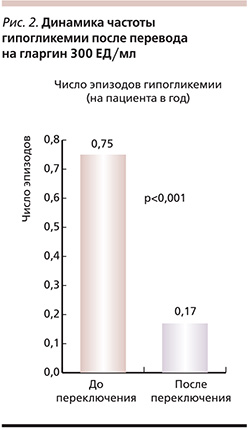
Анализ количества гипогликемических событий продемонстрировал высокую безопасность гларгина 300 МЕ/мл по сравнению с ранее применяемыми инсулинами. Так, частота гипогликемий после перевода на гларгин 300 МЕ/мл была существенно ниже (ОР – 0,23, 95% ДИ – 0,16–0,32; p<0,0001; рис. 2).
При применении гларгина 300 МЕ/мл суточная доза базального инсулина была численно ниже по сравнению с исходной инсулинотерапией (разница в дозах составила -0,09 ЕД/кг, 95% ДИ от -0,21 до -0,03), однако различия оказались статистически незначимыми (p=0,1395). Перевод на гларгин 300 МЕ/мл способствовал снижению количества инъекций инсулина у многих пациентов. При прежних режимах инсулинотерапии 43,2% участников исследования получали 2 инъекции в сутки (учитывались только больные, получавшие инсулины гларгин 100 ЕД/мл и детемир). После перевода на гларгин 300 МЕ/мл только 9,8% пациентов продолжили получать инъекции дважды в сутки. Кроме того, стоит отметить, что количество вводимого инсулина было сходным для всех режимов терапии: у пациентов, получавших инсулин 1 раз в сутки, средняя его доза составила 0,53 и 0,56 ЕД/кг в периоды до и после перевода на гларгин 300 МЕ/мл соответственно (разница 0,03 ЕД/кг, 95% ДИ от -0,12 до 0,18; p=0,684); у пациентов, получавших инсулин дважды в сутки, средняя доза препарата составила 0,94 и 0,76 ЕД/кг в периоды до и после перевода на гларгин 300 МЕ/мл соответственно (разница -0,18 МЕ/кг, 95% ДИ от -0,48 до 0,12; p=0,230).
Таким образом, было продемонстрировано, что при переводе с инсулинотерапии различными базальными инсулинами на инсулин гларгин 300 МЕ/мл в РКП наблюдается статистически значимое снижение уровня HbA1c, частоты гипогликемических событий, а также количества инъекций с равной суточной дозой инсулина. Полученные результаты согласуются с таковыми программы клинических испытаний EDITION в отношении эффективности и возможности снижения частоты гипогликемии [10]. Помимо этого результаты демонстрируют возможность улучшить режим инсулинотерапии пациентов, получающих две инъекции инсулина, а также отсутствие значимого увеличения дозы базального инсулина при переводе на гларгин 300 МЕ/мл.
Необходимо отметить, что два описанных исследования имели некоторые ограничения. В исследование были включены лица, медицинские карты которых были доступны на момент исследования для заполнения on-line-опросников; таким образом, полученные данные не могут быть экстраполированы на все население (в частности, США) с СД2, получающее гларгин 300 МЕ/мл или гларгин 100 МЕ/мл.
В дополнение: на основании имеющихся данных не представлялось возможным проанализировать влияние сопутствующей медикаментозной терапии в связи с временными ограничениями (только небольшая часть пациентов имела достаточно продолжительный период наблюдения). Эта информация может быть получена и проанализирована в последующих исследованиях, когда применение гларгина 300 МЕ/мл станет более распространенным.
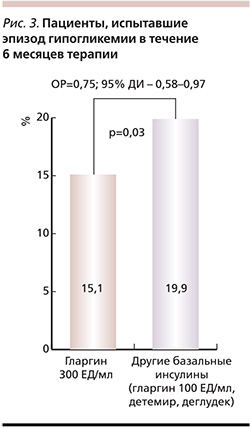 Риск гипогликемических событий после перевода на гларгин 300 МЕ/мл по сравнению с другими базальными инсулинами (исследование DELIVER2)
Риск гипогликемических событий после перевода на гларгин 300 МЕ/мл по сравнению с другими базальными инсулинами (исследование DELIVER2)
В исследовании DELIVER2 были проанализированы данные более 5000 пациентов, полученные из электронных медицинских записей в США.
F.L. Zhou и соавт. [11] провели ретроспективную оценку клинических исходов в РКП у пациентов с СД2, получавших базальный инсулин (гларгин 100 МЕ/мл или детемир) и переведенных на гларгин 300 МЕ/мл и другие базальные инсулины (гларгин 100 МЕ/мл, детемир, деглудек). Данные были получены из базы реальных электронных медицинских записей Predictive Health Intelligence Environment, которая представляет собой 26 интегрированных сетей медицинских услуг. Были включены данные пациентов с СД2, получавших базальный инсулин в течение как минимум 12 месяцев до включения в исследование и в течение полугода периода наблюдения. Анализ был проведен на стандартизованных равных по количеству группах пациентов: по 947 участников в группу гларгина 300 МЕ/мл и в группу других базальных инсулинов. Точками оценки результатов служили динамика уровня HbA1c, измеренного менее чем за 6 месяцев до перевода на другой инсулин и более чем через 90 дней после этого; число пациентов, достигших целевого уровня HbA1c <7 и <8%; частота гипогликемических событий. Исходный средний уровень HbA1c составил 8,89 и 8,92% у пациентов группы гларгин 300 МЕ/мл и других базальных инсулинов соответственно. Через 6 месяцев после перехода на новую терапию было отмечено статистически значимое снижение уровня HbA1c до 8,42 и 8,50% в группах гларгина 300 МЕ/мл и других базальных инсулинов соответственно (p<0,0001 в обоих случаях по сравнению с исходным). В обеих когортах снижение уровня HbA1c было сопоставимым: -0,48% для гларгина 300 МЕ/мл и -0,41% для других базальных инсулинов; p=0,44. Также было сопоставимым число пациентов в группах гларгина 300 МЕ/мл и других базальных инсулинов, достигших через 6 месяцев уровня HbA1c <7,0% (16,9 и 18,7% соответственно; p=0,35) и <8,0% (45 и 42% соответственно; p=0,31).
Вместе с тем в течение 6-месячного периода наблюдения гипогликемии зарегистрированы у существенно меньшего числа участников исследования в группе гларгина 300 МЕ/мл, нежели в группе других базальных инсулинов (15,1 и 19,9% соответственно; p=0,03; рис. 3). Терапия гларгином 300 МЕ/мл по сравнению с другими базальными инсулинами была ассоциирована с более низкой частотой случаев гипогликемии как через 3, так и через 6 месяцев (в последнем случае разница составила 2,67 события/100 пациенто-месяцев; p=0,001), а также с существенно более низкой частотой гипогликемий, требующих госпитализации или неотложной помощи.
Таким образом, в условиях РКП перевод пациентов на гларгин 300 МЕ/мл связан со значимо меньшим риском гипогликемий, чем назначение других базальных инсулинов.
Результаты перевода пожилых пациентов на инсулин гларгин 300 МЕ/мл по сравнению с переводом на другие базальные инсулины (исследование DELIVER3)
С учетом высокого риска развития неврологических нарушений на фоне критического снижения уровня гликемии у пожилых лиц очень важно в этой группе пациентов наряду со стремлением к достижению целевых значений показателей гликемии минимизировать риск гипогликемических событий.
В серии клинических испытаний EDITION продемонстрировано более выраженное снижение риска гипогликемии на фоне применения гларгина 300 МЕ/мл, чем при использовании гларгина 100 МЕ/мл. Помимо этого в исследовании DELIVER2 показано, что и в условиях РКП при переводе взрослых пациентов на гларгин 300 МЕ/мл наблюдалось меньше гликемий, чем при переводе на другие базальные инсулины [11]. Ретроспективное исследование DELIVER3 преследовало цель оценить эффективность и безопасность (в частности, гликемический контроль и риск гипогликемий) гларгина 300 МЕ/мл по сравнению с другими базальными инсулинами при применении у пожилых пациентов (≥65 лет) с СД2 в РКП [12].
Данные были получены тем же способом, что и в упомянутом ранее исследовании DELIVER2: при помощи базы данных Predictive Health Intelligence Environment. Были включены пациенты с СД2 в возрасте ≥65 лет, переведенные на терапию гларгином 300 МЕ/мл или другими базальными инсулинами (гларгин 100 МЕ/мл, детемир, деглудек). В течение периода наблюдения оценивались уровень HbA1c, частота гипогликемических событий, достижение целевого уровня HbA1c <7 и <8% за 6 месяцев.
Число пациентов, включенных в исследование, составило 468 в группе гларгин 300 МЕ/мл и 1142 – в группе других базальных инсулинов. Средний возраст участников в указанных группах составил 71,8±5,3 и 73,1±6,4 года соответственно; средний уровень исходного HbA1c – 8,52±1,52 и 8,34±1,78% соответственно (p=0,04).
В течение периода наблюдения разницы в динамике HbA1c между двумя группами отмечено не было (-0,09%; p=0,24). Кроме того, сопоставимое число пациентов в обеих группах достигло целевого значения HbA1c <7% (отношение шансов [ОШ] – 0,798, 95% ДИ – 0,581–1,098; p=0,166) и <8% (ОШ – 0,967, 95% ДИ – 0,749–1,248; p=0,797).
У пациентов группы гларгин 300 МЕ/мл гипогликемия встречалась на 57% реже, чем в группе других базальных инсулинов (ОШ – 0,432, 95% ДИ – 0,307–0,607; p<0,0001). Были выявлены факторы, существенно влияющие на частоту гипогликемий: исходно высокая частота гипогликемии, более старший возраст, женский пол и др. После повторного анализа с учетом этих факторов установлено, что пациенты, получавшие гларгин 300 МЕ/мл, на 47,9% реже сталкивались с гипогликемиями, чем пациенты, получавшие другие базальные инсулины (5,37 и 10,31 случая/100 пациенто-месяцев; разница – -4,94 случая/100 пациенто-месяцев; p=0,0002).
Таким образом, перевод пожилых людей на гларгин 300 МЕ/мл ассоциирован с меньшим риском гипогликемических событий по сравнению с переводом на другие базальные инсулины. В отношении гликемического контроля эффекты гларгина 300 МЕ/мл и других базальных инсулинов были сопоставимыми.
Заключение
Как видно из полученных результатов, в исследованиях РКП, так же как и в исследованиях EDITION, инсулин гларгин 300 МЕ/мл обладал сопоставимой эффективностью в отношении управления гликемией у взрослых и пожилых пациентов с СД2 с существенно меньшим риском гипогликемических событий по сравнению с гларгином 100 МЕ/мл и группой пациентов, получавших другие базальные инсулины. В отличие от трех исследований EDITION, включивших пациентов с СД2, где за период наблюдения в группе гларгина 300 МЕ/мл доза инсулина была достоверно выше по сравнению с дозой инсулина гларгин 100 ЕД/мл, в исследованиях РКП показано, что при переводе с других базальных инсулинов на инсулин гларгин 300 МЕ/мл в рутинной практике разницы в суточной дозе инсулина не было. Помимо этого в одном из исследований была продемонстрирована возможность уменьшения количества инъекций до 1 раза в сутки у пациентов, ранее получавших базальный аналог дважды в сутки.
Исходя из представленных данных, можно прогнозировать потенциальную перспективу улучшения гликемического контроля с меньшим риском гипогликемии на фоне применения гларгина 300 МЕ/мл, что приведет к большей удовлетворенности пациентов и улучшению приверженности лечению. Безусловно, с целью подтверждения полученных данных в ходе осуществленных ретроспективных исследований РКП, которые имели свои ограничения, требуется проведение проспективных крупномасштабных исследований с большим числом участников.


