Учитывая многофакторный патогенез подавляющего большинства дерматозов, их успешное лечение зависит от комплексного применения различных лечебных методов: психотерапии, фармакотерапии, диетотерапии, витамино-, гормоно-, химиотерапии, физических методов лечения, курортного лечения и соблюдения принципов местной терапии воздействия лекарственных форм. Классические терапевтические подходы традиционно подразумевают применение фармакологических препаратов и немедикаментозных методов лечения, направленных на различные факторы патогенеза дерматозов: противовоспалительные, десенсибилизирующие, иммуномодулирующие и т.п. [1]. При этом большое значение придается коррекции сосудистых и микроциркуляторных нарушений кожи.
Микроциркуляция – одно из ключевых условий поддержания нормального обмена веществ в организме. Структурные изменения сосудов кожи и их функциональное состояние оказывают влияние на протекание воспалительных и дистрофических процессов, а также на поддержание тургора и эластичности кожи, качество репарации тканей при повреждении. Для коррекции микроциркуляции наряду с наружными средствами целесообразно и патогенетически обосновано использовать различные группы биологически активных веществ, действующих на реологические свойства крови и состояние сосудов микроциркуляторного русла изнутри [2]. Поэтому средства коррекции сосудистых изменений традиционно входят в комплексное лечение дерматозов различной этиологии – генетически обусловленной, гормональной, нервно-аллергической и т.п. [3–6]. Однако для реализации персонализированного подхода к лечению, правильного выбора ангиотропных препаратов или физиотерапии и для минимизации риска полипрагмазии следует адекватно оценивать степень сосудистых нарушений в коже больного дерматозом. Метод исследования при этом должен быть удобным для применения в амбулаторной практике, информативным и высокочувствительным, давать возможность фиксировать самые ранние признаки патологии микроциркуляторного русла. В качестве такового используется иммунологический метод определения сывороточных уровней аутоантител (ААТ) – маркеров состояния естественного аутоиммунитета.
Данный метод исследования активно применяется в настоящее время для ранней диагностики различной органной патологии. Теоретическим обоснованием этой возможности является представление об исключительно важной роли иммунной системы в поддержании общего метаболического гомеостаза, причем защита от инфекций является лишь одним из частных проявлений этой глобальной функции. Эта теория более 100 лет назад была предложена И.И. Мечниковым [7] и получила развитие в исследованиях конца 1990-х – начале 2000-х гг. [8–12]. Антитела (АТ) являются высокоспецифичными продуктами клеток иммунной системы. На долю иммуноглобулинов типа G (IgG) приходится более 70% всех сывороточных иммуноглобулинов, и не менее 20–30% синтезируемых ежедневно de novo составляют естественные ААТ, т.е., АТ, способные специфически взаимодействовать с антигенами (АГ) собственных клеток организма. Значительную биологическую активность этих ААТ обеспечивает их высокая пермеабильность из сыворотки крови в любые компартменты клеток, органов и тканей, в т.ч. отделенные от общего кровотока гистогематическими барьерами. Этот факт лежит в основе развития ряда т.н. аутоиммунных патологий. Сывороточное содержание ААТ одной и той же конкретной антигенной специфичности является примерно одинаковым у здоровых людей и заметно меняется при развитии болезни. Изменения сывороточных уровней ААТ начинаются задолго до клинической манифестации, что позволяет использовать метод определения сывороточных уровней ААТ в диагностических и прогностических целях [13].
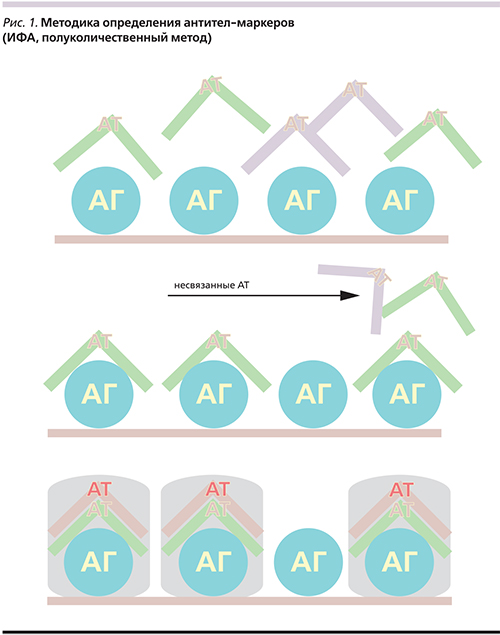
Принцип метода определения АТ – маркеров естественного аутоиммунитета в сыворотке крови с помощью иммуноферментного анализа (ИФА), состоит в следующем: к антигенам различной специфичности, фиксированным в лунках планшета, добавляется сыворотка крови больного и контрольная сыворотка с известным содержанием АТ; часть АТ из сыворотки больного связывается с АГ, не связавшиеся АТ отмываются; затем добавляется специальный раствор, окрашивающий образовавшиеся комплексы АГ–АТ и по интенсивности окраски, оцениваемой фотометрически (оптической плотности растворов), рассчитывается содержание АТ в относительных единицах (рис. 1). Результаты в исследованных группах пациентов с дерматозами сравнивались с нормативными значениями показателей в группе здоровых лиц (n=135). Нормальные значения показателей располагались в диапазоне от +20 до -30 отн. ед.
Материал и методы
Проведено обследование 143 больных различными дерматозами: 36 – ангиитами (васкулитами) кожи, 32 – ограниченной склеродермией, 37 – красным плоским лишаем (КПЛ) и 38 – псориазом. Целью исследования была оценка эффективности одного из физических методов лечения – кислородно-озоновой терапии (озонотерапии). Наряду с оценкой клинического эффекта в качестве критерия эффективности терапии применялось определение динамики различных иммунологических показателей, в т.ч. сывороточных уровней некоторых ААТ. Определение уровня АТ-маркеров в сыворотке крови проводилось до начала лечения и через 3–5 дней после окончания озонотерапии методом ИФА. В работе использовались наборы для определения антител МИЦ «Иммункулус» (Москва).

При обследовании у пациентов определяли содержание:
- ААТ, отражающих наличие признаков системного воспалительного процесса (ААТ к двуспиральной, нативной ДНК; ААТ к β-2-гликопротеину; ААТ к β-2-гликопротеин-связывающим АТ («антитела к антителам»); ААТ к Fc-фрагменту молекул иммуноглобулинов (Fc-Ig) – т.н. ревматоидный фактор (РФ); ААТ к интерферону-γ (АТ к ИФН) и к его рецепторам (АТ к р-рам ИФН);
- ААТ, определяющих состояние соединительной ткани (ААТ к коллагену; ААТ к фибриллярному белку миозину);
- ААТ, характеризующих наличие сосудистых изменений:
- ААТ к цитоплазматическому антигену ANCA, экспрессируемому эндотелием малых сосудов при воспалительных изменениях в их стенках, т.е. при васкулитах различного генеза;
- ААТ к ряду белков мембран тромбоцитов (АТ к антигенам TrM-001-15, TrM-008-10, TrM-015-12) – повышение их уровней указывает на наличие ангио- и тромбоцитопатии различного генеза, в т.ч. аутоиммунного, а также является признаком начинающегося васкулита;
- ААТ к эндотелиальному ферменту NO-синтаза (АТ к NOs) – белку, участвующему в продукции оксида азота (NO) из L-аргинина и регуляции сосудистого тонуса; рост сывороточного содержания ААТ к NOs типичен для нарушений регуляции сосудистого тонуса.
Результаты исследования
Проведенное исследование параметров естественного аутоиммунитета выявило у большинства (69,2%) обследованных больных различными дерматозами иммунологические проявления активного воспалительного процесса, выразившиеся в существенном повышении сывороточных уровней ААТ.
У пациентов с ангиитами кожи были выявлены ожидаемые признаки аутоиммунного воспаления сосудов (табл. 1).
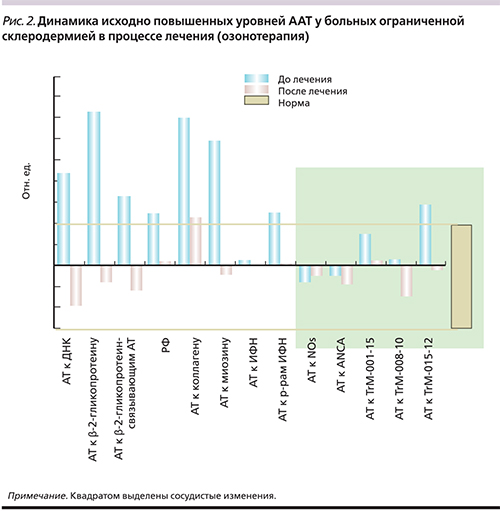
У больных ограниченной склеродермией также были зафиксированы изменения со стороны сосудистых показателей. Однако они были разнонаправленными по сравнению с таковыми у больных ангиитами, а именно: большинство «сосудистых» иммунных показателей у больных склеродермией находились в диапазоне нижней границы нормальных значений, т.е. демонстрировали признаки скорее не активного аутоиммунного воспаления сосудистой стенки, а иммуносупрессии (рис. 2). Выявленные изменения со стороны сосудистой системы у больных ангиитами и склеродермией были ожидаемы и закономерны с учетом современных представлений о патогенезе этих дерматозов.
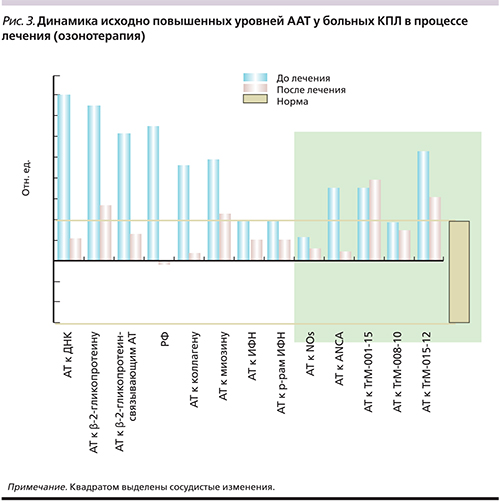
Однако достаточно неожиданной находкой оказалось выявление стойких признаков выраженного аутоиммунного воспаления сосудов малого калибра и тромбопатии у пациентов с КПЛ (табл. 2, рис. 3).
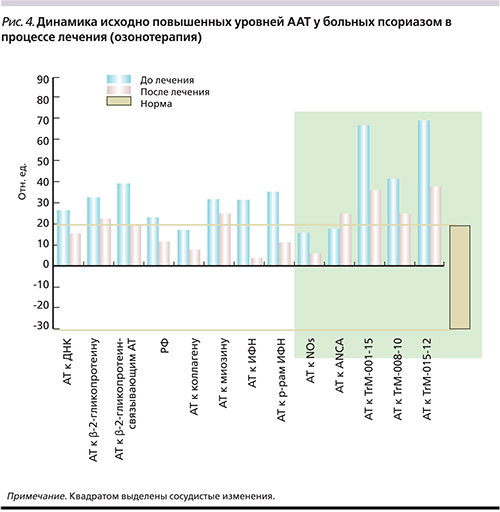
Аналогичные изменения были зафиксированы у пациентов с псориазом (рис. 4), например, уровень ААТ к NO-синтазе изначально составлял 26,4±15,9 отн. ед. по группе, после лечения – 17,2±13,2 (Δ ↓9; p<0,05).
После курса комплексного лечения, включившего кислородно-озоновую терапию, обладавшую выраженным ангиотропным действием и способностью повышать эффективность микроциркуляции [6, 14], у больных ангиитами кожи и ограниченной склеродермией была отмечена нормализация большинства разнонаправленно измененных иммунных показателей (табл. 1, рис. 2), отражающих сосудистые изменения. Исходно повышенные иммунные показатели достоверно снижались или демонстрировали тенденцию к снижению, при этом исходно нормальные показатели после лечения не претерпели существенных изменений.

Однако у обследованных больных КПЛ и псориазом выявленные в процессе исследования стойкие признаки ангио- и тромбопатии сохранялись и после курса кислородно-озоновой терапии (рис. 3, 4).
Обсуждение
Выявленные у пациентов с КПЛ и псориазом изменения сывороточных уровней ААТ, в т.ч. ААТ, характеризующих сосудистые изменения, вероятно, оказались следствием ухудшения клиренса соответствующих органов от продуктов естественного катаболизма. Стойкие признаки ангио- и тромбопатии сохранялись у этих больных и после курса кислородно-озоновой терапии. Кислородно-озоновая терапия у пациентов с КПЛ и псориазом не оказала заметного влияния на сывороточные уровни «сосудистых» аутоантител (ААТ к NO-синтазе, ААТ к антигенам эндотелия сосудов и ААТ к белкам мембран тромбоцитов), что указывает на неполную компенсацию признаков аутоиммунной ангио- и тромбоцитопатии и на целесообразность включения в комплексное лечение данных дерматозов ангиотропных препаратов, в т.ч. дезагрегантов и антикоагулянтов. Традиционные взгляды на значимые факторы в патогенезе КПЛ и псориаза, признавая наличие микроциркуляторных расстройств кожи, тем не менее не придают им достаточного значения. Поэтому применяемые наиболее часто в повседневной клинической практике схемы лечения этих дерматозов, состоящие из иммуносупрессивных и противовоспалительных средств системного и местного применения, как правило, не содержат сосудистых препаратов [15, 16]. Не в последнюю очередь это связано с опасностью «перегрузить» системное медикаментозное лечение дерматозов и спровоцировать вследствие полипрагмазии развитие аллергических реакций и обострения кожного процесса. Однако микроциркуляторные расстройства кожи у ряда больных, особенно с длительно протекающим кожным заболеванием, могут носить достаточно выраженный характер, что, безусловно, будет ослаблять лечебное действие медикаментозных средств, особенно наружного применения, и потребует включения в комплексное лечение соответствующих сосудистых препаратов.
С учетом полученных результатов исследования при выявлении соответствующих нарушений в комплексное лечение больных КПЛ и псориазом целесообразно рекомендовать включение ангиопротекторов – лекарственных средств, укрепляющих стенки сосудов и повышающих их эластичность (витамины С, Р, Е), и венотоников, содержащих диосмин и/или гесперидин, троксерутин и биофлавоноиды рутозид, эскулин и дигидроэргокристин. Большинство сосудоукрепляющих препаратов с венотоническим эффектом, повышающих напряжение стенок венозных сосудов путем сокращения мышечных элементов, содержащихся в средней оболочке сосуда, обладает также противовоспалительным, капилляропротективным и противоотечным действиями, т.е. способностью снижать проницаемость капиллярных стенок, препятствуя таким образом проникновению плазмы крови в окружающие ткани и образованию отеков, что дополнительно будет способствовать получению положительного терапевтического результата.
В тех же целях в ряде случаев могут быть использованы препараты растительного происхождения, содержащие эсцин или экстракт конского каштана, тиамин, экстракт донника или экстракт красных виноградных листьев [19, 20].
Ценность метода контроля сывороточных уровней ААТ заключается в его чувствительности, обеспечивающей возможность ранней диагностики различной органной, в т.ч. сосудистой, патологии, а также возможность объективного динамического контроля эффективности проводимого лечения. В случае если выявленные у некоторых больных КПЛ и псориазом с помощью данного метода изменения значительно отличаются от нормальных значений и носят стабильный характер, т.е. не корректируются «мягкими» (наружными или физиотерапевтическими) методами сосудистой коррекции, данным пациентам следует рекомендовать более целенаправленную и углубленную диагностику состояния сосудов микроциркуляторного русла кожи и эффективности их функционирования с применением ультразвуковых и лазерных допплеровских методов исследования. Состояние микроциркуляции также может быть изучено на системном и локальном уровнях, например с помощью микроскопии бульбарной конъюнктивы и капилляроскопии ногтевого ложа, после чего будет определено преобладание того или иного вида микроциркуляторных изменений (системного или периферического) и назначено соответствующее лечение. В случае обнаружения при углубленном исследовании сосудов таких изменений, как микроаневризмы, микротромбозы, образование «монетных столбиков», сладж-синдром, целесообразно рассмотреть возможность включения в комплексное лечение также антиагрегантов – препаратов, препятствующих тромбообразованию и адгезии клеточных элементов крови на интиме микрососудов [21]. С этой целью можно рекомендовать прием малых доз препаратов ацетилсалициловой кислоты, получивший широкое распространение в амбулаторной практике при различных ангиопатиях и с профилактическими целями. Для соматически сохранных пациентов с дерматозами, у которых выявлена патология только микрососудов кожи, может оказаться полезным препарат пентоксифиллин, в котором антиагрегационный эффект сочетается со спазмолитическим, но при этом не влияет на частоту сердечных сокращений. Весьма полезным для коррекции и профилактики нарушений микроциркуляции любого типа может оказаться применение в составе комплексного лечения препарата Курантил на основе антиагреганта и вазодилататора дипиридамола. Преимуществом данного препарата является хорошая переносимость, отсутствие в списке противопоказаний беременности и грудного вскармливания, а также сопутствующий иммуномодулирующий эффект за счет стимуляции выработки интерферона.
Выводы
Выявленные изменения уровней специфических ААТ к сосудистым аутоантигенам у больных КПЛ и псориазом, устойчивые к проводимой ангиотропной физиотерапии, очевидно, отражают наличие стойких признаков патологии сосудов и тромбопатии. Следовательно, учитывая выявленные признаки аутоиммунного поражения сосудов, включение в комплексное лечение данных дерматозов медикаментозных препаратов, обладающих ангиопротекторным, антиагрегантным и вазодилатирующим действиями, имеет существенное значение для достижения терапевтического эффекта.
Изменение показателей аутоиммунитета является одним из наиболее тонких стигматов раннего поражения органов и систем. Динамика сывороточных уровней ААТ к тканевым аутоантигенам может служить маркером патологии сосудов кожи у больных различными дерматозами и может быть использована для определения ранних изменений сосудистого русла при формировании комплексного персонализированного лечения, а также служить показателем его эффективности.
Дальнейшими направлениями развития темы сосудистых и микроциркуляторных нарушений у больных хроническими воспалительными дерматозами могут быть разработка диагностических методов, определяющих вид и степень тяжести сосудистой патологии, а также определение оптимальных терапевтических комбинаций для ее коррекции.


