Внастоящее время проблема аллергии чрезвычайно актуальна во всем мире: до 40% населения в целом и 10–12% детской популяции страдают различными аллергическими заболеваниями [1, 2]. Эпидемиологические исследования последних лет подтверждают высокую распространенность как аллергического ринита (АР), так и бронхиальной астмы – БА [3, 15]. АР – представляет собой широко распространенное заболевание, нередко начинающееся в детском возрасте. Эпидемиологическое многоцентровое исследование по программе ISAAC (International Study of Asthma and Allergy in Childhood), охватившее более 1 млн детей 6–14 лет в 103 странах, показало, что частота симптомов АР варьируется от 0,8 до 39,7%. Распространенность АР в различных регионах России колеблется от 12 до 24% [4, 5].
Слизистая оболочка носа подвергается воздействию самых разнообразных факторов внешней среды. В развитии местных клинических проявлений со стороны слизистой оболочки носа принимают участие все интегральные системы организма (иммунная, нервная, эндокринная и др.), которые являются неотъемлемой частью врожденного защитного механизма. Выделяют сезонный АР, который связан с воздействием основных групп аллергенов (пыльцы растений и спор плесневых грибов), и интенсивность симптомов зависит от концентрации пыльцы в воздухе. Круглогодичный АР характеризуется периодической или постоянной симптоматикой без выраженных сезонных колебаний на протяжении всего года. Проявления АР могут наблюдаться с первых лет жизни [18], однако не всегда диагностируются.
У 87% пациентов отмечается сочетание БА с АР [6]. У 64% пациентов АР предшествовал БА или развивался одновременно с БА у 70% пациентов всех возрастных групп [7, 17]. У 68% детей с АР выявляется гиперреактивность бронхов, что еще раз подчеркивает их тесную взаимосвязь. Отек слизистой оболочки при АР снижает качество жизни, нарушает дыхательную, кондиционирующую и защитную функции носа. Следствием отека соустий околоносовых пазух и слуховой трубы является предрасположенность к возникновению синуситов и отитов [8].
Ключевым звеном патогенеза АР считается генетически детерминированный повышенный синтез иммуноглобулина Е (IgЕ). В последние годы наблюдается активный интерес ученых к эпителиальным клеткам, являющимся механическим и иммунологическим барьером для окружающих факторов. Эпителиальные клетки представляют не только барьер первой линии защиты и экспрессии распознающих рецепторов, но и стимулируют врожденные иммунные клетки к продукции медиаторов аллергического воспаления [9].
Аллергические заболевания сходны друг с другом в том, что слизистые барьеры и кожа отвечают Т2-клеточно-опосредованным иммунитетом. При попадании аллергена на слизистую оболочку активируется иммуноклеточный ответ 2-го типа с вовлечением большого количества тучных клеток, базофилов, эозинофилов и макрофагов [9]. Под влиянием аллергенов эпителиальные клетки дыхательных путей вырабатывают хемокины и цитокины, которые активируют молодые дендритные и другие клетки врожденного иммунитета, что приводит к эозинофилии верхних дыхательных путей. Синтезируемый интерлейкин-4 (ИЛ-4) способствует образованию В-клетками IgЕ. Т-хелперы 2-го типа синтезируют ИЛ-9, вызывающий активацию тучных клеток и тимусного стромального лимфопоэтина. Также Т-хелперы синтезируют амфирегулин (Areg), способствующий регенерации эпителия после повреждений вследствие контакта с аллергеном [10].
Барьер эпителиальных клеток является достаточно непроницаемым из-за образования на поверхности слизи и в результате плотного контакта, а также соединения эпителиальных клеток друг с другом. Однако многие аллергены, вызывающие клеточно-опосредованный иммунный ответ 2-го типа, проходят сквозь эпителиальный барьер благодаря выработке протеиназы, которая расщепляет слизь и плотные контакты клеток, например аллерген клеща домашней пыли Dermatophagoides pteronyssinus (Der p1). Инициация клеточно-опосредованного иммунитета 2-го типа в слизистых барьерах является очень сложным процессом, требующим быстрого и четкого ответа многих клеток на иммунные стимулы.
Кроме цитокинов барьерные эпителиальные клетки могут регулировать клеточно-опосредованный иммунитет 2-го типа путем выработки эндогенных молекулярных фрагментов – аларминов – эндогенных активаторов воспаления и врожденного иммунитета, которые регулируют защитные реакции организма [10]. Интенсивность защитных реакций и скорость их развертывания будут определяться силой и продолжительностью действия повреждающего агента. В связи с этим защита эпителиального барьера является важнейшей составляющей в ведении детей с АР, что может предотвращать в дальнейшем развитие аллергических реакций.
Терапия АР является комплексной и в первую очередь предусматривает устранение контакта с аллергенами, использование различных групп лекарственных средств (назальные глюкокортикостероиды, антигистаминные препараты, антагонисты лейкотриеновых рецепторов, кромоны, деконгестанты), а также аллергенспецифической иммунотерапии.
В сезон цветения для снижения концентрации аллергенов и их контакта со слизистыми оболочками рекомендуется держать закрытыми окна и двери, использовать системы кондиционирования воздуха в помещении, ограничивать время пребывания на улице. На практике основные проблемы заключаются в невозможности полного устранения многих аллергенов (пыльца, домашняя пыль и др.), а также в отсутствии/недостаточной информации о концентрации аллергенов в воздухе [11].
Важно, что медикаментозные средства разных фармакологических групп для терапии АР воздействуют на выраженность воспаления или его симптомы уже после того, как произошел контакт организма с аллергеном и реакция аллергического ответа запущена.
Известно также, что при аллергическом воспалении повышается проницаемость слизистых оболочек к аллергенам, что облегчает формирование аллергии. В связи с этим особую актуальность приобретают методы, снижающие/предупреждающие проницаемость естественных барьеров для аллергенов, что может предупреждать трансбарьерную сенсибилизацию и развитие аллергических проявлений.
Особое внимание барьерным методам необходимо уделять в тех случаях, когда у детей с АР имеются серьезные ограничения к приему фармакологических препаратов, такие как лекарственная аллергия и непереносимость, активные физические нагрузки, занятия спортом, когда ограничен прием гормональных, сосудосуживающих и антигистаминных препаратов.
К барьерным средствам относится назальный спрей Превалин Кидс, который, покрывая слизистую оболочку носа, образует защитный слой, что препятствует контакту с аллергенами, проникновению аллергенов, восстанавливает мукоцилиарный клиренс, нормализует функции реснитчатого эпителия [12, 16].
В состав препарата входит бентонит (голубая глина – природный глинистый материал, обладающий свойством разбухать в присутствии воды с образованием плотного геля), кунжутное масло (обладает противовоспалительным и регенерирующим действиями), мятное масло – сосудосуживающий компонент. Этот комплекс масел и эмульгаторов, обладает тиксотропными свойствами, т.е. вязкость его может меняться. В стандартных условиях препарат представляет собой гель. После энергичного встряхивания он меняет свое агрегатное состояние, становится жидким и может распыляться на слизистую оболочку носа, где возвращается в свое исходное гелеобразное состояние. Гель формирует в полости носа тончайший барьер, непроницаемый для аллергенов, предупреждает попадание аллергенов в организм и запуск аллергической реакции с выделением медиаторов воспаления [3]. Адсорбированные на геле аллергены естественным путем выводятся из организма с помощью реснитчатого эпителия слизистой оболочки носа.
Материал и методы
На базе амбулаторно-поликлинического отделения УДКБ «Первый МГМУ им. И.М. Сеченова» было проведено открытое наблюдательное исследование безопасности, переносимости, эффективности применения препарата Превалин Кидс в форме спрея для интраназального введения в 1-й группе детей с сезонным и круглогодичным АР легкой и средней степеней тяжести; во 2-ю группу вошли дети, у которых АР легкой и средней тяжести сочетался с БА легкой и средней степенями тяжести (терапия БА в период наблюдения не менялась, дополнительно был назначен Превалин Кидс); в 3-й группе детей с АР Превалин Кидс сочетался с антигистаминными препаратами и ирригационной терапией (натуральная морская вода – Физиомер). В каждую группу вошли по 20 детей в возрасте от 6 до 14 лет (средний возраст – 9,4±2,5 года). Спрей Превалин Кидс назначали детям по 2 распыления до 3 раз в сутки в течение 3 недель. Физиомер – по 1 орошению 3 раза в сутки использовали перед аппликацией Превалина Кидс. Антигистаминные препараты назначали в возрастных дозировках.
Эффективность лечения оценивали по выраженности симптомов в баллах, данным осмотра ЛОР-врача (передняя риноскопия) на 7-й, 14, 21-й дни использования Превалина Кидс и через неделю после окончания курса. Оценивали блокаду носового дыхания, выделения из полости носа и их характер, чихание, зуд в полости носа, зуд глаз, слезотечение: 0 баллов – отсутствие симптомов; 1 балл – симптомы имеются, но не влияют на образ жизни; 2 балла – симптомы оказывают умеренное влияние на обычный образ жизни; 3 балла – симптомы выраженной степени ухудшают состояние и мешают заниматься повседневными делами. Безопасность оценивали по частоте возникновения побочных эффектов на фоне проводимого лечения.
Исследовали функцию внешнего дыхания всех детей по данным компьютерной бронхофонографии (КБФГ), т.к. известно, что АР и БА даже без клинических проявлений могут сопровождаться гиперреактивностью бронхов и обструкцией. КБФГ – метод, основанный на анализе амплитудно-частотных характеристик спектра, возникающих при дыхании. Сканирование респираторного цикла производится в частотном диапазоне от 200 до 12 600 Гц. Выделяют три зоны частотного спектра: 200–1200 (низкочастотный диапазон), >1200–5000 (средние частоты), >5000 (высокочастотный диапазон). С помощью КБФГ оценивается акустический феномен дыхания, связанный с усилением турбулентности воздушных потоков по респираторному тракту, обусловленный бронхиальной обструкцией [13]. Компьютерный комплекс позволяет отображать дыхательный паттерн на экране монитора, сопоставлять полученные у пациентов данные с опорными показателями детей без респираторной патологии. Наличие осцилляций в зоне высоких частот (≥5 кГц) коррелирует с обструкцией дыхательных путей [14]. Оценивается акустический компонент работы дыхания (АКРД) в мкДж. Метод КБФГ позволяет расширить функциональную оценку проходимости верхних и нижних дыхательных путей, получаемую рутинными методами обследования, а также в динамике оценить эффективность проводимой терапии.
Результаты исследования
Из 60 обследуемых детей с АР у 44 (73%) (10 девочек и 34 мальчика) имелся сезонный АР и у 16 (27%) (5 девочек и 11 мальчиков) – круглогодичный АР. Практически у всех пациентов была отягощенная наследственность по аллергическим заболеваниям (82%).
У 25 (42%) детей уже с первых месяцев жизни отмечались аллергические реакции на пищу в виде атопического дерматита, а также аллергической сыпи, отеков Квинке.
Почти у всех детей при аллергологическом обследовании отмечалась сенсибилизация к бытовым, эпидермальным аллергенам, аллергия на пыльцу растений. Аллергический конъюнктивит отмечался у 5 (8,3%) детей. Клинические проявления бронхиальной обструкции в виде непостоянных сухих хрипов отмечались преимущественно в группе детей с АР и БА. Но и у 4 детей без БА также отмечались эпизоды затруднения дыхания и появление сухих хрипов. По данным КБФГ, у детей с АР (в группе 1 и 3) выявлено нарушение бронхиальной проходимости у 67%, у детей с АР и БА (в 2-й группе), несмотря на отсутствие обострения БА, в высокочастотной части спектра выявлялись осцилляции выше опорных показателей у 75%.
Положительный клинический эффект Превалина Кидс получен у 52 (86%) пациентов. Все 52 пациента закончили курс лечения (21 день), отметив значительное клиническое улучшение и снижение выраженности всех симптомов АР.
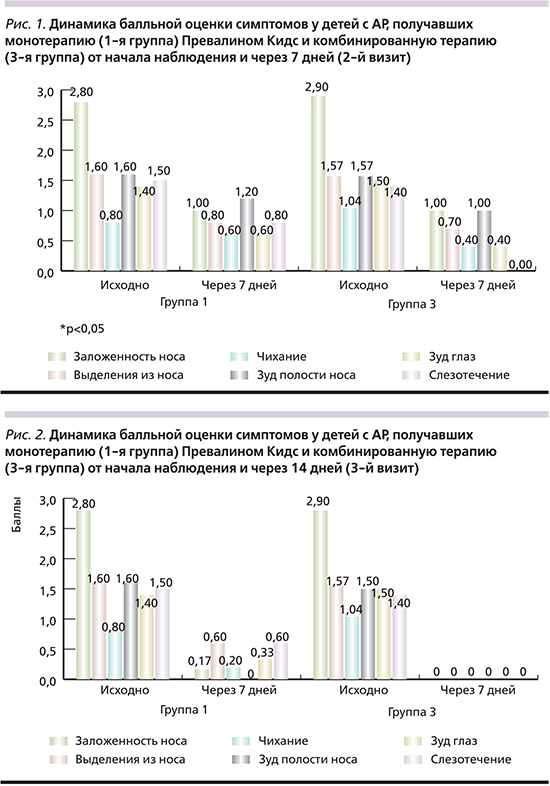
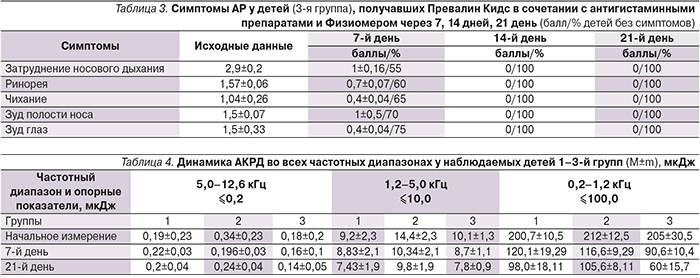
Через 7 дней имело место значительное снижение выраженности симптомов АР во всех трех группах: затруднение носового дыхания достоверно уменьшилось с 2,8±0,49 до 1±0,7 балла в 1-й группе (р<0,05), с 2,83±0,17 до 1,07±0,26 балла во 2-й (р<0,0001), с 2,9±0,2 до 1±0,16 балла в 3-й группе (р<0,05); ринорея – с 1,6±0,51 до 0,8±0,37 у детей 1-й группы (р<0,03), с 1,5±0,56 до 0,9±0,04 (р<0,04) во 2-й; с 1,57±0,06 до 0,7±0,07 в 3-й группе (р<0,02). Также достоверно уменьшилась выраженность чихания, зуд глаз и слезотечение; зуд в полости носа достоверно уменьшился и исчез только в 3-й группе при сочетании Превалина Кидс с АГ-препаратами (табл. 1, 2, 3; рис. 1).
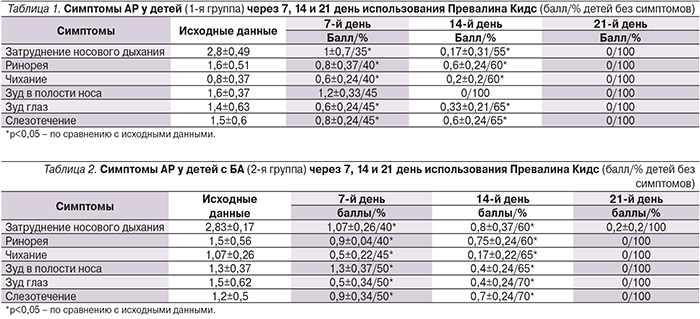
Через 14 дней отмечено существенное достоверное снижение выраженности симптомов во всех трех группах: улучшение носового дыхания до 0,17±0,31, 0,8±0,37 и до 0 баллов в 1-й, 2-й и 3-й группах соответственно (р<0,05); ринорея уменьшилась до 0,6±0,24, 0,75±0,24 и 0 баллов (р<0,05) в 1-й, 2-й и 3-й группах; чихание – до 0,2±0,2, 0,17±0,22, и 0 баллов; слезотечение – до 0,6±0,24, 0,7±0,34, и 0 баллов в 1-й, 2-й и 3-й группах соответственно (табл. 1, 2, 3; рис. 2).
Следует отметить, что в 3-й группе детей с АР, получавших комбинированную терапию, у большинства детей симптомы исчезали уже через 7 дней, что составило 55% детей по сравнению с 35% детей в 1-й группе. Через 2 недели в 3-й группе практически не было симптомов, тогда как при монотерапии симптомы отсутствовали у 55–60% детей.
Таким образом, через 2 недели в группе детей с АР, получавших Превалин Кидс в сочетании с антигистаминными препаратами и Физиомером, симптомы купировались у 95% детей, в 1-й и 2-й группах – у 65% детей.
Через 21 день отмечено исчезновение практически всех симптомов у большинства пациентов с АР и АР и БА. У 3 детей 2-й группы сохранялось небольшое затруднение носового дыхания.
Наблюдение в течение недели после прекращения использования спрея Превалина Кидс показало, что все пациенты чувствовали себя хорошо, симптомы не возобновлялись.
У 8 (15%) детей препарат был отменен. В 1-й группе у 3 пациентов с АР среднетяжелого течения наблюдались побочные эффекты при использовании Превалина Кидс в виде блокады носового дыхания, зуда в полости носа, у 2 пациентов с легким течением АР наблюдалось усиление чихания, во 2-й группе у 2 пациентов отмечено усиление блокады носового дыхания, в 3-й группе у 1 ребенка с АР и среднетяжелой БА препарат также был отменен в связи с появлением кашля. У 3 пациентов отмечены неприятные ощущения, характеризующиеся появлением горького вкуса во рту, не требовавшие отмены препарата.
Таким образом, на фоне приема препарата Превалин Кидс выявлено отчетливое влияние на клинические симптомы у пациентов как с АР, так и при сочетании АР и БА. При его комбинации с антигистаминными препаратами симптомы исчезали значительно быстрее, уже к 14-му дню наблюдения.
В целом к концу 2–3-й недели терапии полностью исчезли такие симптомы, как выделения из носа, чихание, зуд в полости носа, зуд глаз, слезотечение у 82% детей; незначительное затруднение носового дыхания сохранялось только у детей с тяжелым течением АР и среднетяжелым течением БА. У 40% детей симптомы исчезли быстро – в течение первой недели применения Превалина Кидс, и положительный эффект сохранялся при наблюдении в последующие 2–3 недели.
Эффективность лечения подтверждалась объективным осмотром ЛОР- врача и субъективной оценкой самих пациентов. При передней риноскопии у всех 52 детей с положительным эффектом лечения наблюдалось уменьшение или отсутствие отека, водянистых выделений и гиперемии слизистой оболочки носа.
У всех обследуемых пациентов исходно выявлено увеличение АКРД в низкочастотной части спектра, что обусловлено нарушением назальной проходимости, и во 2-й группе детей с АР и БА отмечены усиление АКРД в высокочастотной части спектра до начала применения Превалина Кидс у 75% детей, что может характеризовать наличие бронхиальной гиперерактивности и небольших проявлений бронхиальной обструкции. Уже к 7-му дню наблюдения по мере уменьшения симптомов АР визуальные показатели спектральной плотности воздушного потока, обусловленные факторами, усиливающими турбулентность, снижались до опорных показателей у детей, не имеющих нарушений со стороны респираторного тракта (табл. 4).
Заключение
Таким образом, в настоящем исследовании у 86% больных АР установлена значимая клиническая эффективность и высокая безопасность применения спрея Превалин Кидс качестве как монотерапии, так и в комбинации с антигистаминными препаратами и Физиомером, что характеризется восстановлением носового дыхания, уменьшением отека слизистой оболочки носа, уменьшением слизистого отделяемого из носа, исчезновением таких симптомов, как чихание, зуд в полости носа. Важно, что при использовании данного препарата уменьшаются глазные симптомы аллергии (зуд в глазах и слезотечение) в связи со снижением попадания аллергенов из носа по носослезному каналу.
Предотвращая развитие симптомов АР, Превалин Кидс сохраняет обоняние и свободное дыхание, действуя непосредственно в месте развития аллергической реакции – слизистой оболочке носа. Благодаря отсутствию системного действия он не имеет побочных эффектов и противопоказаний, подходит взрослым и детям с 6 лет, беременным и кормящим женщинам [19], не вызывает сонливости и привыкания, сочетается с любой сопутствующей терапией. Препарат используется при первых симптомах аллергической реакции, а также может применяться для профилактики при ожидаемом контакте с аллергенами. Наилучший результат дает при его использовании до контакта с аллергеном или при появлении первых признаков аллергии (зуд в носу и глазах, чихание). У большинства детей отмечена хорошая переносимость препарата и отсутствие седативного действия [12].
Длительность терапевтического эффекта составляет 4–6 часов, поэтому его нужно применять не реже 2–3 раз в сутки. Если момент первых признаков упущен и клиническая картина АР развилась полностью, Превалин Кидс может сочетаться со стандартным лечением АР, предотвращая дальнейшее попадание аллергена в организм [11]. Препарат можно использовать несколько раз в году в периоды обострения АР по 1,0–1,5 месяца.
Из 8 пациентов, у которых отсутствовал клинический эффект и которые прекратили прием препарата, у 5 при передней риноскопии сохранялись явления аллергического воспаления (отек, гиперемия слизистой оболочки, водянистые выделения из носа); у 3 детей с жалобами на кашель при осмотре отмечались признаки присоединившейся респираторной инфекции. Улучшение назальной проходимости сочеталось с улучшением функции внешнего дыхания, по данным КБФГ.
Эффект определяется созданием барьера, защищающего дыхательные пути от попадания аллергена на слизистую оболочку носа и дальнейшего проникновения аллергена, что предотвращает развитие аллергической реакции, в частности обострение АР. Применение препарата Превалин Кидс в терапии обострений АР, а также в комплексной терапии АР и БА способствует повышению клинического эффекта лечения и улучшению качества жизни пациентов. Полученный опыт и данные литературы позволяют рекомендовать его в качестве препарата выбора в симптоматической терапии АР легкого и среднетяжелого течения у детей.



