Инфекции мочевыводящих путей (ИМП) являются основной причиной экстрагенитальной инфекционной патологии в акушерской практике. По локализации они делятся на инфекции верхних (пиелонефрит, абсцесс и карбункул почек) и нижних отделов мочевых путей (цистит, уретрит, бессимптомная бактериурия). По состоянию мочевыводящих путей и наличию сопутствующих заболеваний ИМП делятся на неосложненные и осложненные. Осложненные инфекции характерны для пациенток с нарушением уродинамики на фоне обструктивных уропатий, нейрогенных нарушений, наличия инородного тела, а также при ряде сопутствующих заболеваний: сахарный диабет, почечная недостаточность, иммуносупрессия и др. Таким образом, ИМП в акушерской практике всегда будут относиться к осложненным инфекциям, т. к. для беременности характерно как нарушение уродинамики, так и транзиторная иммуносупрессия. Распространенность бессимптомной бактериурии в популяции беременных женщин в среднем составляет 6 %. Острый цистит и острый пиелонефрит встречаются несколько реже – в 1,0–2,5 % случаев. В итоге каждая десятая беременная страдает той или иной формой ИМП, что в 3 раза чаще, чем в популяции небеременных женщин. ИМП в свою очередь могут быть причиной ряда серьезных осложнений беременности и родов – это анемия, гипертензия, преждевременные роды, преждевременное излитие околоплодных вод, рождение детей с низкой массой тела (2500). Как следствие – перинатальная смертность среди этого контингента пациенток возрастает в 3 раза.
Этиология и патогенез
Патогенез ИМП у беременных обусловлен сочетанием сразу четырех факторов:
- механическое сдавление мочевых путей за счет увеличивающейся матки;
- снижение тонуса мочеточников и мочевого пузыря вследствие высокого уровня прогестерона;
- увеличение рН мочи, глюкозурия;
- иммуносупрессия.
Этиология ИМП определяется их близостью к одной из основных экониш организма человека – желудочно-кишечному тракту. Поэтому наиболее распространенным уропатогеном для беременных остается Esherichia coli – 80 %. Гораздо реже определяются другие представители семейства Enterobacteriaceae и грамположительная микрофлора:
- E. coli (80 %);
- Klebsiella spp., Proteus spp., Enterobacter spp. (5–10 %);
- Staphylococcus epidermidis, Staphy-lococcus saprophyticus, Enterococcus faecalis, Streptococcus (gr. B) (10–15 %).
 При осложненных и нозокомиальных ИМП частота выделения E. coli несколько снижается и чаще встречаются другие возбудители: Pseudomonas spp., Enterobacter spp., Klebsiella, Proteus, Candida spp. (преимущественно C. albicans).
При осложненных и нозокомиальных ИМП частота выделения E. coli несколько снижается и чаще встречаются другие возбудители: Pseudomonas spp., Enterobacter spp., Klebsiella, Proteus, Candida spp. (преимущественно C. albicans).
Нередко в моче определяются такие микроорганизмы, как Gardnerella vaginalis, Mycoplasma hominis и Ureaplasma urealyticum, однако сколько-нибудь существенного значения в развитии патологического процесса они, очевидно, не имеют и отражают лишь высокий уровень контаминации нижней трети уретры влагалищной микрофлорой.
Диагностика и скрининг
Бессимптомная бактериурия:
- бактериурия < 105 КОЕ/мл в двух последовательных пробах мочи, взятых с интервалом минимум 24 часа (3–7 дней) при обнаружении одного и того же вида бактерий или < 108 КОЕ/мл в одной пробе;
- отсутствие клинических признаков инфекции;
- пиурия +/-.
Острый цистит:
- клиническая симптоматика (дизурия, частые императивные позывы на мочеиспускание, боль над лобком;
- пиурия (< 10 лейкоцитов в 1 мкл нецентрифугированной мочи);
- бактериурия: < 102 КОЕ/мл (для колиформных микроорганизмов), < 105 КОЕ/мл (для других уропатогенов).
Если при описанной клинической картине острого цистита нет бактериологического подтверждения, то речь идет об остром уретральном синдроме. В большинстве случаев это будет хламидийный уретрит. Таким образом, обнаружение бактериурии является ключевым моментом в диагностике острого цистита.
Острый пиелонефрит:
- клиническая симптоматика (лихорадка, озноб, тошнота, рвота, боли в поясничной области, дизурия);
- пиурия (< 10 лейкоцитов в 1 мкл нецентрифугированной мочи);
- бактериурия < 104 КОЕ/мл.
В 75 % случаев при остром пиелонефрите поражается правая почка, в 10–15 % левая, и еще в 10–15 % процесс носит двусторонний характер.
С учетом широкой распространенности ИМП в акушерской практике и высокого риска серьезных осложнений всем беременным должно производиться бактериологическое исследование мочи при первом же посещении врача. Некоторые эксперты, однако, рекомендуют это делать в 16–7 недель беременности. В случае подтверждения стерильности мочи в отсутствие факторов риска и симптоматики ИМП дальнейших культуральных исследований не требуется, т. к. только у 1–2 % пациенток развивается клиника ИМП после первого отрицательного результата.
Лечение
Ряд лекарственных препаратов лечения ИМП не рекомендуется применять при беременности в связи с высоким риском для плода и новорожденного:
- сульфаниламиды (ядерная желтуха, гемолитическая анемия у новорожденных);
- триметоприм – антиметаболит фолиевой кислоты (нарушения иннервации);
- нитрофураны – дефицит глюкозо-6-фосфатдегидрогеназы (гемолитическая анемия, III триместр беременности);
- аминогликозиды (нефротоксическое, ототоксическое действие);
- хинолоны/фторхинолоны (артропатии);
- нитроксолин (периферические полиневриты, атрофия зрительного нерва).
На практике при лечении ИМП у беременных по рекомендации FDA (Управление по контролю качества пищевых продуктов и лекарственных препаратов, США) чаще всего используют три группы препаратов: пенициллины, цефалоспорины и фосфомицин трометамол. В подавляющем большинстве случаев этого вполне достаточно для проведения адекватной химиотерапии.
Антибактериальная терапия инфекций нижних отделов мочевыводящих путей у беременных (бессимптомная бактериурия и острый цистит) проводится перорально в амбулаторных условиях.
Рекомендуемые схемы:
- Фосфомицин трометамол 3 г однократно.
- Цефуроксим аксетил 250–500 мг 2–3 раза в сутки, 7 дней, или цефтибутен 400 мг 1 раз в сутки, 7 дней, или цефиксим 400 мг 1 раз в сутки, 7 дней.
- Амоксициллин/клавуланат 625 мг 3 раза в сутки или 1000 мг 2 раза в сутки, 7 дней.
- Альтернативная схема: нитрофурантоин 100 мг 4 раза в сутки, 7 дней.
 В случае отсутствия эффекта от двух последовательных курсов этиотропного антибактериального лечения показана супрессивная терапия вплоть до родоразрешения + 2 недели после родов. При этом должны быть исключены осложненные формы ИМП, прежде всего обструктивные уропатии.
В случае отсутствия эффекта от двух последовательных курсов этиотропного антибактериального лечения показана супрессивная терапия вплоть до родоразрешения + 2 недели после родов. При этом должны быть исключены осложненные формы ИМП, прежде всего обструктивные уропатии.
Супрессивная терапия: фосфомицин трометамол 3 г каждые 10 дней, нитрофурантоин 50–100 мг 1 раз в сутки.
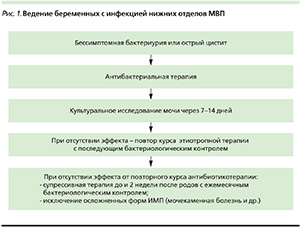
Алгоритм ведения беременных с инфекцией нижних отделов мочевыводящих путей представлен на рис. 1.
Антибиотикотерапия беременных с острым пиелонефритом должна проводиться в госпитальных условиях и начинаться с парентерального введения препаратов.
Рекомендуемые схемы:
- Амоксициллин/клавуланат 1,2 г в/в 3–4 раза в сутки.
- Цефуроксим 0,75–1,5 г в/в 3 раза в сутки. Цефтриаксон 1–2 г в/в 1 раз в сутки.
- Цефотаксим 1–2 г в/в 3–4 раза в сутки.
Длительность терапии – не менее 14 дней (5 дней парентеральное введение препаратов, далее per os).
В случае отсутствия признаков клинического улучшения в течение 48–72 часов от начала терапии требуется уточнение диагноза с целью исключения обструкции мочевых путей (возможна необходимость катетеризации мочеточников или оперативного лечения мочекаменной болезни). Рецидивы острого пиелонефрита среди беременных встречаются достаточно часто: 10–30 %.
Поэтому в качестве профилактики возможно применение либо супрессивной терапии (см. выше), либо культурального исследования мочи каждые 2 недели вплоть до родов.
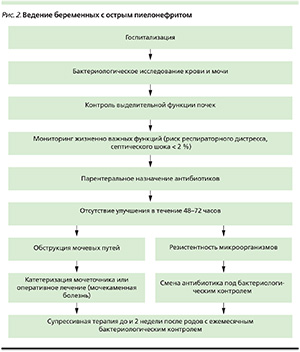
Алгоритм ведения беременных с острым пиелонефритом представлен на рис. 2.
Особенно следует подчеркнуть нецелесообразность использования в терапии ИМП незащищенных пенициллинов (ампициллин, амоксициллин), поскольку резистентность к этим антибиотикам уропатогенных штаммов E. coli превышает 30 %.
К сожалению, подобная практика весьма распространена в России вплоть до настоящего времени.



