Обоснование
Пациенты с сахарным диабетом 2 типа (СД2) составляют основную группу наблюдения у врача-эндокринолога амбулаторного звена. Доля пациентов с этим диагнозом, наблюдающихся у меня в поликлинике по профилю эндокринология, составляет более 90%. Заболеваемость СД среди населения растет, несмотря на меры, принимаемые сотрудниками системы здравоохранения по профилактике заболевания. Его распространенность в мире за последние 10 лет увеличилась не менее чем на 30% [1, 2]. Полагают, что доля лиц с СД среди взрослых в общей популяции составляет около 9,5%. В 2020 г. в США эта цифра достигала 14%, у 30,7% из них СД еще не был диагностирован, а в некоторых странах Южной Азии – даже 30% [2]. В Российской Федерации число лиц с установленным диагнозом СД составляет более 5 млн (3,1% населения). Считается, что примерно у такого же (если не более значительного) числа больных СД остается недиагностированным [1, 3].
Нарастание дисфункции β-клеток на фоне инсулинорезистентности или аутоиммунный процесс в островках Лангерганса приводят к инсулинопении и прогрессированию гипергликемии. Для контроля гликемии отечественные и международные эксперты рекомендуют оценку уровней гликированного гемоглобина (HbA1с) не реже 2 раз в год, а если целевые уровни не достигнуты или лечение было изменено, то 4 раза в год [1, 2]. Благодаря возможности регулярно контролировать анализы пациентов в условиях поликлиники, коррекция терапии происходит с необходимой регулярностью для предотвращения стойкой декомпенсации углеводного обмена. Интенсификация сахароснижающей терапии инсулином имеет определенные риски, ассоциированные, в первую очередь, с развитием гипогликемических состояний. Для меня, практикующего эндокринолога, важна минимизация рисков гипогликемии у пациентов. Инсулин деглудек полностью отвечает этому требованию, являясь препаратом выбора в моей личной практике. Стоит помнить, что гипогликемии увеличивают риски смерти от сердечно-сосудистых осложнений в 2,5 раза [4].
Клинический пример 1
Пациентка М., 65 лет, была госпитализирована в Клиническую инфекционную больницу им. С.П. Боткина в августе 2017 года с диагнозом «гемолитическая анемия». На фоне терапии дексаметазоном было отмечено повышение уровня глюкозы крови более 20,0 ммоль/л. Находясь в стационаре, эндокринолог поставил диагноз «СД 2 типа (стероид-индуцированный)», с целевым уровнем HbA1с менее 7%. Также выявлено ожирение 2-й степени. За время госпитализации пациентка похудела на 11 кг, достигнув веса 98 кг. После проведенного лечения пациентка была выписана из стационара в октябре 2017 г. с улучшением общего состояния.
Из анамнеза известно, что пациентка в 2001 г. перенесла острую воспалительную демиелинизирующую полирадикулоневропатию или Синдром Гийена–Барре (СГБ). СГБ – это быстро прогрессирующее заболевание, сопровождающееся процессами демиелинизации периферической нервной системы с развитием тетрапареза. Пациентка М. не могла самостоятельно передвигаться, проходила стационарное лечение в МСЧ № 122. В течение года неврологический дефицит практически восстановился, но периодически отмечает слабость в ногах, преимущественно в бедрах, слабость в кистях рук.
Перенесенные заболевания: ветряная оспа (10 лет), гипертоническая болезнь диагностирована в 52 года.
В течение всего периода артериальной гипертензии пациент получает антигипертензивную терапию: эналаприл 10 мг/сут, амлодипин 5 мг/сут. Острых сердечно-сосудистых заболеваний в анамнезе не было. Наследственность по СД не отягощена.
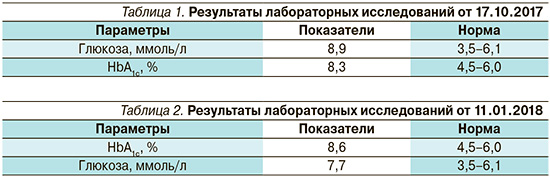
На основании лабораторных обследований (табл. 1) уровень НbА1с составил 8,3%, что превышает целевой уровень на 1,3% и позволяет назначать комбинированную терапию уже на старте лечения [5]. При выписке из стационара было назначено: гликлазид с модифицированным высвобождением 60 мг по 1 таблетке утром и гларгин 100 ЕД/мл 8 ЕД вечером в 20.00. Рекомендовано ведение дневника самоконтроля гликемии, диета – стол 9, контрольная явка через 1 месяц с дневником самоконтроля гликемии, посещение занятий по программе «Школа диабета» на базе поликлиники, посещение Диабетологического центра.
Из-за избыточной массы тела и выраженной слабости пациентка передвигалась с трудом. Одышка и головокружение исключили занятия спортом. Также отсутствие аппетита приводили к нарушениям рекомендаций по питанию.
Обратившись к врачу-эндокринологу в декабре 2017 г., пациентка М. призналась в нерегулярном приеме терапии, отсутствии дневника самоконтроля и несоблюдении диеты. Со слов пациентки М., уровни гликемии натощак составляли от 8 до 13 ммоль/л, в течение дня уровни гликемии не контролировала.
На приеме по глюкометру уровень гликемии составил 9,1 ммоль/л, решено было перевести пациентку на традиционную схему инсулинотерапии, основанную на ежедневном использовании минимального числа инъекций одной и той же дозы инсулина. Был назначен смешанный инсулин лизпро двухфазный 50 в дозировке 15 ЕД утром и 10 ЕД вечером с обязательным соблюдением принципов питания при СД. Пациентка была обучена подсчету хлебных единиц (ХЕ), оговорены варианты составов приемов пищи в течение дня. Было рекомендовано выполнение лабораторных исследований и ведение дневника самоконтроля гликемии в течение 2 недель до следующей явки.
В январе 2018 г. пациентка посетила врача после выполнения назначений. Выполнен лабораторный контроль основных показателей (табл. 2).
Повышение уровня НbА1с до 8,6% свидетельствует о декомпенсации СД. Повышаются риски развития макрососудистых осложнений.
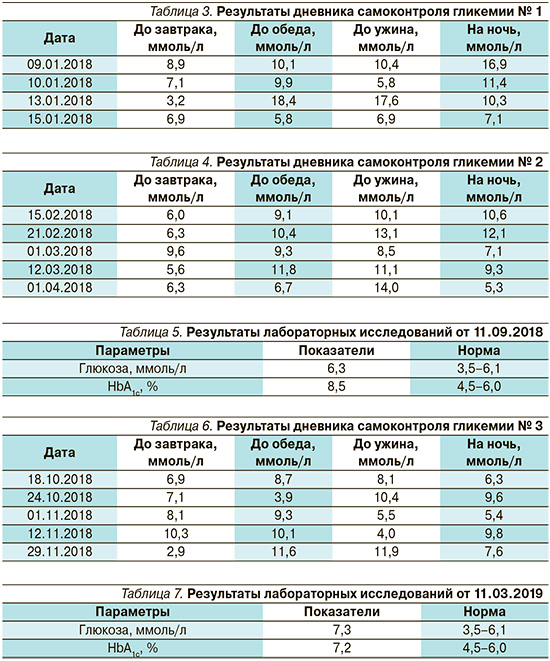
Целевые показатели, рекомендованные врачом, – 5,0–6,5 ммоль/л до еды на основании дневника самоконтроля гликемии не были достигнуты (табл. 3). Пациентка обращает внимание на периодическое головокружение, слабость и апатию. Купирует приступы приемом быстрых углеводов (сладкий чай), уровень гликемии в тот момент не контролирует, списывает состояние на перенесенную гемолитическую анемию. По дневнику самоконтроля гликемии отмечается значительная вариабельность.
Проведена беседа по принципам питания при СД и пользе от него, объяснены перспективы развития хронических осложнений СД. Рекомендовано контролировать уровни гликемии при ухудшении самочувствия.
В начале апреля 2018 г. пациентка была на приеме у врача с результатами дневника самоконтроля гликемии (табл. 4), предъявляла жалобы на периодическую слабость, потемнение в глазах и приступы холодного пота 1 раз в 2–3 недели. В момент ухудшения самочувствия неоднократно измеряла уровень гликемии, который варьировался от 3,0 до 4,0 ммоль/л.
По результатам беседы пациентка М. призналась в самостоятельной коррекции дозировки инсулина перед приемом пищи: при нормальном уровне гликемии (целевом) она сокращала или отменяла инъекцию инсулина, избегая тем самым, на ее взгляд, эпизодов гипогликемии. Типичный страх для пациентов, столкнувшихся с неоднократным гипогликемическим состоянием. Пациентка М. отказывалась соблюдать рекомендации по назначенным дозировкам инсулинотерапии. Была направлена к врачу-психотерапевту на консультацию.
Коррекция и оценка назначенной терапии в сложившихся условиях оказалась невозможной.
В августе 2018 г. пациентка М. посетила врача-эндокринолога, жалоб активно не предъявляла. Гипо-гликемические состояния отрицала. Питание полноценное, старалась придерживаться диеты стол 9, не строго.
По результатам показаний глюкометра пациентки М.: уровни гликемии в течение дня 7,0–8,5 ммоль/л до еды и 10,0–11,9 ммоль/л через 2 часа после еды, что не укладывалось в рекомендованные врачом целевые показатели.
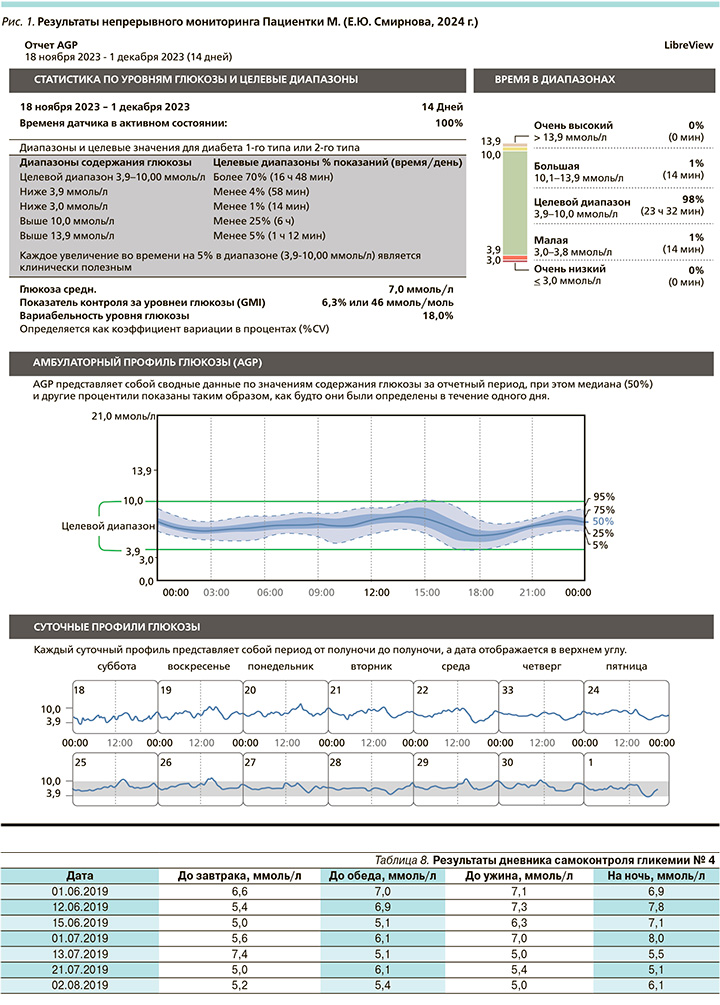
В сентябре 2018 г. выполнен контроль лабораторных анализов (табл. 5).
По данным анализов крови, снижение уровня НbА1с на 0,1% с октября 2018 г. не доказывало эффективности принимаемой терапии, но по результатам измерения уровней гликемии отсутствовала вариабельность. Пациентка М. отмечала улучшение самочувствия.
В очередной раз рекомендовано следить за своим питанием и рационом, соблюдать диету, а также повторно объяснены причины развития гипогликемии. Рекомендовано продолжить ведение дневника самоконтроля гликемии, соблюдение рекомендаций врача и контроль анализов крови в динамике.
Выполнена коррекция терапии: инсулин лизпро двухфазный 50 в дозировке 18 ЕД утром и 12 ЕД вечером.
В декабре 2018 г. пациентка М. на приеме была с дневником самоконтроля гликемии (табл. 6).
По результатам дневника самоконтроля гликемии – регулярные гипогликемические состояния, доставлявшие неудобства и угрожавшие здоровью пациентки. Принято решение об изменении терапии.
Пациентке М. рекомендована терапия: инсулин гларгин 100 ЕД/мл в дозе 16 ЕД в 20.00, вилдаглиптин 50 мг по 1 таблетке утром и вечером, гликлазид 30 мг по 1 таблетке утром.
На фоне терапии в марте 2019 г. пациентка обратилась для контроля лабораторных показателей (табл. 7).
По результатам лабораторных анализов уровень НbА1с значительно снизился и приблизился к целевому показателю в 7,0%. При этом отсутствовали жалобы на гипогликемические состояния. Пациентке рекомендовано увеличение дозы вечернего инсулина гларгин 100 ЕД/мл до 18 ЕД в 20.00 и дозы препарата гликлазида до 60 мг.
В мае 2019 г. на приеме пациентка в очередной раз предъявила жалобы на гипогликемические состояния, преимущественно по утрам после пробуждения, иногда просыпалась в середине ночи от кошмаров. Было принято решение о смене терапии инсулина гларгин 100 ЕД/мл на инсулин деглудек с сохранением дозировки в 18 ЕД в 20.00.
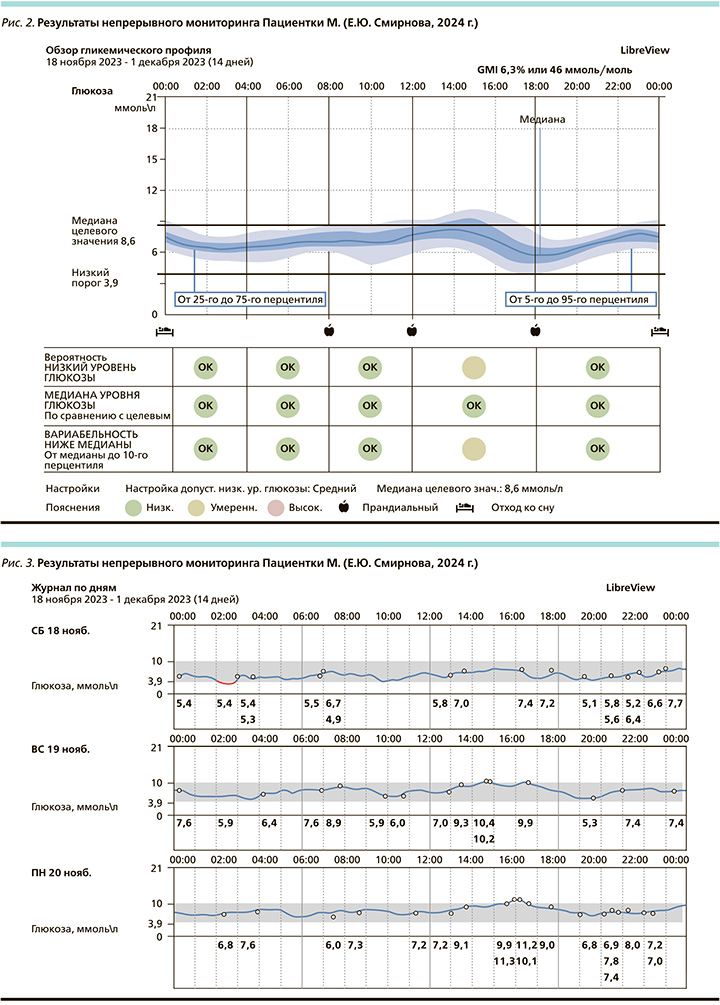
По данным дневника самоконтроля гликемии (табл. 8), все показатели находились в целевом диапазоне. Полученные показатели подтверждают успешность назначенной терапии. Пациентке М. рекомендовано продолжить терапию назначенными препаратами.
При динамическом наблюдении у данной пациентки происходила коррекция терапии. В апреле 2021 г.: инсулин дегдудек 20 ЕД в 20.00, вилдаглиптин 50 мг 2 таблетки в сутки, гликлазид отменен.
В мае 2021 г.: инсулин деглудек 20 ЕД в 20.00, отмена вилдаглиптина, к терапии добавлен инъекционный препарат арГПП-1 дулаглутид 1 раз в неделю.
Пациентка регулярно посещала врача и контролировала уровни гликемии, выполняла лабораторный контроль основных показателей, повторно посетила занятия по программе «Школа диабета», ежегодно обследуется в районном Диабетологическом центре.
По состоянию на январь 2024 г. (табл. 9) терапия пациентки М.: инсулин деглудек 20 ЕД в 20.00, дулаглутид 1 раз в неделю, эмпаглифлозин 25 мг утром, метформин 1000 мг по 1 таблетке утром и 2 таблетке вечером.

На основании представленных данных у пациентки достигнута стойкая компенсация стероидного СД на терапии современными препаратами (рис. 1–3). Достигнуты целевые показатели. Время нахождения в целевом диапазоне составило 98%. Небольшие отклонения в 1% в сторону повышения или понижения уровней гликемии пациентка М. списывает на калибровку датчика. Прогнозы ведения данной пациентки благоприятные. Смены или коррекции терапии в настоящее время не требуется.
Клинический пример 2
Пациент З. 41 год. В начале 2020 г. проживал в Сибирском Федеральном округе, где и перенес краснуху. После перенесенного заболевания выявлено повышение уровней гликемии до 15,0 ммоль/л, установлен диагноз «сахарный диабет впервые выявленный, декомпенсация». Целевой уровень HbA1c менее 6,5%. Назначена терапия: глибенкламид 3,5 мг утром и метформин 1000 мг вечером.
Наследственность по СД не отягощена. Сопутствующие заболевания: аутоиммунный тиреоидит, гипотиреоз, компенсация на заместительной гормональной терапии (левотироксин натрия 25 мкг/сут). Дислипидемия. Постоянно принимал аторвастатин 10 мг/сут. Ожирение 1-й степени (рост – 182 см, масса тела – 110 кг, ИМТ – 33,21 кг/м2).
Летом 2020 г. пациент З. переехал в г. Санкт-Петербург и встал на учет в поликлинику по месту жительства. На приеме у врача-эндокринолога жалобы на потерю массы тела (12 кг за 3 месяца), слабость, учащенное мочеиспускание, тошноту, сухость во рту. Уровни гликемии по результатам предоставленного глюкометра 3,0–21,0 ммоль/л. Диету строго не соблюдал.
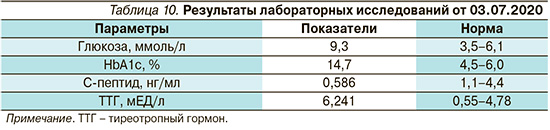
При оценке показателей (табл. 10) – декомпенсация углеводного обмена. Пациенту установлен диагноз «сахарный диабет 1 типа», целевой НbА1с менее 6,5%, назначена инсулинотерапия в базис-болюсном режиме. Таблетированные сахароснижающие препараты отменены. Препаратом выбора для минимизации риска гипогликемических состояний стали инсулин деглудек 10 ЕД в 20.00 и инсулин аспарт, имеющий в составе никотинамид и аргинин по 2–6 ЕД перед приемом пищи с учетом ХЕ. Пациент прошел обучение по программе «Школа диабета», научился считать ХЕ, обучился технике введения инсулина. Также с целью компенсации гипотиреоза назначена терапия левотироксином натрия в дозе 50 мкг/сут.
Выданы рекомендации по ведению дневника самоконтроля, пациент З. демонстрировал его на приеме каждые 2 недели. Титрация дозы инсулина деглудек происходила постепенно с шагом в 2 ЕД и достигла 18 ЕД.
В сентябре 2020 г. выполнен повторный лабораторный контроль основных показателей (табл. 11).
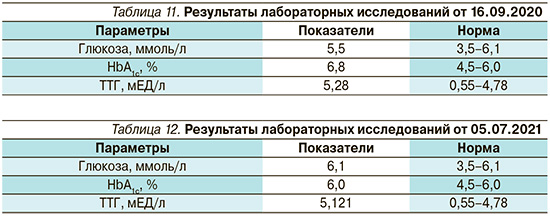
На фоне полученных данных (табл. 11) проведена коррекция терапии гипотиреоза, доза левотироксина натрия увеличена до 75 мкг/сут. Коррекции инсулинотерапии не требовалось. Пациент не предъявлял активных жалоб. Следующие 10 месяцев приходил лишь на выписку рецептов, ссылаясь на сильную занятость на работе.
В тот период пациент прекратил ведение дневника самоконтроля гликемии, на приемах предоставлял глюкометр для оценки показателей углеводного обмена. Самостоятельно увеличил дозы прандиального инсулина до 10–15 ЕД. Отказался от контроля лабораторных показателей.
В июле 2021 г. по настоятельной просьбе врача-эндокринолога выполнил лабораторный контроль анализов крови (табл. 12).
После посещения врача выполнена коррекция инсулинотерапии в связи с жалобами на гипогликемические состояния в течение дня. Рекомендовано уменьшение дозировки инсулина инсулина аспарт, имеющего в составе никотинамид и аргинин до изначальных доз в соотношении 1 ЕД инсулина на 1 ХЕ и повторное обучение по программе «Школа диабета»», обучение подсчету ХЕ.
Динамическое наблюдение продолжается в рамках амбулаторных посещений и регулярного контроля анализов крови. При постоянном контроле уровень НbА1с от 24.03.2022 – 5,8%, от 07.12.2022 – 6,1%, от 24.05.2023 – 5,7%, от 06.10.2023 – 5,9% (рис. 4–6).
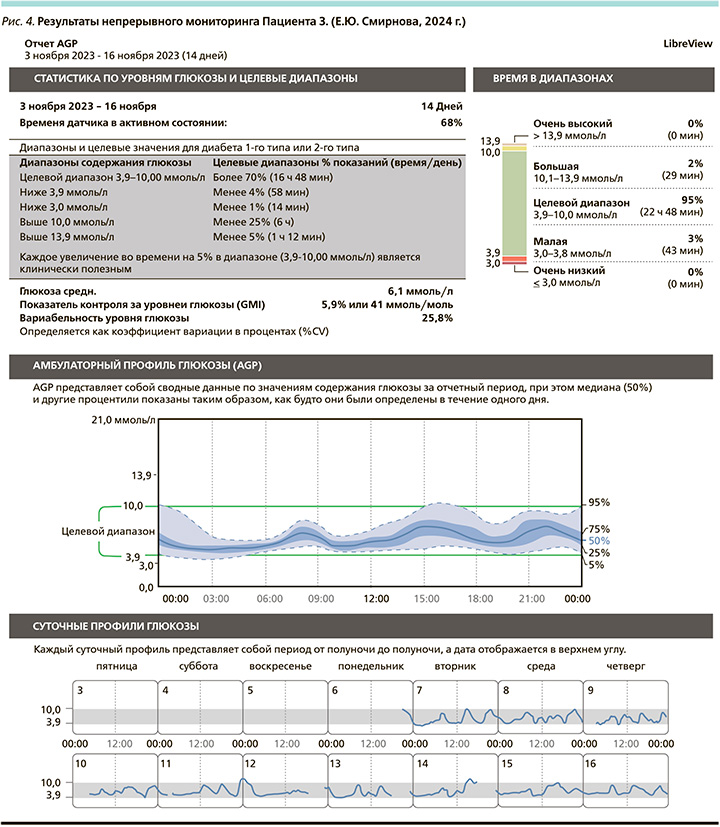
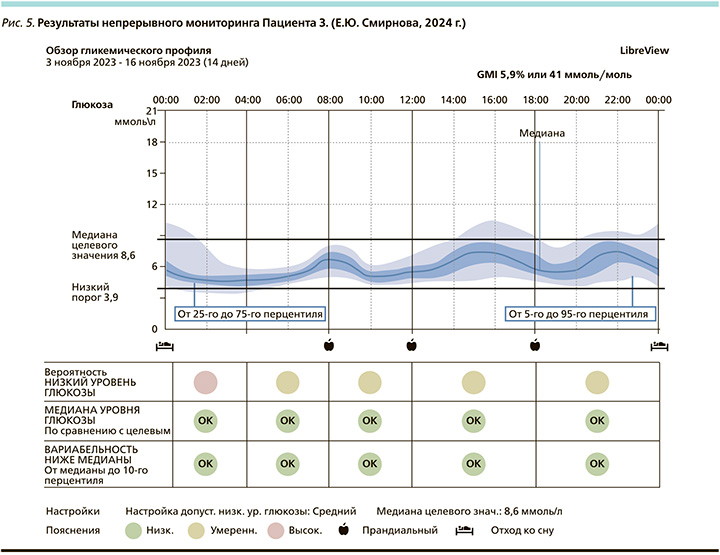
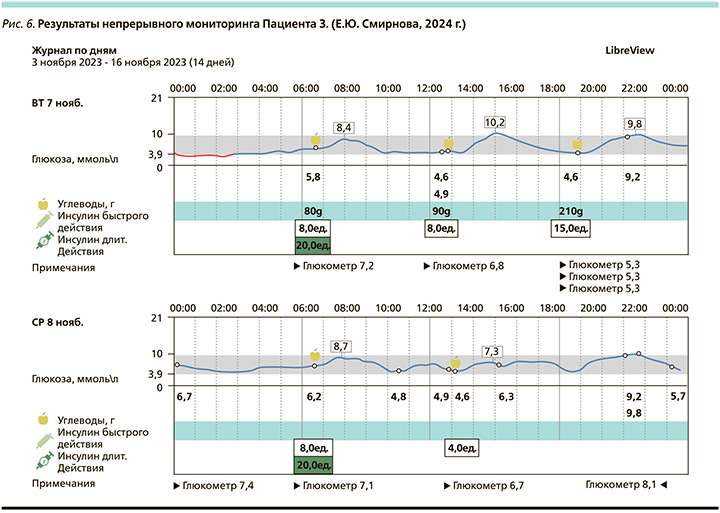
При появлении возможности выписки датчиков FreeStyle Libre и оценки результатов истории уровня глюкозы в приложении LibreView получено подтверждение компенсации заболевания, ошибочные гипогликемии пациент списывает на неудачную постановку датчика.
Пациент З. ответственно относится к своему заболеванию и в настоящее время тщательно следит за его течением. Терапия на момент последнего посещения врача: инсулин деглудек 20 ЕД утром (самостоятельное решение в связи с изменением графика работы) и инсулин аспарт, имеющий в составе никотинамид и аргинин по 2–10 ЕД перед приемом пищи с учетом ХЕ. При возможных праздничных мероприятиях и обильном питании грамотно увеличивает дозировки прандиального инсулина и перепроверяет уровень гликемии глюкометром.
Заключение
В ходе подбора терапии и лечения у пациентов в представленных клинических случаях возникали гипогликемические состояния. Наблюдая пациентов в амбулаторных условиях сложно контролировать все аспекты их жизни. Регулярные посещения врача, беседы о правильном питании, режиме дня, важности самоконтроля повышают приверженность пациентов лечению. Анализ результатов лабораторных показателей и дневников самоконтроля, а также данных системы непрерывного мониторинга позволили подтвердить эффективность и безопасность интенсификации сахароснижающей терапии инсулином деглудек. Длительный период наблюдения за представленными пациентами позволяет сделать вывод о высокой эффективности и низком риске гипогликемий при применении инсулина деглудек.



