Больной Л. 54 лет госпитализирован с жалобами на приступы тяжести за грудиной при ходьбе средним шагом и при эмоциональных нагрузках, проходящие в покое или купирующиеся нитроглицерином, одышку при физической нагрузке, головную боль, головокружение при повышении артериального давления (АД), стягивающие боли в икроножных мышцах при ходьбе, зябкость ног.
Анамнез и результаты обследования
С 17 лет у больного периодически регистрировали повышение АД до 140/90 мм рт. ст., не обследовался. С 50 лет страдает артериальной гипертензией (АГ), антигипертензивные препараты принимал непостоянно. Максимальные показатели АД – 180/100 мм рт. ст., адаптирован к 140–150/90–100 мм рт. ст. С 52 лет присоединилась стенокардия напряжения, перенес инфаркт миокарда без зубца Q, возобновление стенокардии через месяц. Наряду со стенокардией стала беспокоить одышка при физической нагрузке. Лечился нерегулярно. В течение последнего месяца частота приступов стенокардии – 3–4 раза в неделю, количество потребляемого короткодействующего нитроглицерина – 3 таблетки в неделю.
Курит в течение 25 лет по пачке сигарет в сутки. Отец страдал АГ, умер в 58 лет после острого инфаркта миокарда, у старшего сына (29 лет) периодически регистрируется повышение АД до 150/100 мм рт. ст.
При осмотре: состояние удовлетворительное, больной избыточного питания (масса тела – 86 кг, рост – 170 см, окружность талии – 108 см, индекс массы тела – 29,6 кг/м²). Отеков нет. В легких дыхание жесткое, несколько ослаблено в нижних отделах. Умеренное количество рассеянных сухих хрипов. Частота дыхательных движений – 20 в минуту. Тоны сердца приглушены, ритмичны, акцент II тона на аорте. АД – 145/90 мм рт. ст., частота сердечных сокращений (ЧСС) – 68 в минуту. Снижение пульсации на дорзальной и тибиальной артериях стоп с обеих сторон. Живот мягкий, безболезненный. Печень у края реберной дуги, селезенка не пальпируется. Физиологические отправления в норме.
В общем анализе крови и мочи патологических изменений не выявлено. В биохимическом анализе крови – гиперлипидемия IIа фенотипа (общий холестерин – 7,8 ммоль/л, холестерин липопротеидов низкой плотности – 5,9 ммоль/л, холестерин липопротеидов высокой плотности – 1,2 ммоль/л, триглицериды – 1,5 ммоль/л), остальные показатели в пределах нормы (глюкоза – 5,2 ммоль/л).
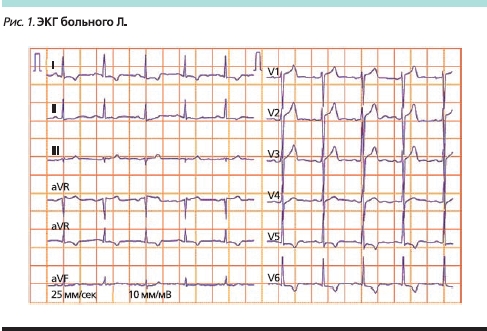
На ЭКГ (рис. 1) ритм синусовый, правильный с ЧСС 60–62 в минуту. Горизонтальное положение электрической оси сердца. Недостаточный прогресс зубца R и в отведениях V1–V3. Гипертрофия миокарда левого желудочка. Признаки недостаточности кровоснабжения передней и передне-боковой стенок левого желудочка.
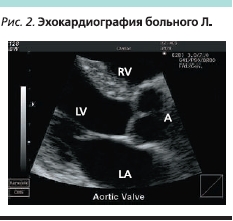
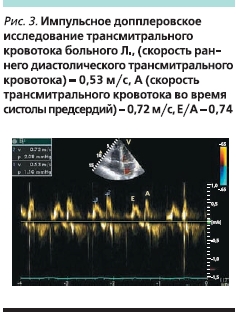
Данные эхокардиографии (рис. 2): умеренный фиброз створок аортального клапана. Отложение кальция в базальных сегментах створок аортального клапана, в фиброзном кольце митрального клапана. Небольшая дилатация полости левого предсердия, размеры остальных камер сердца, показатели глобальной систолической функции (фракция выброса – 58 %) в пределах нормы. Гипокинез базального и среднего передне-перегородочных сегментов. Гипертрофия стенок левого желудочка. По данным трансмитрального диастолического кровотока в импульсном допплеровском режиме (рис. 3) выявлена диастолическая дисфункция (Е/А – 0,74; IVRT – 112 мс, DT – 237 мс), что было расценено как начальные проявления нарушения релаксации.
Холтеровское суточное мониторирования ЭКГ: за время исследования зарегистрирован синусовый ритм с ЧСС 69–120 в минуту днем и 57–98 в минуту ночью. Желудочковая эктопическая активность представлена монотопными желудочковыми экстрасистолами (n = 821), наджелудочковыми экстрасистолами (n = 415), пауз не выявлено. В утренние часы (в 7.15 и в 8.05) выявлено 2 эпизода ишемии с горизонтальной депрессией сегмента ST на 1,0–1,2 мм. По дневнику пациента данная динамика сегмента ST сопровождалась ощущением тяжести за грудиной, одышкой при физической нагрузке.
Проводился велоэргометрический тест: ступенчато-возрастающая нагрузка каждые 3 минуты на 30 вт. Проба прекращена через 260 секунд (пороговая мощность нагрузки – 60 Вт) в связи с появлением горизонтальной депрессии сегмента ST в отведении V4 и косонисходящей депрессии сегмента ST в отведениях V5–V6 на 1,7–2,2 см в сочетании с ощущением тяжести за грудиной и одышкой. Пороговая ЧСС – 109 в минуту, максимальное АД – 170/100 мм рт. ст. Исчезновение признаков ишемии на ЭКГ и стенокардии на 2-й минуте отдыха, восстановление показателей гемодинамики – на 5-й минуте. Заключение: проба положительная, низкая толерантность к физической нагрузке, реакция сердечно-сосудистой системы по гипертоническому типу.
Стресс Эхо-КГ с физической нагрузкой: проба прекращена на 260-й секунде нагрузки при появлении ишемической депрессии сегмента ST на ЭКГ. Наряду с ранее существовавшими зонами нарушения локальной сократимости возник гипокинез верхушки и верхушечно-перегородочных сегментов левого желудочка, усилились признаки диастолической дисфункции (Е/А – 0,68; IVRT – 119 мс, DT – 240 мс).
При дуплексном сканировании плечевой артерии диаметр составил 4,0 мм, линейная скорость кровотока – 31,8 см/с, объемная скорость кровотока – 2,4 л/с. При пробе с реактивной гиперемией через 70 секунд после декомпрессии выявлено увеличение диаметра ПА артерии до 4,1 мм (+2,5 %), линейной скорости кровотока – до 54,2 см/с, объемной скорости кровотока – до 4,3 л/с. Эндотелий-независимая вазодилатация на введение нитроглицерина составила 23 %. Заключение: выраженная дисфункция эндотелия (эндотелий-зависимая вазодилатация +2,5 % при норме > 10 % в пробе с реактивной гиперемией) на фоне исходной стандартной терапии ИБС.
На рентгенограмме органов грудной клетки перибронхиальный склероз, что подтверждает наличие хронического бронхита; пневмосклероз базальных сегментов, повышение прозрачности легочных полей в связи с эмфиземой. Изменен кардиоторакальный индекс за счет расширения влево границ тени сердца.
Таким образом, больному поставлен следующий клинический диагноз: ишемическая болезнь сердца (ИБС), стенокардия напряжения II функционального класса. Постинфарктный кардиосклероз (инфаркт миокарда без зубца Q; 2004). Нарушения сердечного ритма: желудочковая и наджелудочковая экстрасистолия. Артериальная гипертензия 3-й стадии, 2-й степени, риск – 4. Недостаточность кровообращения 0 степени. Атеросклероз аорты. Облитерирующий атеросклероз сосудов нижних конечностей. Гиперлипидемия IIа фенотипа. Ожирение. Хронический бронхит курильщика, эмфизема легких, пневмосклероз.
На фоне приема ацетилсалициловой кислоты (Тромбо АСС 100 мг/сут), аторвастатина (Липримар 20 мг/сут), β-адреноблокатора бисопролола (Конкор 5 мг/сут), изосорбида мононитрата нитрата (Моночинкве 50 мг/сут) больному был назначен ингибитор АПФ периндоприл (Престариум А; Servier, Франция) в дозе 5 мг 1 раз в сутки в течение первых 2–4 дней с последующим увеличением суточной дозы до 10 мг на 6 недель.
Переносимость препарата была хорошей, через 6 недель лечения пациент отметил уменьшение числа приступов стенокардии до 1–2 в неделю, потребность в нитроглицерине снизилась до 1–2 таблеток в неделю. ЭКГ без динамики. По данным суточного мониторирования ЭКГ по Холтеру на фоне синусового ритма (ЧСС средняя – 67 в минуту) выявлено уменьшение числа желудочковых экстрасистол до 616, наджелудочковых экстрасистол – до 314 в сутки. Зарегистрировано уменьшение частоты эпизодов ишемии миокарда до 1 в сутки (дневной безболевой эпизод ишемии с горизонтальной депрессией сегмента ST до 1,4 мм продолжительностью 2 минуты).
По данным велоэргометрии отмечено увеличение толерантности к физической нагрузке: при неизменной пороговой мощности нагрузки (60 Вт) длительность нагрузки составила 290 секунд. Условия прекращения нагрузки соответствовали данным теста до назначения Престариума А. Пороговая ЧСС – 111 в минуту, максимальное АД – 170/95 мм рт. ст. Проба положительная, соответствует II функциональному классу стенокардии.
При Эхо-КГ в покое сохранялись зоны гипокинеза и признаки диастолической дисфункции левого желудочка. В условиях физической нагрузки при проведении стресс-Эхо-КГ отмечено улучшение локальной сократимости левого желудочка и отсутствие дискинезии в верхушечной области. При дуплексном сканировании плечевой артерии ее диаметр составил 4,1 мм, линейная скорость кровотока – 32,4 см/с, объемная скорость кровотока – 2,5 л/с. В пробе с реактивной гиперемией через 70 секунд после декомпрессии выявлено увеличение диаметра артерии до 4,5 мм (на 9,8 %), линейной скорости кровотока – до 56,0 см/с, объемной скорости кровотока – до 4,5 л/с. Согласно данным литературы, прирост эндотелий-зависимой вазодилатации в ответ на лечение ≥ 4,5 % рассматривают как достоверный показатель улучшения функционального состояния эндотелия. После лечения Престариумом А у данного больного прирост составил 7,3 %, эндотелий-независимая вазодилатация на введение нитроглицерина – 23 %.
Обсуждение
Частое сочетание АГ и ИБС, двух наиболее опасных с точки зрения высокого риска развития сердечно-сосудистых и цереброваскулярных осложнений состояний, показано в рамках крупного международного проспективного регистра REACH, составленного на основании данных, собранных в 44 странах мира, включая Россию [1].
Клиническая эффективность ингибиторов АПФ практически на всем протяжении сердечно-сосудистого континуума, в т. ч. при АГ и ИБС, объясняется их способностью модулировать деятельность ренин-ангиотензин-альдостероновой системы (РААС), хроническая активация которой является важнейшим фактором, ведущим к формированию эндотелиальной дисфункции. Одним из основных компонентов РААС является ангиотензинпревращающий фермент (АПФ), большая часть которого локализована непосредственно на мембранах эндотелиальных клеток крупных и мелких артерий и артериол, а также в адвентиции сосудов [2–4].
Поэтому применение ингибиторов АПФ с целью коррекции эндотелиальной дисфункции представляется патогенетически обоснованным и целесообразным подходом. Наибольшего эффекта следует ожидать от ингибиторов АПФ с высокой тканевой специфичностью, т. к. известно, что до 90 % АПФ локализовано в органах и тканях, в частности в мембранах клеток эндокарда и эндотелиальных клетках, и лишь 10 % – в плазме крови. Одним из ингибиторов АПФ, обладающим наиболее высокой тканевой специфичностью, является периндоприл (Престариум А).
Возможные пути улучшения (восстановления) функционального состояния эндотелия сосудов под влиянием Престариума А представлены на рис 4.
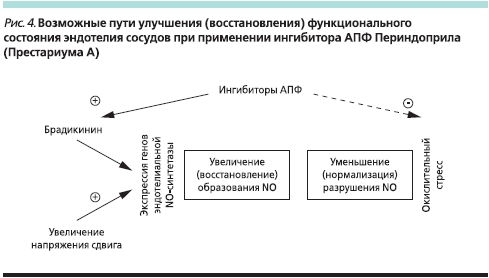
Воздействие ангиотензина II на эндотелий считается одним из основных повреждающих факторов в развитии и прогрессировании атеросклероза. Тканеспецифичный ингибитор АПФ периндоприл, блокируя этот механизм, оказывает антиатеросклеротическое действие. С одной стороны, за счет увеличения содержания брадикинина происходит нарастание экспрессии генов эндотелиальной NO-синтетазы, с другой – уменьшается окислительный стресс. В итоге происходит повышение образования NO с ослаблением его деградации [5].
Эффективность Престариума А для больных ИБС продемонстрирована в клинических исследованиях последних лет [6–9]. Наш собственный опыт также подтверждает высокий потенциал Престариума А в коррекции коронарного и миокардиального резервов у больных ИБС [10, 11].
Представленный клинический случай наглядно свидетельствует, что прием Престариума А – ингибитора АПФ с высокой тканеспецифичностью в суточной дозе 10 мг в течение 6 недель в комплексе с другими антиангинальными препаратами больным ИБС, стенокардией напряжения II функционального класса оказал восстановительный эффект в отношении дисфункции эндотелия, а также дополнительные антиангинальный и антиишемический эффекты в виде уменьшения выраженности стенокардического синдрома, увеличения толерантности к физической нагрузке, уменьшения количества эпизодов ишемии миокарда по данным холтеровского мониторирования ЭКГ, частоты экстрасистол, коррекции зон дискинезии в условиях стресс-Эхо-КГ.


