Адекватное лечение метастатического поражения костей является одной из актуальных проблем в паллиативной онкологии. По данным аутопсии, частота метастатического поражения костей скелета при раке молочной железы (РМЖ) и предстательной железы (РПЖ) составляет 73 и 68 % соответственно, при раке щитовидной железы – 42 %, раке легкого – 36 %, раке почки – 35 %; раке яичников – 9 %, раке желудочно-кишечного тракта (ЖКТ) и злокачественных лимфомах – по 5 %. Около 60 % больных РМЖ имеют либо определимые, либо доклинические микрометастазы уже в начале первичного лечения и до 75 % – в более поздний период, большинство из которых составляют метастазы в кости [5, 12].
Продолжительность жизни онкологических больных с костными метастазами определяется наличием других органных метастазов и чувствительностью опухоли к специфическому противоопухолевому лечению. Пятилетняя выживаемость больных РМЖ, РПЖ, раком щитовидной железы составляет около 20–45 %, при раке почки, легкого – лишь 5 %. Медиана выживаемости пациентов с костными метастазами колеблется от 6 до 48 месяцев в зависимости от типа опухоли, а при использовании современных методов лечения может быть и значительно больше [5, 12].
Костные метастазы существенно отягчают состояние пациентов. Поэтому особое значение приобретает качество жизни больных. Более половины из них имеют т. н. скелетные осложнения.
К скелетным осложнениям относятся следующие:
• патологические переломы костей, в т. ч. компрессионные переломы тел позвонков (со снижением высоты тела позвонка на 25 % и более между двумя рентгенологическими исследованиями);
• компрессия спинного мозга;
• появление или усиление болей, связанных с метастазами в кости.
Частота указанных осложнений варьируется в зависимости от характера опухоли и интенсивности проводимого лечения. Патологические переломы костей возникают в среднем через 11 месяцев после установления диагноза метастатического поражения костей [3].
Патогенез боли при метастазах связан с нарушением структуры и нормальной анатомии кости (микротрещинами в костной трабекуле, растяжением периоста, вовлечением нервных окончаний) и воздействием на рецепторы боли биологически активных веществ, вырабатываемых опухолевыми клетками [6].
Высок риск скелетных осложнений у больных РМЖ с остеолитическими метастазами. Ежегодное число скелетных осложнений у них составляет около 4, включая 2 патологических перелома, на 100 пациенток. Развитие скелетных осложнений не только снижает качество жизни больных с диссеминированными злокачественными новообразованиями с метастазами в кости, зачастую приводя к инвалидизации, но и препятствует продолжению специфического противоопухолевого лечения, снижая продолжительность жизни таких больных.
С экономической точки зрения предотвращение развития костных осложнений, снижение их частоты и увеличение времени до их развития представляются, очевидно, более целесообразным, чем лечение костных осложнений и социальная адаптация пациентов с осложнениями костных метастазов.
Многочисленные клинические и экспериментальные исследования в области биологии развития костных метастазов позволили ученым разработать новый класс препаратов, названных бисфосфонатами. Бисфосфонаты по своей химической структуре являются аналогами пирофосфатов костного матрикса, устойчивых к расщепляющему действию ферментов (щелочной фосфатазы). Бисфосфонаты снижают активность остеокластов, что приводит к подавлению резорбции костной ткани. Кроме того, в ряде исследований показана способность бисфосфонатов потенцировать противоопухолевый эффект цитостатиков, гормонов и лучевой терапии [4]. Внедрение в клиническую практику бисфосфонатов, действие которых направлено на специфическую коррекцию нарушений минерального обмена и избирательное воздействие на метастатически измененную кость, открыли новые возможности для помощи онкологическим больным.
Бисфосфонаты первого поколения, в частности клодронат (клодроновая кислота), в связи с низкой биодоступностью при пероральном введении требовали использования больших доз (до 3200 мг), что было неудобно для больных и вызывало побочные эффекты со стороны ЖКТ (тошнота, рвота, эзофагит, боли в животе, диарея). Внутривенное введение клодроната в дозе 1500 мг требовало медленного многочасового введения для предупреждения почечной токсичности. Первые азотосодержащие бисфосфонаты – памидронат (памидроновая кислота) и алендронат (алендроновая кислота), созданные в 1980-х гг., оказались более активными ингибиторами костной резорбции, чем бисфосфонаты первого поколения [4, 12].
Золедроновая кислота [1-Гидрокси-2(1H-имидазол-1-ил)этилиден] бис[фосфоновая кислота] – бисфосфонат третьего поколения. В молекуле золедроновой кислоты содержится два атома азота (у других бисфосфонатов – один), что делает препарат не только активным в отношении зон дефектов в костях, вызванных метастазами, но и действующим против самих опухолевых клеток. В настоящее время использование бисфосфонатов преимущественно в виде внутривенных ежемесячных инъекций является международным стандартом лечения онкологических больных с костными метастазами независимо и одновременно с проведением других видов терапии [7, 8].
Применение бисфосфонатов должно начинаться сразу же после обнаружения костных метастазов и продолжаться неопределенно долго – в зависимости от переносимости, при регулярном мониторировании функции почек (определении уровня креатинина перед каждым очередным введением препарата). Рекомендации ASCO по использованию бисфосфонатов при метастазах РМЖ и миеломной болезни, а также консенcусные рекомендации по применению бисфосфонатов при РПЖ и раке легкого содержат указания на необходимость именно внутривенного использования современных бисфосфонатов с момента обнаружения костных метастазов в течение длительного времени одновременно с химио- и гормонотерапией [7, 8].
Большинство практических онкологов отдают предпочтение препаратам золедроновой кислоты, избирательно действующей на костные метастазы. Проникая в костную ткань, она концентрируется вокруг остеокластов и в лакунах резорбции, задерживает созревание и миграцию остеокластов, вызывает их апоптоз, снижает секрецию лизосомальных ферментов (кроме Р450), что приводит к нарушению адгезии опухолевых клеток в кости и прекращению опухолевой резорбции костной ткани. В отличие от других бисфосфонатов золедроновая кислота обладает способностью угнетать новообразование сосудов в опухоли (антиангиогенный эффект) и вызывать апоптоз опухолевых клеток. Противоопухолевое действие золедроновой кислоты ранее было доказано в исследованиях в отношении клеток РМЖ и миеломы. В 2007 г. появились аналогичные данные в отношении клеток РПЖ и рака легкого. В ряде клинических исследований показано потенцирующее действие золедроновой кислоты на противоопухолевый эффект цитостатиков, применяемых в химиотерапии опухолей [1, 5, 9, 11].
Особый интерес представляет изучение прямого противоопухолевого действия бисфосфонатов. В экспериментах показана возможность влияния золедроновой кислоты на опухолевый рост in vitro и in vivo путем как прямого воздействия на адгезию и инвазию опухолевых клеток, так и непрямого воздействия на ангиогенез, а также возможность синергизма золедроновой кислоты и классических противоопухолевых препаратов, таких как таксаны [2].
Первый российский дженерик и пока единственный, имеющий успешный опыт клинического применения – Резорба (“Фарм-Синтез” ЗАО). Резорба выпускается в виде лиофилизата для приготовления раствора для инфузий; 1 флакон содержит 4 мг золедроновой кислоты –дозу, необходимую для однократного введения. Лиофилизат перед введением разводят в 100 мл физиологического раствора и вводят внутривенно не менее 15 минут.
Нежелательные явления при лечении Резорбой обычно незначительны и преходящи. Побочные эффекты Резорбы принципиально не отличаются по частоте и выраженности от таковых других внутривенных бисфосфонатов, т. е. являются характерными для всей лекарственной группы [4].
Повышение температуры, боли в мышцах и спине, гриппоподобный синдром чаще отмечаются в первые двое суток после инфузии Резорбы, легко купируются приемом неспецифических противовоспалительных средств. Золедроновая кислота выводится в неизмененном виде через почки; на фоне терапии Резорбой может отмечаться повышение уровня сывороточного креатинина, а у больных почечной недостаточностью – ухудшение состояния функции почек. При лечении Резорбой возможны реакции со стороны ЖКТ (тошнота, рвота). Локальные реакции в месте введения, такие как покраснение и припухлость, наблюдаются нечасто. В большинстве случаев требуется неспецифическое лечение и симптомы стихают в течение 24–48 часов.
Исследование эффективности Резорбы проводилось в Ростовском НИИ онкологии в 2006–2010 гг.
Материал и методы
Было проведено лечение 124 больным с диссеминированным РМЖ в возрасте от 28 до 70 лет, имевшим множественные метастазы в кости, которые сопровождались выраженным болевым синдромом и значительным ограничением объема движений (табл. 1).

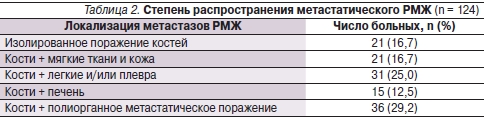
С целью купирования боли всем больным назначали ненаркотические анальгетики. У большинства пациенток костные метастазы сочетались с поражением внутренних органов и/ или кожи (табл. 2).
Все больные параллельно с терапией Резорбой подвергались цитостатической терапии комбинациями химиопрепаратов, включавших антрациклины и таксаны в стандартных дозах (доксорубицин 50 мг/м², паклитаксел 175 мг/м², доцетаксел 75 мг/м²). Резорбу вводили в дозе 4 мг внутривенно капельно 1 раз в 4 недели. Перед введением контролировали уровень сывороточного креатинина.
До лечения и спустя 3–4 месяца от начала лечения Резорбой больным проведено исследование костей с помощью остеосцинтиграфии, спиральной компьютерной томографии или рентгенографии.
Результаты
Уже после первого введения Резорбы 103 (83,3 %) больных отметили значительное уменьшение болевого синдрома, снижение потребности в анальгетиках и увеличение объема движений. У 98 (79,2 %) больных наблюдались репаративные изменения в очагах остеолиза, у 26 (20,8 %) пациенток деструктивные изменения в костях сохранялись на прежнем уровне, что было расценено как стабилизация процесса [5]. Нарастания степени метастатического поражения костей отмечено не было.
Переносимость Резорбы была удовлетворительной у всех больных. У 37 (30 %) женщин отмечены побочная реакция в виде гипертермии и усиление болей в первые сутки после введения препарата. Других нежелательных эффектов на фоне лечения Резорбой не наблюдалось.
У 15 (12,5 %) больных в течение 6-месячного периода от момента начала лечения Резорбой имели место скелетные осложнения в виде усиления боли в метастатически измененных костях, в 10 (8,3 %) случаях проводилась паллиативная лучевая терапия на зоны поражения. Медиана времени до первого скелетного осложнения не достигнута. Проведенный анализ показывает эффективность и хорошую переносимость отечественного препарата золедроновой кислоты Резорба у больных РМЖ с множественными метастазами в кости.
Доступность препарата в аптечной сети, включение в список по льготному обеспечению многим пациентам с костными метастазами дает возможность успешного лечения и сохранения удовлетворительного качества жизни.


