Введение
За последние годы резко возросла частота назначений прямых оральных антикоагулянтов (ПОАК) для профилактики тромбоэмболических осложнений у пациентов, находящихся в связи с этим в группе риска, в первую очередь у пациентов с фибрилляцией предсердий (ФП) [1, 2]. Это связано с тем, что ПОАК не только не уступали варфарину (а некоторые даже превосходили его) в эффективности профилактики инсульта в соответствующих рандомизированных клинических исследованиях, но и их прием был ассоциирован с меньшим риском развития внутричерепных кровоизлияний [1–3]. Кроме того, использование ПОАК в отличие от варфарина более удобно в клинической практике как для больного, так и для лечащего врача, поскольку не требует специального лабораторного мониторинга, длительного подбора и титрации дозы [3]. ПОАК ориентированы на одну фармакологическую мишень, реализующую их антикоагуляционный эффект: тромбин – для дабигатрана этексилата; фактор Ха – для апиксабана, ривароксабана и эдоксабана (последний не зарегистрирован в России по состоянию на 2022 г.) [1, 3]. Это позволяет выбирать стандартную фиксированную дозу препарата без лабораторного контроля международного нормализованного отношения [1, 3].
Однако прием некоторых ПОАК ассоциирован с повышенным риском развития желудочно-кишечных кровотечений (ЖКК) и может вызывать диспепсические явления [3, 4]. В частности, имеются данные, согласно которым применение дабигатрана этексилата и ривароксабана может быть ассоциировано с повышением риска кровотечения более чем на 30% по сравнению с варфарином [5–7], при этом 0,4–0,7% пациентов в год переносят ПОАК-опосредованные ЖКК, что предполагает 13,6–23,8 тыс. ПОАКопосредованных ЖКК в год [3]. В связи с этим в настоящее время эксперты рекомендуют рассмотреть в отношении пациентов, принимающих антикоагулянты (в т.ч. в сочетании с антиагрегантами), сопутствующее назначение гастропротекторов, прежде всего ингибиторов протонной помпы (ИПП) – «золотого» стандарта снижения желудочной секреции [2, 3]. Такая стратегия особенно важна для пациентов с наличием ЖКК в анамнезе или для тех, кто страдает язвенным поражением желудочно-кишечного тракта (ЖКТ) [8].
Еще одним классом гастропротекторов являются H2-антигистаминные препараты, которые также могут применяться для профилактики осложнений со стороны ЖКТ при применении ПОАК. Вместе с тем следует отметить, что найдены данные о снижении биодоступности отдельных ПОАК (например, дабигатрана этиксилата) на фоне приема ИПП или Н2-антигистаминных препаратов в виде уменьшения их абсорбции из ЖКТ на 15–20%, не влияющей, однако, на их клиническую эффективность [9].
В настоящее время новым препаратом защиты ЖКТ является ребамипид, который оказывает комплексное протективное действие, обеспечивает восстановление плотных контактов в эпителии кишечной трубки и реализует свои эффекты на всем ее протяжении [10–12]. Уникальной особенностью ребамипида служит широкий спектр плейотропных эффектов на уровне как пищеварительной системы, так и целостного организма: препарат стимулирует секрецию муцинов, активирует репарацию эпителия ЖКТ и улучшает микроциркуляцию в подслизистом слое [10, 12]. На сегодняшний день есть данные исследований, подтверждающие эффективность ребамипида в защите ЖКТ пациентов, получающих антитромботическую, в т.ч. антикоагулянтную, терапию [13–16].
Вместе с тем на данный момент практически отсутствуют сведения о реальной клинической практике применения гастропротекторов и препаратов для защиты ЖКТ пациентов, принимающих ПОАК. Такие данные были бы востребованы для разработки оптимальных стратегий защиты ЖКТ у больных, находящихся на антитромботической терапии (АТТ), изучения их эффективности в рамках клинических исследований и повышения информированности врачей о необходимости такой тактики ведения пациентов, поскольку от этого напрямую зависит улучшение прогноза последних.
Цель исследования: оценка частоты и структуры назначения лекарственных средств (ЛС) гастропротективного действия пациентам, получающим ПОАК.
Методы
Проведено многоцентровое кросссекционное (одномоментное) фармакоэпидемиологическое исследование, в котором ретроспективно проанализированы данные пациентов, проходивших обследование в различных научных центрах и лечебно-профилактических учреждениях России (26 научных центров 15 городов, 13 амбулаторных центров и 13 стационаров) с июня 2021 по март 2022 г.
Таким образом, отбор пациентов в исследование осуществлялся ретроспективно, согласно данным медицинской документации, и включал пациентов, как обследуемых на амбулаторном этапе (изучению подлежала амбулаторная карта больного), так и госпитализированных в стационар (изучению подлежала история болезни пациента). В первом случае отбору подлежали пациенты, обратившиеся в амбулаторно-поликлиническое учреждение и посетившие прием врача общей практики, врача-кардиолога, врача-терапевта за период в один календарный месяц до момента включения в исследование, которые получали ПОАК ранее и будут продолжать их применение, согласно решению врача, а также пациенты, которым впервые ПОАК были назначены непосредственно в течение анализируемого в исследовании временнóго периода. Во втором случае отбору подлежали пациенты, госпитализированные в стационар в течение одного календарного месяца до момента включения в исследование, которые на этапе стационарного лечения получали ПОАК в соответствии с показаниями к применению данных препаратов, а также пациенты, получавшие ПОАК ранее и продолжившие их прием в стационаре. Критерии включения: пациенты любого пола в возрасте от 18 лет и старше, принимавшие ПОАК (апиксабан, дабигатрана этексилат, ривароксабан) в соответствии с наличием показаний к их применению. Критерии невключения: пациенты, не принимавшие ПОАК или принимавшие ПОАК не в соответствии с показаниями к их применению.
Периоды включения пациентов в исследование и общей его длительности составили 6 месяцев. Период наблюдения предусмотрен не был.
С учетом ретроспективных данных была сформирована группа больных (n=662), получавших ПОАК, о которых проанализирована следующая информация: данные анамнеза, данные физикального исследования, в т.ч. индекс массы тела (ИМТ), уровень артериального давления (АД), частота сердечных сокращений (ЧСС), сопутствовавшие заболевания, в т.ч. все заболевания ЖКТ, наличие анемии, данные лабораторного обследования, включившего клинический и биохимический анализы крови; данные инструментального обследования, включившего результаты эзофагогастродуоденоскопии (ЭГДС) при ее наличии, фармакотерапия.
Характеристика включенных в исследование пациентов представлена в табл. 1. Поскольку общая группа обследуемых пациентов включила как стационарных больных, так и пациентов амбулаторного звена, в их характеристике данные по АД и лабораторным показателям (гемоглобин, креатинин) представлены в виде двух категорий: «при поступлении/на приеме» и «при выписке».
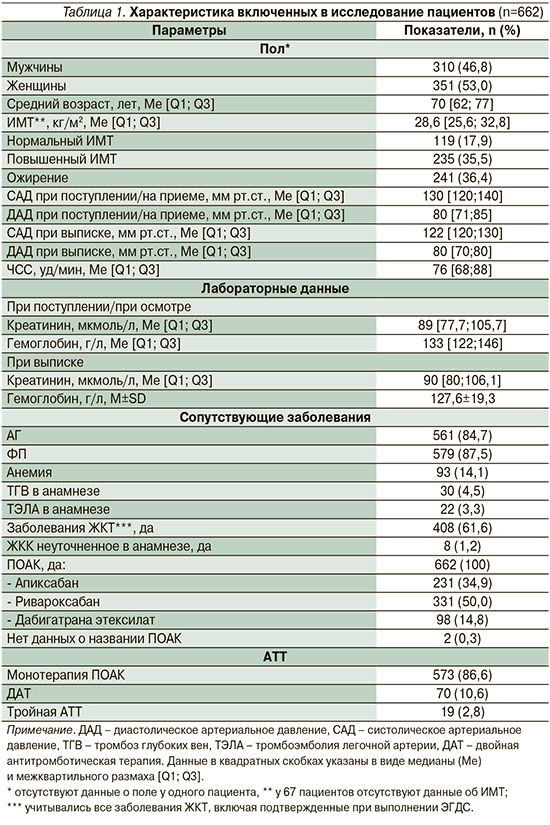
Статистический анализ проводили с использованием пакетов статистической программы SPSS v.23.0. Нулевая гипотеза о соответствии распределения нормальному закону проверялась с использованием теста Колмогорова– Смирнова. Описание выборки для ненормально распределенных параметров производили с помощью подсчета медианы (Ме) и интерквартильного размаха в виде 25-го и 75-го процентилей [Q1; Q3], для нормально распределенных параметров – путем определения среднего значения (mean) со стандартным отклонением (SD – standart deviation). Качественные данные представлены в виде абсолютных чисел и относительных частот.
Результаты
Все 662 пациента, включенных в исследование, принимали ПОАК, из них 50% получали ривароксабан, 34,9% – апиксабан и 14,8% – дабигатрана этексилат. В 0,3% случаев данных о названии ПОАК получено не было. Ранее ПОАК получали 429 (64,8%) пациентов, в 230 (34,7%) случаях они были назначены впервые, у 3 (0,5%) пациентов данная информация в медицинской документации отсутствовала. Следует отметить, что среди тех 429 пациентов, которые ранее принимали ЛС данной группы, длительность терапии ПОАК составила 14 [8; 36] месяцев, при этом 20 пациентов принимали ПОАК в течение ≤1 месяца, 57 – 1–6 месяцев, 82 – 6–12 месяцев, 60 – 1–2 года, 34 – >2 лет, но <3 лет, 62 пациента – >3 лет. Из этой группы 45 пациентов принимали ПОАК длительно, без указания на срок приема препарата, у 69 пациентов данные о длительности приема ЛС отсутствовали.
Среди пациентов, принимавших ривароксабан, 187 (56,5%) принимали препарат в дозе 20 мг/сут, 92 (27,8%) – в дозе 15, 23 (6,9%) – в дозе 10, 1 (0,3%) – в дозе 5 мг/сут (у данного пациента не было ФП, но он имел очень высокий риск тромботических осложнений и получал комбинированную терапию ривароксабаном и антиагрегантом). В 28 (8,5%) случаях данные о назначенной дозе ривараксабана отсутствовали.
Среди пациентов, получавших апиксабан, у 133 (57,6%) было возможно определить, что они получали полную дозу препарата 10 мг/сут.
У остальных 98 (42,4%) пациентов данные о назначенной дозе апиксабана отсутствовали.
Шестидесяти одному (62,3%) пациенту дабигатрана этиксилат был назначен в дозе 300 мг/сут, 35 (35,7%) – в сниженной дозе, равной 220 мг/сут. В 2 (2,0%) случаях данные о дозе дабигатрана этиксилата отсутствовали.
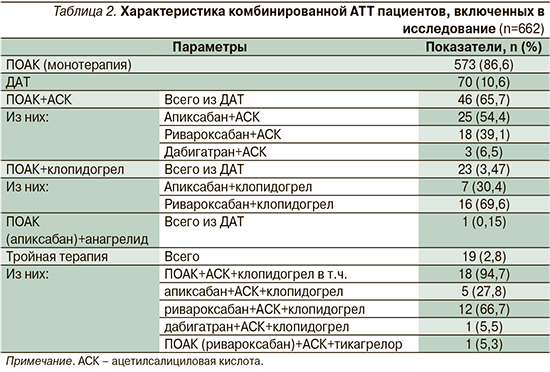
Из пациентов, включенных в исследование, монотерапию ПОАК получали 573 (86,6%) пациента. ДАТ (ПОАК+антиагрегант) была назначена в 70 (10,6%) случаях, тройная (ПОАК+два антиагреганта) – в 19 (2,8%). Характеристика комбинированной АТТ приведена в табл. 2.
Гастропротективная терапия (ГПТ) была назначена 378 (57,1%) пациентам, включенным в исследование. Монотерапию каким-нибудь одним гастропротектором получали 337 (89,2% от числа пациентов, кому была назначена ГПТ, и 50,9% от общего числа включенных в исследование) пациентов, а комбинированную терапию, включившую два и более гастропротектора в различных комбинациях, – 41 (10,8% от числа пациентов, кому была назначена ГПТ, и 6,2% от общего числа включенных в исследование) пациент. Характеристика ГПТ представлена в табл. 3.
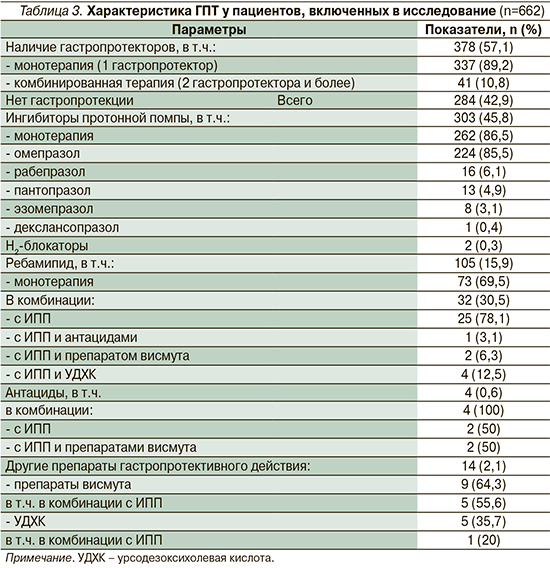
Исходя из данных, представленных в табл. 3, видно, что наиболее часто назначаемыми пациентам, принимающим ПОАК, гастропротекторами, оказались ИПП (в 45,8% случаев среди всех пациентов, включенных в исследование, и в 80,2% в случае ПОАК+ГПТ) и ребамипид (в 15,9% случаев среди всех пациентов, включенных в исследование, и в 27,8% среди пациентов, принимавших ПОАК+ГПТ). Причем как в первом, так и во втором случае данные препараты использовались преимущественно в виде монотерапии. Также отмечается, что монотерапия ИПП в большинстве случаев была представлена приемом омепразола, а ребамипид в составе ГПТ чаще всего комбинировали с ИПП.
К следующим важным аспектам, описывающим структуру назначения лекарственных препаратов гастропротективного действия пациентам, получавшим ПОАК, относится характеристика ГПТ при различных схемах назначения антитромбоцитарной терапии (табл. 4).
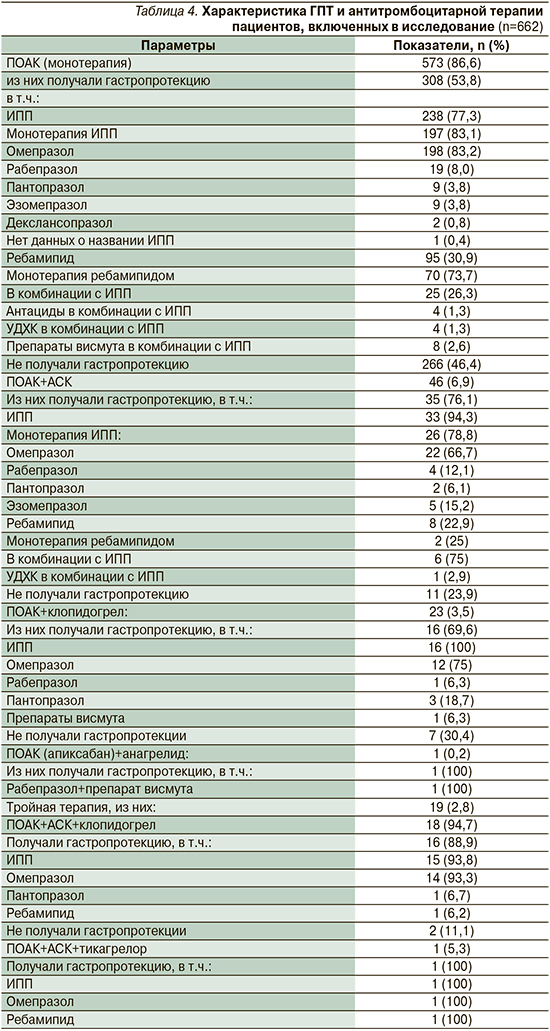
В результате, как видно из табл. 4, в случае монотерапии ПОАК из 573 пациентов ГПТ получали 308 (53,8%) человек. При этом следует отметить (данные не представлены в табл. 4), что из 308 больных 197 (63,9%) принимали ИПП в виде монотерапии, 70 (22,7%) – ребамипид в виде монотерапии, и только 41 (13,4%) больному была назначена комбинированная ГПТ. Последняя включила комбинацию ИПП с другим гастропротектором, самым частым из которых был ребамипид (25/60,9% пациентов из 41). Двойную терапию (ПОАК+АСК) получали 46 (6,9%) пациентов. Из данных пациентов ГПТ была назначена в 35 (76,1%) случаях. Гастропротекторы в основном были представлены в виде ИПП (монотерапия либо комбинация) или ребамипида. ИПП были назначены 33 (94,3%) пациентам, ребамипид 8 (22,9%). Среди тех, кто получал ИПП, были 26 (78,8%) больных, лечившихся в режиме монотерапии, 6 (18,2%) пациентов получали комбинацию ИПП с ребамипидом, 1 (3,0%) – комбинацию ИПП с УДХК. Одиннадцать (23,9%) пациентов из числа тех, кому была назначена двойная терапия ПОАК+АСК, ГПТ не получали.
Двойную терапию (ПОАК+клопидогрел) получали 23 (3,5%) пациента. Из данных пациентов ГПТ была назначена в 16 (69,6%) случаях. Во всех случаях, когда пациенты получали ГПТ, был назначен ИПП, в 1 (6,3%) случае в комбинации с ИПП был назначен препарат висмута. Семь (30,4%) пациентов из числа тех, кому была назначена двойная терапия ПОАК+клопидогрел, ГПТ не получали.
В 1 (0,2%) случае двойная терапия была представлена комбинацией ПОАК и анагрелида. Пациенту была назначена комбинированная ГПТ ИПП и препаратом висмута.
Девятнадцати (2,8%) пациентам была назначена тройная (ПОАК+два антиагреганта) терапия. В 1 (5,3%) случае терапия была представлена апиксабаном, АСК в дозе 100 мг и тикагрелором, а в остальных 18 (94,7%) – ПОАК+АСК+клопидогрел. ГПТ была назначена17(89,5%)из19пациентов,при этом в случае ПОАК+АСК+тикагрелор она включала комбинацию ИПП (чаще всего омепразол) и ребамипида, а в случае ПОАК+АСК+клопидогрел – ИПП (93,8%) или ребамипид (6,2%).
Обсуждение
Настоящее исследование показало, что частота назначения ГПТ пациентам, получающим ПОАК, в реальной клинической практике в РФ составила 57,1%, при этом ИПП, ребамипид, антациды и Н2-блокаторы назначали в 80,2%, 27,8, 1,1 и 0,5% случаев соответственно из числа всех гастропротекторов.
При проведении ретроспективного анализа 200 историй болезней пациентов с ишемической болезнью сердца (ИБС), находившихся в кардиологическом отделении ЧУЗ «КБ “РЖД-Медицина” г. Воронежа» в период с 2020 по 2021 г., ГПТ ИПП пантопразолом была назначена 45% пациентов, принимавших АСК 100 мг/сут (n=104), 100% пациентов, принимавших АСК+клопидогрел (n=41), и 100% пациентов (n=55), принимавших ПОАК (ривароксабан 15 мг/ сут)+АСК или ПОАК (ривароксабан 15 мг/сут)+АСК+клопидогрел [17]. В настоящем исследовании получены отличные, более низкие цифры по частоте назначения гастропротекции пациентам, принимавшим двойную терапию ПОАК+АСК или тройную терапию ПОАК+2 антиагреганта, которые составили 76,1 и 89,5% соответственно. Причиной может послужить недостаточная информированность врачей о необходимости назначения ГПТ пациентам с высоким риском ЖКК, обусловленным двойной/тройной терапией.
В одноцентровом проспективном РЕГистре длительной Антитромботической ТерАпии (РЕГАТА), проведенным на базе ФГБУ «НМИЦ кардиологии» и включившем 934 пациента со стабильной ИБС, было показано, что частота назначения ГПТ, а именно ИПП, составила в целом 28,3%, у 76% пациентов, принимавших двойную антитромбоцитарную терапию (АСК+клопидогрел) в течение 6–12 месяцев после плановых чрескожных коронарных вмешательств, – 30,1% [18]. При этом авторы отмечают, что 48 (5,1%) пациентов исследования принимали антикоагулянты в связи с развитием ФП или венозной тромбоэмболии (из них 23 пациента получали комбинацию антикоагулянта и антиагрегантов). ИПП назначили всем пациентам с наличием ЖКК в анамнезе, а также всем принимавшим нестероидные противовоспалительные средства, включая АСК, или антикоагулянты [18]. Поскольку в настоящем исследовании оценивалось назначение ГПТ только пациентам, принимавшим ПОАК, сравнить с нашими результаты данного регистра не представляется возможным, вместе с тем следует обратить внимание на то, что частота ИПП у пациентов с двойной антитромбоцитарной терапией довольно низкая, хотя в Российских клинических рекомендациях по стабильной ИБС (2020) [19] в данном случае рекомендуется использовать ИПП для защиты слизистой оболочки желудка и профилактики ЖКК. Причем во избежание возможного ослабления антитромбоцитарного эффекта клопидогрела предпочтительнее использовать пантопразол или рабепразол.
Для сравнения частоты применения гастропротекторов у пациентов, принимающих АТТ, приведем данные исследования китайских ученых, направленного в первую очередь на оценку характеристики моделей назначения и целесообразности назначения ИПП взрослым пациентам. Исследователями было установлено, что частота совместного использования антикоагулянтов и ИПП составила 91% в целом и 0,8% от всех новых случаев назначения ИПП, а антиагрегантов и ИПП – 61% в целом и 0,5% от всех новых случаев назначения ИПП [19]. При этом среди широко используемых ИПП с одновременным назначением антитромбоцитарной терапии чаще всего применяли омепразол, а в сочетании с антикоагулянтами, напротив, в основном применяли пантопразол [19]. Кроме того, авторы пришли к выводу, согласно которому 50% назначений ИПП необоснованны, а тем пациентам, кто принимал ИПП впервые, в 47% случаев терапия была назначена по неутвержденным показаниям для данной группы препаратов. Исследователи также выявили недостаточную частоту назначения гастропротекции пациентам, имевшим факторы риска ЖКК и принимавшим глюкокортикостероиды.
Таким образом, результаты проведенного исследования свидетельствуют, что ГПТ получали 54% пациентов, лечившихся ПОАК в виде монотерапии, и 70–76% больных, находившихся на комбинированной АТТ. Среди ЛС, примененных для защиты ЖКТ, наиболее часто назначаемыми были ИПП и/или ребамипид.
Анализ литературных данных свидетельствует, что назначения гастропротекторов пациентам, принимающим АТТ, в особенности включающую антикоагулянты и их комбинацию с антиагрегантами, недостаточно как в нашей стране, так и в международной практике.
Заключение
В России в реальной клинической практике частота назначения гастропротекторов пациентам, принимающим ПОАК, составляет всего 57,1%, а поскольку от этого напрямую зависит улучшение прогноза последних, необходимо проводить дополнительные меры, направленные на повышение информированности врачей о необходимости такой тактики ведения пациентов.


