Пищевод Барретта (ПБ) определяется как изменения эпителия нижней трети пищевода, которые могут быть охарактеризованы как цилиндрический тип метаплазии и верифицированы как кишечная метаплазия при морфологическом исследовании пищевода [1]. Сейчас принято считать, что ПБ служит осложнением гастроэзофагеальной рефлюксной болезни (ГЭРБ), которое происходит при хроническом повреждении слизистой оболочки пищевода при контакте с компонентами рефлюксата [2, 3]. Предполагается, что ПБ развивается у 10% пациентов с ГЭРБ [4]. За последнее время внимание к проблеме ПБ увеличивается в связи с ростом случаев развития аденокарциномы пищевода в Западной Европе и Северной Америке [5].
Распространенность ПБ до настоящего времени изучена недостаточно.
В качестве примера подобной работы мы приводим собственные исследования, выполненные в нескольких регионах Восточной Сибири.
Материал и методы
Выполнено одномоментное (поперечное) исследование в Абакане (Хакасия), Кызыле (Тыва) и Дудинке (Таймыр). В Абакане клиническое обследование и фиброэзофагогастродуоденоскопия выполнены 4325 представителям европеоидной расы (2006 мужчин и 2319 женщин; средний возраст – 43,4 года), в Кызыле – 1861 пришлому жителю (988 мужчин и 873 женщины; средний возраст – 42,3 года), в Дудинке – 1177 представителям европеоидной расы (881 мужчина и 296 женщин; средний возраст – 40,6 года).
Во время эндоскопического исследования в соответствии с рекомендациями D. Armstrong в случае смещения Z-линии и подозрения на наличие участков цилиндрического эпителия проводили окрашивание 2,5%-ным раствором Люголя. Для этого подозрительный участок слизистой оболочки орошали красителем «прямым» способом (к месту исследования краситель вводили шприцем по полихлорвиниловому катетеру, проведенному через рабочий канал эндоскопа), промывали дистиллированной водой, оценивали результаты окрашивания, определяли место для взятия биопсии [6]. Взятие биопсийного материала осуществлено по 4-квадратному методу, начиная в гастроэзофагеальном соединении и проксимальнее каждые 1–2 см к проксимальному краю слизистой оболочки Барретта, а также из любого подозрительного участка. Верификация диагноза ПБ осуществлена морфологическим методом при обнаружении в биоптатах пищевода метаплазии кишечного типа [7].
Статистическая обработка была проведена на персональном компьютере при помощи пакета прикладных программ «Statistic for Windows» (версия 7,0), SPSS v.12,0 for Windows, «Panalyzer». Для определения достоверности различий показателей применено вычисление отношения шансов (ОШ) и доверительного интервала (ДИ) для ОШ. Критический уровень значимости при проверке статистических гипотез принимали равным 0,05.
Результаты и обсуждение
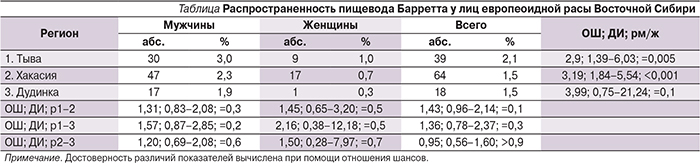
Распространенность ПБ среди лиц европеоидной расы в южных и северных регионах Восточной Сибири не имела существенных колебаний и варьировалась от 1,5 до 2,1%. Во всех регионах фактором риска развития заболевания был мужской пол (см. таблицу).
Распространенность ПБ широко варьируется. В США эта патология встречается среди 5,6% населения [8]. В популяционном исследовании в Швеции ПБ был диагностирован у 1,6% жителей [9]. Азиатские ученые дают более низкие цифры его выявляемости – от 0,4 до 1,2% [10].
Ведение пациентов с ПБ до настоящего времени остается сложной задачей. В связи с этим только в США в 2015 г. появилось 2 новых гайдлайна по диагностике и лечению ПБ [11, 12]. Скрининг ПБ рекомендуется проводить пациентам с симптомами ГЭРБ в возрасте старше 50 лет с наличием нескольких факторов риска, среди которых выделяют мужской пол, курение и ожирение [13, 14]. Вместе с тем надо учитывать, что треть пациентов с ПБ не имеют симптомов.
В связи с этим сейчас быстро развиваются методы определения генетических биомаркеров, позволяющих прогнозировать развитие дисплазии и рака [15].
Для диагностики ПБ рекомендуется применять увеличительную и узкоспектральную эндоскопию в сочетании с витальным окрашиванием участков пищевода, подозрительных на наличие метаплазии. Следует выделять пациентов с длинным сегментом ПБ (больше 3 см), у которых вероятность прогрессирования заболевания в рак пищевода относительно высока [16]. Точка зрения Британского гайдлайна [17] о важности определения клеток Гоблета для диагностики ПБ не находит поддержки со стороны других авторов [13].
Большое значение для выработки тактики ведения пациентов имеет определение степени дисплазии эпителия пищевода. В отсутствие дисплазии Британский гайдлайн рекомендует эндоскопическое наблюдение пациентов с коротким сегментом ПБ каждые 3–5 лет, лиц с длинным сегментом ПБ – каждые 2–3 года [17]. Пациенты с ПБ с дисплазией низкой степени должны наблюдаться эндоскопически через 6–12 месяцев. Для эрадикации участков метаплазии сейчас широко применяют аргоно-плазменную коагуляцию, фотодинамическую терапию и радиочастотную аблацию. Применение радиочастотной аблации позволяет добиваться 98% пациентов удаления метаплазии через 2 года [18]. Пациенты с ПБ с дисплазией высокой степени нуждаются в раннем применении эндоскопического или хирургического лечения после определения стадии опухолевого процесса при помощи эндоскопического ультразвукового метода [16].
Продолжает уточняться вопрос о применении ингибиторов протонной помпы (ИПП) для ведения пациентов с ПБ. Значительную роль в этом плане сыграл мета-анализ, опубликованный в 2014 г. в журнале Gut. Авторы этой работы пришли к заключению, что применение ИПП уменьшает риск рака пищевода у лиц с ПБ на 71%. Курсы ИПП больше 3 лет по сравнению с короткими курсами ИПП имели тенденцию к большей эффективности профилактики рака пищевода [19].
В связи с этим Американская гастроэнтерологическая ассоциация безусловно поддерживает применение ИПП пациентами с ПБ как без дисплазии, так и с наличием дисплазии [13, 16]. Точка зрения Британского гайдлайна более консервативна и заключается в том, что ИПП могут применяться только для контроля симптомов ГЭРБ [17].
Авторы различных мета-анализов и обзоров в целом поддерживают применение малых доз аспирина и нестероидных противовоспалительных средств для профилактики рака пищевода у больных ПБ [16, 17, 20, 21]. Следует выделить возможности использования урсодезоксихолевой кислоты для терапии пациентов с ПБ. В нашем 5-летнем проспективном исследовании комбинация препарата урсодезоксихолевой кислоты и ИПП была отчетливо более эффективна для лечения ПБ и эзофагита по сравнению с монотерапией ИПП [22].
Сохраняется интерес к хирургическим методам лечения ПБ, среди которых чаще используется фундопликация по Ниссену [23]. Вместе с тем современный мета-анализ демонстрирует отсутствие преимущества антирефлюксной хирургии перед медикаментозной терапией [24].
Заключение
В настоящее время в связи с быстрым ростом заболеваемости раком пищевода в США и Западной Европе наблюдается огромное внимание к проблеме ПБ. Диагностика и лечение этой патологии стремительно развиваются. Практическим врачам следует понимать, что основные цели терапии ГЭРБ сейчас включают не только борьбу с симптомами рефлюкса, но и раннюю диагностику предраковых изменений в пищеводе и профилактику рака пищевода.



