Актуальность проблемы
Качество жизни пациентов с иммуноопосредованными заболеваниями значительно ухудшается по мере прогрессирования патологического процесса. Псориатическая болезнь, при которой поражаются в т.ч. костно-суставные структуры, к сожалению, зачастую диагностируется поздно, особенно если отсутствуют кожные проявления. Прогрессирование псориатического артрита (ПсА) приводит к необратимым изменениям и инвалидизации, выраженно ухудшая качество жизни пациента и повышая риск развития тяжелых депрессивных состояний [1]. До 70% больных ПсА имеют аксиальные поражения [2, 3]. Более того, в таких случаях боль не всегда коррелирует с тяжестью воспаления или рентгенологическими показателями заболевания [4]. Интересно, что ПсА развивается у каждого четвертого пациента с псориазом гладкой кожи [5]. Поэтому возрастает роль дерматовенерологов в решении проблемы ранней диагностики ПсА и оптимизации терапевтических тактик. В многочисленных исследованиях доказано, что ключевую роль в развитии энтезитов, раннего воспаления периферических и межпозвоночных суставов, костного повреждения играет именно интерлейкин-17А (ИЛ-17А).
Ингибиторы ИЛ-17A демонстрируют эффективность при лечении многих патологических состояний, включая псориаз кожи, энтезит, синовит, спондилит. Кроме того, блокаторы ИЛ-17 предотвращают развитие эрозий костей, аномальных очагов формирования костной ткани, что демонстрирует важную роль в терапии ПсА [6]. Поэтому в настоящее время не только ведутся исследования по оценке эффективности ингибиторов ИЛ-17А в лечении псориаза и ПсА, но и обсуждается возможность их раннего назначения при доклинической стадии аксиальных поражений с целью предупреждения прогрессирования патологического процесса и инвалидизации [7, 8].
Нетакимаб представляет собой рекомбинантное гуманизированное моноклональное антитело иммуноглобулина-G1 (IgG1) против ИЛ-17А с модифицированным фрагментом Fc и областями CDR. В III фазе клинического исследования безопасности и эффективности применения нетакимаба в дозе 120 мг от 194 пациентов с G1 (ClinicalTrials.gov ID NCT03598751) получены данные об эффективности нетакимаба в отношении суставных проявлений артрита: достижение ответа со стороны периферических суставов на 24-й неделе терапии отмечено у 82,5%, полное разрешение энтезитов и дактилитов – у 63 и 77% пациентов соответственно [9]. Нетакимаб вызывает выраженный эффект в отношении аксиальных проявлений ПсА, а достижение ACR20 (American College of Radiology) на 24-й неделе наблюдается у 82% больных [9]. Нетакимаб демонстрирует сохранение высокой эффективности в отношении псориатического спондилита к году терапии: BASDAI <4 у 83% пациентов. В III фазе клинического исследования оценивалась безопасность и эффективность применения нетакимаба в дозе 120 мг для 228 пациентов с анкилозирующим спондилитом (ClinicalTrials.gov ID NCT03447704). Результаты исследования показывают, что лечение нетакимабом привело к снижению активности спондилита, улучшению функциональных и метрологических показателей, улучшению качества жизни. Уровни С-реактивного белка (СРБ) значительно снизились к 4-й неделе по сравнению с исходным уровнем и оставались на достигнутом уровне до 16-й недели. Кроме того, уже после 1-й инъекции отмечено выраженное уменьшение боли в спине [10].
Многочисленные исследования подтверждают быстрое и значительное уменьшение боли в спине при спондилоартрите и ПсА при использовании ингибиторов ИЛ-17А [11, 12]. Такие клинические исследования, как FUTURE и PSARTROS, также сообщают об эффективности раннего применения ингибиторов ИЛ-17А в терапии ПсА. У 80% пациентов на фоне терапии ингибитором ИЛ-17А имеет место полное разрешение дактилитов и более чем у 70% пациентов наблюдаются полное разрешение энтезитов [13], а также клиническая ремиссия синовитов, остановка катаболических и анаболических изменений костей [14]. Кроме того, при терапии ингибиторами ИЛ-17А 60% пациентов с ПсА и аксиальными артритами ASAS20 достигали уже на 12-й неделе [15]. Через 24 недели терапии разрешение синовита, по данным магнитно-резонансной томографии (МРТ), коррелировало с оценкой пациентами боли в суставах (с учетом визуальной аналоговой шкалы).
Нежелательными явлениями при использовании ингибиторов ИЛ-17А являются инфекционные заболевания. Однако в исследовании ASTERA не было обнаружено различий в частоте инфекций в группах нетакимаба по сравнению с плацебо [10]. Достоверное снижение артралгии, синовита и воспаления, по данным МРТ, а также отсутствие прогрессирования эрозий у пациентов с псориазом и очень ранним ПсА дают возможность обоснования ранней терапии нетакимабом с целью предотвращения прогрессирования ПсА [5].
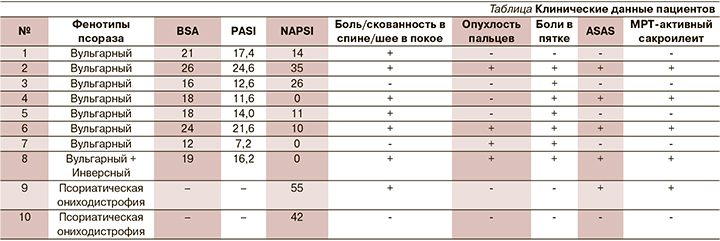
В данной статье представляем серию клинических случаев (n=10) терапии пациентов с тяжелым псориазом и доклинической стадией ПсА препаратом нетакимаб. В ходе обследования на приеме дерматовенеролога выявлены жалобы со стороны костно-суставного аппарата (боли и/или скованность в области позвоночника в покое, боли в пятках при ходьбе, отеки пальцев рук). Опросник mPEST соответствовал 3 баллам и более. Ни у одного из больных до настоящего обращения не был диагностирован ПсА. Пациенты были направлены к ревматологу, где после дообследования подтверждался диагноз ПсА на доклинической стадии. Данным пациентам назначен нетакимаб по показаниям: распространенный бляшечный псориаз средней или тяжелой степени в дозе 120 мг, после индукционного периода (3 недели) поддерживающая терапия проводилась в той же дозе 1 раз в месяц. Период наблюдения составил 1 год. Информация о пациентах представлена в таблице.
К моменту первой контрольной точки (после инициации) у пациентов наблюдалась положительная динамика в виде уменьшения инфильтрации и шелушения элементов, а также регресс мелких очагов (достижение PASI- 50–75, см. рисунок). В дальнейшем отмечалось нарастание эффекта: достижение PASI-100 – 4 из 8 и PASI-90 – 4 из 8 пациентов. Имело место существенное улучшение состояния ногтей по индексу NAPSI начиная с 12-й недели и нарастающее на протяжении года терапии – редукция индекса на 89%.
Кроме того, у пациентов наблюдалось выраженное снижение скованности, болевых ощущений в позвоночнике и в суставах (коленные, голеностопные), а также уменьшение отечности в проекции суставов. К концу периода наблюдений по данным ультразвукового исследования отмечено уменьшение исходного утолщения ахиллова сухожилия, кальцификации, синовиальный выпот не определялся, т.е. разрешение энтезитов. При обследовании у пациентов выявляли МРТ-неактивный сакроилеит, разрешение дактилитов и синовитов.
У всех пациентов улучшились показатели качества жизни (оценка согласно ДИКЖ – Дерматологическому индексу качества жизни, см. рисунок) и увеличилась физическая активность.

Заключение
Псориаз – хроническое системное иммуновоспалительное заболевание с широким спектром клинических проявлений, вариантов течения и исходов [16]. Лечение больных псориазом в соответствии с концепцией достижения конечных целей – это как можно более раннее начало терапии и соблюдение клинических рекомендаций, которые основываются на использовании методов с высокой доказательной базой. На сегодняшний день у пациентов даже с небольшими поражениями кожи отмечается очень низкий уровень качества жизни, пациенты считают свою болезнь большой проблемой в повседневной жизни. В настоящее время целью терапии считается достижение полного или почти полного очищения кожного покрова (PASI-90–PASI-100) [17]. Псориатическая болезнь затрагивает не только кожу, но и суставы; в этих случаях заболевание характеризуется прогредиентным течением и может приводить к инвалидизации. При этом у каждого четвертого пациента с псориазом кожи развивается ПсА [5]. До 70% больных ПсА имеют аксиальные поражения [2, 3].
По данным ряда авторов, при исследовании с применением МРТ признаки энтезопатий присутствуют более чем у 90% пациентов с псориазом без признаков ПсА [18]. У 40% пациентов с псориазом без клинических признаков ПсА обнаруживаются энтезиты и синовиты (данные УЗИ) [19]. Таким образом, у пациентов с псориазом существует проблема задержки постановки диагноза ПсА. В то же время ПсА развивается с течением времени и до развернутой клинической картины отмечается субклиническая стадия, когда возможности генно-инженерной терапии можно рассматривать с позиции вторичной профилактики ПсА. В этом плане именно ингибиторы ИЛ-17А являются наиболее приемлемой стратегией в тактике ведения пациентов данной категории, т.к. ИЛ-17А – ключевой в патогенезе и псориаза, и ПсА.
До недавнего времени ингибиторы фактора некроза опухоли-α (ФНО-α) были единственным вариантом лечения для пациентов с ПсА и аксиальным спондилоартритом. Однако до 30–40% пациентов со спондилоартритом имеют недостаточный эффект или не переносят терапию препаратами анти-ФНО-α [20]. Недавно было доказано, что ключевую роль в развитии энтезитов, раннего воспаления периферических и межпозвоночных суставов, костного повреждения играет именно ИЛ-17А. Нетакимаб – полностью гуманизированное моноклональное антитело IgG1 κ ИЛ-17A. Данный генно-инженерный биологический препарат используется в лечении псориаза средней и тяжелой степеней, ПсА и анкилозирующего спондилита.
В настоящее время многие специалисты поднимают тему раннего назначения генно-инженерных биологических препаратов при аксиальных поражениях, энтезитах и дактилитах с целью предупреждения инвалидизации. В данном сообщении мы представили клинический опыт применения нетакимаба в терапии тяжелого вульгарного псориаза, инверсного псориаза и псориатической ониходистрофии, а также его эффективность при ранних проявлениях аксиальных поражений на фоне ПсА.


