Введение
Остеопороз (ОП) является системной патологией скелета, характеризуется повышенной хрупкостью костей в результате снижения массы костной ткани и нарушения ее структуры [1]. Заболеваемость данной нозологией ежегодно увеличивается, а 2/3 пациентов представлены лицами пожилого возраста [2]. ОП в России наблюдается у каждой третьей женщины и каждого четвертого мужчины старше 50 лет [3].
Остеопоротические переломы могут приводить к тяжелым последствиям: снижению качества жизни, большим финансовым затратам, нередко и к смертности. Самые тяжелые из них – переломы шейки бедренной кости и чрезвертельные переломы позвонков. Поэтому важная задача здравоохранения – выявление пациентов с высоким риском низкоэнергетических переломов. Также требуется понимание, какой уровень риска можно считать достаточно высоким для того, чтобы целесообразным было терапевтическое вмешательство [1, 3].
В мировой практике с 2008 г. используется разработанный Всемирной организацией здравоохранения (ВОЗ) алгоритм расчета 10-летнего абсолютного риска остеопоротических переломов FRAX, который помогает определить вероятность возникновения перелома у определенного пациента в зависимости от его возраста, сопутствующей патологии, наличия клинических факторов риска [1].
Однако единственным стандартизованным методом диагностики ОП считается оценка минеральной плотности кости (МПК) с помощью денситометрии – двухэнергетической рентгеновской абсорбциометрии (DXA) [4]. Согласно критериям ВОЗ, значения МПК, отклоняющиеся по Т-критерию по DXA менее, чем на -1 SD, расцениваются как норма, значения от -1 SD до -2,5 SD – остеопения, превышающие -2,5 SD – ОП [5].
Главной целью терапии данной патологии скелета считается уменьшение риска низкоэнергетических переломов в результате улучшения качества и прочности костей при приеме определенных лекарственных препаратов. С целью оценки эффективности лечения в основном применяют следующие признаки – динамика МПК при DXА-исследовании, которое проводится не чаще 1 раза в 12 месяцев [5], и маркеров костного обмена (остеокальцин, 25-ОН витамин D, β-CrossLaps и др.).
В настоящее время доказано, что бисфосфонаты (БФ) способны длительно находиться в костном матриксе и оказывать пролонгированное действие после прекращения введения, что служит основанием для выбора индивидуальной тактики ведения больных в зависимости от риска перелома [6, 7]. Минимальный срок лечения БФ составляет 3 года для золедроновой кислоты и 5 лет для пероральных препаратов (ризедроновая, ибандроновая, алендроновая кислоты). При отсутствии новых низкоэнергетических переломов во время терапии, множественных переломов позвоночника, низкого показателя FRAX и МПК общего показателя бедра по Т-критерию выше -2,5 стандартных отклонений пациенты могут быть переведены на «лекарственные каникулы». Лечение возобновляют при доказанном снижении показателей денситометрии или возникновении нового остеопоротического перелома. При очень высоком риске переломов лечение БФ следует продлить до 10 лет, а затем сделать небольшой перерыв на 1–2 года до появления отрицательной динамики МПК или нового перелома [8].
Другие лекарственные средства, применяемые для лечения или профилактики ОП (терипаратид, деносумаб, селективные модуляторы эстрогеновых рецепторов, заместительная гормональная терапия), обладают обратимым действием при отмене, имеют ограниченные сроки применения (например, терипаратид можно применять не более 24 месяцев) или вызывают побочные эффекты, ограничивающие их длительное назначение из-за увеличения риска обострения сопутствующих заболеваний (эстрогены и стронция ранелат) [7].
Витамин D и препараты кальция в случае недостаточного его потребления с пищей являются также важным дополнением к терапии ОП [5, 9].
Цель описания данного клинического случая – показать эффективность своевременно начатого лечения постменопаузального остеопороза.
Клинический пример
Пациентка М. 50 лет обратилась к ревматологу 25.11.2019. На момент осмотра беспокоили ноющие боли в правом плечевом и локтевом суставах.
Из анамнеза. Боли в суставах отмечает в течение 10 месяцев. Консультирована ревматологом в июне 2019 г., выставлен диагноз: «плечелопаточный периартрит справа, латеральный эпикондилит справа. ФНС-1». Назначены нестероидные противовоспалительные препараты, проводилась локальная терапия № 2: бетаметазон 1,0+лидокаин 2,0 в правый плечевой и локтевой суставы 24.06.2019, 1.07.2019. Много лет наблюдается у невролога по поводу шейно-поясничной дорсопатии, хронической цервиколюмбалгии. Курсы лечения у невролога – 1–2 раза в год.
18.10.2019 пациентка самостоятельно прошла денситометрию (порекомендовали знакомые), выявлен выраженный ОП в поясничном отделе позвоночника (Т-критерий до -3,5 стандартных отклонений), в правом тазобедренном суставе. В левом тазобедренном суставе – остеопения.
При более детальном опросе выяснено, что больная страдает склерополикистозом яичников; были гинекологические операции: резекция правого яичника в 1992 г., удаление левой маточной трубы по причине внематочной беремености в 1992 г., резекция левого яичника по поводу кисты в 1994 г. Менопауза с 2009 г. Заместительную гормональную терапию не получала. Низкоэнергетических переломов не зафиксировано. Наблюдается у эндокринолога по поводу узлового зоба I cтепени, эутиреоза. Курит с 17 лет по 5–7 сигарет в день. Молочные продукты принимает редко.
На момент осмотра индекс массы тела пациентки – 19,9 кг/м2. Локальный статус: болезненность периартикулярных точек правого плечевого и правого локтевого суставов, движения в правом плечевом, правом локтевом суставе сохранены, болезненны.
На рентгенограммах плечевых суставов от 20.11.2019 признаки артроза 1-й стадии.
Диагноз «артроз плечевых суставов 1-й ст. Плечелопаточный периартрит справа, латеральный эпикондилит справа. ФНС 0-1. Постменопаузальный остеопороз без патологических переломов». Проведена локальная терапия № 1: бетаметазон 1,0+лидокаин 4,0 в правый плечевой и локтевой суставы. Пациентке рекомендованы занятия лечебной физкультурой, ходьба, тренировка равновесия. Назначены нестероидные противовоспалительные препараты по требованию, курсы хондропротекторов 2 раза в год.
Для лечения ОП после дообследования рекомендованы БФ: препараты алендровой или золедроновой кислоты, препараты кальция и витамина D постоянно. В течение 1 месяца больная принимала только кальция карбонат 500 мг+колекальциферол 200 МЕ 2 раза в день, отменила самостоятельно из-за побочных эффектов (выраженные запоры).
13.01.2020 вновь обратилась к ревматологу. По анализам от 10.01.2020: общий кальций – 2,17 ммоль/л (норма – 2,2–2,6), фосфор – 1,0 ммоль/л (норма – 0,81–1,45), щелочная фосфатаза – 196 EД/л (норма до 240), уровень витамина D – 20,6 нг/мл (норма более 30 нг/мл) – недостаточность.
При подробном опросе и осмотре выявлена низкая приверженность пациентки ежедневному приему противоостеопоротических препаратов, достаточный уровень дохода.
Рекомендовано начать терапию ОП золедроновой кислотой 5 мг внутривенно капельно 1 раз в год+альфакальцидол 0,5 мкг ежедневно длительно. Первое внутривенное введение золедроновой кислоты проведено 6.02.2020 в условиях терапевтического отделения, перенесла удовлетворительно: температура не повышалась, ощущала небольшой озноб и слабость в течение 3 часов. Общие анализы крови, мочи, биохимические показатели после введения БФ в норме.
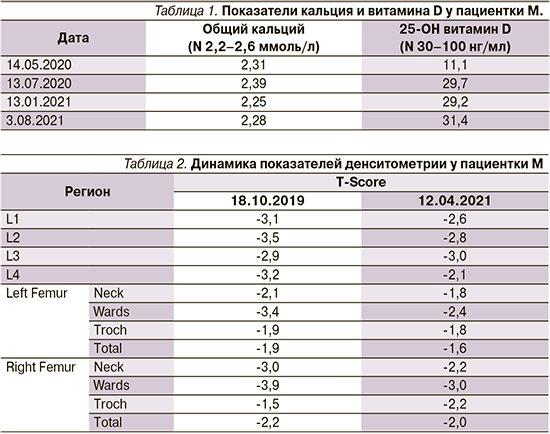
Контроль у ревматолога в мае 2020 г., уровень витамина D от 14.05.2020 на уровне дефицита, общий кальций в норме (табл. 1).
Рекомендован прием витамина D в каплях по 15 капель в день (500 МЕ в 1 капле), контроль витамина D и общего кальция через месяц.
Повторные анализы пациентка сдала 13.07.2020: уровень витамина D в пределах минимальной недостаточности, общий кальций в норме (табл. 1).
Пациентка начала принимать альфакальцидол 0,25 мкг+кальций 200 мг 2 раза в день.
Следующий контроль у ревматолога 27.01.2021. Диагноз тот же. Уровень витамина D от 13.01.2021 – в рамках небольшой недостаточности, общий кальций в норме (табл. 1). Рекомендовано продолжить прием препаратов кальция и витамина D, повторное введение золедроновой кислоты, контроль денситометрии через полгода.
Внутривенный БФ введен 8.02.2021 в условиях дневного стационара, переносимость хорошая. Общие анализы крови, мочи, биохимические показатели в норме. Пациентка сделала контрольную денситометрию 12.04.2021.
21.04.2021 пришла на прием к ревматологу. Предъявляла жалобы на редкие периодические боли в плечевых, локтевых суставах нагрузочного характера, в поясничном отделе позвоночника по ночам. Утренняя скованность до 5 минут.
Практически по всем показателям денситометрии наблюдалась положительная динамика (табл. 2), в поясничном отделе позвоночника показатели соответствуют ОП, однако Т-критерий стал меньше (до -3,0 стандартных отклонений). МПК обоих тазобедренных суставов соответствует остеопении. Переломов не было.
Диагноз «артроз плечевых суставов 1-й ст. ФНС 0. Постменопаузальный остеопороз без патологических переломов, положительная динамика».
Рекомендовано продолжить прием витамина D и препаратов кальция.
Контроль анализов от 3.08.2021: уровень витамина D и кальция в норме (табл. 1). Рекомендовано продолжить принимать альфакальцидол 0,25+кальций 200 мг 2 раза в день. Пациентке назначено третье введение золедроновой кислоты в феврале 2022 г., контроль денситометрии в октябре–декабре 2022 г.
Обсуждение
Проблема ОП приобретает все большее значение в настоящее время, с ростом диагностики происходит увеличение заболеваемости данной нозологией. Успешное ведение патологии скелета усложняет то, что она находится на стыке специальностей, с первичным и вторичным ОП часто сталкиваются эндокринологи, гинекологи, ревматологи, неврологи. Но не всегда сразу уточняется анамнез и выявляется высокий риск никоэнергетических переломов, который становится показанием к проведению более ранней диагностики болезни – денситометрии.
В нашем случае пациентка имела факторы риска раннего ОП (курение, низкая масса тела, гинекологические операции, ранняя менопауза), часто рецидивирующий шейно-грудной остеохондроз, на которые должным образом внимания никто не обратил. В итоге сделанная пациенткой денситометрия в возрасте 50 лет подтвердила наличие выраженого ОП. Результаты анализов показали наличие дефицита витамина D.
Эффективное лечение любого хронического заболевания зависит не только от правильно выбранного препарата для его терапии, но и от соблюдения пациентом рекомендаций по его приему. ОП относится к патологии, не имеющей определенных и ярко проявляющихся симптомов, уменьшение выраженности которых на фоне лечения может показать больному, что используемое им лекарственное средство оказывает положительное влияние на его самочувствие [10]. Низкий комплаенс терапии ОП является частой проблемой здравоохранения, вызывает ухудшение состояния МПК и повышение риска остеопоротических переломов, а также неблагоприятно влияет на соотношение «стоимость–эффективность» лечения, увеличивает расходы со стороны государства и самого пациента на лечение последствий ОП [11, 12].
В нашем примере с больной была проведена разъяснительная работа, благодаря чему она настроилась на длительный прием препаратов. Положительный эффект от терапии также влияет на комплаенс: вовремя назначенная адекватная терапия привела к нормализации уровня витамина D у пациентки, улучшению показателей рентгеновской денситометрии. Однако ОП сохраняется в поясничном отделе позвоночника, что требует продолжения противоостеопоротической терапии (введение золедроновой кислоты 3-й раз) с контролем денситометрии для решения вопроса о возможности «лекарственных каникул», продолжение приема препаратов кальция и витамина D.
Заключение
Таким образом, выявление и лечение ОП являются одной из важных задач современной медицины. Для раннего выявления данной патологии скелета следует тщательно собирать анамнез и своевременно направлять пациентов на дообследование, а также беседовать с пациентом о неблагоприятных последствиях ОП. Для стабилизации процесса и улучшения показателей МПК необходима длительная, тщательно контролируемая противоостеопоротическая терапия и коррекция гиповитаминоза D.



