Введение
Инфекционные поражения центральной нервной системы составляют группу наиболее тяжелых заболеваний детского возраста по своим органическим последствиям и влиянию на дальнейшее развитие ребенка. В детском возрасте нейроинфекции характеризуются наибольшей тяжестью течения и быстрым развитием неотложных состояний, обусловливающих возможный летальный исход [1].
В настоящее время доказано, что существует связь между частотой развития определенных неотложных состояний, угрожающих жизни пациента при нейроинфекциях, и этиологическим фактором основного заболевания [2]. По данным ДНКЦИБ, частота неотложных состояний при бактериальных менингитах максимальна при пневмококковой инфекции (52%), убывая при гемофильной (37%) и менингококковой (21%) инфекциях. Среди неотложных состояний, развивающихся на фоне нейроинфекций, одним из наиболее частых и опасных для здоровья пациента считается синдром внутричерепной гипертензии (ВЧГ). Нельзя не отметить, что синдром ВЧГ занимает важное место в структуре неотложных состояний при нейроинфекциях у детей.
Воспаление тканей центральной нервной системы (ЦНС) при менингитах и энцефалитах, протекающее с развитием ВЧГ, – одна из частых причин развития полиэтиологического синдрома нарушений секреции антидиуретического гормона (АДГ) и центрального (нейрогенного, гипоталамического) несахарного диабета (ЦНД) [3,4]. По данным германских исследователей, в течение 9 месяцев после перенесенных тяжелых форм нейроинфекции приблизительно у 11% пациентов отмечаются какие-либо формы нарушений экскреции гормонов гипоталамо-гипофизарной оси [3].
В основе синдрома нарушений секреции АДГ лежат два механизма [4]. Первый из них – нарушение выделения АДГ, проявляющееся полиурией и жаждой. Организм теряет воду, что в отсутствие замещения ее потерь приводит к формированию гиповолемии и гипернатриемии. Второй вариант, встречающийся значительно реже, – это синдром избыточной секреции АДГ. Данный синдром проявляется формированием гиперволемии и гипонатриемии.
ЦНД – тяжелое нейроэндокринное заболевание, характеризующееся неспособностью почек реабсорбировать воду и концентрировать мочу, имеющее в своей основе дефект синтеза, транспорта или осморегулируемой секреции АДГ, проявляющееся выраженной жаждой и экскрецией массы разведенной мочи. Распространенность данного состояния в популяции составляет 0,004–0,01% [4]. В последние годы отмечается общемировая тенденция к росту распространенности ЦНД [5]. В нашей стране число больных ЦНД составляет примерно 21,5 тыс. [4].
Необходимо отметить, что диагностика ЦНД при нейроинфекциях остается трудной задачей, т.к. многие клинические критерии, служащие указанием к его манифестации (жажда, дегидратация, общая слабость, повышенная утомляемость, полиурия), могут быть маскированы симптомами инфекционного заболевания или проводимой на его фоне терапии. Угнетение сознания, часто имеющее место при нейроинфекциях, также затрудняет оценку ряда субъективных симптомов (полидипсия, общая слабость) начала ЦНД.
Целью данной публикации является расширение представлений о клинических проявлениях, диагностике и коррекции нейроэндокринных осложнений ЦНС.
Принципы диагностики ЦНД
Диагностика ЦНД осуществляется на основании ряда кинических и лабораторных показателей.
Его основные клинико-лабораторные критерии:
- Снижение осмолярности мочи <300 мосм/кг.
- Снижение относительной плотности мочи <1,003 г/л.
- Наличие полиурии (темп диуреза у детей >3 мл/кг/ч).
- Нормальный или повышенный уровень натрия плазмы крови.
- Наличие жажды и полидипсии при сохранном сознании и отсутствии психических нарушений.
- Развитие дегидратации и гипернатриемии в отсутствие возмещения потерь воды и адекватной терапии.
Важным критерием, подтверждающим диагноз ЦНД, служит подтверждение отсутствия надпочечниковой недостаточности. Несахарный диабет не проявляется в условиях первичной надпочечниковой недостаточности, потому что для продукции гипоосмолярной мочи необходима хотя бы минимальная минералокортикоидная активность.
Развитие полиурии при ЦНД требует проведения дифференциальной диагностики с несколькими клиническими состояниями:
- нефрогенным несахарным диабетом;
- психогенной полидипсией;
- осмотическим диурезом (последствия осмотерапии, глюкозурия);
- использованием диуретических препаратов (фуросемид, гидрохлоротиазид и т.д.).
В повседневной клинической практике основной трудностью представляется дифференциальная диагностика синдрома гипернатриемии в рамках ЦНД, от чего напрямую зависит безопасность и эффективность дальнейшего лечения [4].
Сценарий развития гипернатриемии и гиповолемии у пациента с несахарным диабетом – это потеря свободной воды. При этом наиболее часто полиурия в течение некоторого времени остается незамеченной.
Затрудняет раннюю диагностику полиурии, связанной с ЦНД, и то обстоятельство, что проводимая при инфекциях ЦНС терапия большими дозами осмотического диуретика маннитола приводит к значительному повышению темпа диуреза. Основным критерием, позволяющим провести дифференциальную диагностику между двумя состояниями, служит тот факт, что введение маннитола всегда сопровождается выделением мочи с осмолярностью >300 мосм/л [6].
Терапия ЦНД при нейроинфекциях
Ведение пациента с ЦНД, развившимся на фоне нейроинфекции, требует проведения ряда мероприятий. В первую очередь важно проведение постоянного мониторинга водного баланса в виде подсчета почасового диуреза.
В качестве стартовой и базовой инфузионной терапии оптимален выбор растворов, содержащих ионы натрия в меньшем количестве, чем они содержатся в плазме крови пациента (Нормофундин, Ацесоль, 0,45% NaCl). В то же время при коррекции синдрома гипернатриемии следует помнить, что применение безнатриевых растворов угрожает развитию отека набухания головного мозга и может приводить к развитию жизнеугрожающих состояний [7].
Важным условием успешного ведения пациентов с ЦНД также является постоянный мониторинг концентраций основных электролитов крови.
В остром периоде необходим контроль уровня натрия не менее чем раз в 6 часов. При выявлении гипернатриемии ее коррекция должна проводиться со скоростью не быстрее чем 1 ммоль/ч.
Слишком быстрая коррекции гипернатриемии приводит к резкому возрастанию осмолярности внутриклеточной жидкости, устремлению жидкости внутрь клеток и как следствие – к отеку/набуханию головного мозга.
В отсутствие эффекта от проводимой корригирующей инфузионной терапии возможно применение экстракорпоральных методов гемофильтрации [8].Обязателен учет введенной в организм (внутривенная инфузия, энтеральное, парентеральное питание) и выделенной жидкости (диурез, потери с рвотой, стулом, отделяемое по зонду, дренажам).
С 1974 г. и до последнего времени в качестве препарата выбора при заместительной терапии больных ЦНД применяется десмопрессин для подкожного, внутривенного, интраназального и перорального применений, представляющий собой синтетический аналог природного вазопрессина, лишенный сосудосуживающей активности и обладающий более выраженным и продолжительным антидиуретическим эффектом. Он регулирует реабсорбцию воды, воздействуя непосредственно на почки через V2-рецепторы [9].
Целевая дозировка для назальных форм десмопрессина составляет от 10 до 40 мкг в сутки в зависимости от эффекта. Для пероральных форм доза достигает 0,1 мг 1–3 раза в сутки с последующим увеличением кратности приема по показаниям. Всегда рекомендуется подбор дозировки по эффекту.
При использовании назальных и пероральных форм десмопрессина полный эффект в виде снижения темпа диуреза достигается через 20–30 минут, длительность действия – 6–8 часов.
Опыт работы отделения интенсивной терапии ДНКЦИБ ФМБА свидетельствует: при терапии водно-электролитных нарушений у больных ЦНД необходим пересмотр каждые 6 часов. Обязателен учет введенной в организм (внутривеннвя инфузия, энтеральное, парентеральное питание) и выделенной жидкости (диурез, потери со рвотой, стулом, отделяемое по зонду, дренажам).
Важно вовремя остановиться при восстановлении объема циркулирующей крови, понять причину полиурии, установить, не является ли она ответом на мощную жидкостную терапию.
После начальной дозировки препарата стоит проанализировать необходимость увеличения кратности введения по достигнутому эффекту. По имеющемуся опыту, после применения адекватной дозы десмопрессина темп полиурии снижается в пределах 20–30 минут. Эта дозировка должна назначаться каждые 6–8 часов по необходимости (сохранение/нарастание полиурии в совокупности с гипернатриемией).
При отсутствии или неудовлетворительном эффекте на терапию десмопрессином следует принять решение о необходимости применения экстракорпоральнх методик гемокоррекции.
Иллюстрацией актуальности применения алгоритмов диагностики и лечения ЦНД при нейроинфекции может служить следующий клинический случай.
Клинический случай
Пациент П. 3 лет поступил в клинику ДНКЦИБ ФМБА переводом из другого стационара, минуя приемный покой, с диагнозом «генерализованная вирусно-бактериальная инфекция. Бактериальный гнойный менингит. Сепсис. Септический шок».
Из анамнеза заболевания известно, что оно началось с рвоты до 3 раз в сутки, лихорадки до 39,4°С максимально. На вторые сутки заболевания ребенок стал плохо и неохотно вставать, отмечалось нарастание вялости и слабости, достигших максимума к полудню, при осмотре педиатром амбулаторно зафиксировано нарушение сознания до уровня оглушения. Госпитализирован в стационар в связи с дальнейшим ухудшением состояния, ночью со 2-го на 3-й день болезни переведен на искусственную вентиляцию легких (ИВЛ).
Из анамнеза жизни известно, что ребенок от первой беременности, первых родов. Течение беременности и родов физиологическое. Масса тела при рождении – 4200 г, длина тела – 56 см.
Период новорожденности без особенностей. Вскармливание на первом году жизни естественное, продолжалось до 6 месяцев. Семейный анамнез, со слов родителей, не отягощен. Привит по возрасту.
На момент осмотра при поступлении состояние крайне тяжелое. Сознание: медикаментозная седация. Менингеальные симптомы положительные. Зрачки узкие. Фотореакция сохранена, вялая. Судороги отсутствуют. Микроциркуляция не нарушена. Гемодинамически стабилен без поддержки. Дыхание с применением ИВЛ. Печень не увеличена. Диурез адекватный. Масса тела – 16 кг. Температура тела – 38°С.
Состояние крайней тяжести, обусловленное сепсисом, септическим шоком, развитием на фоне шока синдрома полиорганной недостаточности (церебральная недостаточность 3-й ст., сердечно-сосудистая недостаточность 3-й ст., дыхательная недостаточность 3-й ст.).
Начато лечение:
- инфузионная терапия из расчета 2/3 физиологической потребности;
- антибактериальная терапия;
- респираторная терапия ИВЛ в условиях медикаментозной седации;
- инотропная и вазопрессорная поддержка;
- симптоматическая терапия.
На 3-й день заболевания (1-е сутки госпитализации в ОРИТ ДНКЦИБ ФМБА) состояние оставалось прежним, по данным исследования крови методом ПЦР выделены ДНК Haemophilus influenzae, диагностирован гемофильный менингит.
На фоне противоотечной терапии манитолом клинических и параклинических данных за нарастание ВЧГ, отека головного мозга не было.
С 4-х суток пребывания в ОРИТ (7-й день заболевания) отмечено резкое увеличение диуреза до 6 мл/кг/ч, достигшее максимума на 5-е сутки и составившее 9,7мл/кг/ч, а также нарастание гипернатриемии максимально до 168 ммоль/л.
С учетом наличия в анамнезе заболевания выраженного синдрома ВЧГ (потребовавшего перевода пациента на ИВЛ в условиях медикаментозного сна), развития полиурии, низкого удельного веса мочи, прогрессирующей гипернатриемии состояние расценено как проявление несахарного диабета в клинике нейроинфеционного заболевания.
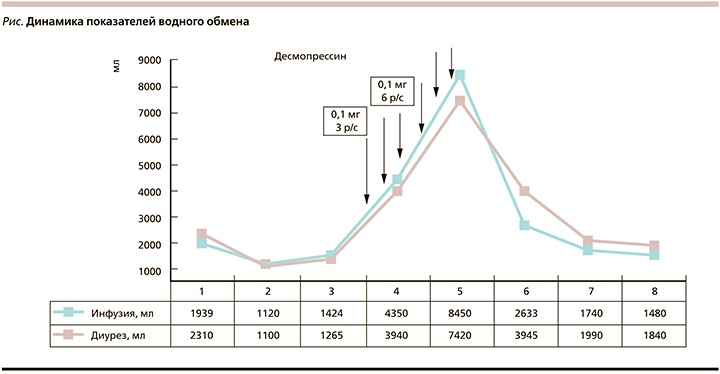
На 5-е сутки болезни к терапии был добавлен десмопрессин назальный в стартовой дозе 0,1 мг каждые 8 часов, увеличен темп инфузии (коллоиды+кристаллоиды) с учетом полиурии. Пациенту проведен почасовой контроль диуреза для коррекции инфузии (см. рисунок), контроль электролитов каждые 6 часов (см. таблицу).
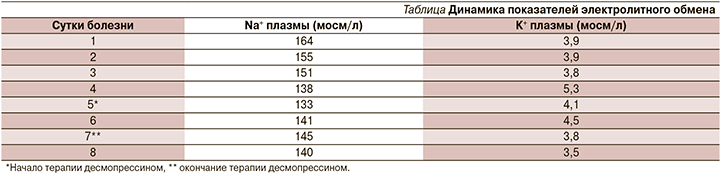
Первые 6 часов после интенсификации терапии в отношении несахарного диабета сохранялась полиурия на фоне инфузии с учетом патологических потерь до 9 мл/кг/ч, уровень гипернатриемии не нарастал, интервалы между введениями назального десмопрессина назального снижены до 4 часа
Через 12 часов от начала терапии ЦНД полиурия сохранялась с учетом инфузии до 8,5 мл/кг/ч, уровень гипернатриемии не нарастал. Принято решение сменить темп инфузионной терапии по физиологической потребности, на этом фоне сохранялась полиурия до 8,5 мл/кг/ч. Продолжена терапия десмопрессином 0,1 мг каждые 4 часа.
Через 24 часа от начала терапии ЦНД на фоне сохранения полиурии с учетом инфузии до 8,2 мл/кг/ч отмечено снижение уровня гипернатриемии до 155 ммоль/л.
При смене темпа инфузионной терапии по физиологической потребности темп диуреза снизился до 5,7 мл/кг/ч. Продолжена терапия десмопрессином 0,1 мг каждые 4 часа, темп инфузии с учетом 100%-ного водного баланса.
Через 32 часа от момента начала терапии полиурия с учетом инфузии снизилась до 5,4 мл/кг/ч, отмечено дальнейшее снижение уровня гипернатриемии до 153 ммоль/л. Терапия десмопрессином прекращена, темп инфузии с учетом 100%-ного водного баланса.
Таким образом, с применением основных принципов ведения несахарного диабета синдром полиурии с гипернатриемией был полностью купирован у ребенка за 2 суток. Уровень натрия нормализовался через 62 часа с момента начала введения синтетического аналога АДГ без развития клинических и параклинических признаков декомпенсации церебральной недостаточности.
Данный клинический случай иллюстрирует важность пересмотра терапии водно-электролитных нарушений при развитии синдрома несахарного диабета у пациентов с нейроинфекцией каждые 6 часов. Это позволяет подбирать эффективную дозу синтетических аналогов вазопрессина, определять причину полиурии, избегать попадания объема циркулирующей крови в замкнутый круг полиурия–восполнение с учетом патологических потерь, а также своевременно принимать решение о необходимости подключения к лечению экстракорпоральных методик.
Заключение
Таким образом, ЦНД является одним из частых и чрезвычайно опасных осложнений нейроинфекций у детей. Развитие данного состояния в отсутствие адекватного подхода к ведению пациента и поздней диагностики может приводить к быстрому прогрессированию отека головного мозга и гибели пациента.
В то же время при своевременной коррекции гипернатриемии, добавлении к терапии синтетических аналогов АДГ, при применении при необходимости методов экстракорпоральной гемофильтрации можно добиться стабилизации состояния пациента и избежать неблагоприятных исходов данного осложнения. Знание алгоритмов дифференциальной диагностики и терапии указанных состояний необходимо в повседневной практике врачам-реаниматологам, инфекционистам и педиатрам и будет способствовать повышению уровня оказываемой медицинской помощи, снижению смертности детей от осложнений нейроинфекций.


