Несахарный диабет (НД) является гетерогенным клиническим синдромом, возникающим вследствие нарушения секреции антидиуретического гормона (АДГ) [центральный несахарный диабет (ЦНД)], резистентности почек к действию АДГ [нефрогенный несахарный диабет (ННД)] или избыточного потребления жидкости [первичная полидипсия].
Несахарный диабет проявляется выделением массы мочи (полиурия) с низкой осмоляльностью (осмоляльность – менее 300 мосм/кг), полидипсией (объем потребляемой жидкости превышает > 2 л/м2/сут) и плохой прибавкой в весе. Полиурией считается выделение мочи в объеме, превышающем 2 л/м2/сут или приблизительно 150 мл/кг/сут для новорожденных, 100–110 мл/кг/сут для детей до 2 лет и 40–50 мл/кг/сут для детей более старшего возраста и взрослых [1].
Классификация НД, клинические проявления этого состояния, диагностические процедуры, направленные на выявление НД и определение его типа, изложены в многочисленных руководствах и методических рекомендациях по НД [2–5].
Основная задача терапии НД у детей – это снижение объема выделяемой мочи и (в большинстве случаев) уменьшение жажды, что в свою очередь позволит ребенку поддерживать нормальный образ жизни. Специфическая терапия НД зависит от этиологии заболевания.
Для решения этих задач необходимо:
- обеспечение свободного доступа ребенка к воде;
- оптимизация пищевого рациона с целью уменьшения объема выделяемой жидкости (преимущественно у детей с ННД);
- для терапии ЦНД – применение аналога вазопрессина – десмопрессина;
- для терапии ННД – использование препаратов, усиливающих реабсорбцию воды в почках;
- терапия основного заболевания [6].
У детей с НД должен постоянно быть свободный доступ к воде. При этом длительный прием большого количества жидкости может приводить к дискинезии желчевыводящих путей, опущению желудка, развитию синдрома раздраженного кишечника, а также к развитию гидронефроза.
Центральный несахарный диабет
В настоящее время при лечении ЦНД препаратом выбора является десмопрессин (1-дезамино-8-D-аргининвазопрессина). Десмопрессин является синтетическим аналогом антидиуретического гормона, в котором дезаминирован 1-цистеин и в 8-й позиции L-изомер аргинина замещен на D-изомер. За счет этого десмопрессин оказывает более выраженный антидиуретический эффект, обладает большей продолжительностью действия по сравнению с АДГ. Одновременно с этим вазопрессорный эффект десмопрессина в 2000–3000 раз меньше такового вазопрессина [5].
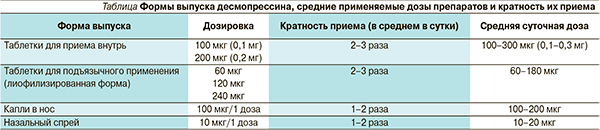
Десмопрессин применяют в форме интраназальных спрея или капель, пероральных таблеток и таблеток с лиофилизированной (мелт) субстанцией для сублингвального применения. Интраназальная форма препарата наиболее часто применяется во время операций, в послеоперационном периоде, при наличии у ребенка тошноты и/или рвоты, при резко выраженном негативизме по отношению к таблетированным препаратам. К преимуществам таблетированных форм препарата относятся хорошая всасываемость, более широкие возможности изменения и подбора оптимальных доз препарата, в большинстве случаев – хорошая комплаентность пациентов. Кроме того, возможность давать десмопрессин в таблетках в очень маленьких дозах (до 0,025 мг/прием) сводит к минимуму риск передозировки препарата у детей 3–5 лет и пациентов с низкой потребностью в заместительной терапии. В таблице представлены формы выпуска десмопрессина, указаны средние применяемые дозы препаратов и кратность их приема.
Следует помнить, что длительность и сила действия препарата могут сильно варьироваться, поэтому частота его приема и доза подбираются индивидуально. К детям до 3 лет лекарственная терапия центрального НД в большинстве случаев не применяется из-за опасности передозировки десмопрессина с развитием гипонатриемии. Последняя приводит к гипоосмоляльности внеклеточной жидкости и переходу воды в клетки, в т. ч. в клетки мозга. Как следствие – возможно развитие грозного осложнения: отека мозга [7].
У маленьких детей достаточно сложно контролировать количество выделяемой мочи, поэтому целесообразно ориентироваться на объем потребляемой жидкости и/или уровень натрия в сыворотке крови. Если симптомы НД выражены значительно, повышенная жажда и частое мочеиспускание негативно влияют на развитие и состояние маленького ребенка, возможно очень аккуратное применение препаратов десмопрессина под строгим контролем уровня натрия и/или осмоляльности сыворотки крови. Целесообразно использовать десмопрессин в виде назального спрея, при этом препарат разводят физиологическим раствором в соотношении 1 : 10. Разведенный препарат назначают перорально 1–2 раза в сутки [8, 9].
Детям с ЦНД старше 3 лет терапию препаратами десмопрессина начинают с небольших доз, постепенно увеличивая их по мере необходимости. Кроме того, при первоначальном подборе терапии каждую следующую дозу препарата рекомендуется применять после 1–2 часов диуреза в объеме > 4 мл/кг/ч, т. е. после того как в течение некоторого времени у пациента возникает обильное мочеиспускание, моча при этом становится светлой. Это способствует выведению осмотически свободной мочи и предотвращению развития гипонатриемии.
При назначении препаратов десмопрессина проводятся тщательный ежедневный подсчет и запись количества выпитой и выделенной жидкости; ежедневное определение уровня электролитов (натрия, калия) в сыворотке крови, при повышенном/сниженном уровне натрия определение проводится несколько раз в сутки (обычно 2–3 раза); пациента ежедневно взвешивают для контроля над балансом жидкости. Все эти мероприятия проводятся до стабилизации состояния. В последующем контрольные определения электролитов и баланса жидкости проводятся 1 раз в 3–6 месяцев [3–5]. Важно объяснять пациентам и их родителям необходимость контроля над балансом жидкости. Для предотвращения возможной передозировки препарата дозу десмопрессина для длительной заместительной терапии следует подбирать таким образом, чтобы суточное количество выделенной жидкости несколько превышало нормальные значения суточного диуреза (в норме количество выделяемой мочи составляет 15–30 мл/кг в сутки). В среднем суточный диурез у детей с ЦНД в возрасте до 4–5 лет не должен быть меньше 1000 мл, в возрасте до 10 лет – 1200–1500 мл, у детей более старшего возраста – 1800–2000 мл.
Особенно тщательный подход к назначению и подбору заместительной терапии препаратами десмопрессина требуется пациентам, перенесшим хирургическое вмешательство по поводу опухоли гипоталамо-гипофизарной области или травматическое повреждение головного мозга. В этих случаях НД может иметь различные варианты развития.
Послеоперационный НД может начинаться остро с полиурии со спонтанным разрешением в течение нескольких дней [10]. Выраженное интраоперационное повреждение или серьезная травма способны приводить к развитию перманентного НД. Несахарный диабет может также иметь «трехфазное» течение: первая фаза полиурии, вызванная повреждением гипоталамо-гипофизарной области и снижением уровня секреции АДГ, длится от нескольких (12–36) часов до нескольких дней. Затем наступает вторая фаза, длящаяся от 2 до 14 дней, т. н. антидиуретическая фаза, которая сопровождается неконтролируемым выделением АДГ из поврежденных нейронов. Затем следует третья фаза – фаза полиурии. Во время второй фазы важно не вызвать у пациента гипергидратации, что на фоне неадекватной секреции АДГ приводит к развитию гипонатриемии. У пациентов, перенесших нейрохирургическое вмешательство, независимо от характера течения ЦНД после операции (при условии проведения адекватной инфузионной терапии, введении препаратов десмопрессина), при уровне натрия в сыворотке ≤ 145 ммоль/л чаще всего наступает спонтанное исчезновение симптомов НД (как правило, через 3–6 месяцев после операции). Если у пациентов в послеоперационном периоде уровень натрия в сыворотке ниже 145 ммоль/л, высока вероятность развития перманентного НД [11]. Эти особенности течения ЦНД в послеоперационном периоде важно учитывать при подборе дозы десмопрессина. Важно предупреждать пациентов и/или их родителей о необходимости контроля выпитой и выделенной жидкости, отмены препарата при появлении отеков и/или изменении баланса жидкости с последующей консультацией у лечащего эндокринолога.
В ряде случаев после объемного хирургического вмешательства по поводу опухоли гипоталамо-гипофизарной области у пациентов наряду с полиурией, вызванной развитием ЦНД, наблюдается олиго- или адипсия. Сочетание полиурии с недостаточным поступлением жидкости в организм приводит к быстрому развитию гипернатриемии и гиперосмолярного состояния. Для предотвращения подобных осложнений проводится принудительное выпаивание таких пациентов (часто, но небольшими, по 50–100 мл, объемами воды), параллельно проводится подбор дозы десмопрессина, при необходимости – соответствующая инфузионная терапия. Этой группе пациентов в течение первых 4–6 месяцев после операции необходимо проводить определение уровня натрия и/или осмоляльности крови 1 раз в 10–14 дней с соответствующей коррекцией дозы десмопрессина.
Нефрогенный несахарный диабет
В основе развития ННД лежит резистентность почек к действию АДГ, поэтому применение десмопрессина пациентами с данным заболеванием неэффективно. Первоочередная задача лечения ННД – обеспечить поступление достаточного количества воды в организм, особенно маленьким детям, не имеющим возможность взять воду самостоятельно.
В отношении детей грудного возраста следует отдавать предпочтение естественному вскармливанию, поскольку грудное молоко создает меньшую осмотическую нагрузку. С учетом неспособности маленького ребенка реагировать на наличие жажды каким-либо специфическим образом грудным детям и детям до 3 лет следует давать воду каждые 2 часа как днем, так и ночью. У детей данной возрастной группы потребление больших объемов жидкости может усиливать физиологический желудочно-пищеводный рефлюкс, что в свою очередь может потребовать соответствующего лечения. Необходимо тщательно следить за аппетитом детей с ННД и темпами их физического развития [12].
Определенные изменения в пищевом рационе ведут к уменьшению водной нагрузки на почки, что особенно важно для пациентов с ННД. Детям с НД рекомендуется диета с пониженным содержанием натрия и белка. Ограничение потребления соли до 100 мЭкв/сут (2,3 г натрия) и белка до 2 г/кг/сут может приводить к значимому уменьшению полиурии. Однако диету с подобными ограничениями достаточно сложно поддерживать в течение длительного времени. Кроме того, детям белки необходимы для роста и развития организма, поэтому для них целесообразно строже ограничивать потребление соли [13]. Для предотвращения развития дилатации и дисфункции мочевого пузыря всем пациентам с выраженной полиурией следует рекомендовать частое «двойное» мочеиспускание (т. е. после мочеиспускания необходимо подождать несколько минут, а затем попробовать еще раз опорожнить мочевой пузырь полностью).
Диета с пониженным содержанием натрия в сочетании с приемом тиазидных диуретиков парадоксальным образом ведет к уменьшению полиурии. Считается, что при таком подходе происходит выведение натрия, сопровождающееся уменьшением объема экстрацеллюлярной жидкости, снижением скорости клубочковой фильтрации и усилением реабсорбции натрия и воды в проксимальном отделе канальцев [14]. Применяют тиазиды в следующих дозировках: хлортиазид – 30 мг/кг/сут (или 1 г/м2/сут) внутрь в 3 приема; гидрохлортиазид – 3 мг/кг/сут (или 0,1 г/м2/сут) внутрь в 3 приема. Эффективной представляется комбинация гидрохлортиазида (3 мг/кг/сут) с калийсберегающим диуретиком амилоридом (0,3мг/кг/сут); препараты принимаются внутрь 3 раза в день, вначале амилорид, через 2–3 часа гидрохлортиазид. Этот способ позволяет обходиться без добавления калия к пище и почти не вызывает отдаленных побочных реакций [15, 16].
В настоящее время существует комбинированный препарат Модуретик, в состав которого входят амилорид (5 мг) и гидрохлортиазид (50 мг), однако безопасность его применения для детей изучена еще недостаточно.
Ингибиторы циклооксигеназы (ЦОГ), как неспецифические, например индометацин, так и специфические ингибиторы ЦОГ-2, например нимесулид, могут значимо уменьшать объем диуреза. Индометацин назначают в дозах 1,5–3,0 мг/кг массы тела. Длительное применение препарата может вызывать серьезные побочные эффекты со стороны почек и желудочно-кишечного тракта.
Последние годы при лечении ННД чаще применяются селективные ингибиторы ЦОГ-2 – нимесулид в дозе 1,5 мг/кг в сочетании с тиазидными диуретиками в вышеуказанных дозах [17].
Первичная полидипсия (психогенная или дипсогенная)
Предпочтение отдается ограничению жидкости, однако в случае психогенной полидипсии выполнение подобных рекомендаций представляет трудности. Психиатрические расстройства, которые могут лежать в основе состояния, требуют соответствующей терапии. В случае психогенной полидипсии нельзя применять препараты десмопрессина и/или тиазиды, поскольку это может приводить к гипонатриемии. Для пациентов с дипсогенной полидипсией полезным может оказаться замена чрезмерных объемов жидкости на употребление кислых леденцов, жевательной резинки или ледяной крошки [18].
Заключение
Несахарный диабет является редким для детей заболеванием, проявляющимся полидипсией и гипотонической полиурией. Заболевание может быть вызвано одной из трех причин: 1) сниженной секрецией АДГ, как при ЦНД; 2) отсутствием реакции почек на действие АДГ – при ННД; 3) избыточным потреблением жидкости – первичная полидипсия. Терапия НД включает коррекцию существующего дефицита жидкости и предотвращение ее потерь в дальнейшем. Эффективной терапией ЦНД остается применение препаратов десмопрессина. Первоначально необходимо тщательно титровать дозу, начиная с минимально эффективной. Это позволит предотвращать развитие гипонатриемии. С меньшим эффектом проводится лечение ННД с помощью диетических мероприятий (в первую очередь ограничение соли), применение тиазидных диуретиков в комбинации с селективными ингибиторами ЦОГ-2. Для лечения первичной полидипсии применяют ограничение потребления жидкости. Чаще всего пациенты с первичной полидипсией не страдают от каких-либо осложнений и могут поддерживать стабильный гомеостаз путем повышенного потребления и выделения жидкости. Именно поэтому попытки ограничить жидкость далеко не всегда приводят к успеху. Несмотря на то что НД является доброкачественным заболеванием, ограничение достаточного количества воды (независимо от причин) может приводить к развитию жизнеугрожающего состояния.


