Диуретики являются одними из наиболее широко применяемых сердечно-сосудистых препаратов. Они занимают важное место в лечении артериальной гипертензии (АГ), сердечной недостаточности (СН), хронической почечной недостаточности (ХПН). Без них практически невозможно представить повседневную работу терапевта [1]. Наибольшее распространение из тиазидных (или тиазидоподобных) диуретиков получили гидрохлоротиазид в Европе и хлорталидон в США, которые используются при лечении АГ с конца 1950-х гг., а также присоединившийся к ним в последние годы индапамид. Согласно новым рекомендациям Европейского общества АГ/Европейского общества кардиологов 2013 г., диуретики наряду с препаратами, блокирующими ренин-ангиотензиновую систему (РАС), β-адреноблокаторами (БАБ) и блокаторами кальциевых каналов относятся к препаратам первой линии для лечения АГ [2].
Выраженная экскреция ионов натрия (мочегонное действие короткодействующих петлевых диуретиков), происходящая в течение нескольких часов в сутки, компенсируется значительной задержкой ионов натрия по окончании их мочегонного действия (т.е. на протяжении большей части суток). «Феномен рикошета» является объяснением того факта, что при приеме 1 раз в сутки петлевые диуретики (фуросемид) обычно не увеличивают суточную экскрецию ионов натрия и не оказывают существенного антигипертензивного действия. Для выведения избытка ионов натрия из организма петлевые диуретики необходимо назначать 2–3 раза в сутки [3].
До недавнего времени практически единственным петлевым диуретиком, широко применяемым в отечественной медицинской практике, оставался фуросемид. Наличие мощного и быстрого диуретического эффекта и низкая стоимость сделали этот препарат основным средством лечения отеков различного генеза, острых и хронических застойных явлений в легких и гипертонических кризов. Однако такие его свойства, как непродолжительность диуретического воздействия, вторичная РАС и симпато-адреналовая активация, риск развития гиповолемии, гипокалиемии, тромбофилии, метаболических и других осложнений, значительно ограничили применение фуросемида для лечения АГ [4].
В исследованиях было показано, что фуросемид и буметанид при одно- или двукратном назначении в сутки, как правило, недостаточно эффективны как антигипертензивные препараты. Снижение артериального давления (АД) при применении фуросемида 2 раза в сутки меньше, чем гидрохлоротиазида при приеме 1 раз в сутки. Эти данные привели к тому, что петлевые диуретики короткого действия не рекомендовались для широкого использования пациентами с АГ, а их применение ограничивалось случаями на фоне ХПН [3].
Согласно общепринятым рекомендациям экспертов, петлевые диуретики в настоящее время не рассматривают в качестве препаратов 1-го ряда для длительного лечения АГ, поскольку фуросемид как средство длительной медикаментозной профилактики менее эффективен, чем тиазидные диуретики. Среди аргументов против применения петлевых диуретиков больными АГ называют их способность вызывать существенное ухудшение качества жизни за счет увеличения диуреза и частоты мочеиспусканий [1].
Петлевые диуретики для пациентов с АГ могут рассматриваться в качестве препарата выбора в следующих случаях:
- у пациентов с резистентной АГ;
- при АГ, ассоциированной с хронической сердечной недостаточностью (ХСН);
- при стойком снижении скорости клубочковой фильтрации (СКФ) у больных АГ;
- для купирования гипертонических кризов [1].
Задача лечения АГ была успешно решена с помощью менее агрессивных и длительно действующих тиазидных диуретиков. Применение этих препаратов в малых дозах позволило существенно снизить риск развития метаболических и других побочных эффектов, однако при этом существенно снизился диуретический эффект, необходимость которого увеличивается у больных по мере прогрессирования нефроангиосклероза и присоединения СН. Таким образом, определенной и достаточно большой группе больных АГ необходимо более интенсивное диуретическое воздействие с целью поддержания водно-электролитного баланса и контроля АД. Последняя задача может быть решена за счет применения торасемида – петлевого диуретического препарата нового поколения с более плавным и длительным действием [4].
Фармакокинетические свойства торасемида отличаются от таковых фуросемида, отличия представлены в таблице.
При пероральном применении торасемид быстро абсорбируется, при этом пик концентрации в плазме достигается в течение часа. Действие торасемида начинается через час после приема внутрь, пик наступает через 1–2 часа, продолжительность эффекта составляет в среднем 6–8 часов. При приеме препарата в дозе 2,5–100 мг/сут объем выделенной жидкости, а также экскреция натрия и хлоридов возрастают линейно в зависимости от дозы. Площадь под кривой зависимости концентрации от времени пропорционально возрастает при увеличении дозы при применении доз 2,5–40 мг/сут здоровыми добровольцами или 20–200 мг больными ХПН [1].
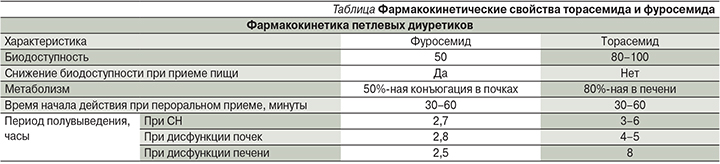
К важным преимуществам торасемида относится высокая биодоступность, которая составляет более 80% и превосходит таковую у фуросемида (50%). Биоусвояемость торасемида не зависит от приема пищи, в связи с чем в отличие от фуросемида появляется возможность применять его в любое время суток. Высокая и предсказуемая биодоступность определяют надежность диуретического действия торасемида при ХСН и позволяют более успешно применять препарат перорально, даже в случаях тяжелой ХСН [5]. Однократный прием торасемида в сутки повышает приверженность пациентов лечению, согласно данным исследования, на 13% по сравнению с терапией фуросемидом [6].
Метаболизм торасемида на 75–80% происходит в печени с образованием активных метаболитов и на 20% – в почках. Период полувыведения препарата удлиняется у пожилых больных и в незначительной степени – при нарушении функции печени [1].
Большинство исследований с оценкой эффективности торасемида были проведены еще в 1990-х гг.
В 12-недельном двойном слепом исследовании 147 больных АГ торасемид в дозах 2,5–5 мг/сут по антигипертензивной активности достоверно превосходил плацебо [7]. Диастолическое АД нормализовалось у 46–50% больных, получавших торасемид, и у 28% больных группы плацебо. Препарат сравнивали с различными тиазидными и тиазидоподобными диуретиками, в т.ч. в различных схемах комбинированной терапии. По данным одного из исследований, натрийуретический, диуретический и антигипертензивный эффекты торасемида в суточных дозах от 2,5 до 5 мг сравнимы с таковыми 25 мг гидрохлоротиазида, 25 мг хлорталидона и 2,5 мг индапамида в сутки и превосходили действие фуросемида, назначенного в дозе 40 мг 2 раза в сутки. Торасемид снижал концентрацию калия в сыворотке в значительно меньшей степени, чем гидрохлоротиазид и другие тиазидные диуретики, и практически не вызывал нарушений углеводного и липидного обменов [3, 8].
Проведенные экспериментальные и клинические исследования показали, что торасемид ингибирует реабсорбцию натрия и хлоридов в восходящей части петли Генле. В отличие от фуросемида эффект торасемида развивается более плавно и сохраняется дольше, при этом происходит меньшее увеличение экскреции калия и блокируются эффекты альдостерона [9, 10]. Наличие плавного и длительного диуретического действия сделало возможным более широкое применение торасемида для лечения АГ [4].
Максимальный антигипертензивный эффект достигается приблизительно после 12 недель использования и остается устойчивым при длительной терапии. Известно, что у больных мягкой и умеренной АГ субдиуретические дозы торасемида эффективны более чем в 70% случаев, что сопоставимо с эффективностью наиболее часто назначаемых антигипертензивных препаратов [11, 12].
На основании результатов проведенных сравнительных исследований [1, 13–17] можно сделать вывод, согласно которому доза торасемида 2,5 мг/сут для лечения АГ оптимальна. Для больных мягкой и умеренной АГ эта доза эффективна в 60–70% случаев, что сопоставимо с эффективностью наиболее часто назначаемых антигипертензивных препаратов. Торасемид «выдержал испытание» в нескольких сравнительных исследованиях. Препаратами сравнения были тиазидные и калий-сберегающие диуретики. Есть все основания полагать, что эффект торасемида развивается более постепенно, чем таковой тиазидных диуретиков; препарат не вызывает столь выраженного пикового снижения АД [18]. Мягкий антигипертензивный эффект торасемида особенно важен для пожилых пациентов, у которых тиазидные диуретики могут вызывать выраженные ортостатические реакции. При лечении АГ препарат можно успешно комбинировать с ингибиторами ангиотензинпревращающего фермента и БАБ [10]. При изучении усредненных суточных профилей АД на фоне длительной терапии торасемидом и триамтереном торасемид не изменяет циркадный ритм АД. При АГ торасемид обычно назначают один раз в сутки, при необходимости возможно назначение дважды в сутки [19].
Важное преимущество торасемида заключается в том, что транспорт его к клеткам толстого восходящего сегмента петли Генле во многом осуществляется с током крови. Поэтому его диуретическое и натрийуретическое действия меньше зависят от величины СКФ. Установлено, что фармакокинетические параметры торасемида не меняются при III (СКФ 30–59 мл/мин) и IV (СКФ 15–29 мл/мин) стадиях хронической болезни почек. Период полувыведения и длительность действия торасемида не изменяются по сравнению с таковыми у лиц, имеющих нормальную функцию почек, а кумуляции препарата при почечной недостаточности не происходит [20]. Торасемид метаболизируется цитохромом Р450, чем объясняется отсутствие изменений его фармакокинетических свойств у пациентов с СН или хронической болезнью почек. В связи с этим фармакокинетика торасемида существенно не зависит от функции почек, в то время как период полувыведения фуросемида увеличивается у больных почечной недостаточностью [6].
Главным преимуществом торасемида является наличие у него камедьсодержащей оболочки, которая замедляет высвобождение действующего вещества, что уменьшает колебания его концентрации в крови и, следовательно, обеспечивает более стойкий и длительный эффект [21].
Помимо более длительного диуретического эффекта торасемида при длительном применении больными АГ на фоне снижения СКФ в проводившихся исследованиях отмечается и ряд других важных свойств, выделяющих данный препарат среди не только петлевых диуретиков, но и всего класса диуретических средств. В экспериментальных и клинических исследованиях продемонстрировано торможение миокардиального фиброза при применении торасемида. Морфологическое исследование ткани миокарда межжелудочковой перегородки, полученной при биопсии у пациентов с ХСН II–IV функциональных классов (ФК), выявило достоверное уменьшение экспрессии проколлагена 1-го типа и коллагена 1-го типа в группе пациентов, принимавших торасемид; у тех, кому назначали фуросемид, указанные изменения отсутствовали. Прием торасемида, но не фуросемида сопровождается угнетением карбокситерминальной протеиназы проколлагена 1-го типа – фермента, обусловливающего внеклеточное накопление коллагена в миокарде, активируемое избытком альдостерона [1, 22]. Лечение торасемидом больных ХСН не сопровождается ростом плазменной концентрации норадреналина, в то время как при применении азосемида наблюдалось достоверное увеличение этого показателя (с 370±170 до 481±247 пг/мл, р<0,05). Таким образом, торасемид в отличие от большинства других петлевых диуретиков не усугубляет нежелательную гиперактивацию симпатической нервной системы у пациентов с ХСН и/или стойким снижением СКФ [23].
Торасемид является единственным мочегонным средством, эффективность которого подтверждена в крупных многоцентровых исследованиях [24–26]. Так, в одно из самых крупных до настоящего времени исследований TORIC (TORasemide In Chronic heart failure) были включены 1377 больных ХСН II–III ФК, рандомизированных к приему торасемида (10 мг/сут) или фуросемида (40 мг/сут), а также других диуретиков. В исследовании оценивали эффективность, переносимость терапии, динамику клинической картины, а также смертность и концентрацию калия в сыворотке крови. По результатам данного исследования, терапия торасемидом была достоверно эффективней, позволяла улучшать ФК у пациентов с ХСН и значительно реже на данной терапии отмечалась гипокалиемия (12,9 против 17,9% соответственно; р=0,013). Также в ходе исследования была выявлена достоверно более низкая общая смертность в группе пациентов, принимавших торасемид (2,2 против 4,5% в группе фуросемида/другие диуретики; p<0,05).
В целом исследование TORIC показало, что у больных ХСН терапия торасемидом по сравнению с фуросемидом или другими диуретиками ассоциируется со снижением общей, сердечно-сосудистой и внезапной смертности на 51,5%, 59,7 и 69,9% соответственно [26].
Полученные данные свидетельствуют о том, что терапия торасемидом более эффективно и безопасно улучшает клинический статус пациента, тем самым снижает число госпитализаций в стационар, а также имеет более благоприятный прогноз для больных ХСН, что напрямую отражает фармакоэкономическую выгоду для государства при лечении пациентов с ХСН оригинальным петлевым диуретиком пролонгированного действия — торасемидом.
Достоверное снижение общей и сердечно-сосудистой смертности на фоне торасемида напрямую связано с влиянием препарата на ремоделирование сердца за счет уменьшения конечного диастолического объема левого желудочка (КДО ЛЖ) [27]. На основе этих данных возникло предположение о способности торасемида уменьшать активацию проколлаген-I-карбоксипротеиназы, что способствует замедлению фиброза стенки ЛЖ [28]. В исследовании TORAFIC было подробно изучено действие пролонгированной формы торасемида на замедление кардиального фиброза. Согласно полученным данным, достоверного влияния на уровень проколлаген-I-карбоксипротеиназы не было выявлено [29]. Таким образом, уменьшение КДО ЛЖ вследствие применения торасемида, скорее всего, связано с закономерным уменьшением объема циркулирующей крови. Однако одно остается неоспоримым фактом: торасемид достоверно снижает выраженность ремоделирования миокарда желудочков.
Торасемид, как и все диуретики, обладает антигипертензивным эффектом, но обычно петлевые диуретики используют лишь при гипертонических кризах и резистентности к тиазидным диуретикам. Торасемид — первый петлевой диуретик, получивший более широкое применение лицами с АГ. Антигипертензивный эффект торасемида обусловлен снижением общего периферического сосудистого сопротивления за счет нормализации нарушений электролитного баланса, в основном – снижения содержания ионов кальция в гладкомышечном слое артерий [30]. Доказаны прямые сосудистые эффекты торасемида, выражающиеся в достоверном увеличении вазодилатации как у здоровых волонтеров, так и у пациентов с АГ с помощью механизма, связанного с высвобождением оксида азота (NO), а также с блокирующим воздействием в отношении вазоконстрикторного действия эндотелина-1 [31]. Механизм антигипертензивного действия торасемида объясняется его антиальдостероновыми свойствами: блокадой АII-индуцированной продукции альдостерона и уменьшением связывания альдостерона в тубулярных клетках почек [11]. Наличие антиальдостеронового эффекта у торасемида немаловажно, т.к. позволяет не только строго контролировать АД, но и замедлять прогрессирование поражений органов-мишеней, во многом опосредуемых именно избытком альдостерона, наблюдающимся у пациентов с АГ. Известно, что на фоне приема торасемида уменьшается активность РАС, а также чувствительность рецепторов к AII первого типа. Известно также, что торасемид ингибирует образование тромбоксана-А2 и увеличивает высвобождение простациклина сосудистой стенкой [32, 33].
Пациенты с АГ, как правило, являются коморбидными по сопутствующей патологии, поэтому метаболический профиль при назначении антигипертензивного лечения – это один из ключевых моментов выбора. В исследовании G. Brunner и соавт. с включением 3074 пациентов с АГ была цель оценить метаболический профиль терапии торасемидом. Препарат назначался в дозе 5–10 мг/сут на протяжении 6 месяцев. Согласно полученным данным, торасемид является метаболически нейтральным препаратом, который не способствует повышению уровня глюкозы, мочевой кислоты, общего холестерина, липопротеидов низкой плотности, липопротеидов высокой плотности и калия [34]. На основе данных результатов возможно применение торасемида пациентами с АГ и сахарным диабетом, наличием гиперурикемии, дислипидемии.
Несомненно, полезным для подбора лечения больных будет более широкое использование комбинированного суточного мониторирования АД и диуреза (КСМАДД). Это исследование позволяет выявлять показание к применению диуретического средства – наличие ассоциированного с АГ водного дисбаланса – и использовать в качестве критерия эффективности лечения степень его восстановления [4]. Применение КСМАДД позволило сформулировать важный количественный критерий назначения торасемида – наличие дневной задержки жидкости (дневной диурез менее 50%) с никтурией. Клинический анализ показал, что подобная ситуация наиболее часто развивается у пожилых пациентов с длительным стажем АГ, у пациентов с избыточной массой тела, при гиподинамии, у курильщиков и лиц, злоупотребляющих алкоголем. Перечисленные клинические критерии могут быть использованы при решении вопроса о назначении диуретической терапии в антигипертензивных целях [4].
Торасемид является эффективным петлевым диуретиком. Высокая биодоступность и более длительная продолжительность действия делают применение торасемида при ряде патологических состояний более предпочтительным, чем традиционных диуретиков. Торасемид – перспективное средство для лечения АГ как в виде монотерапии, так и в комбинации с другими антигипертензивными препаратами. Побочные эффекты торасемида количественно и качественно не отличаются от побочных эффектов других диуретиков. Препарат даже при длительном применении практически не влияет на уровень кальция крови и метаболизм липидов [10].
Таким образом, торасемид благодаря уникальному фармакологическому профилю, наличию плейотропных свойств, нейтральному метаболическому воздействию имеет преимущества перед другими петлевыми диуретиками по эффективности, безопасности и приверженности лечению пациентов с АГ и ХСН. Все эти свойства делают торасемид достойным широкого применения в современной клинической практике.



