Основные функциональные расстройства (ФР) желудочно-кишечного тракта (ЖКТ), с которыми сталкиваются интернисты, – функциональная диспепсия (ФД) и синдром раздраженного кишечника (СРК). Данные заболевания представляют собой функциональные симптомокомплексы гастродуоденальной области и кишечника в отсутствие любых органических, системных и/или метаболических патологических процессов, способных объяснить имеющуюся клиническую симптоматику [1]. Римские критерии-III (РК-III) систематизировали подходы к функциональным синдромам ЖКТ: ФД (FSD – functional gastroduodenal disorders) и СРК (IBS – irritable bowel syndrome) [2]. Однако, как показывает практика, клиническая картина ФД и СРК слагается не только из симптомов, предлагаемых РК-III, но и массы жалоб, не связанных с данной патологий, но играющих немаловажную роль в снижении качества жизни пациентов. Кроме диспепсических и кишечных жалоб у больных ФД и СРК зачастую присутствуют симптомы, относящиеся к другим отделам ЖКТ (синдром «перекреста», или «overlap syndrome»), а также вегетативные дисфункции: головная боль, кардиалгии, гипервентиляционый синдром, нейрогенный мочевой пузырь. Кроме того, ФР ЖКТ часто коморбидны с хронической тазовой болью, диссомнией, фибромиалгией, синдромом хронической усталости, эректильной дисфункцией, тревожно-депрессивным синдромом и т.д.
ФД принадлежит к числу наиболее распространенных гастроэнтерологических жалоб и встречается в популяции, по разным данным, от 5 до 70%. В развитых странах Западной Европы она диагностируется примерно у 30–40% населения и служат причиной 4–5% всех обращений к врачам общей практики. В некоторых странах Африки частота синдрома диспепсии в популяции достигает 61%. Наличие диспепсических симптомов существенно снижает качество жизни больных. Однако к врачу обращаются лишь 20–25% больных. При этом, как показали исследования, меньшая часть (35–40%) приходится на долю заболеваний, входящих в группу органической диспепсии, а бóльшая часть (60–65%) – на долю ФД. У женщин ФД встречается в 1,5 раза чаще, чем у мужчин. Наиболее распространена ФД в возрасте 20–40 лет. В более старшем возрасте ФД встречается реже или коморбидна с другими хроническими заболеваниями пищеварительного тракта, обусловливающими клинические проявления [3]. Согласно РК-III, ФД определяется постпрандиальной тяжестью в эпигастрии, чувством раннего насыщения, болями в эпигастрии или жжением в отсутствие органического заболевания, которые объясняют симптомы пациентов. РК-III далее разделяют ФД на постпрандиальный дистресс-синдром (ПДС) и эпигастральный болевой синдром (ЭБС). Кардинальные особенности ПДС – это раннее насыщение и чувство тяжести в эпигастрии после еды, в то время как главной особенностью ЭБС является боль или жжение в эпигастральной области [4].
СРК – функциональное заболевание, этиология которого до конца не известна, а в лечении его остается больше вопросов, чем ответов. СРК объединяет такие клинические состояния, как боли и/или дискомфорт в животе, которые облегчаются после дефекации и связаны с изменением частоты дефекации и/или формой фекалий [5]. СРК был даже определен как синдром «войны в Персидском заливе», когда много солдат, которые участвовали в войне в Персидском заливе 1991 г., страдали от этого заболевания [6]. Распространенность СРК в большинстве стран мира составляет в среднем 20%, варьируясь от 9 до 48% в различных популяциях. Социальный и культурный уровни населения во многом определяют показатель обращаемости населения по поводу заболевания. Исследования, проведенные в США, показали, что СРК приводит к заметным финансовым потерям для работодателей. Распространенность СРК, например, в Турции 7,4–19,1% и чаще встречается у женщин от 64 до 69% [7, 8]. Аналогичные показатели были зарегистрированы в США и Европе и в диапазоне от 6,2 до 25% [9, 10]. Многие пациенты с СРК не обращаются за помощью своевременно, а когда они это делают, диагноз может оказаться сложной задачей. Наличие СРК является тем заболеванием, которое встречается в популяции от 5 до 20%, что описывается в ряде обзоров [11–13]. Распространенность заболевания варьируется в зависимости от диагностических тестов, используемых для определения СРК: от критериев Мэннинга, которые не определяют минимальной временной продолжительности симптомов и приводят к более высокой распространенности заболевания, чем РК [14].
В целом распространенность увеличивается среди молодых людей, женщин и тех пациентов, которые страдают другими функциональными заболеваниями ЖКТ [15]. В России за медицинской помощью обращаются не более 10% больных, страдающих СРК, поэтому сведения о частоте и распространенности заболевания нельзя считать достоверными. Подавляющее большинство, 55% пациентов, впервые обращаются к участковым терапевтам, составляя 12% от всего числа больных. Впервые приходят к гастроэнтерологу 25% пациентов, что составляет 28% контингента больных, наблюдающихся у гастроэнтеролога. В структуре гастроэнтерологической патологии на СРК приходится 28–70% всех обращений за медицинской помощью. На лечение больных СРК уходит 50% рабочего времени врача-гастроэнтеролога. Примерно 15% больных изначально обращаются к психиатру по поводу той или иной психопатологии, сопровождающей течение СРК. К врачам других специальностей – чаще всего к гинекологам, хирургам, эндокринологам, попадают 5% больных [16]. Предикторы для обращаемости за медицинской помощью при СРК включают тяжелые симптомы (в частности, боль) и психологические проблемы (например, тревога, депрессия, насилие, болезни поведения, соматические атрибуции).
Положительная характеристика СРК заключается в том, что при этом не увеличивается риск развития более серьезных заболеваний, таких как неспецифический язвенный колит и рак толстой кишки. С другой стороны, это расстройство раздражает (в лучшем случае) или становится изнурительным и тревожным (в худшем) и может быть трудным для диагностики и лечения, резко ухудшая качество жизни пациентов [17].
СРК имеет определенную симптоматику – АВСD синдрома раздраженной кишки (The ABCDs of irritable bowel syndrome) [18]:
- А – боль в животе или дискомфорт, обычно в нижней части живота, но может быть без четкой локализации по всему животу (Abdominal pain or discomfort).
- В – вздутие живота или ощущение распирания (Bloating or visible distention).
- С – запор: затрудненная эвакуация при дефекации или редкая дефекация (Constipation: hard, difficult-to-evacuate, or infrequent stools).
- D – диарея: кашицеобразный, водянистый или частый стул (Diarrhea: loose, watery, or frequent stools).
Экстракишечными симптомами являются такие, как усталость, головная боль, боли в спине, боль в мышцах, нарушения сна (Extra-bowel symptoms such as fatigue, headache, backache, muscle pain, and sleep disturbance).
Функциональные заболевания ЖКТ, как говорилось выше, достаточно часто встречаются в популяции. Тем не менее лишь часть пациентов с этими заболеваниями обращаются в лечебные учреждения. Пациенты с легкой и часто средней степенью тяжести ФР ЖКТ не обращаются к врачу, т.к. достигают ремиссии заболевания самостоятельно. Большинство из них занимаются самолечением, получая информацию из средств массовой информации (Интернет, телевидение, печатные издания). Немаловажную роль в лечении таких больных играют аптеки. И только небольшая часть пациентов со средней степенью тяжести и пациенты с тяжелым течением ФР ЖКТ регулярно посещают врачей: от терапевтов или гастроэнтерологов до психиатров, иногда длительно не достигая ремиссии. Адекватная медицинская помощь при этом необходима всем пациентам. Автор статьи периодически сталкивается с ситуацией, когда пациенту с ФР ЖКТ назначают целую группу различных препаратов, например тройные/четвертные дозы ингибиторов протонной помпы, мебеверин вместе с итопридом или другие лекарственные комбинации с антагонистическим механизмом действия, а в итоге – клиническая картина остается прежней или ухудшается. Бывают и другие ситуации на приеме; например, пациенту порекомендовали в аптеке препарат Иберогаст®, но предупредили, что без назначения врача его можно принимать только месяц. По истечении месяца пациент прекращает принимать Иберогаст®, симптоматика возвращается и он идет к врачу и просит продлить рекомендации по приему препарата, который значительно улучшил его качество жизни (из собственной практики автора статьи).

Как известно, постановка диагноза ФР ЖКТ сложна и трудоемка. Очень важно, чтобы пациент получал адекватное лечение уже на этапе обследования. Стандарты диагностики ФД и СРК включают ряд этапных исследований, в т.ч. необходимо учитывать коморбидность ФР ЖКТ с другими заболеваниями. Еще до появления РК-III в ряде исследований изучали коморбидность ФД, гастроэзофагеальной рефлюксной болезни и СРК с использованием II Римских критериев. Например, в одном из этих исследований отмечали частое сочетание симптомов диспепсии верхнего и нижнего этажей ЖКТ у пациентов с СРК (в 75% случаев), особенно у пациентов с СРК-запорами [19]. Еще одно большое исследование выявило частое сочетание ФД, гастроэзофагеальной рефлюксной болезни и СРК с высокой распространенностью диспепсии (23%) наряду с внекишечными болями – такими, как головная боль (27%) и боли в пояснице (16%) [20]. Объем исследований при ФЗ ЖКТ подробно описан в ряде рекомендаций и стандартов [21, 22]. Диагностический поиск нередко занимает весьма длительный период, на этапе которого пациент или получает неадекватное лечение, или не получает его вовсе.
Главной задачей в лечении пациентов с ФР ЖКТ остается улучшение качества их жизни. Кроме «изматывающего» болевого синдрома пациентов беспокоит диспепсия – желудочная или кишечная. У части больных формируется ситофобия (страх приема пищи) из-за постпрандиального ухудшения самочувствия. Современные фармакологические подходы к лечению ФР ЖКТ основаны исключительно на купировании симптомов, многие пациенты остаются неудовлетворенными и недовольными своим качеством жизни. Кроме того, медикаментозные подходы к лечению нередко связаны с побочными эффектами, которые уменьшают пользу терапии для пациента с точки зрения результатов лечения [23, 24]. Лечение, например, СРК также зависит от конкретного его подтипа. В то время как пациенты с СРК с запорами в основном страдают от боли в животе из-за медленного кишечного транзита и редких дефекаций, пациенты с СРК с диареей страдают от социальной стигмы в связи с частыми дефекациями, что требует непосредственной близости к туалетной комнате, но больных обоих подтипов беспокоят вздутие живота и повышенный метеоризм [24–27]. Коморбидность ФР ЖКТ с депрессивными и тревожными расстройствами четко определены, хотя по-прежнему неизвестно, какая патология из них служит причиной, а какая следствием [28–31]. Эффективность антидепрессантов в лечении этих заболеваний свидетельствует о том, что некоторые депрессивные и тревожные расстройства играют серьезную роль в патофизиологии ФР ЖКТ [30–34]. Установлено, что «ось кишка–мозг», которую также называют брюшной нервной системой, соединяет афферентные и эфферентные нейроны и влияет на моторику кишечника, главным образом на его серотонинергическую и холинергическую иннервацию [35, 36].
Как уже упоминалось, в настоящее время фармакологические подходы к лечению обеспечивают пациентам с ФР ЖКТ ограниченное симптоматическое облегчение. Это приводит к значительному увеличению использования дополнительных и альтернативных лекарственных средств пациентами и интернистами, чтобы добиться необходимого повышения качества жизни [37–40]. Важно отметить, что медикаментозное лечение не должно быть заменено на альтернативные методы: необходим интегративный подход, который обеспечит как максимальное облегчение симптомов, так и повышение качества жизни пациентов с ФР ЖКТ. Лекарственная терапия ФР ЖКТ подробно описана в различных рекомендациях и стандартах.
Широкий выбор альтернативных методов лечения (АМЛ) включает основные изменения в диете и образе жизни, такие как увеличение потребления клетчатки или регулярные физические упражнения, а также конкретное использование растительных лекарственных средств, механические вмешательства (иглоукалывание или массаж), поведенческую психотерапию терапию (когнитивно-поведенческие, релаксационные методы и гипноз) [41, 42]. AMЛ часто используются для терапии хронических заболеваний либо самостоятельно, либо в сочетании с фармакотерапией. Около половины пациентов с СРК используют АМЛ отдельно или в сочетании с назначенным лекарственным препаратом [40, 43]. Последние систематические обзоры показывают, что различные варианты AMЛ могут принести пользу больным ФР ЖКТ и улучшить качество их жизни [44, 45].
Наиболее часто используемыми вмешательствами АМЛ, которые были оценены в клинических испытаниях, являются диетические изменения, использование пробиотиков, лечебная физкультура, фитотерапия, сочетание гипнотерапии, акупунктуры и методов релаксации [46].
Помимо диеты и изменения образа жизни самым частым является использование фитопрепаратов в виде отдельных растений или в комбинации. Многие обычно используемые фитопрепараты эволюционировали из народных и традиционных средств для лечения желудочно-кишечных расстройств. Из лекарственных средств растительного происхождения большие надежды при лечении функциональных заболеваний ЖКТ связывают с использованием комбинированных препаратов, содержащих большое количество активных ингредиентов с различными точками приложения, т.е. обладающих многофакторным действием [47]. Эта современная концепция – многоцелевая терапия – представляется вполне обоснованной при лечении таких гетерогенных (полиэтиологических) расстройств, как ФД и СРК. Это и определяет место и роль в терапии функциональных желудочно-кишечных расстройств немецкого фитофармацевтического препарата Иберогаст®, который в полной мере соответствует концепции многоцелевой терапии [48–51].
Иберогаст® – это комбинированный продукт, к которому проявили интерес пациенты и медицинские работники, смесь из девяти растительных экстрактов растений [52, 53.]. Раститель-ный комбинированный препарат Иберогаст® (Iberogast®, Steigerwald Arzneimittelwerk GmbH, Дармштадт, Германия) был подробно изучен при лечении функциональных желудочно-кишечных расстройств верхней и нижней частей живота. Иберогаст® содержит спиртовые экстракты из вытяжки свежего растения иберийка горькая (Iberis amara totalis recens) и восьми высушенных лекарственных растений: корень дягиля (Angelicae radix), цветки ромашки (Matricariae flos), плоды тмина (Carvi fructus), плоды расторопши (Cardui mariae fructus), листья мелиссы (Melissae folium), листья мяты перечной (Menthae piperitae folium), трава чистотела (Chelidonii herba), корни солодки (Liquiritiae radix), и используется для лечения ФР ЖКТ в течение пяти десятилетий [54]. Переносимость Иберогаста® была благоприятной как в клинических, так и в постмаркетинговых исследованиях.
U. Simmen и соавт. изучили действие компонентов Иберогаста® на конкурентное связывание интестинальных рецепторов. Иберогаст® показал сродство к интестинальным 5-НТ3, 5-НТ4, мускариновым М3, опиоидным рецепторам, которое более чем в 10 раз выше именно к трем последним типам рецепторов. Сравнение девяти компонентов препарата Иберогаст по связывающей способности к этим рецепторам выявило разную степень селективности. В то время как экстракт иберийки горькой селективно ингибирует связывание с мускариновыми М3-рецепторами, спиртовые экстракты чистотела и ромашки были селективны к серотониновым 5-НТ4-рецепторам, а экстракт корня солодки – к серотониновым 5-НТ3-рецепторам. Эти данные показали вовлеченность в связывание с рецепторами семи из девяти компонентов Иберогаста®, используемого для лечения таких функциональных желудочно-кишечных заболеваний, как ФД и СРК. В заключение можно отметить, что данные in vitro подтвердили значимость компонентов препарата Иберогаст® для эффективного лечения функциональных желудочно-кишечных заболеваний, т.к. они действуют на ключевые мишени, включая 5-НТ3, 5-НТ4, М3 и опиоидные рецепторы [55]. Мы составили сводную таблицу по основным механизмам действия Иберогаста®, которые были изучены в различных исследованиях (табл. 1).
J. Melzer и соавт. провели анализ плацебо-контролируемых исследований с Иберогастом® с участием 273 пациентов с ФД [56]. Авторы сделали вывод, что Иберогаст® является значительно более эффективным, чем плацебо, средством для облегчения симптомов у пациентов с ФД.
Иберогаст® для лечения СРК изучался в течение 4 недель в двойном слепом рандомизированом плацебо-контролируемом исследовании с участием 208 пациентов с различными подтипами СРК в США [57]. Исследо-вание показало, что Иберогаст® значительно улучшает качество жизни и уменьшает боль в животе у больных СРК [58]. Иберогаст® был признан средством целевой терапии СРК в качестве потенциального адьювантного лечения [59].
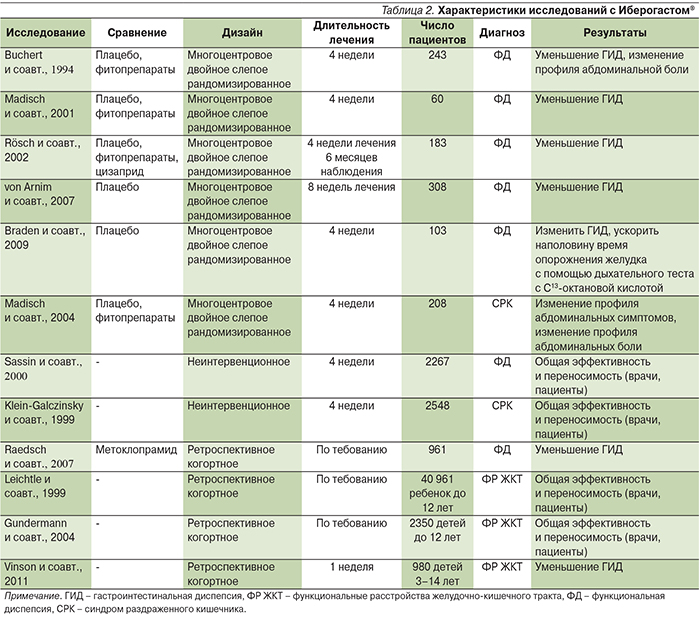
B. Ottillinger и соавт. проанализировали ряд клинических исследований с Иберогастом® (табл. 2) и представили информацию об их результатах [58].
В своей работе они приводят:
Шесть контролируемых и рандомизированных исследований с Иберогастом®, пять по ФД и одно по СРК [53, 57, 60–63].
Исследования по ФД также были включены в несколько мета-анализов [56, 64, 65].
Два постмаркетинговых исследования различных желудочно-кишечных заболеваний, в т.ч. ФД и СРК, и одно ретроспективное когортное исследование по ФД. [66–68].
Два ретроспективных исследования наблюдения и одно неинтервенционное исследование детей с желудочно-кишечными симптомами, в т.ч. ФД и СРК [69–71].
В некоторых странах Иберогаст® утвержден в качестве единственного препарата для лечения ФД и СРК. Еще в ряде стран Иберогаст® включен в руководства по терапии функциональных желудочно-кишечных расстройств [72, 73]. Доклинические и клинические исследования показали, что Иберогаст® не имеет значимых побочных эффектов, в т.ч. гепатотоксичности [58].
Сегодня, когда происходит достаточно много обращений пациентов с ФР ЖКТ с болевым абдоминальным и диспепсическим синдромами в аптеки, к терапевтам и гастроэнтерологам, очень важно давать им адекватные рекомендации по лечению: на первом этапе в период обследования, в комплексной терапии заболевания, в период затухающего обострения и по потребности в период ремиссии. Иберогаст® является препаратом выбора на всех этапах лечения ФР как верхнего, так и нижнего этажей ЖКТ.
Разнонаправленные терапевтические эффекты, хорошая переносимость без значимых побочных эффектов, возможность длительного применения – отличительные характеристики Иберогаста®.


