Введение
Мигрень и головокружение – самые распространенные неврологические расстройства в популяции, нередко их сочетание наблюдается у одного и того же пациента. Некоторые эпидемиологические исследования показали, что сочетание мигрени и головокружения встречается чаще, чем этого можно было бы ожидать при случайном совпадении двух весьма распространенных симптомов. Более того, у больных мигренью часто выявляются те или иные вестибулярные нарушения. Эти данные послужили основанием к изучению взаимосвязи между мигренью и головокружением, легли в основу представления о мигрень-ассоциированном головокружении, или о вестибулярной мигрени (ВМ), которая в настоящее время остается одной из наиболее дискуссионных проблем неврологии.
Для определения одних и тех же по сути состояний используют различные термины: «мигрень-ассоциированное головокружение», «доброкачественное рецидивирующее головокружение», «связанная с мигренью вестибулопатия» и др. Впервые ВМ была описана R. Slater в 1979 г. [22].
Эпидемиология вестибулярной мигрени
Частота ВМ среди населения, по последним эпидемиологическим данным, составляет около 1% [6]. ВМ может впервые возникнуть в любом возрасте. Женщины чаще, чем мужчины, подвержены ВМ. Так, мета-анализ нескольких крупных популяционных исследований, включивших более 35, 461 млн человек в возрасте 18–65 лет, показал, что распространенность мигрени составляет около 12% с соотношением мужчины/женщины, равным 0,4 [19]. Распространенность головокружения составляет около 20–30%, оно также доминирует над женщинами (соотношение мужчины/женщины равно 0,37), а пациенты с коморбидностью этих состояний составляют в общей популяции около 4%.
Крупное эпидемиологическое популяционное исследование в Германии показало, что распространенность мигрени среди населения в целом составляет около 14%, а распространенность головокружения в течение жизни – 7%. Вероятность их случайного совпадения составляет около 1%, что позволяет сделать следующий вывод: среди взрослого населения наличие в анамнезе как мигрени, так и головокружения отмечается примерно в 3 раза чаще, чем это можно было бы наблюдать при простом совпадении, а именно у 3,2% людей в популяции [6]. Существуют и другие данные, свидетельствующие о неслучайной коморбидности мигрени и головокружения. Около 61% пациентов с вестибулярными нарушениями страдают мигренью. В исследовании наличие головокружения было выявлено у 47,5% пациентов, страдающих мигренью, с интенсивностью головной боли от 7 и более баллов по шкале ВАШ, где 0 баллов – это отсутствие боли, а 10 баллов – невыносимая головная боль [20].
Эпидемиологические исследования ассоциаций мигрени и головокружения подчеркивают двунаправленный характер взаимоотношений между ними. С одной стороны, мигрень чаще встречается среди пациентов с головокружением. Так, распространенность мигрени, полностью соответствующей критериям Международной классификации головных болей (МКГБ)-3 бета версии, среди пациентов, страдающих головокружением (38%), оказалась в 1,6 раза выше, чем среди пациентов, обратившихся за медицинской помощью с другими жалобами (24%).
Y. Cha и соавт. [13] обнаружили, что из 208 пациентов с доброкачественным рекуррентным головокружением 87% страдали мигренью, причем 70% из них отвечали диагностическим критериям ВМ, предложенным H. Neuhauser и соавт. (табл. 1) [29]. По данным другого исследования, из 72 участников с доброкачественным рекуррентным головокружением мигренью страдали в 6 раз больше пациентов, чем в контрольной группе, сопоставимой по полу и возрасту (61 и 10% соответственно). C. Rassekh и L. Harker выявили, что распространенность мигрени среди пациентов с доброкачественным рекуррентным головокружением составляет 81%, тогда как среди пациентов с болезнью Меньера – 22% [18]. При этом у пациентов с головокружением мигрень вызывает большую дезадаптацию и чаще приводит к развитию симптомов депрессии.
Коморбидность с головокружением характерна в большей степени именно для мигрени, а не для других форм головной боли: распространенность головокружения среди пациентов с головной болью напряжения составляет 8%, а среди пациентов с мигренью – 27%. По другим данным, на головокружение жалуются 30% пациентов с головной болью напряжения и 55% пациентов с мигренью. При этом несистемное головокружение возникает у 28–30% пациентов с мигренью, а системное – у 25–26% [18].
Мигрень нередко сосуществует с некоторыми периферическими вестибулярными заболеваниями, такими как болезнь Меньера и доброкачественное пароксизмальное позиционное головокружение, так что часть случаев совпадения мигрени и головокружения, по-видимому, может быть объяснена этим обстоятельством [22].
Таким образом, эпидемиологические исследования, в которых изучались различные варианты ассоциаций мигрени и головокружения, показывают, что между ними существуют более тесные взаимосвязи, чем это может наблюдаться при случайном совпадении этих весьма распространенных клинических симптомов.
Виды головокружения при мигрени
Под понятием головокружения при мигрени часто имеют в виду весьма различные ощущения. Принято выделять две разновидности головокружения – системное и несистемное. Под системным головокружением понимают ощущение мнимого движения или вращения окружающих предметов вокруг собственного тела или самого тела в пространстве, тогда как несистемным головокружением называют различные состояния, среди которых прежде всего выделяют ощущение неустойчивости, дурноты, «легкости» в голове или приближающейся потери сознания. Собственно, системное головокружение, определяемое как иллюзия вращательного движения, служат отличительным признаком повреждения вестибулярной системы. Мигрень-ассоциированное головокружение – это приступы умеренного или выраженного головокружения, неустойчивости, тошноты, иногда рвоты, которые сопровождаются мигренозной головной болью. Такие приступы могут продолжаться от нескольких минут до нескольких часов, реже – более суток. В период приступа головокружения могут возникать спонтанный нистагм, фото- и фонофобия [26].

Выделяют два варианта системного головокружения при мигрени: спонтанное и позиционное [25]. В отличие от болезни Меньера приступ головокружения при ВМ не сопровождается ухудшением слуха [24]. Вывод о вестибулярном происхождении головокружения при ВМ делается на основании наличия во время приступа патологического нистагма, указывающего на центральную вестибулярную дисфункцию [21]. В некоторых случаях признаки вестибулярной дисфункции находят при тщательном обследовании и в межприступном периоде. Эти находки отличают мигрень от головокружения, возникающего вследствие психических заболеваний, побочных эффектов антимигренозных средств и ортостатической гипотонии. Как уже указывалось выше, во время пароксизма мигренозного головокружения могут отмечаться сопутствующие симптомы, типичные для приступа мигрени: фотофобия (70%), фонофобия (64%) и даже зрительные феномены (36%). Снижение слуха и шум в ушах в целом не характерны [22].
Патогенез вестибулярной мигрени
ВМ является заболеванием, развитию которому способствуют генетические, эпигенетические факторы, а также особенности окружающей среды. Патофизиология ВМ на сегодняшний день недостаточно известна, тем не менее за последние несколько лет проведено множество исследований, которые вносят значительный вклад в понимание нейрофизиологических процессов, участвующих в развитии ВМ. Текущие гипотезы основываются главным образом на знании патофизиологии самой мигрени [31]. В настоящее время рассматриваются три основных механизма развития мигрени. Первый связан с сужением или расширением внутри- и внечерепных артерий. Второй обусловлен разрядом, возникающим в триггерной зоне среднего мозга (возможно, в серотонинергических дорсальных ядрах шва ствола мозга). Наконец третий механизм представляет собой возбуждение нейронов ядра тройничного нерва в стволе мозга (т.н. тригемино-васкулярной системы – ТВС). Аксоны этих нейронов заканчиваются в стенках артерий и выделяют вазоактивные нейропептиды. Роль каждого из этих механизмов в патогенезе мигрени не совсем ясна.
В настоящее время наиболее распространена гипотеза возникновения вестибулярных симптомов при мигрени, предложенная F.M. Cutrer и R.W. Baloh в 1992 г. [21]. Согласно этой гипотезе, ВМ рассматривается как мигренозная аура, обусловленная распространяющейся депрессией (волной торможения) по коре головного мозга от первичного очага. Этой волне сопутствует сужение сосудов, сменяющееся их расширением. В тех случаях когда приступ головокружения не сопровождается головной болью, вестибулярные нарушения могут быть обусловлены высвобождением нейропептидов (субстанция Р, нейрокинин А, кальцитониноподобный пептид). Нейропептиды обладают стимулирующим действием на фоновую импульсную активность сенсорного эпителия внутреннего уха и вестибулярных ядер ствола мозга [22]. Асимметричное высвобождение нейропептидов приводит к возникновению головокружения. При симметричном высвобождении нейропептидов больной испытывает дискомфорт во время движения из-за повышенной фоновой импульсной активности вестибулярных структур. Позиционное головокружение, возникающее в конце приступа вестибулярной мигрени, Cutrer и Baloh объясняют гормоноподобным действием кальцитониноподобного пептида и других нейропептидов, проникающих во внеклеточную жидкость. Участие стволовых механизмов в генерации феномена распространяющейся корковой депрессии (РКД) при ВМ обсуждается и в концепции J. Furman и соавт. [23], согласно которой в основе мигренозного головокружения лежат функциональные нарушения между вестибулярными ядрами, тригеминальной системой и таламокортикальными связями, а мигренозное головокружение в этих случаях может быть эквивалентом аллодинии и центральной сенситизации [18, 22].
Кроме того, проведены исследования, в которых доказывается наследственный характер ВМ с передачей по аутосомно-доминантному типу [12]. Bahmad и соавт. изучали семью, включавшую 10 членов, страдавших ВМ с аутосомно-доминантным типом наследования. Генетический анализ показал, что ген заболевания расположен между маркерами rs244895 и D5S2073 в хромосоме 5q35 [31].
В работе Juan M. Espinosa-Sanchez и Jose A. Lopez-Escamez, изучавших наличие генетического фактора в патогенезе ВМ, было выявлено, что мутации в гене CACNA1A, кодирующем центральную порообразующую субъединицу CaV2.1-й (P/Q-типа) кальциевых каналов, вызывают по крайней мере три неврологических синдрома, при которых возникает патология кальциевых каналов: эпизодическую атаксию 2-го типа, семейную гемиплегическую мигрень 1-го типа и спиноцеребеллярную атаксию 6-го типа. Накопленные данные свидетельствуют о том, что в патогенез мигрени и ВМ может быть вовлечена патология субъединицы CaV2.1 кальциевого канала. Следовательно, мигрень может считаться результатом патологии каналов, в которых РКД является результатом различных мутаций в гене, увеличивающих чувствительность кальциевых каналов к РКД путем воздействия на несколько ионных каналов, участвующих в основном в глутаматном гомеостазе. Таким образом, конечный результат будет приводить к увеличению концентрации глутамата и ионов К+ во внеклеточном пространстве синоптической щели, которые могут способствовать активации ТВС, центральной сенсибилизации и инициации РКД [31]. В работе Juan M. Espinosa-Sanchez и Jose A. Lopez-Escamez также изучались семейные случаи возникновения ВМ, что, как говорилось выше, подтверждает генетический генез возникновения данной болезни. В одной семье может быть наличие нескольких родственников, страдающих ВМ, некоторые члены семьи могут иметь простую мигрень, а некоторые с детства страдают доброкачественным пароксизмальным головокружением, что свидетельствует о наличии фенотипической гетерогенности данного заболевания [31].
Следует также упомянуть, что в совместной работе T. Brandt, A.M. Bronstein описан механизм шейного головокружения, которое может быть следствием нарушения цервикопроприоцептивных механизмов, что может наблюдаться и при ВМ [33].
С учетом множества потенциальных взаимодействий между мигренью и вестибулярной системой вполне вероятно, что головокружения при ВМ являются многофакторными и могут включать как лабиринтные, так и неврологические компоненты.
Вестибулярная мигрень и критерии диагностики
В настоящее время в МКГБ выделено две формы мигрени, проявляющиеся вестибулярным головокружением: базилярная мигрень и доброкачественное пароксизмальное головокружение детского возраста. Обе эти формы крайне редко встречаются в клинической практике. Напротив, ВМ, как свидетельствуют многочисленные эпидемиологические исследования, не является клинической редкостью. Однако дискуссия по поводу клинической самостоятельности, отсутствие утвержденных критериев диагностики и четких представлений о патогенезе болезни позволяют обсуждать эту форму только в Приложении (Appendix) к МКГБ [44].
Диагноз ВМ устанавливается на основании соответствующей клинической картины заболевания. Он наиболее обоснован для больных, имеющих в анамнезе типичные приступы мигрени с аурой или без ауры, у которых возникают приступы головокружения, сопровождающиеся характерной мигренозной головной болью, фото- и фонофобией. Также в период приступа головокружения могут возникать рвота и спонтанный нистагм. Головокружение уменьшается постепенно, при этом может усиливаться при изменениях положения головы, приобретая позиционный характер. При приступе не возникает шум, звон в ушах или снижение слуха. Постоянное сочетание приступа вестибулярного головокружения с мигренозной головной болью отмечается только у части (24%) пациентов с мигренью. При неврологическом обследовании у большинства пациентов выявляется неустойчивость в позе Ромберга и при ходьбе, некоторые пациенты полностью утрачивают способность самостоятельно стоять и ходить, но нормально выполняют координаторные пробы в конечностях.
Клиническая картина приступа головокружения существенно варьируется как у разных пациентов, так и у одного пациента во время различных приступов. Неврологическое исследование вне приступа не выявляет изменений, однако у многих пациентов с ВМ отмечается небольшая неустойчивость в пробе Ромберга и при ходьбе, что отражает имеющуюся дисфункцию вестибулярной системы. При калорической пробе в 10–20% случаев выявляют вестибулярную гипофункцию. При электронистагмографии и видеоокулографии иногда находят небольшие нарушения плавных и саккадических следящих движений глаз, центральный позиционный нистагм. Многие больные вне приступа отмечают повышенную чувствительность к движениям и страдают укачиванием.
Длительность приступа головокружения колеблется от нескольких секунд до нескольких часов и даже дней.
У 10–30% пациентов продолжительность головокружения соответствует таковой мигренозной ауры – 5–60 минут, у 20–30% приступы короткие – менее 5 минут, а у 20–50% пациентов головокружение продолжается от нескольких часов до нескольких суток [20]. Частота возникновения приступов также различна: от нескольких раз в день до одного в несколько лет. Отсутствует определенная регулярность возникновения атак. Непостоянная зависимость развития приступа головокружения и мигрени также вариабельна: головокружение может предшествовать развитию головной боли, возникать во время или после нее. У 45% пациентов мигренозное головокружение всегда сочетается с головной болью, у 48% – не при всех приступах, а в некоторых случаях (6%) головокружение и головная боль никогда не возникают вместе [22].
H. Neuhauser и T. Lepmpert предложили диагностические критерии ВМ (табл. 1), которые широко используются на сегодняшний день в современных клинических исследованиях [29]. Несмотря на то что они еще не получили общего признания, эти критерии имеют практическое значение. Обследование 75 пациентов с достоверным диагнозом ВМ, установленным на основании критериев H. Neuhauser, показало, что спустя 105±16 месяцев у 84% из них диагноз оставался прежним и лишь в 16% случаев был изменен [22, 29].
Важно еще раз подчеркнуть, что диагностические критерии ВМ подразумевают наличие у больного вестибулярного головокружения (т.е. ощущение мнимого вращения или движения окружающих предметов или самого больного в пространстве) или очевидного ощущения неустойчивости, а не таких неспецифических проявлений, как чувство дурноты, слабости, «легкости в голове» или, например, приближающейся потери сознания.
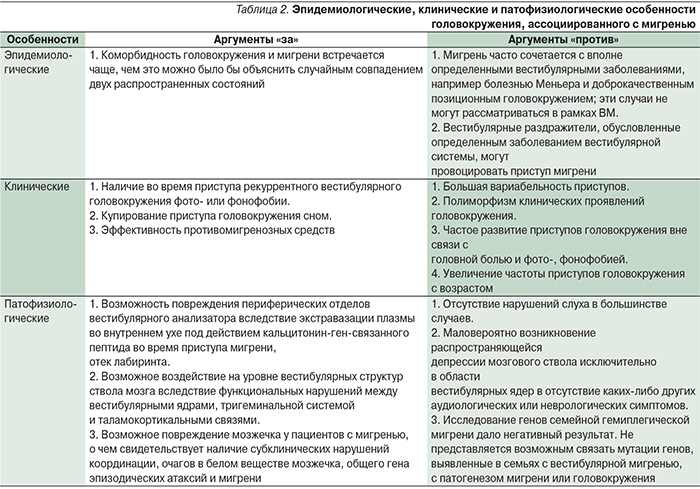
Подводя итоги, на сегодняшний день можно выделить ключевые аргументы «за» и «против» нозологической самостоятельности ВМ, обобщенные в табл. 2.
Развитие приступов вестибулярного головокружения существенно снижает качество жизни пациентов с мигренью. Так, в работе немецких ученых, изучавших качество жизни 4869 пациентов, страдавших ВМ, путем анкетирования по шкале SF-8, было выявлено достоверное снижение качества жизни таких пациентов [30].

Лечение вестибулярной мигрени
В настоящее время терапевтические подходы, ориентированные на лечение ВМ, скудны и недостаточны, а большинство лечебных рекомендаций для ВМ основываются на знаниях, накопленных при лечении простой мигрени.
Для купирования приступов ВМ используют триптаны. Их эффективность в отношении головокружения считается косвенным доказательством мигренозной природы головокружения. Механизм действия триптанов, являющихся селективными агонистами 5-НТ1b/5НТ1d-рецепторов, включает нейрогенный и сосудистый компонент. Триптаны подавляют выход из периферических окончаний тройничного нерва вазоактивных веществ, вызывающих вазодилатацию, и стимуляцию болевых рецепторов нервных окончаний тройничного нерва, а также вызывают сокращение расширенных во время приступа сосудов, что препятствует экссудации и раздражению болевых рецепторов альгогенными веществами, проникающими из плазмы крови в периваскулярное пространство. Кальцитонин-ген-связанный пептид (CGRP), выделяющийся в окончаниях тройничного нерва во время мигренозного приступа, попадает в кровоток и может воздействовать на сенсорный эпителий полукружных каналов на стороне боли и вызывать приступ системного головокружения. Подавляя выделение CGRP, триптаны способны прекращать не только мигренозную боль, но и ассоциированное с ней головокружение. Клиническая эффективность таблеток суматриптана 50 и 100 мг при приеме внутрь при мигрени исследована во множестве слепых плацебо-контролируемых исследованиях [40–43]. Так, при приеме суматриптана в дозе 100 мг уменьшение болевого синдрома почувствовали 59% пациентов против 28% в группе плацебо. Полное купирование атаки удалось достичь в 29% случаев. Эффективность препарата в дозах 50 и 100 мг была сходной, а число нежелательных реакций меньше при приеме меньшей дозы препарата [37, 38].
В Клинике головной боли и вегетативных расстройств им. Александра Вейна было проведено постмаркетинговое исследование препарата Сумамигрен (суматриптан), результаты которого представлены в табл. 3 [39]. В исследовании участвовали 14 пациентов, Сумамигрен использовался для купирования трех приступов, т.е. было проанализировано наличие эффекта препарата в 42 приступах.
Из табл. 3 видно, что действие Сумамигрена начинается быстро: уже через 30 минут после приема препарата достоверное уменьшение болевого синдрома отмечалось у 21,4% пациентов. Через 2 часа у 38% пациентов приступы купировались полностью, у 64% – головная боль уменьшилась наполовину и более. Возврат головной боли – ее повторное усиление или появление после улучшения в результате действия Сумамигрена наблюдалось в 48% приступов. Резистентными к препарату оказались около 15% пациентов. По данным результатов исследований различных триптанов, резистентность к препаратам этой группы колеблется от 20 до 30%. Таким образом, Сумамигрен служит эффективным средством купирования мигренозных приступов, что позволяет также рекомендовать его пациентам, страдающим ВМ [39].
Профилактическое лечение ВМ не отличается от профилактического лечения простой мигрени и включает пропранолол 80–240 мг, метопролол 50–200 мг, бисопролол 5–10 мг или флунаризин 5–10 мг ежедневно. Можно также назначать топирамат в дозе 25–100 мг и вальпроаты в дозе 500–600 мг. Пациенты, преимущественно жаловавшиеся на головокружение с типичной аурой, но без повторяющейся мигренозной головной боли, могут быть успешно пролечены ламотриджином в дозе 25–100 мг в день.
До сих пор нет современных публикаций, посвященных профилактике ВМ. Этот вопрос изучается в проходящих в настоящее время рандомизированных плацебо-контролируемых исследованиях, а до получения их результатов терапевтические тактики, утвержденные при простой мигрени, могут быть применены и к ВМ [34].
Вестибулярная гимнастика оказывает положительное влияние на пациентов с ВМ как в сочетании с медикаментозным лечением, так и в качестве самостоятельного метода лечения [34]. Эффективность вестибулярной гимнастики у пациентов, получавших медикаментозную профилактическую терапию, показана в исследовании с участием 36 пациентов с ежедневными вестибулярными симптомами (20 – с ВМ и 16 – с вестибулярными нарушениями), принимавших участие в 9-дневной реабилитационной программе [36].
Возможно, что при ВМ могут быть эффективны изменения поведения. В одном интересном исследовании, изучавшем эффект отказа от кофеина (n=34), улучшение при применении такой методики было продемонстрировано на 14% пациентов с ВМ. Для сравнения следует отметить, что аналогичное исследование показало, что топирамат уменьшал симптомы у 25% пациентов, а нортриптиллин вызывал снижение головокружения у 46% пациентов (p=0,007). В итоге 75% пациентов с ВМ отметили преимущества такого терапевтического подхода по сравнению с другими методами лечения [34, 35].
Заключение
Таким образом, на сегодняшний день состояние проблемы ВМ содержит множество вопросов, которые пока не находят ответов в современных клинических и экспериментальных исследованиях. Однако накоплено достаточно эпидемиологических, клинических и патофизиологических данных, свидетельствующих о тесной взаимосвязи между мигренью и головокружением. Уточнение деталей этих взаимосвязей требует продолжения исследований в данном направлении. При этом подобные исследования вряд ли возможны без разработки единой терминологии. Необходимо определиться, какие ощущения, называемые пациентами головокружением, могут стать предметом изучения в отношении их взаимосвязи с мигренью. Представляется, что предметом таких исследований могут быть лишь рекуррентное пароксизмальное именно системное (истинное) головокружение и, возможно, неустойчивость. Дальнейшей разработки требуют также терапевтические подходы к лечению ВМ.



