Головная боль и психические расстройства – одно из наиболее актуальных междисциплинарных направлений на сегодняшний день. Взаимосвязь психических расстройств и головной боли чрезвычайно многогранна, имеются общие механизмы развития этих заболеваний, а также диагностические и терапевтические подходы.
Эмоционально-аффективные расстройства, такие как тревога и депрессия, коморбидны многим формам первичных головных болей, но особенно изучены при мигрени. Эти нарушения не только утяжеляют течение мигрени, но и являются доказанными факторами ее хронификации. Аддиктивное поведение и тревожные нарушения лежат в основе развития злоупотребления обезболивающими средствами при головной боли (абузусной головной боли). Наконец выделена группа вторичных головных болей, связанных с психическими расстройствами (глава 12 Международной классификации головных болей III [МКГБ III], включающая головную боль, связанную с соматизированным расстройством [12.1], и головную боль, связанную с психотическим расстройством [12.2]) [9].
Определение, что первично – головная боль или психическое расстройство, может быть весьма сложным. Если головная боль возникла впервые вместе или на фоне уже существующего психического расстройства и имеется отчетливая взаимосвязь с ним, то это вторичная головная боль, связанная с психическим расстройством. Если цефалгия присутствовала до психического расстройства, но с его развитием стала существенно хуже (частота/тяжесть возросла по крайней мере в два раза), то ставятся два диагноза – первичной головной боли и головной боли, связанной с психическим расстройством. Если не прослеживается взаимосвязи между головной болью и имеющимся психическим расстройством, выставляются два диагноза – головной боли и психического расстройства.
Головная боль при психозе и соматизированном расстройстве
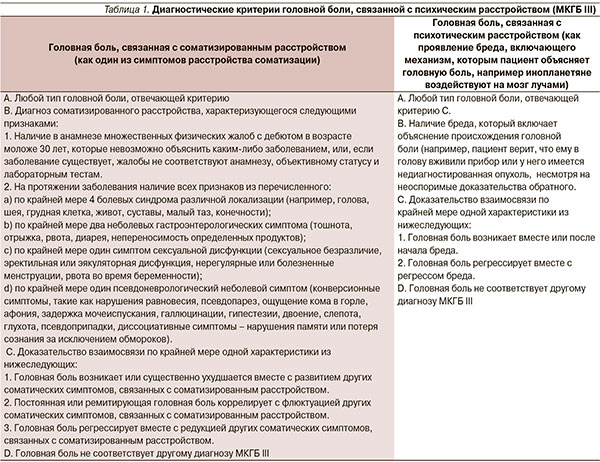
Согласно МКГБ III (2013), вторичные головные боли, связанные с психическим расстройством, включают две основные формы – головная боль при психозе и соматизированном расстройстве (табл. 1). Эти формы головной боли встречаются в практике редко – распространенность в специализированном центре составляет 1,02 % [15]. Головная боль, связанная с психическим расстройством, наиболее часто обладает характеристиками головной боли напряжения (51 %), мигрени (21 %) или имеет атипичные симптомы (26 %). Более чем у половины пациентов отмечается хроническая головная боль [15].
Важно подчеркнуть, что соматизированное расстройство не включено в классификацию психических расстройств DSM-V (2013). Это заболевание перемещено в раздел «Расстройства соматизации», характеризующиеся наличием одного или более соматических симптомов, связанных с диспропорциональными и персистирующими мыслями о серьезности этого симптома (симптомов), сопровождающимися высоким уровнем тревоги относительно своего здоровья и тратой большей части времени и усилий на обследование, лечение и т. д.
Головную боль, связанную с психотическим расстройством, необходимо дифференцировать с редким проявлением ауры мигрени, которая также может проявляться психическими нарушениями. Одним из примеров является синдром Алисы в Стране Чудес, включающий пароксизмальные искажения схемы тела, деперсонализацию, дереализацию, зрительные галлюцинации, искажение чувства времени, ощущение deja vu, jamais vu. Зрительные галлюцинации в рамках синдрома Алисы отличаются от таковых при психических заболеваниях следующими признаками: возникают пароксизмально, стереотипны, представляют собой образы людей или животных, четко очерчены, локализованы в конкретной точке пространства, образы «проплывают» из одной стороны в другую или возникают из потоков воздуха, а затем «растворяются», пациенты полностью критичны к зрительным галлюцинациям [10].
От коморбидности головной боли и психических расстройств к диагностике головной боли, связанной с эмоционально-аффективными нарушениями
В течение всего прошлого столетия в изучении мигрени существовала концепция «мигренозной личности», включившая такие качества, как депрессивность, тревожность, повышенная умственная и физическая утомляемость, апатия, а также перфекционизм и ригидность [23]. Проведенные в 1990-х гг. крупные эпидемиологические исследования коморбидности мигрени и некоторых психических нарушений перевернули эти представления.
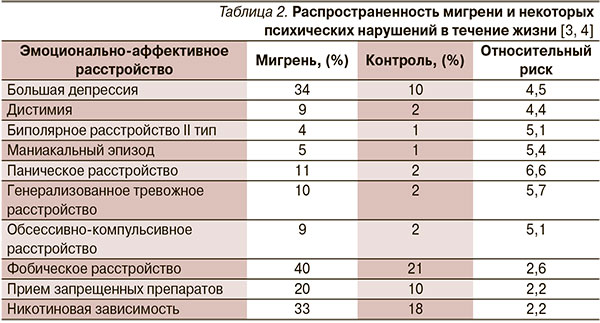
В крупных популяционных исследованиях показано, что у людей, страдающих мигренью, в 3 и более раза выше риск развития депрессивных и тревожных расстройств, чем в популяции в целом (табл. 2) [11, 12]. Дополнительный анализ подтипов мигрени и депрессивных нарушений с поправкой на пол и возраст позволил вычислить, что распространенность большой депрессии при хронической или «трансформированной» мигрени составляет 57 %. Риск развития генерализованного тревожного расстройства в 2,0, а большого депрессивного эпизода в 2,5 раза выше при хронической мигрени по сравнению с эпизодической [16]. Паническое расстройство встречается в 2–5 раз чаще при хронической мигрени по сравнению с эпизодической.
Несколько лонгитудинальных исследований показали двустороннюю взаимосвязь между мигренью и депрессией, при которой каждое из заболеваний повышает риск другого [8]. В обсервационном исследовании K.E. Waldie и соавт. [22], которое продолжалось 26 лет, была показана некая закономерность развития мигрени и эмоционально-аффективных расстройств. В первую очередь развиваются тревожные расстройства, затем манифестирует мигрень, далее присоединяется депрессия.
В основе такой коморбидности лежат общие звенья патогенеза мигрени и эмоционально-аффективных нарушений, наиболее вероятно связанные с серотонинергической дисфункцией. Серотонинергическая дисфункция в рамках коморбидности мигрени и депрессии, по-видимому, имеет наследственный характер, что было доказано в близнецовых исследованиях [19]. Обсуждается роль генов транспортера серотонина, а также гена мозгового нейротрофического фактора (BDNF) как общие генетические механизмы развития мигрени и депрессии [2]. У пациентов с мигренью в межприступном периоде обнаруживается снижение уровня серотонина в плазме крови и его повышение во время приступа. Предполагается, что во время мигренозного приступа нарушается серотонинегрическая трансмиссия в области ядра шва – одной из структур антиноцицептивной системы. Другой концепцией, объясняющей коморбидность эмоционально-аффективных нарушений и хронической мигрени, является теория лимбического усиления болевого синдрома (LAPS). Клинически синдром LAPS проявляется рефрактерным болевым синдромом, в т. ч. рефрактерной мигренью, а также изменением настроения, нарушениями сна, повышенной утомляемостью, снижением концентрации внимания, снижением либидо, раздражительностью. Согласно этой концепции, связанные с негативными переживаниями нейропластические изменения в кортико-лимбической области приводят к сенситизации структур, участвующих в формировании ощущения боли, а также болевого аффекта [18]. Позднее методами функциональной нейровизуализации было выявлено снижение активности орбито-фронтальной коры и передней поясной извилины, что подтвердило функциональные изменения в лимбической системе при хронической мигрени.

В основной части МКГБ III выделяют две основные формы головной боли, связанной с психическими расстройствами (раздел 12): головная боль, связанная с расстройством соматизации, и головная боль, связанная с психотическим расстройством. Однако взаимосвязь эмоционально-аффективных расстройств и цефалгии столь тесная, что в приложении МКГБ III (2013) диагностические критерии головной боли, связанной с психическими расстройствами, были значительно расширены (табл. 3). Эти критерии пока не являются обязательными, но они открывают возможность для лучшей диагностики и более эффективной терапии.
Рассмотрим использование критериев на клиническом примере.
У пациентки Д. 36 лет с юности отмечались приступы мигрени без ауры с частотой 1 раз в 1–2 месяца. Головная боль была умеренно интенсивной (7–8 баллов по визуальной аналоговой шкале), пульсирующей, преимущественно правосторонней, сопровождалась тошнотой, свето- и звукобоязнью. Приступы купировались простыми анальгетиками. Шесть месяцев назад у пациентки развились подавленность настроения большую часть времени, плаксивость, нарушения сна, постоянное чувство усталости и невозможность сконцентрировать внимание. Вместе с этими симптомами приступы мигрени участились до 8–10 в месяц и интенсивнее: плохо купировались анальгетиками, сопровождались рвотой, требовали постельного режима. Появилась также фоновая, практически ежедневная, головная боль – двусторонняя, распирающая, 4–5 баллов по визуальной аналоговой шкале. Таким образом, в соответствии с рекомендациями МКГБ III пациентке ставится два диагноза: хроническая мигрень и головная боль, связанная с депрессивным расстройством. Следовательно, пациентка Д. должна получать как профилактическое лечение мигрени, так и антидепрессанты. Трициклические антидепрессанты обладают противомигренозным действием, однако их применение зачастую бывает ограничено плохой переносимостью. Большинство международных руководств по ведению пациентов с головной болью рекомендует использовать селективные ингибиторы обратного захвата серотонина (СИОЗС) и селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) как средства второй линии для профилактики мигрени и головной боли напряжения. Однако эти рекомендации составлены на основании мета-анализа, проведенного более 10 лет назад – еще до появления многих новых препаратов. Кроме этого период наблюдения в данном мета-анализе составлял 2 месяца, тогда как для решения об эффективности препарата на сегодняшний день необходим период 3 месяца [13]. К настоящему времени появились данные, что антидепрессанты групп СИОЗСН и СИОЗС также снижают частоту приступов мигрени. Например, в одном из исследований эсциталопрам (Ципралекс) урежал мигренозные приступы даже у пациентов с мигренью без депрессии [21]. СИОЗС могут быть высокоэффективными в случае головной боли, связанной с депрессивным расстройством или различными вариантами тревожных расстройств. Так, после 2 месяцев приема эсциталопрама у пациентки Д.
регрессировали симптомы депрессии и уменьшилась частота приступов мигрени. Одним из положительных эффектов, отмеченных пациенткой Д., было улучшение концентрации внимания и регресс постоянного чувства сонливости.
Абузусная головная боль и психические нарушения
Особый интерес представляют психологические аспекты формирования абузусной головной боли (головной боли, связанной с чрезмерным приемом обезболивающих средств). Существует несколько точек зрения относительно генеза лекарственного абузуса. С одной стороны, абузус может рассматриваться как форма аддиктивного поведения, а именно безудержное желание и дефицит контроля приема обезболивающих. Как уже упоминалось, у пациентов с мигренью чаще, чем в популяции, отмечается злоупотребление алкоголем, а также прием запрещенных препаратов. Эти нарушения связаны с дисфункцией орбито-фронтальной коры, что подтверждается методами функциональной нейровизуализации [7]. Психологическое исследование показало, что для пациентов с лекарственным абузусом в отличие от пациентов с мигренью без абузуса характерен дефицит принятия решения, оцененный по шкале IGT, что является клиническим коррелятом орбито-фронтальной дисфункции [17]. В другом исследовании [5] было показано, что для пациентов с абузусной головной болью, вызванной опиатами и резистентных к терапии, характерны такие признаки аддиктивного поведения, как непреодолимое желание начать или продолжить прием препарата, желание испытать эффект препарата, постоянство состояния, когнитивная составляющая.
Другой точкой зрения является то, что бесконтрольный прием лекарственных средств – проявление субклинического обсессивно-компульсивного расстройства, одной из форм тревожных нарушений.
В исследовании L. Cupini с соавт [6] у пациентов с абузусной головной болью суммарный балл по шкале Йель–Браун был достоверно выше, чем у пациентов без мигрени. Еще одна форма тревожного расстройства, обсуждаемая при абузусной головной боли, – это боязнь головной боли. Непреодолимый страх приступа заставляет пациентов принимать обезболивающее, даже когда боль не наступила, – «для профилактики». Степень выраженности боязни головной боли имеет прямую корреляцию с частотой приступов мигрени [14].
В одном из исследований проанализировали причины, по которым пациенты продолжают принимать препарат от головной боли.
Было выделено три основные группы причин:
Убеждение, что отсутствие лечения головной боли разрушит жизнь (головная боль непереносима; головная боль – дополнительное бремя, купирование боли позволяет адаптироваться и работать; боязнь пропустить важное событие из-за головной боли).
Анальгетик – единственный способ лечения головной боли (опробованы различные способы снятия боли, но, кроме анальгетика, ничего не помогает; скепсис по отношению к профилактическому лечению; необходимо всегда иметь анальгетик под рукой).
Недальновидное использование анальгетиков (прием наиболее доступного анальгетика, а не того, который нужен; при приеме анальгетика мысли заняты только головной болью; отрицание вреда анальгетиков; еще больший прием анальгетиков в период стрессовых событий; понимание взаимосвязи между нарастающей частотой головной боли и приемом анальгетиков).
Таким образом, формирование абузусной головной боли представляет собой сложный феномен, включающий наличие тревожного расстройства (фобического или обсессивно-компульсивного), убеждений пациентов относительно необходимости приема анальгетиков, а также элементов аддиктивного поведения.
Наиболее точно диагностировать различные формы эмоционально-аффективных нарушений у пациентов с абузусной головной болью может психиатр. В специализированных центрах ведением случаев головной боли с лекарственным абузусом, рефрактерной головной боли занимаются цефалголог, психиатр и психотерапевт. Для скрининговой диагностики обсессивно-компульсивного расстройства можно использовать опросник Йель–Браун, для выявления фобии головной боли – опросник фобии головной боли (табл. 4).
СИОЗС являются препаратом выбора лечения тревожных расстройств. Более того, это единственная группа препаратов с доказанным действием в отношении обсессивно-компульсивного расстройства. В двойном слепом плацебо-контролируемом исследовании была показана эффективность эсциталопрама (Ципралекса 20 мг) при обсессивно-компульсивном расстройстве, которая оценивалась с помощью шкалы Йель–Браун, также был отмечен более выраженный эффект эсциталопрама по сравнению с пароксетином [20]. В другом контролируемом исследовании [1] эсциталопрам показал эффективность в отношении специфической фобии. Препараты группы СИОЗС успешно используются в схемах лечения сочетания цефалгии с различными формами эмоционально-аффективных нарушений. Расширение возможностей диагностики эмоционально-аффективных расстройств и их специфическая терапия – один из перспективных путей ведения «трудных» пациентов с головной болью.