Всвязи с высокой распространенностью запор сегодня относят к социально значимым заболеваниям. В развитых странах частота запора в популяции составляет от 10 до 17–19% [1–3]. Это связано с тем, что за последние 100 лет изменился характер питания, уменьшилось количество употребляемых в рационе пищевых волокон и снизилась физическая активность.
Частота стула у здоровых людей варьируется и зависит от характера питания, образа жизни, привычек. Временнáя задержка стула не во всех случаях должна рассматриваться как признак какого-либо патологического состояния. Однако возникновение запора у лиц среднего или пожилого возраста должно вызывать в первую очередь онкологическую настороженность.
По данным Е.К. Хаммад, Г.А. Григорьевой, после исключения случаев развития запоров, связанных с особенностями образа жизни, среди причин хронического запора (ХЗ) в возрастной группе до 20 лет доминируют анатомические особенности толстой кишки; в возрасте 20–40 лет – патология аноректальной зоны; после 40 лет одинаково часто встречаются психогенные, неврогенные, эндокринные, гастроэнтерологические причины запоров и причины, связанные с патологией аноректальной зоны [4].
Согласно определению, запором (обстипация, constipation (лат.) – спресованные, столпившиеся вместе) следует считать задержку опорожнения кишечника более чем на 48–72 часа, сопровождающуюся затруднением акта дефекации, чувством неполного опорожнения с отхождением малого количества (менее 100 г) и повышенной твердости кала (I или II типы по Бристольской шкале). Некоторые авторы объективным критерием запора считают массу фекалий менее 35 г/сут [5].
Проблема запора усугубляется с возрастом, и среди людей старше 60 лет запор встречается у 50–60% [6]. По данным популяционного исследования МУЗА, утвердительный ответ на прямой вопрос о запоре дали 34,3% респондентов, Римским критериям соответствовали из них только 16,5%. Частота запоров увеличивается с возрастом и составляет в группе от 18 до 24 лет 3,6%, от 25 до 34 лет – 7,5, от 35 до 44 лет –15,8, от 45 до 54 лет –17,8, от 55 до 64 лет – 21,5, старше 65 лет – 32,8% [1]. У больных пожилого и старческого возраста на фоне полиморбидности наличие запора отягощает течение как сопутствующей патологии желудочно-кишечного тракта (ЖКТ), так и других органов и систем. В работе О.Б. Яновой и соавт. доказано, что запор служит одним из трех основных факторов, которые повышают риск развития рефлюкс-эзофагита (относительный риск [ОР]=1,65 при 95% доверительном интервале [ДИ] 1,05–2,6; р=0,02), а устранение запора у больных гастроэзофагеальной рефлюксной болезнью приводит к снижению кратности приема ингибиторов протонной помпы (в режиме «по требованию») у 23,1 против 2,5% больных с сохраняющимся запором (р<0,05) [7].
По данным одного крупного обзора, снижение качества жизни при ХЗ сопоставимо с таковым у больных ишемической болезнью сердца, бронхиальной астмой, хроническими воспалительно-дистрофическими заболеваниями суставов [8]. Тяжелые запоры увеличивают риск кардиоваскулярных событий у пожилых женщин в постменопаузе на 23% (ОР=1,28, 95% ДИ – 1,08–1,53), а умеренные в – 1,13 раза (95% ДИ – 1,03–1,24) [9].
Другой проблемой больных старших возрастных групп с полиморбидностью является вынужденная полипрагмазия. Некоторые лекарственные препараты могут быть причиной нарушения моторики кишки. К ним относятся трициклические антидепрессанты, антипаркинсонические (антихолинергические, дофаминергические) средства, антациды, содержащие гидроксид алюминия или карбонат кальция, М-холинолитики, анальгетики (кодеин, морфин и его производные), противокашлевые, в состав которых входят кодеин и его производные, диуретики (торасемид, салуретики), некоторые представители антигипертензивных средств: ингибиторы ангиотензинпревращающего фермента, верапамил, клонидин, антибиотики (цефалоспорины и др.), препараты двух- и трехвалентного железа. Влияние на моторику кишки зависит от дозы и длительности приема препарата.
Иногда уже при опросе больного можно установить, является ли запор первичным, т.е. когда морфологические изменения толстой кишки не обнаружены или симптомом органического поражения ЖКТ, а в некоторых случаях и проявлением экстрагастроинтестинальных заболеваний. Заболевания, которые могут быть причиной запора, представлены в таблице.
При сборе анамнеза врач должен установить давность возникновения жалоб, выяснить характер стула в детстве и попытаться проследить возможную связь запора с переменой места жительства, диетой и т.д. Короткий анамнез, начало заболевания после 50 лет, потеря массы тела без видимой причины, эпизоды повышения температуры, отягощенный семейный анамнез (по наличию злокачественных опухолей), кишечное кровотечение или положительный анализ кала на скрытую кровь, анемия, лейкоцитоз, ускорение СОЭ) являются показанием к углубленному обследованию ЖКТ, прежде всего к эзофагогастродуодено- и колоноскопии.
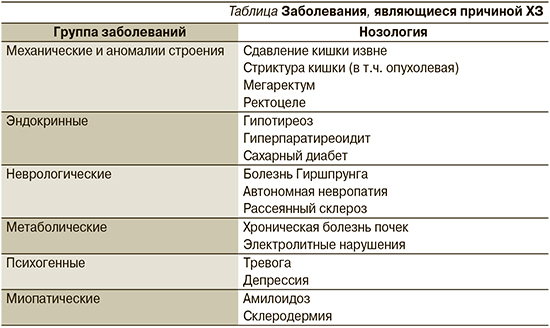
Поскольку риск колоректального рака увеличивается после 50 лет, этой категории больных также требуется детальное обследование кишечника.
ХЗ может быть первичным и вторичным. Запор считается первичным, или функциональным, если его причину не удается связать с морфологическими изменениями кишечника.
Вторичные запоры развиваются при заболеваниях толстой кишки, фармакологических и нутритивных влияниях, вызывающих нарушения ее структуры и моторики. С точки зрения особенностей патогенеза ХЗ делятся на три варианта:
- запор вследствие дискинезии кишечника (функциональный запор и синдром раздраженного кишечника (СРК) с преобладанием запоров;
- запор вследствие медленного продвижения кишечного содержимого по толстой кишке (инертная толстая кишка);
- запор вследствие нарушения координации мышечного аппарата, обеспечивающего дефекацию (диссинергическая дефекация), на долю которой приходится до 25% от общего числа функциональных запоров [10].
В 2006 г. в Римских критериях (Rome III) функциональных расстройств ЖКТ сформулированы критерии диагноза хронического функционального запора, имеющего шифр Международной классификации болезней – К 59.0 [11, 12].
Для постановки диагноза необходимо наличие хотя бы двух из следующих критериев, присутствующих в течение не менее 3 месяцев, с дебютом за 6 месяцев до постановки диагноза:
- натуживание в течение по крайней мере 25% дефекаций;
- шероховатый или твердый стул по крайней мере в 25% дефекаций;
- ощущение неполной эвакуации по крайней мере в 25% дефекаций;
- ощущение аноректальной обструкции/блокады по крайней мере для 25% дефекаций;
- необходимость мануальных приемов для облегчения по крайней мере в 25% дефекаций (например, пальцевая эвакуация, поддержка тазового дна);
- меньше трех дефекаций в неделю;
- невозможность самостоятельного стула без использования слабительных средств;
- недостаточность критериев для СРК.
Основным критерием диагноза СРК (К 58), который принципиально отличает его от хронического функционального запора, считается наличие абдоминальной боли или дискомфорта, ассоциированного с дефекацией и/или изменением частоты и/или формы стула.
Лечение запора
Лечение должно начинаться с рекомендаций по изменению образа жизни. Однако для пациентов старших возрастных групп – это непростая задача.
Увеличение в рационе массы пищевых волокон. Рекомендуемая норма – 25–32 г/сут, что соответствует приблизительно 400–450 г овощей и фруктов. Чтобы предотвратить или уменьшить избыточное газообразование в кишечнике, нужно акцентировать внимание больного на постепенном (в течение нескольких недель) увеличении ежедневного приема овощей и фруктов. Тепловая обработка пищи также способствует снижению газообразования.
Прием достаточного количества жидкости (в среднем не менее 1,5 л/сут).
Физическая активность. Например, ежедневная 30-минутная ходьба быстрым темпом.
Формирование привычки к ежедневному опорожнению кишки в одно и то же время (физиологичнее в утренние часы – после завтрака, который запускает гастроилеальный симптом Поргеса: быстрое перемещение содержимого подвздошной кишки в слепую при раздражении слизистой оболочки желудка пищей) в привычных для больного условиях.
Уже на этапе диетических рекомендаций больному можно назначить отруби. Количество отрубей следует увеличивать с 1–2 чайных ложек до 6–8 столовых в течение 2–4 недель [13].
Отруби могут служить примером принципа рациональной фармакотерапии для больных пожилого и старческого возраста, а именно – многоцелевой монотерапии, т.е. возможности использовать системные эффекты одного средства для одновременной коррекции нарушенных функций нескольких органов или систем (Л.Б. Лазебник, 1993).
В качестве базисной терапии каждому больному хроническим функциональным запором следует назначать вещества, увеличивающие объем содержимого кишечника (метилцеллюлоза, отруби, семя льна и др.), т.к. сочетание этих веществ с другими группами слабительных препаратов обладает синергизмом действия, что позволяет повышать эффективность терапии запоров.
Применение в качестве слабительных средств сульфата магнезии, касторового масла, алоэ, сенны упоминается еще в египетских папирусах и документах Древней Греции, в т.ч. и в Афоризмах Гиппократа.
Назначая слабительные средства, необходимо помнить, что при их длительном (на протяжении 6–12 месяцев) приеме может развиваться психологическая зависимость и наряду с этим феномен привыкания.
Классификация слабительных средств по механизму действия
Вызывающие химическое раздражение рецепторов: антрахиноны (производные сенны, крушины), дифенолы (бисакодил, пикосульфат натрия), касторовое масло.
Обладающие осмотическими свойствами: солевые (магния сульфат), слабоабсорбируемые ди- и олигосахара (лактулоза), многоатомные спирты (сорбитол), полиэтиленгликоль.
Увеличивающие объем содержимого кишечника: балластные вещества (метилцеллюлоза, отруби, семя льна, псиллиум и др.)
Способствующие размягчению кала и улучшающие его скольжение (жидкий парафин, вазелиновое масло).
Исследование, проведенное в России в 2011 г. IPSOS, и бизнес-аналитика при изучении рынка терапии запора показали, что 67% лиц, страдающих запором, лечатся самостоятельно, по рекомендациям Интернета, соседей и научно-популярных публикаций, 13% обращаются за советом к провизору, 11% не лечатся совсем и только 13% обращаются за помощью к врачу. Перед обращением к врачу 70% больных уже перепробовали различные способы терапии [14].
По данным J. Tack и соавт., уровень неудовлетворенности эффектами слабительных препаратов как в нашей стране, так и в других странах составляет около 47% [2]. Это может быть обусловлено следующими причинами: отсутствием комплексного подхода к лечению запора, непониманием больного необходимости регулярного соблюдения подобранного режима и желанием получить быстрый эффект.
Назначая препарат для лечения запора, врач должен точно понимать цель назначения и предполагаемую длительность лечения.
Препараты раздражающего действия эффективны для лечения «запора путешественника» (не более 7 дней), но не могут быть рекомендованы в качестве монотерапии для нормализации стула у пациентов с хроническим функциональным запором, т.к. при длительном приеме быстро развивается привыкание.
Осмотические слабительные: полиэтиленгликоль, многоатомные спирты (сорбитол), солевые (магния сульфат), действуют только в просвете кишки, не оказывая системных побочных эффектов. За счет связывания воды в просвете кишки они увеличивают объем кишечного содержимого и тем самым стимулируют перистальтику. Данные препараты высокоэффективны и могут быть назначены на сроки от нескольких недель до нескольких месяцев.
Слабоабсорбируемые ди- и олигосахара (лактулоза) обладают пребиотическими свойствами и за счет роста сахаролитических бактерий в кишке изменяют внутрипросветное рН, повышая осмотическое давление в просвете кишки. Это вызывает увеличение объема содержимого кишечника и стимулирует пропульсивную моторику кишечника.
К общим недостаткам этих препаратов относятся вздутие живота, урчание. Эти побочныеэффекты преодолевают индивидуальным подбором дозы с постепенным ее увеличением.
Вазелиновое масло (Oleum vaselini seu Parafinum liquidum, «жидкий парафин») способствует размягчению каловых масс, облегчению их скольжения по кишке и оказывает слабое стимулирующее воздействие на моторику кишечника. Применяется внутрь 1 раз в сутки по 1–2 столовые ложки через 2 часа после приема пищи. Продолжительность терапии – не более 5 дней, т.к. длительное применение вазелинового масла может вызывать нарушение всасывания жирорастворимых витаминов A, E, K, а также атонию кишечника. Следует обратить внимание на то, что из-за раздражения слизистой оболочки прямой кишки и анального канала для больных пожилого и старческого возраста при приеме вазелинового масла внутрь может увеличиться риск неудержания и недержания кала.
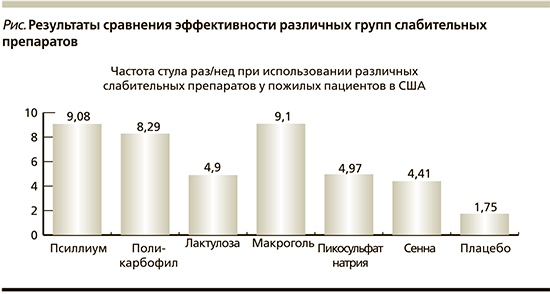
Ниже представлены результаты мета-анализа 31 исследования (обследованы 808 пациентов), в которых проводилось сравнение эффективности различных групп слабительных препаратов [15] (см. рисунок).
В отсутствие эффекта на фоне приема всех ранее перечисленных слабительных средств в качестве моно- или комбинированной терапии препаратом выбора остается полный агонист серотонинергических рецепторов 4-го типа (5-HT4) прукалоприд, который оказывает выраженный слабительный эффект у 73% больных в дозе 2 мг [20]. Данный препарат активирует 5-НТ4-рецепторы, расположенные в гладкой мускулатуре и нейронах нервно-мышечного сплетения в стенке кишки, что приводит к увеличению перистальтики путем стимулирования вторичных мессенджеров (ацетилхолин и кальцитонин), сокращения проксимальных гладких мышечных волокон и расслабления периферических гладких мышечных волокон. Фармакокинетика прукалоприда имеет прямую корреляцию с дозой в диапазоне до 20 мг/сут.
При длительном приеме препарата 1 раз в сутки в дозе 2 мг не развивается привыкания. В отличие от своего предшественника тегасерода прукалоприд в терапевтических дозах не оказывает побочных эффектов на сердечно-сосудистую систему в виде развития жизнеугрожающих аритмий.
С учетом принципа многоцелевой монотерапии для стимуляции работы толстой кишки можно рекомендовать прием препаратов, не относящихся к группе слабительных. Таким препаратом является блокатор опиоидных рецепторов тримебутин, снижающий длительность толстокишечного транзита с 105±19 до 60±11 часов против плацебо (с 103±17 до 95±10 часов), р<0,001, повышая электрофизиологическую активность кишечника у пациентов с хроническими идиопатическими запорами при дозировке по 100–200 мг 3 раза в сутки [16].
В настоящее время недостаточно доказательств, подтверждающих эффективность использования невсасывающихся антибиотиков и пробиотиков для лечения запора. Только в единичных исследованиях показано, что Bifidobacterium animalis могут ускорять толстокишечный транзит как у здоровых людей, так и у больных СРК, а Lactobacillus casei и Bifidobacterium lactis DN-173010 эффективны при хронических запорах [17‒19].
К проблемам запора в пожилом возрасте можно отнести снижение порога болевого восприятия [19], снижение уровня серотонина и частое развитие депрессии. С учетом прямой корреляции развития запоров на фоне большой депрессии разработаны рекомендации ведения таких больных с точки зрения психосоматического подхода [20].
По данным Н.П. Чернусь и соавт. [21], тревожная и астеническая депрессия чаще всего ассоциировались с более тяжелым вариантом течения функционального запора. Добавление антидепрессанта к стандартной терапии позволило улучшить психоэмоциональное состояние больных функциональным запором и достигчь длительной ремиссии.
Успешное лечение запоров в любом возрасте, в т.ч. и у пациентов старших возрастных групп, заключается в установлении причин возникновения и правильном выборе программы лечения.



