Синдром раздраженного кишечника (СРК) в настоящее время определяется как хроническое функциональное расстройство, основным дескриптором которого является рецидивирующий абдоминальный болевой синдром, связанный с дефекацией в неразрывной ассоциации с нарушением частоты или формы (консистенции) стула [1]. Актуальность процесса активного изучения этой нозологической формы диктуется не только ее значительной распространенностью, но и существенным снижением качества жизни пациентов.
Постановка диагноза СРК зависит от тщательно выверенной интерпретации временных соотношений абдоминальной боли с преобладающим типом изменений характеристик дефекаций пациента. При этом авторы Римских критериев-IV (Rome-IV) подчеркивают, что хотя основной целью разработки «критериев» было предоставление готовой, легко применимой в практической работе структуры постановки диагноза СРК, по-прежнему нет идеального специфического только для данного заболевания теста [2].
Диагноз СРК устанавливается при соответствии жалоб пациента диагностическим критериям Rome-IV, при этом обязательно должны быть исключены симптомы «тревоги»: немотивированное снижение массы тела, ночная симптоматика, дебют в пожилом возрасте, постоянные абдоминальные боли как единственный симптом заболевания, семейный анамнез колоректального рака, целиакии, воспалительные заболевания кишечника, лихорадка, изменения органов при физикальном обследовании, кровь в стуле в отсутствие геморроя или анальных трещин, лейкоцитоз, железодефицитная анемия, ускорение СОЭ, изменения в биохимических показателях крови [3].
Хронический абдоминальный болевой синдром с нарушениями транзита по желудочно-кишечному тракту (ЖКТ), характерный для СРК, имеет сходство с симптомами, возникающими при массе заболеваний. В целом абдоминальная боль была и остается серьезной проблемой внутренних болезней и гастроэнтерологии [4]. Понимание механизмов, лежащих в основе формирования болевого синдрома, отчасти может помочь в установлении его причины и выборе пути его купирования. Наиболее частым механизмом абдоминальной боли служит висцеральная боль, которая вызывается повышением давления, растяжением, натяжением, расстройством кровообращения во внутренних органах и может быть результатом как органических, так и функциональных заболеваний. Боль обычно носит тупой, спастический, жгучий характер, не имеет четкой локализации. Она нередко сопровождается разнообразными вегетативными проявлениями: потливостью, беспокойством, тошнотой, рвотой, бледностью. Благодаря большому количеству синапсов между нейронами нередко возникает двойная иннервация, лежащая в основе иррадиации: отражении болевых ощущений при интенсивном висцеральном импульсе в области зон повышенной кожной чувствительности, в месте проекции других органов, иннервируемых тем же сегментом спинного мозга, что и вовлеченный орган [5].
Вариабельные характеристики абдоминального болевого синдрома при СРК [6, 7]:
- чаще всего боль диффузная, без иррадиации;
- локализуется в нижних отделах живота (чаще в левых отделах);
- при наличии т.н. газовых карманов в области печеночного или селезеночного изгибов боль может локализовываться в правом или левом подреберье;
- эпизоды острой боли часто налагаются на более постоянную тупую боль;
- прием пищи, как правило, провоцирует или усиливает боль;
- дефекация обычно облегчает боль, но может не полностью ее купировать.
Висцеральный генез болевого синдрома при СРК нередко сочетается с психогенными механизмами. Дефицит ингибирующих факторов и/или усиление нормальных входящих афферентных сигналов вследствие поражения центральных контролирующих механизмов и/или снижения синтеза биологически активных субстанция (брадикинин, серотонин, гистамин, простагландины и др.) приводят к изменению порога чувствительности сенсорных рецепторов либо напрямую их активируют. Те же процессы могут провоцировать или усугублять спазм гладкой мускулатуры кишечника, что в свою очередь вызывает раздражение ноцицепторов и ощущение боли [8].
Дифференциальный диагноз при СРК традиционно проводит с такими заболеваниями, как [9, 10]:
- воспалительные заболевания кишечника;
- микроскопические колиты;
- энтеропатии (целиакия, лактазная недостаточность);
- колоректальный рак;
- дивертикулярная болезнь кишеч-ника;
- паразитарные (инфекционные) колиты;
- гинекологическая патология (эндометриоз, рак яичников, воспалительные заболевания органов малого таза).
По нашему мнению, этот перечень необходимо дополнить еще одной патологией, о которой крайне редко вспоминают врачи-интернисты. Одной из причин абдоминального неблагополучия, включающего запоры, диарею и боли, может стать анатомическая аномалия развития толстой кишки.
В период эмбриогенеза нарушение развития толстой кишки может затронуть любые процессы ее формирования. По классификации Г.И. Воробьева и соавт. (1989), выделяют аномалии интрамуральной нервной системы, врожденную ангиодисплазию толстой кишки, врожденное удлинение толстой кишки, врожденное нарушение положения и фиксации толстой кишки, удвоение толстой кишки, сочетание различных аномалий [10].
Долихоколон – удлинение всей ободочной кишки или одного из ее отделов, представляет собой самую частую аномалию развития толстой кишки. Удлинение ободочной кишки диагностируется у каждого второго пациента, длительно страдающего запором. Частота выявления данного состояния у новорожденных составляет более 30%. По данным педиатрических исследований, данная аномалия встречается у 30–40% детей с хроническими запорами и болями в животе. У взрослых долихоколон встречается практически с одинаковой частотой в разных возрастных группах (от 23,8 до 31,0%) [11].
По анатомическому принципу долихоколон классифицируется исходя из отдела ободочной кишки, длина которого превышает среднестатистические значения.
Выделяют следующие виды долихоколона [10]:
- долихосигма;
- левосторонний долихоколон;
- долихотрансверзум;
- правосторонний долихоколон;
- субтотальный долихоколон;
- тотальный долихоколон.
С практической точки зрения большее значение имеет клинический принцип классификации, на основании которого долихоколон подразделяется на следующие формы [11]:
- долихоколон без клинических проявлений (бессимптомный долихоколон);
- долихоколон с нарушением транзита по толстой кишке;
- осложненный долихоколон.
К осложнениям долихоколон относятся заворот кишки, инвагинация и узлообразование. При этом заворот сигмовидной кишки прочно занимает 3-е место среди причин острой кишечной непроходимости, а летальность при развитии этого осложнения достигает 15%, в случае некроза – 46%.
Ведущее клиническое проявление долихоколона – картина запора. По данным М.Ф. Осипенко [12], диагностическая специфичность запоров при долихоколоне составляет 76%, чувствительность – 80%. Риск запоров существенно выше при наличии удлинения сигмовидной кишки по сравнению с другими вариантами долихоколон. При этом задержка стула до 3 дней часто не сопровождается другими жалобами, тогда как более длительный и выраженный запор сочетается с дискомфортом в животе, болями, метеоризмом вплоть до ухудшения общего самочувствия, социальной дезадаптации, развития приступов динамической кишечной непроходимости.
Абдоминальный болевой синдром – второй по значимости критерий долихоколона – чаще наблюдается у женщин. При этом возможно проявление абдоминального дискомфорта в виде диспареунии, что часто приводит к задержкам в установлении истинной причины болевого синдрома. Абдоминальные боли при долихоколоне вполне соответствуют критериям СРК: имеют связь с дефекацией, часто ассоциированы с изменениями консистенции стула. Определение ректальной чувствительности у лиц с запорами методом баллонно-дилатационного теста не выявило различий в группах пациентов с долихосигмой и СРК [12].
Наиболее информативным методом диагностики аномалий развития и положения толстой кишки является рентгенологический. Исследование позволяет сразу же определить положение толстой кишки в брюшной полости, форму и размеры всех ее отделов, подвижность при проведении исследования в положении больного стоя и лежа. Следующие клинические примеры продемонстрируют диагностическую ценность данного метода диагностики.
Клинический случай 1
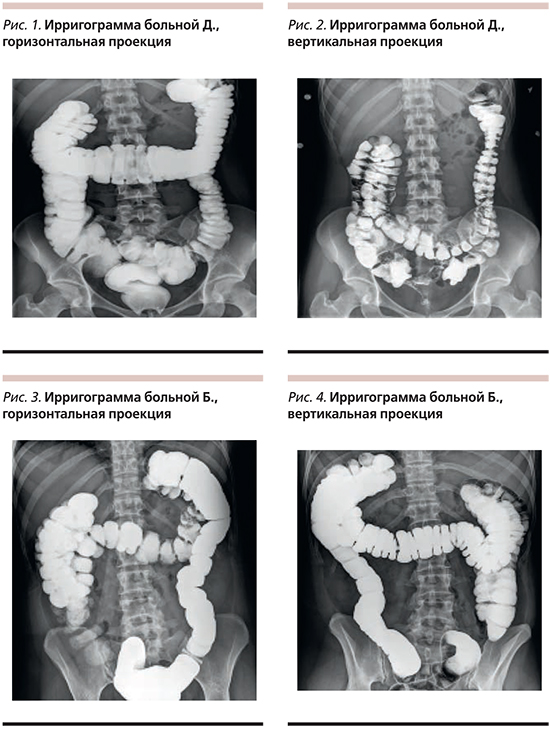
Пациентка Д. 26 лет обратилась с жалобами на боли в нижних отделах живота без связи с актом дефекации, нарушениями стула; вздутие живота, «живот как каменный». При ирригоскопии (рис. 1) толстая кишка удлинена, образует дополнительные петли в области селезеночного и печеночного углов, поперечно-ободочный отдел опускается до уровня L4–L5. Восходящий отдел также удлинен, купол слепой кишки в малом тазу на уровне ректо-сигмоидного перехода. В вертикальной проекции (рис. 2) печеночный угол смещается до уровня крыла подвздошной кости, купол слепой кишки и часть поперечно-ободочной кишки в проекции малого таза.
Клинический случай 2
Пациентка Б. 37 лет на момент осмотра жалоб активно не предъявляет, периодически отмечает дискомфорт в мезогастрии, вздутие живота. Ранее была госпитализирована в связи с внезапно развившимся болевым приступом: вздутием живота, болями в правой подвздошной области. При обследовании данных за острую хирургическую патологию не выявлено, рекомендован прием спазмолитиков, эффект не стойкий. Через месяц вновь появились боли в мезогастрии, тошнота, вздутие живота. Нарушений стула не отмечает. При ирригоскопии (рис. 3) ободочная кишка удлинена, за счет поперечно-ободочного и восходящего отделов образует дополнительные петли в области селезеночного и печеночного углов, купол слепой кишки на уровне входа в малый таз, дополнительная петля печеночного угла опускается до уровня S1–S2. В вертикальной проекции (рис. 4) отмечается смещение правого фланка книзу, купол слепой кишки располагается на уровне ампулы прямой кишки.
Клинический случай 3
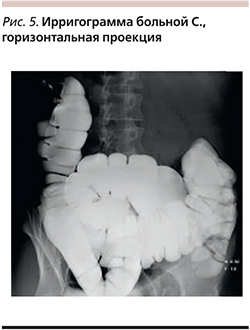 Пациентка С. 34 лет обратилась с жалобами на боли в мезогастрии, в нижних отделах живота, дипареунию, вздутие живота. Осмотрена гинекологом – без органической патологии. При ирригоскопии (рис. 5) толстая кишка удлинена за счет сигмовидной кишки, также удлинена поперечно-ободочная кишка, которая имеет дополнительные изгибы в области печеночного и селезеночного углов, центральная часть поперечно-ободочной кишки расположена над входом в малый таз.
Пациентка С. 34 лет обратилась с жалобами на боли в мезогастрии, в нижних отделах живота, дипареунию, вздутие живота. Осмотрена гинекологом – без органической патологии. При ирригоскопии (рис. 5) толстая кишка удлинена за счет сигмовидной кишки, также удлинена поперечно-ободочная кишка, которая имеет дополнительные изгибы в области печеночного и селезеночного углов, центральная часть поперечно-ободочной кишки расположена над входом в малый таз.
Обсуждение
Выбор тактики лечения долихоколона основывается на клинической форме болезни. Бессимптомный долихоколон не требует консервативного или хирургического лечения, однако пациенты должны быть предупреждены о возможном развитии в дальнейшем медленнотранзитного запора и о потенциальной угрозе осложнений. Таким пациентам необходима первичная профилактика запора, прежде всего коррекция питания [13]. Диета должна быть физиологически полноценной, рекомендуется исключать из рациона продукты, усиливающие процессы гниения и брожения в толстой кишке, богатые эфирными маслами, экстра-активные вещества. Рацион больного должен обогащаться трудноперевариваемыми пищевыми волокнами, улучшающими пропульсивную моторику кишечника (пищевыми прокинетиками). Однако следует помнить, что состояние пациентов с долихоколоном на фоне высокошлаковой диеты может ухудшаться за счет усиления метеоризма и тяжести в животе.
Лечение долихоколона с нарушением транзита по толстой кишке должно проводиться в соответствии с принципами лечения медленнотранзитных запоров [14]. Помимо диетических мероприятий необходимо соблюдение водно-питьевого режима, проведение лечебной физкультуры, физиотерапевтическое лечение (накожная и ректальная электростимуляция толстой кишки, иглорефлексотерапия, лазеротерапия), а также медикаментозная терапия.
Медикаментозная терапия включает назначение средств, увеличивающих объем кишечного содержимого (препараты семян подорожника, мелкокристаллическая целлюлоза), осмотических слабительных препаратов (лактулоза, магния сульфат, полиэтиленгликоль), энтерокинетиков (тримебутин). При болевом синдроме показано добавление к терапии селективных спазмолитических препаратов (пинаверия бромид, мебеверин), возможно также использование антидепрессантов. Назначение каждого препарата должно быть обосновано с позиций эффективности и безопасности [2, 14].
В случае неэффективности консервативной терапии долихоколона, сопровождающегося нарушением транзита по толстой кишке, может быть рассмотрена возможность хирургического лечения [15]. Показанием к хирургическому вмешательству служит неэффективность консервативной терапии при выраженном нарушении качества жизни. Хирургическое лечение долихоколона подразумевает резекцию толстой кишки в объеме субтотальной резекции, реже – выполнение фиксирующих операций (мезосигмопликации, сигмопексии, цекопексии), однако последние, как правило, сопровождаются неудовлетворительными функциональными результатами.
Заключение
Несмотря на присутствие в Международной классификации болезней Q43.8, других уточненных врожденных аномалий кишечника в качестве отдельной, самостоятельной нозологической формы, долихоколон, как правило, не рассматривается, а диагностика и лечение этого состояния обсуждаются в рамках других болезней. Клинические проявления долихоколона по ряду основных маркеров соответствуют критериям такой распространенной функциональной патологии, как СРК. Однако долихоколон, будучи врожденной анатомической аномалией, не может быть отнесен к функциональной патологии, поскольку нередко сопровождается развитием осложнений, требующих неотложного хирургического вмешательства.
Пациенты с типичными симптомами СРК в отсутствие тревожных признаков обычно не нуждаются в проведении дополнительных инструментальных обследований. Однако при рефрактерном к терапии течении СРК есть смысл задуматься о проведении целенаправленного обследования – ирригоскопии, с целью объяснения истинной причины абдоминальных болей и нарушения транзита по ЖКТ. Объяснение генеза симптомов, прежде всего абдоминальной боли, приводит к установлению доверительных отношений между врачом и пациентом и способствует повышению приверженности лечению. Основное внимание в терапии должно уделяться устранению симптомов и восстановлению качества жизни пациентов.


