Введение
Несмотря на произошедшие в мире демографические сдвиги, приведшие к повсеместному постарению населения (к началу III тысячелетия средняя продолжительность жизни достигла 85 лет для женщин и 80 – для мужчин), по-прежнему мало внимания уделяется изучению состояния органов пищеварения в возрастном аспекте. Вместе с тем распространенность заболеваний желудочно-кишечного тракта с возрастом не уменьшается, а их клинические проявления, осложнения и лечение могут быть отличными от таковых у пациентов молодого возраста. Данный класс болезней – частая причина заболеваемости и смертности в пожилом и старческом возрасте [1, 2].
По мере старения изменения в пищеварительном тракте начинаются с полости рта и связаны как с нарушениями жевательного аппарата, так и атрофией жевательной мускулатуры, инволюцией слюнных желез со снижением секреции слюны.
В пищеводе развивается атрофия слизистой оболочки, замедляется перистальтическая активность, самоочищение, снижается тонус нижнего пищеводного сфинктера [1, 3, 4]. Эпидемиологическими исследованиями подтверждено увеличение частоты развития грыж пищеводного отверстия диафрагмы, их размеров с возрастом [5–7].
Изменения со стороны желудка проявляются разнообразными моторными нарушениями, в первую очередь замедлением эвакуации, снижением секреторной активности желудочных желез, ростом распространенности инфицирования H. pylori (HP) [8–10]. Замедление процессов рубцевания эрозивно-язвенных поражений слизистой оболочки происходит главным образом из-за нарушения репаративных процессов [11]. Кроме того, нарушается восприятие боли, что нередко приводит в безболевому течению заболевания [3, 12].
Таким образом, возрастные изменения физиологии желудочно-кишечного тракта сводятся к нарушению моторики и чувствительности, снижению секреторной активности, что в совокупности с сопутствующей патологией и принимаемыми лекарственными препаратами, длительной персистенцией HР-инфекции приводит к повышению уязвимости слизистых оболочек верхних отделов пищеварительного тракта для повреждающих агентов [13, 14].
Целью настоящего исследования стало клинико-эндоскопическое изучение состояния верхних отделов пищеварительного тракта и рациональный выбор антисекреторной терапии пациентов старческого возраста.
Материал и методы
В исследование включены 356 пациентов старческого возраста (средний возраст – 78,7±2,4 года, из них 64,6% женщин). Эндоскопическое изучение состояния верхних отделов пищеварительного тракта проведено в рамках ежегодного диспансерного наблюдения (в 59,3% случаев) и по различным показаниям (40,7% больных), оценивалось наличие язвенной болезни желудка/двенадцатиперстной кишки, гастроэзофагеальной рефлюксной болезни (ГЭРБ) в анамнезе, прием ульцерогенных препаратов. Все пациенты перенесли исследование хорошо, осложнений при проведении процедуры отмечено не было.
Результаты клинического обследования пациентов
Анализ данных анамнеза, включенных в исследование больных, показал, что в течение последних 3 месяцев 236 (66,3%) пациентов принимали более 5 препаратов ежедневно, среди которых были лекарственные средства, оказывавшие прямое повреждающее действие на слизистую оболочку пищеварительного тракта, и непрямое, снижая давление в нижнем пищеводном сфинктере, нарушая двигательную активность пищевода, желудка, двенадцатиперстной кишки. В т.ч. пациентами принимались ацетилсалициловая кислота (АСК) – 146 человек (41%), АСК в сочетании с нестероидными противовоспалительными препаратами (НПВП) – 44 (12,6%), АСК в сочетании с клопидогрелом – 23 (6,5%), варфарин с НПВП – 38 (10,7%), НПВП – 26 (7,3%), β-адреноблокаторы – 275 (77,3%), нитраты – 165 (46,4%), антагонисты кальциевых каналов – 115 (32,3%), теофиллин – 11 (3,1%). Только 45 (12,6%) больных не получали «кардиальную» терапию либо противовоспалительные препараты.
Необходимо отметить, что 153 пациента принимали АСК и НПВП по назначению врача, а 124 эти препараты «добавляли» к лечению самостоятельно, главным образом для купирования болей.
Перед назначением НПВП на длительный курс лечения, согласно общепринятой практике, 54 больным была выполнена контрольная эзофагогастродуоденоскопия (ЭГДС), в 35 случаях проведена эрадикационная терапия.
Анализ характера жалоб показал, что симптомы желудочной диспепсии имели место в 247 (69,4%) случаях: отрыжка воздухом – 72 (20,2%), изжога – 64 (18%), боли, ощущение дискомфорта, тяжести в подложечной области – 51 (14,3%), анорексия – 27 (7,6%), регургитация – 17 (4,8%), одинофагия – 11 (3,1%), дисфагия – 3 (0,84%), рвота – 2 (0,56%).
Следует отметить, что из 211 (53,9%) пациентов, не предъявлявших активных жалоб со стороны органов пищеварения, у 103 (28,9%) при тщательном расспросе отмечена умеренно выраженная клиническая симптоматика.
Атипичные симптомы были зафиксированы в 55 (15,5%) случаях: некоронарогенные боли за грудиной – 17 (4,8%), непродуктивный кашель – 15 (4,2%), приступы удушья – 9 (2,5%), стоматологический синдром – 8 (2,3%), дисфония – 6 (1,7%). При осмотре полости рта были выявлены мелкоточечные кровоизлияния у 25 пациентов (7%), грибковое поражение слизистой – у 14 (3,9%), осложненные формы кариеса в 121 (34%) случае. При физикальном обследовании болезненность при пальпации в эпигастрии отмечали 135 (37,9%) больных.
По данным ЭГДС патология пищевода была диагностирована в 59 (16,5%) случаях, в т.ч. эрозивный эзофагит – 36 (10,1%), ценкеровский дивертикул – 9 (2,5%), варикозное расширение вен пищевода – 9 (2,5%), грибковое поражение пищевода – 5 (1,4%), лейкоплакия – 1 (0,3%). Патология желудка наблюдалась у 105 (29,5%) больных, включая острые и хронические эрозии антрального отдела – 78 (21,9%), язву желудка – 9 (2,5%), опухоль – 8 (2,3%), полип – 6 (1,7%), ксантому желудка – 4 (1,1%).
Патология 12-перстной кишки имела место в 38 (10,7%) случаях, из них: парафатеральный дивертикул – 10 (2,8%), эрозивный бульбит – 8 (2,3%), эрозивный дуоденит – 6 (1,7%), полип 12-перстной кишки – 5 (1,4%), липома – 4 (1,1%), папиллит – 4 (1,1%), язва – 1 (0,3%).
Обращает на себя внимание преобладание эрозивно-язвенного поражения верхних отделов желудочно-кишечного тракта (138 случаев – 38,8%) в общей патологии (202 случая – 56,7%), при этом с диагнозом ГЭРБ или ЯБ состояли на динамическом наблюдении у гастроэнтеролога в течение последних трех лет лишь 47 (13,2%) человек.
По результатам обследования отмечен дисбаланс между выраженностью клинических проявлений заболевания и эндоскопических изменений: у 43% пациентов при наличии симптомов диспепсии при ЭГДС имели место минимальные изменения слизистой оболочки, в то же время в случае диагностики множественных эрозий и язв 45,5% больных жалоб не предъявляли.
Очевидно, что полипрагмазия, наблюдаемая среди лиц старшей возрастной группы, не только лежит в основе лекарственного поражения пищеварительного тракта, но и способствует манифестации заболевания либо утяжеляет его течение.
Таким образом, у пациентов старческого возраста эрозивно-язвенные поражения верхних отделов пищеварительного тракта встречаются в 38,8% случаев. Отсутствие жалоб, их минимальная выраженность либо наличие атипичной клинической симптоматики диктуют необходимость проведения эндоскопического контроля состояния верхних отделов пищеварительного тракта у данной категории пациентов с целью выявления поражений, своевременного назначения гастропротективной терапии. Необходимость приема массы лекарственных препаратов, неадекватная оценка своего состояния, наличие тяжелых сопутствующих заболеваний требуют от врача индивидуализированного подхода к выбору терапии, коррекции схемы лечения.
Выбор препарата для антисекреторной терапии
Основной группой препаратов, применяемых для лечения кислотозависимых заболеваний и НПВП-гастропатии, в частности, являются ингибиторы протонной помпы (ИПП). Общеизвестно, что длительность основного курса лечения как заболеваний пищевода (ГЭРБ), так и эрозивно-язвенных поражений желудка или двенадцатиперстной кишки всеми из существующих ИПП составляет от 2–4 до 12 недель в зависимости от тяжести поражения слизистой оболочки, купирования симптоматики, динамики эндоскопической картины. После заживления эрозий/язв назначается поддерживающая терапия, которая в случае, например, ГЭРБ может продолжаться от 26 до 52 недель (а при тяжелом эзофагите, возможно, пожизненно).
С учетом всего вышеизложенного, в т.ч. необходимости длительного, возможно пожизненного, приема ИПП, весьма актуальным становится вопрос выбора наиболее мощного, обеспечивающего продолжительное антисекреторное действие агента [15]. А в условиях полиморбидности, когда пациент вынужден принимать несколько лекарственных средств ежедневно, немаловажное значение в принятии решения о выборе блокатора желудочной секреции играет профиль его безопасности [3].
В этой ситуации неизбежно встает вопрос о лекарственном взаимодействии, возможном развитии нежелательных побочных явлений, поскольку, попадая в организм человека, лекарственные средства (ЛС) воздействуют не только на патологический процесс, но и вступают во взаимодействие друг с другом (под взаимодействием ЛС понимают изменение действия одного препарата под влиянием другого). Рациональным сочетанием препаратов удается в ряде случаев уменьшить их токсичность, поскольку хорошо известно, что лекарственное взаимодействие может приводить к очень серьезным неблагоприятным последствиям.
По данным статистических исследований, в результате взаимодействия ЛС развивается около 50% побочных реакций на препараты, а среди пациентов, умерших в результате побочных реакций от лекарств, приблизительно 30% скончались вследствие взаимодействия препаратов. Поэтому с целью предотвращения неблагоприятных эффектов, особенно со стороны пациентов старших возрастных групп, наиболее оправданным является подбор комбинации ЛС с наименьшей степенью взаимодействия. Исходя из этого, становится очевидной значимость оценки возможных лекарственных взаимодействий при подборе терапии.
В условиях когда пациенты пожилого и старческого возраста (в настоящем исследовании 66,3% больных принимали 5 и более препаратов ежедневно) получают одновременно сразу несколько ЛС для лечения их заболеваний, проблема лекарственного взаимодействия представляется крайне важной. Ведь неблагоприятные явления, возникшие вследствие лекарственного взаимодействия, могут приводить к потере терапевтического эффекта или усилению токсичности (передозировке).
По мере накопления практического опыта были выработаны подходы к дифференцированному использованию различных ИПП в зависимости от особенностей их фармакодинамики. Различия касаются в основном скорости наступления и продолжительности кислотоблокирующего эффекта (зависит от их рН-селективности), взаимодействия с другими одновременно принимаемыми препаратами, метаболизирующимися системой цитохрома Р450.
Установлено, что все ИПП, за исключением пантопразола, обратимо связывают или цистеин-813, или цистеин-321 (лансопразол) протонной помпы, что приводит к ковалентной блокаде помпы [16]. В отличие от них пантопразол связывается сразу с двумя цистеинами – 813 и 822. Последний цистеин имеет уникальное значение, т.к. именно он обеспечивает устойчивость связывания и длительность ингибирования протонной помпы и, соответственно, блокады продукции кислоты. Поэтому после прекращения приема других ИПП кислотность восстанавливается за счет нарушения их химической связи с протонной помпой, а при использовании пантопразола – преимущественно в результате синтеза новых помп. В итоге время восстановления секреции кислоты составляет для лансопразола около 15 часов, для омепразола и рабепразола – около 30, а пантопразола – приблизительно 46 часов. Одним словом, пантопразол обеспечивает наиболее продолжительный кислотоснижающий эффект [15, 17–21].
В печени все ИПП подвергаются экстенсивному метаболизму при участии цитохромной системы Р450. Это полифункциональная ферментная система, имеющая в своем составе около 250 установленных на сегодня изоферментов, которые участвуют не только в метаболизме лекарств, но и в синтезе ряда биологически активных субстанций. Описан такой феномен, как полиморфизм Р450, смысл которого состоит в различной активности некоторых изоферментов системы цитохрома у отдельных индивидуумов. Феномен полиморфизма имеет ряд клинически значимых следствий, среди которых наиболее важные – генетически детерминированное снижение скорости метаболизма поступившего в организм ЛС и неизбежное межлекарственное взаимодействие вследствие увеличения нагрузки на соответствующие изоферменты цитохрома Р450. Именно поэтому, метаболизируясь в печени и влияя на микросомальные ферменты гепатоцитов, большинство ИПП ингибируют метаболизм многих ЛС, принимаемых возрастными пациентами, таких как диазепам, фенитоин, варфарин, β-адреноблокаторы, дигоксин, теофиллин, диклофенак, кларитромицин.
Пантопразол не аккумулируется в организме, а повторные приемы препарата в течение суток не влияют на его фармакокинетику. Более того, с учетом особенностей метаболизма нет необходимости в специальном подборе дозы препарата для пожилых больных (или пациентов с почечной или умеренно выраженной печеночной недостаточностью). Поэтому пантопразол в условиях полиморбидности является идеальным антисекреторным препаратом для пациентов пожилого и старческого возраста, одновременно принимающих другие ЛС. По данным 15-летнего опыта применения пантопразола в дозе 40–80–160 мг/сут была доказана не только высокая заживляющая и профилактическая активность препарата при пептической язве, эрозивном эзофагите, но и его высокая безопасность на протяжении многих лет [6].
Одним из достойных представителей пантопразолов на отечественном фармацевтическом рынке является препарат Нольпаза, выпускаемый компанией КPKA.
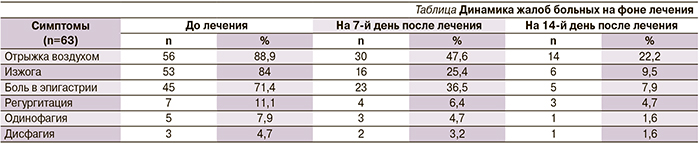
Наш собственный опыт применения Нольпазы в дозе 20 мг/сут 85 пациентами старческого возраста с эрозивно-язвенным поражением верхних отделов пищеварительного тракта (эрозивный эзофагит – 23 [27,1%] случая, острые и хронические эрозии антрального отдела желудка – 50 [59%], язва желудка – 3 [3,5%], эрозивный бульбит – 5 [5,9%], эрозивный дуоденит – 4 [4,7%] случая) показал, что к 7-му дню приема препарата купирование симптомов отмечено более чем у половины пациентов, исходно предъявлявших жалобы, у остальных интенсивность неприятных ощущений значительно уменьшилась, а практически полного прекращения жалоб удалось добиться к 14-му дню (см. таблицу).
При контрольной ЭГДС, выполненной на 28-й день, эндоскопическая ремиссия заболевания установлена в 90,6% случаев. Из оставшихся 13 пациентов 5 самостоятельно прекратили прием Нольпазы до окончания полного курса лечения, 7 категорически отказались от проведения контрольной ЭГДС. Стоит еще раз подчеркнуть, что все пациенты перенесли исследование хорошо, а в процессе лечения никаких нежелательных явлений во время приема Нольпазы зарегистрировано не было. В качестве иллюстрации приводим одно из наших клинических наблюдений.
Клиническое наблюдение
Пациентка З. 79 лет наблюдается в поликлинике с диагнозом ИБС: стенокардия напряжения, 2-й ФК, атеросклеротический и постинфарктный кардиосклероз. Гипертоническая болезнь III ст., 3-я ст., риск 4, НК II ФК (NYHA). Дислипидемия. Хронический гастродуоденит. Хронический бескаменный холецистит. Стеатоз печени. Экзогенно-конституциональное ожирение II ст. Сахарный диабет 2 типа средней тяжести. Диабетическя ангиопатия сосудов нижних конечностей. Диабетическая полинейропатия. Аутоиммунный тиреоидит, гипотиреоз. Дисциркуляторная энцефалопатия 2-й ст. смешанного генеза. Хроническая люмбоишалгия на фоне выраженных дегенеративно-дистрофических изменений позвоночника, деформирующего спондилеза, спондилоартроза, ретроспондилолистеза. Полиостеоартроз. Нарушение пуринового обмена. Хроническая болезнь почек 3-й ст.
По поводу вышеуказанных заболеваний проведено лечение, включившее Конкор 5 мг/сут, Гизаар 50/12,5 мг/сут, Норваск 5 мг/сут, Симгал 20 мг/сут, Тромбо АСС 100 мг/сут, L-тироксин 75 мкг/сут, Глюкованс 5/500 мг 2 р/д, аллопуринол 100 мг/сут. Самостоятельно для купирования болей в пояснице, суставах принимает НПВП (диклофенак).
В марте 2013 г. при обращении к терапевту поликлиники отметила, что в течение последнего месяца периодически беспокоит отрыжка воздухом, изжога, чувство тяжести в подложечной области, но по сравнению с прочими жалобами со стороны сердечно-сосудистой и костно-мышечной системы считала их второстепенными («по возрасту»).
В ходе физикального обследования выявлена болезненность при пальпации в эпигастрии. По данным ультразвукового исследования гепатобилиарной зоны отрицательной динамики не отмечено, имели место диффузные изменения печени, поджелудочной железы по типу жировой инфильтрации. Хронический бескаменный холецистит. С учетом данных анамнеза, результатов осмотра было выполнено эндоскопическое исследование, при котором установлены недостаточность кардии, язва нижней трети пищевода, поверхностный гастродуоденит, дуодено-гастральный рефлюкс, острые эрозии антрального отдела желудка, рубцовая деформация луковицы двенадцатиперстной кишки, H. pylori ++.
По результатам ЭГДС отменен Тромбо АСС, с целью адекватного обезболивания по согласованию с неврологом рекомендован прием нимесулида с одновременным приемом ИПП. С учетом необходимости проведения одновременно противоязвенной и эрадикационной терапии пациентке с хронической болезнью почек в анамнезе, ежедневно принимавшей не менее 8 лекарственных препаратов, с целью снижения риска нежелательных лекарственных взаимодействий и развития побочных эффектов при выборе ИПП предпочтение было отдано пантопразолу (Нольпазе) в дозе 20 мг/сут.
К 7-му дню лечения у больной полностью прекратилась изжога, отрыжка воздухом, уменьшилось ощущение тяжести в эпигастрии, а проведенная на 28-й день контрольная ЭГДС выявила рубцевание язвы пищевода, устранение эрозий. Пациентке было рекомендовано продолжение курса лечения Нольпазой в течение 8 недель, а далее в режиме «по требованию». От проведения эрадикационной терапии решено было воздержаться. Лечение Нольпазой пациентка перенесла хорошо, нежелательных побочных явлений зарегистрировано не было.
Заключение
У пациентов старческого возраста в 56,7% случаев при ЭГДС диагностируются эрозивно-язвенные поражения верхних отделов пищеварительного тракта. Возраст пациента не должен стать ограничением для проведения ЭГДС.
У пациентов старческого возраста имеет место дисбаланс между выраженностью клинических проявлений заболевания и эндоскопической картиной. Отсутствие жалоб или их минимальная выраженность, наличие атипичной клинической симптоматики требуют проведения эндоскопического контроля состояния верхних отделов пищеварительного тракта.
Необходимость приема большого количества лекарственных препаратов, неадекватная оценка своего состояния, наличие тяжелых сопутствующих заболеваний требуют от врача индивидуализированного подхода к выбору терапии, коррекции схемы лечения. Для лечения и профилактики кислотозависимых заболеваний у пациентов старшей возрастной группы в условиях неизбежной полиморбидности, учитывая доказанную эффективность и высокий профиль безопасности, наиболее оправданным следует признать назначение препарата Нольпаза.



