Введение
В настоящее время не вызывает сомнений, что артериальная гипертензия (АГ) и ишемическая болезнь сердца (ИБС) являются патогенетически тесно взаимосвязанными и часто сосуществующими заболеваниями, терапия которых должна проводиться с учетом соответствующих рекомендаций.
Вместе с тем за последние десятилетия одним из активно дискутируемых вопросов остается целесообразность учета гендерных особенностей эффективности и безопасности применения различных препаратов, в т.ч. блокаторов ренин-ангиотензиновой системы (РАС), для пациентов с АГ и стабильной ИБС. Так, хорошо известно, что при АГ использование женщинами ингибиторов ангиотензинпревращающего фермента (иАПФ) в 2 раза чаще, чем мужчинами, сопровождается развитием сухого кашля [1]. В то же время результаты некоторых исследований свидетельствуют о несколько большей эффективности при АГ блокаторов рецепторов ангиотензина II (БРА) для женщин по сравнению с мужчинами [2]. Кроме того, остается недостаточно исследованным вопрос эффективности различных блокаторов РАС для женщин с коморбидной патологией, в частности с сочетанием АГ и стабильной ИБС.
Не менее актуальна и проблема хронофармакотерапии, позволяющей индивидуализировать лечение кардиоваскулярной патологии у конкретного больного. Вместе с тем целесообразность применения хронофармакотерапевтического подхода к женщинам с АГ и ИБС практически не изучена.
В связи с этим целью настоящего исследования стала оценка гипотензивной эффективности иАПФ зофеноприла и БРА валсартана при одно- и двукратном режиме суточного дозирования для женщин с АГ и стабильной ИБС.
Материал и методы
В исследование были включены 100 женщин, средний возраст которых составил 57,2 ± 3,7 года.
Критерии включения пациенток в исследование:
- АГ 2-й степени;
- отсутствие достижения целевого уровня артериального давления (ЦУ АД) на фоне предшествующей (не менее 3 месяцев) антигипертензивной терапии;
- стенокардия напряжения I–II функциональных классов (ФК);
- наличие информированного согласия пациентки на участие в исследовании.
Из исследования исключались женщины с нестабильной стенокардией, перенесенным инфарктом миокарда и/или инсультом в предшествующие 6 месяцев, сложными нарушениями ритма и проводимости, хронической сердечной недостаточностью III–IV ФК (по NYHA – New York Heart Association), сахарным диабетом 1 и 2 типов, вторичной АГ, тяжелыми соматическими или психическими заболеваниями, определяющими неблагоприятный прогноз в ближайшие годы.
АГ 2-й степени диагностировали в соответствии с рекомендациями ВНОК/РМОАГ (Всероссийское научное общество кардиологов/Российское медицинское общество по артериальной гипертонии, 2010) [3]. Вторичный генез АГ исключался на основании анализа анамнестических данных, результатов клинического и лабораторно-инструментального обследований. Стабильная стенокардия II ФК диагностировалась, согласно рекомендациям ВНОК (2008), включая результаты нагрузочного (тредмил) теста [4].
Исследование было проспективным сравнительным открытым рандомизированным в параллельных группах. Для сравнительной оценки эффективности 3 вариантов комбинированной антигипертензивной терапии пациентки с АГ и ИБС были рандомизированы методом «конвертов» в 3 группы лечения:
- больные 1-й группы (n = 37) получали однократно в утренние часы комбинацию иАПФ зофеноприла 30 мг, β-адреноблокатора метопролола сукцината 50 мг и диуретика гидрохлоротиазида 12,5 мг;
- больные 2-й группы (n = 31) получали однократно в утренние часы комбинацию БРА валсартана 160 мг, метопролола сукцината 50 мг и гидрохлоротиазида 12,5 мг;
- пациенткам 3-й группы (n = 32) была назначена комбинированная терапия, включившая валсартан 80 мг 2 раза в сутки (утром и вечером), метопролола сукцинат 50 мг утром и гидрохлоротиазид 12,5 мг утром.
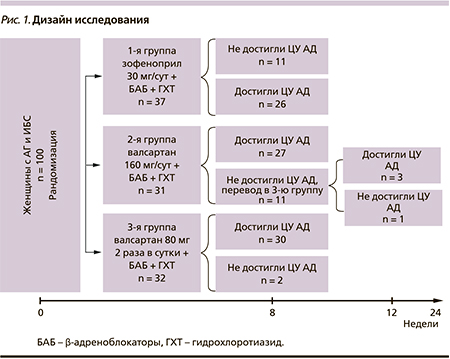
Эффективность стартовой терапии определялась через 8 недель после включения в исследование. Для пациенток 2-й группы предполагалась еще одна ступень в случае недостижения целевого АД – перевод на двукратный прием валсартана с последующей оценкой достигнутого уровня АД через 4 недели наблюдения. Кроме того, в течение наблюдения проводилась титрация дозы β-адреноблокатора для достижения целевых значений числа сердечных сокращений (ЧСС) 55–60 уд/мин. К моменту окончания исследования средняя доза метопролола сукцината была сопоставимой во всех группах и составила 95,7 ± 6,5 мг/сут в 1-й группе, 99,2 ± 5,8 во 2-й, 97,5 ± 5,4 мг/сут в 3-й группах. Дизайн исследования представлен на рис. 1.
В случае недостижения ЦУ АД на фоне лечения, соответствующего дизайну, больным дополнительно назначали амлодипин в дозе 5 мг и исключали их из последующего анализа гипотензивного эффекта.
Кроме антигипертензивной и антиишемической терапии все пациентки получали антиагрегантные (ацетилсалициловая кислота 125 мг/сут) и липидснижающие (розувастатин 10–20 мг/сут) средства, а также им была рекомендована гипохолестериновая диета.
Всем включенным в исследование женщинам исходно, через 8 и 24 недели терапии проведены общеклиническое обследование, биохимический анализ крови (определение уровней креатинина, электролитов, аспартатаминотрансферазы, аланинаминотрансферазы, креатинфосфокиназы, глюкозы, липидного спектра).
Исходно и через 24 недели наблюдения выполнено суточное мониторирование АД (СМАД) с помощью системы Tonoport V (General Electric, Германия). Анализировали среднесуточные, дневные и ночные характеристики АД, показатели вариабельности АД (Вар АД), индекс времени АГ, величину и скорость утреннего подъема АД, а также суточный индекс.
Индекс времени (ИВ) АГ рассчитан как процент измерений, превышающих нормальные показатели отдельно для каждого времени суток. Стабильная АГ диагностировалась при ИВ > 50 % в дневное и ночное время.
Величина утреннего подъема (ВУП) АД определялась в период с 4 до 10 часов утра как разница между максимальным (САДмакс/ДАДмакс) и минимальным (САДмин/ДАДмин) значениями соотношения систолического (САД) и диастолического (ДАД) АД. За нормальные показатели принимались значения, не превышающие 56,5 мм рт. ст.
Скорость утреннего подъема (СУП) АД рассчитывалась раздельно для САД и ДАД. В норме этот показатель не должен превышать 10 мм рт. ст./ч.
С учетом суточного индекса (СИ) выделено 4 типа суточного профиля АД (СПАД): «dipper» – физиологический, «non-dipper» – недостаточное снижение АД ночью, «over-dipper» – чрезмерное снижение АД ночью, «night-peaker» – ночная гипертония.
Результаты исследования были обработаны статистически с использованием пакета программ Statistica 6.1 (StatSoft Inc, США). При анализе применялись методы параметрической статистики, данные представлены в виде M ± m. Множественные сопоставления между качественными признаками проведены по критерию хи-квадрат с уровнем значимости p < 0,05.
Результаты
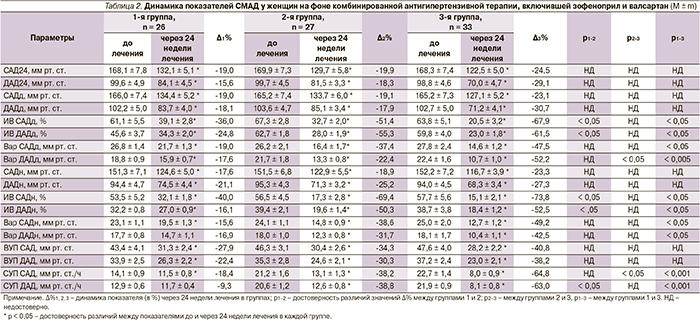
Клиническая характеристика пациенток, включенных в исследование, представлена в табл. 1.
Как следует из табл. 1, по основным изученным клинико-анамнестическим, физиологическим и антропометрическим параметрам группы обследованных женщин статистически значимо между собой не различались.
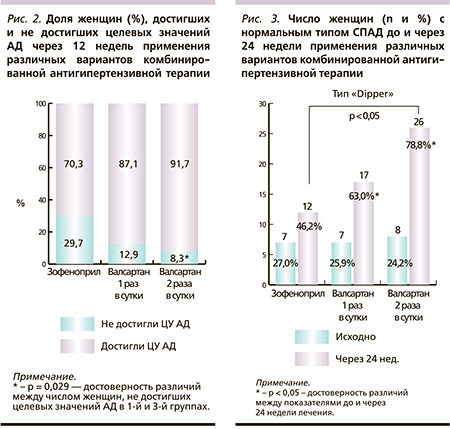
Через 8 недель применения комбинированной антигипертензивной терапии у 26 (70,3 %) женщин 1-й группы, 27 (87,1 %) 2-й и 30 (93,8 %) 3-й был зафиксирован целевой уровень АД.
Больные 1-й и 3-й групп, не достигшие целевого уровня АД через 8 недель в соответствии с дизайном (рис. 1), были исключены из исследования. Во 2-й группе 4 пациенткам был изменен режим применения валсартана с одно- на двукратный прием (утро/вечер), что обеспечило достижение ЦУ АД у трех из них.
Таким образом, через 12 недель терапии наибольшее число пациенток с ЦУ АД (33 человека) было в 3-й группе (рис. 2). В той же группе было достоверно меньше по сравнению с 1-й (терапия, основанная на зофеноприле) женщин, которыми не были достигнуты целевые значения АД (р = 0,029).
Анализ результатов СМАД через 24 недели использования комбинированной антигипертензивной терапии показал, что положительная динамика основных показателей суточного профиля АД отмечена во всех 3 группах наблюдения (табл. 2).
Независимо от выбранного варианта и режима дозирования комбинации антигипертензивных препаратов имело место достоверное снижение среднесуточных, дневных и ночных уровней САД и ДАД, а также показателей «нагрузки давлением» (ИВ САД и ИВ ДАД), Вар АД, величины и скорости утреннего подъема (ВУП и СУП) АД. Вместе с тем снижение Вар ДАД в ночные часы, а также СУП ДАД на фоне терапии зофеноприлом не достигло статистической значимости.
Сравнительный анализ межгрупповой динамики основных показателей СМАД показал, что однократный прием 160 мг валсартана сопровождался достоверно более значимым, чем при использовании зофеноприла, уменьшением ИВ САД и ДАД как в дневные, так и ночные часы, а также существенным снижением СУП ДАД (табл. 2). В группе пациенток, получавших валсартан 2 раза в сутки, по сравнению с терапией зофеноприлом имело место достоверно более выраженное уменьшение ИВ САД и ДАД в дневные и ночные часы, Вар САД и ДАД днем и ночью, а также СУП САД и ДАД. При сравнении двух режимов дозирования валсартана (1 или 2 раза в сутки) отмечены сопоставимые позитивные изменения основных показателей суточного профиля АД (табл. 2).
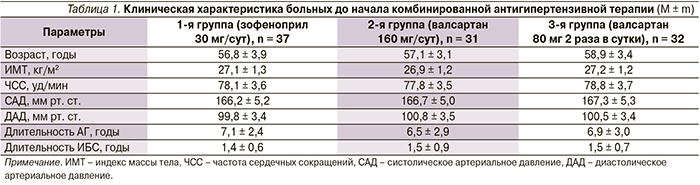
Использование каждого из трех вариантов комбинированной антигипертензивной терапии сопровождалось увеличением числа пациенток с нормальным суточным профилем АД «dipper». Вместе с тем статистически значимо изменилось число женщин с физиологическим профилем АД только во 2-й и 3-й группах, получавших валсартан 1 или 2 раза в сутки (рис. 3). Более того, нормализация СПАД отмечалась достоверно чаще на фоне двукратного приема валсартана по сравнению с применением зофеноприла.
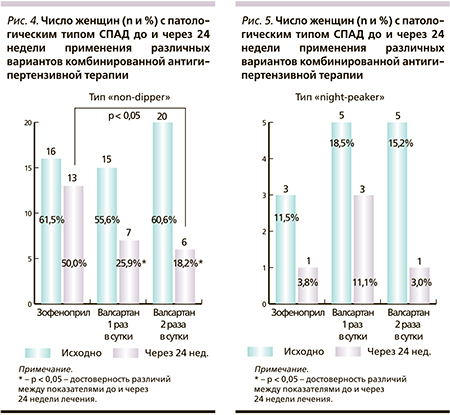
Оптимизация СПАД сопровождалась уменьшением числа больных патологическими типами суточных кривых «non-dipper» и «night-peaker» (рис. 4, 5). В то же время использование валсартана в отличие от терапии зофеноприлом обеспечивало достоверное уменьшение числа больных с профилем «non-dipper». При межгрупповом сравнении было определено, что через 24 недели применения валсартана 2 раза в сутки число женщин с недостаточным снижением АД в ночные часы оказалось в 2 раза меньше, чем при применении зофеноприла (р < 0,05) (рис. 4). Уменьшение числа пациенток с профилем «night-peaker» во всех трех группах не достигло статистической значимости, что могло быть связано с исходно небольшим числом больных с данным типом суточной кривой АД (рис. 4).
Таким образом, применение женщинами с АГ и стабильной ИБС комбинированной антигипертензивной терапии, включившей валсартан, обеспечивало более значимые по сравнению с использованием терапии, основанной на зофеноприле, позитивные изменения основных показателей суточного профиля АД, а также достоверное увеличение числа пациенток с физиологическим снижением АД в ночные часы. Вместе с тем результаты исследования показали, что для данной категории больных двукратный режим приема валсартана имел преимущества как перед однократным его приемом, так и перед применением зофеноприла.
Обсуждение
Современные рекомендации по ведению пациентов с АГ и стабильной ИБС предполагают назначение блокаторов РАС как средств, улучшающих прогноз [3, 4]. Доминирующая роль в этой клинической ситуации отводится иАПФ, а при их непереносимости назначают БРА. В то же время к настоящему времени до конца не определены гендерные особенности эффективности различных блокаторов РАС. Кроме того, активно дискутируются хронофармакотерапевтические аспекты лечения кардиоваскулярной патологии.
В нашем исследовании была предпринята попытка сравнить гипотензивную эффективность комбинированной терапии женщин с неконтролируемой АГ и ИБС с использованием иАПФ зофеноприла и двух режимов дозирования БРА валсартана: прием 1 или 2 раза в сутки.
Как показали результаты проведенного исследования, использование всех трех вариантов комбинированной антигипертензивной терапии было достаточно эффективным и сопровождалось однонаправленными позитивными изменениями показателей СМАД и типов СПАД.
Вместе с тем применение валсартана по сравнению с терапией, основанной на зофеноприле, обеспечило более частое достижение целевых значений АД, способствовало более выраженным позитивным изменениям параметров СПАД и в результате нормализации суточного профиля АД у большинства пациенток. Более того, именно двукратных прием БРА оказался наиболее эффективным вариантом лечения женщин с неконтролируемой АГ и ИБС.
Определенные преимущества БРА перед иАПФ, установленные в нашем исследовании, можно попытаться объяснить с нескольких позиций. Все включенные в исследование женщины находились в менопаузе. Хорошо известно, что в этот период в развитии и поддержании высокого АД важную роль играют гиперактивация РАС и часто вторичный гиперальдостеронизм [5–7]. Не исключено также, что у части пациенток на фоне применения иАПФ может развиваться феномен «ускользания» альдостерона. Кроме того, имеются данные, что у женщин РАС активизируется преимущественно по АПФ-независимому пути с участием химаз, катепсина G, тонина, фермента CAGE и др. тканевых биоактивных веществ, приводящих к синтезу ангиотензина II (АII) [8–10]. Важно и другое: в период менопаузы в условиях дефицита эстрогенов увеличивается экспрессия рецепторов 1-го типа к АII в тканях [11]. Некоторые экспериментальные исследования свидетельствуют о том, что у женщин значительная роль в повышении АД принадлежит именно активации рецепторов к АII [12, 13]. Вероятно, в таких условиях можно ожидать большей эффективности БРА, чем иАПФ.
Одной из задач нашего исследования была оценка эффективности различных режимов дозирования валсартана – одно- или двукратного приема в суточной дозе 160 мг. Полученные нами результаты свидетельствуют, что двукратный прием валсартана был более эффективным, чем его однократное применение, что можно объяснить высокой вариабельностью суточного АД у обследованных женщин, а также возможной гиперактивацией РАС в ночные часы (исходно у всех женщин доминировал тип «non-dipper»), что требовало более равномерного подавления активности РАС [14–16]. Кроме того, блокада рецепторов АII при применении валсартана развивается уже через 2–4 часа, а период полувыведения составляет 6–9 часов, поэтому двукратный прием препарата может, по-видимому, обеспечивать лучший гипотензивный эффект, чем однократный [17–19].
Заключение
Согласно полученным результатам, у женщин с сочетанием АГ и стабильной ИБС комбинированная антигипертензивная терапия, основанная на валсартане, может иметь преимущества по сравнению с использованием зофеноприла. Двукратный прием валсартана (80 мг утром и вечером) оказался эффективнее, чем однократный утренний прием препарата в дозе 160 мг и сопровождался достижением целевых значений АД значительным числом (91,7 %) женщин с АГ и ИБС, улучшением всех основных показателей СМАД и достоверным увеличением числа (78,8 %) лиц с «физиологическим» профилем АД.



