Е жегодно в России регистрируется более 50 млн случаев острых респираторных заболеваний (ОРВИ). Значительно чаще болеют дети, высокая восприимчивость которых обусловлена не только многочисленностью возбудителей, вызывающих заболевания, и отсутствием массовой специфической профилактики, но и особенностями функционирования иммунной системы, в частности недостаточной способностью к синтезу интерферонов – ИФН [1, 2]. Низкий исходный уровень ИФН у детей младших возрастных групп и нарушенная их продукция при реализации заболевания являются факторами, стимулирующими повышенный интерес исследователей к использованию интерфероновых препаратов как для профилактики, так и для лечения респираторных вирусных инфекций. Терапевтические подходы систематически совершенствуются [3, 4]. В настоящее время актуальной проблемой остается создание алгоритма лечения инфекционных заболеваний у детей грудного и раннего детского возраста. Это связано как с ограниченным выбором лекарственных средств, так и с сокращением числа разрешенных к применению препаратов данными возрастными группами детей [5].
Многолетнее успешное использование антибиотиков в лечении инфекционных заболеваний у детей выявило и ряд их побочных эффектов, таких как иммуносупрессивное влияние, возникновение дисбиотических расстройств, склонность клинических проявлений к рецидивированию, формирование резистентных штаммов возбудителей и снижение клинической эффективности.
Указанные недостатки антибактериальной терапии стимулировали разработку альтернативных терапевтических подходов, основанных на применении современных иммунобиологических препаратов, клиническая эффективность которых определяется модуляцией базисной иммунореактивности больного ребенка, что в свою очередь позволяет улучшать исходы и снижать дальнейшее распространение инфекций [6, 7].
С учетом частоты распространения вирусных инфекций, возникновения бактериальных осложнений и затяжного течения у детей, особенно раннего возраста, одним из перспективных направлений терапии следует признать использование готовых лекарственных форм человеческого рекомбинантного ИФН-α-2b. Целесообразность его применения обусловлена тем, что ИФН является естественным фактором в защитной системе организма, играющим особо важную роль у детей. Преимущество рекомбинантных форм ИФН в отличие от нативного составляет возможность введения достаточного количества действующего вещества в малых объемах, не сталкиваясь с возможностью побочных эффектов от приема последнего [8, 9]. Первым препаратом рекомбинантного ИФН-α в суппозиториях, разрешенным к применению детьми раннего возраста, является Виферон® (ООО «Ферон», Россия). Эффективность и безопасность препарата Виферон® были подтверждены в ходе многочисленных клинических исследований по оценке фармакологических свойств данного препарата в терапии ОРВИ и других инфекционно-воспалительных заболеваний у детей грудного возраста начиная с периода новорожденности, в т. ч. у недоношенных [10].
Российской фармацевтической компанией БИОКАД была разработана новая лекарственная форма на основе рекомбинантного ИФН – суппозитории Генферон® Лайт, предназначенные для вагинального и ректального введения. Генферон® Лайт является аналогом широко применяемого в России и за рубежом препарата Генферон®, по составу отличаясь от него сниженным содержанием действующих веществ и отсутствием бензокаина, а по форме – сниженными массой и размерами суппозитория.
Основными действующими веществами лекарственной формы Генферон® Лайт являются ИФН человеческий рекомбинантный α-2b и таурин. ИФН обладает опосредованным противовирусным, противовоспалительным, иммуномодулирующим эффектами и в различных лекарственных формах используется в практике здравоохранения, в т. ч. детьми, на протяжении многих лет. Таурин – незаменимая аминокислота, образующаяся в организме в процессе метаболизма цистеина. Таурин, включенный в состав лекарственной формы, повышает биологический эффект действия ИФН за счет антиоксидантных свойств, а также участвует в усилении регенерации поврежденных тканей, способствует нормализации метаболических процессов, увеличивает работоспособность при физических нагрузках [11–14].
Возрастные дозировки: детям с 6 месяцев до 7 лет – по 1 суппозиторию (125 000 МЕ ИФН-а-2b) 2 раза в сутки, детям старше 7 лет и взрослым (250 000 МЕ ИФН-а-2b) – 2 раза в сутки.
Курс лечения при ОРВИ и других острых заболеваниях вирусной природы у детей: по 1 суппозиторию (125 000 МЕ) ректально 2 раза в сутки с 12-часовым интервалом параллельно основной терапии в течение 5 дней. При сохранении симптоматики курс лечения повторяется после 5-дневного интервала.
Цель исследования: оценить клинико-лабораторную эффективность препарата Генферон® Лайт в комплексном лечении острых респираторных заболеваний у детей.
Материал и методы
В исследование включены 200 пациентов (129 мальчиков и 71 девочка): 100 детей в возрасте от 6 месяцев до 3лети100детейввозрастеот2до7лет с диагнозом ОРВИ, находившихся на стационарном лечении.
Сопоставимые по возрасту и клиническому диагнозу пациенты были распределены в две группы – основную и группу сравнения. Основную группу составили 108 детей, которые получали препарат Генферон Лайт® (125 000 МЕ) ректально 2 раза в сутки одновременно с симптоматической терапией. В группу сравнения включены 92 ребенка, которые получали симптоматическую терапию в сочетании с препаратом Виферон®-1 (150 000 МЕ) ректально 2 раза в сутки в течение 5 дней.
Выполнялись клинико-лабораторные исследования (общие анализы крови и мочи, прямое иммунофлуоресцентное исследование [ПИФ] или полимеразная цепная реакция [ПЦР] для выявления респираторных вирусов) в динамике – до начала лечения и после завершения курса лечения (6-й день).
Статистическая обработка данных выполнена с использованием программ Microsoft Offiсe, Excel 2003 с определением критериев Стьюдента, Шапиро–Уилка, Фишера; непараметрических критериев Манна–Уитни и Вилкоксона.
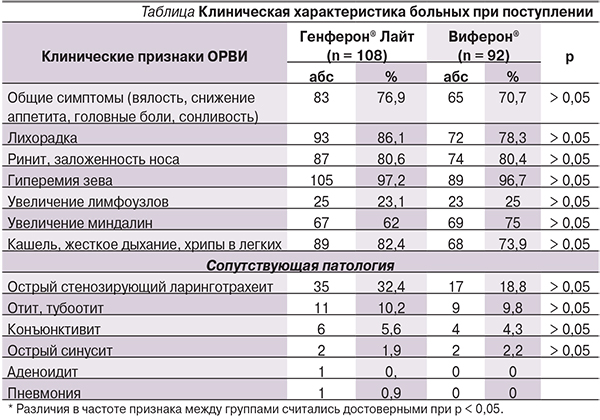
Клиническая картина ОРВИ характеризовалась следующими симптомами (см. таблицу).
Результаты исследования
Оценка эффективности применения препаратов Генферон® Лайт и Виферон® детьми в возрасте от 6 месяцев до 3 лет
Лихорадочный синдром
На момент включения пациентов в исследование лихорадочный синдром наблюдался в 85 % случаев, в среднем температура тела составляла 37,8 ± 0,9 °С, длительность лихорадочного синдрома в основной группе – в среднем 2,79 ± 1,4, в группе сравнения – 2,7 ± 1,5 дня (р > 0,05). По окончании приема исследуемых препаратов лихорадка сохранялась в 9,6 % случаев (у 5 из 52 детей с лихорадкой) в основной группе ив9,1%(у3из33детейслихорадкой) в группе сравнения (р > 0,05).
Заложенность носа
Заложенность носа у больных при поступлении наблюдалась в несколько большем проценте случаев в основной группе (84,5 против 80,1 % в группе сравнения) с одинаковой выраженностью симптома 2 [1–2] балла (медиана и интерквартильный размах), что соответствовало умеренной выраженности. После лечения (6-й день) заложенность носа регистрировалась с частотой, более чем в 2 раза ниже по сравнению с группой Виферона®: 14,3 против 32,4% (р > 0,05).
Ринорея
При поступлении в стационар ринорея наблюдалась в общей сложности у 90 % детей, несколько чаще данный симптом регистрировали в основной группе (94,8 против 83,3 %; р > 0,05) и средней выраженностью в 2 [1–2] балла (слизисто-гнойный характер отделяемого из носа). К моменту завершения терапии у подавляющего большинства детей ринорея отсутствовала, у трети (34 больных) наблюдались остаточные явления в виде скудного слизистого отделяемого (в 32,7 % случаев в основной группе и в 45,7 % – в группе сравнения).
Отечность миндалин
Увеличение миндалин наблюдалось у 59 (59 %) пациентов обеих групп, средний балл составил 2 [1–3]. В конце лечения минимальные проявления отечности миндалин регистрировались у 17 детей (15,5 % участников основной группы и 19 % пациентов группы сравнения; p > 0,05), на 6-й день средняя выраженность симптома составила в обеих группах 0 [0–1] баллов.
Гиперемия задней стенки глотки
Гиперемия задней стенки глотки являлась наиболее часто встречающимся клиническим проявлением ОРВИ и регистрировалась при поступлении в 98,3 % наблюдений в основной группе и в 100 % – в группе сравнения. К 6-му дню от начала лечения данный симптом купировался у половины больных как в основной, так и в группе сравнения, у остальных детей к данному сроку наблюдения отмечена слабовыраженная гиперемия слизистых оболочек (р > 0,05), что соответствовало среднему баллу 1 [0–1].
Количество и характер мокроты
В первый день исследования у 43 (74,1 %) пациентов основной группы и 33 (78,6 %) – группы сравнения наблюдался кашель с отхождением мокроты слизистого характера (р = 0,4). У 6 пациентов основной и 4 – группы сравнения отмечена слизистогнойная мокрота. На 6-й день отхождение мокроты наблюдалось у 18 (31 %) пациентов основной группы и у 16 (38,1 %) – группы сравнения (р = 0,3). При анализе изменений медианы итогового балла в обеих группах выявлено,
что начиная с 3-х суток терапии средний балл тяжести клинических проявлений ОРВИ в основной группе был на один балл меньше, чем в группе сравнения, однако без статистически достоверных отличий. К 6-му дню от начала терапии медиана итогового балла в основной группе составила 2 [0–6], в группе сравнения – 3 [0–7] (критерий Манна–Уитни, р > 0,05).
Элиминация возбудителя ОРВИ
Верификация вирусной природы возбудителя наблюдалась у 66 (66 %) пациентов обеих групп. В группе детей, получавших Генферон® Лайт, возбудитель ОРВИ выявлен у 40 (69 %) детей; из них вирус гриппа А обнаружен у 14 (24,1 %), вирус парагриппа – у 7 (12,1 %), аденовирус – у 6 (10,3 %), респираторносинцитиальный вирус – у 6 (10,3 %), риновирус – у 2 (3,4%), коронавирус – у 1 (1,7 %), бокавирус – у 2 (3,4 %); кроме того, у 2 (3,4 %) пациентов наблюдалось микст-инфицирование (вирус гриппа А + вирус гриппа В). Положительные результаты ПЦР/ ПИФ соскобов из глубоких отделов нижних носовых ходов для определения возбудителя ОРВИ в группе сравнения получены от 26 (62 %) детей: вирус гриппа А обнаружен у 7 (16,7 %) пациентов, вирус парагриппа – у 8 (19 %), аденовирус – у 1 (2,4 %), респираторно-синцитиальный вирус – у 3 (7,1 %), риновирус – у 2 (4,8 %); микст-инфицирование вирусами гриппа А и В наблюдалось у 1 (2,4 %) ребенка, вирусом гриппа А и аденовирусом у 2 детей (4,8 %), вирусом парагриппа и респираторно-синцитиальным вирусом в 1 (2,4 %) случае и вирусом парагриппа и аденовирусом – в1(2,4%).
После проведенной терапии в основной группе элиминация возбудителей наблюдалась в 67,5 % случаев (т. е. из 40 пациентов с верифицированной вирусной этиологией респираторной инфекции элиминация наблюдалась у 27), у одного ребенка к 6-му дню терапии наблюдалось суперинфицирование вирусом гриппа А на фоне элиминации вируса парагриппа, у 2 пациентов выявлены возбудители ОРВИ (грипп А в одном и парагрипп во втором случаях), не обнаруженные при первом обследовании.
В группе сравнения элиминация возбудителей зарегистрирована у 17 (65,4 %) пациентов (из 26), у 1 пациента обнаружен аденовирус, не выявленный при первом исследовании.
Таким образом, элиминация возбудителей ОРВИ на фоне лечения основной и группы сравнения наблюдалась с одинаковой частотой (р = 0,53).
Оценка эффективности применения препаратов Генферон® Лайт и Виферон® детьми в возрасте от 2 до 7 лет
Лихорадочный синдром
У 48 (96 %) больных основной и у 41 (82 %) – группы сравнения обнаружена лихорадка – температура тела выше 37 °С. На фоне лечения большинству больных обеих групп удалось купировать лихорадку. На 5-й день лечения нормализация температуры тела отмечена у 46 (96 %) из 48 больных основной и у 38 (93 %) из 41 больного группы сравнения.
Заложенность носа
Для 97 из 100 детей ОРВИ протекала с заложенностью носа. В результате лечения регресс симптома в основной группе наблюдался у достоверно большего, чем в группе сравнения, числа детей (72 против 52 %, точный критерий Фишера; р = 0,04). Заложенность носа уменьшилась у 13 (28 %) и 21 (44 %) больного соответственно. Только у 2 (4 %) больных группы сравнения не было динамики.
Ринорея
Ринит с наличием отделяемого из носа отмечен у большинства больных – у 83 из 100 детей. До лечения в основной группе количество отделяемого из носа было выражено умеренно (медиана – 2 балла), в группе сравнения данный симптом был выражен слабо (медиана – 1 балл). После лечения ринорея прекратилась в основной группе у 28 (62,2 %) пациентов и в группе сравнения – у 19 (50 %); достоверных различий не выявлено. Уменьшение симптома зарегистрировано у 15 (33,3 %) и 16 (42,1 %) детей обеих групп соответственно.
Отечность миндалин
Отечность миндалин наблюдалась у 71 из 100 больных. По данным полипараметрической таблицы, до лечения у детей обеих групп имела место умеренно выраженная отечность миндалин (медиана – 2 балла). После лечения в обеих группах зарегистрирована выраженная положительная динамика – в большинстве наблюдений к 5-му дню симптом отсутствовал (медиана – 0 баллов).
Так, регресс отечности миндалин наблюдался у достоверно большего числа больных основной группы, чем в группе сравнения (83 против 50 %; р < 0,05). У 5 (14 %) больных основной и 17 (47 %) группы сравнения отечность миндалин стала меньше. У 1 (3 %) ребенка каждой группы сохранялась слабовыраженная отечность миндалин.
Гиперемия задней стенки глотки
Гиперемия задней стенки глотки отмечена у 99 из 100 детей, в обеих группах до лечения она оценивалась как сильно выраженная, а на 5-й день
лечения – слабовыраженная. В основной группе симптом полностью купировался у 23 (47 %) пациентов, уменьшился в 25 (51 %) наблюдениях; у 1 (2 %) ребенка степень выраженности симптома к концу лечения не изменилась (умеренно выраженная гиперемия). Различия в регрессе данного синдрома были статистически достоверными (точный критерий Фишера, р = 0,04). В группе сравнения симптом полностью купировался только у 10 (20 %) больных, уменьшился у 38 (76 %) и у 2 (4 %) остался без динамики.
Количество мокроты
Кашлем с отделением мокроты страдали 52 из 100 больных. В результате лечения симптом купировался у 13 (52 %) больных основной и у 11 (41 %) – группы сравнения (р = 0,25). У остальных (48 и 59 % соответственно) больных после лечения сохранялось небольшое количество мокроты.
Характер отделяемого из носа и мокроты
Отделяемое из носа и мокрота у 91 из 100 больных имели слизистый (преимущественно) или слизисто-гнойный характер. К концу лечения у большинства пациентов отделяемое из носа и мокрота прекратились: у 30 (62,5 %) больных основной и у 21 (49 %) больного группы сравнения (р > 0,05).
До лечения в группе Генферона® Лайт итоговый балл (медиана и интерквартильный размах, рис. 1) составил 11 [10–14], что статистически не отличалось от показателей группы сравнения – 10 [9–13] баллов (критерий Манна–Уитни, р = 0,1), а после лечения итоговый балл был статистически ниже в основной группе больных – 3 [1–5] и 4 [2–6] балла соответственно (критерий Манна–Уитни, р = 0,045).
Элиминация возбудителей ОРВИ
В основной группе возбудители ОРВИ до начала лечения были выявлены у 27 детей, из них – у 23 – один вирус, и у 4 – два вируса. В группе сравнения вирусы выявлены у 28 больных, из них у 22 – один вид возбудителя и у 6 – два.
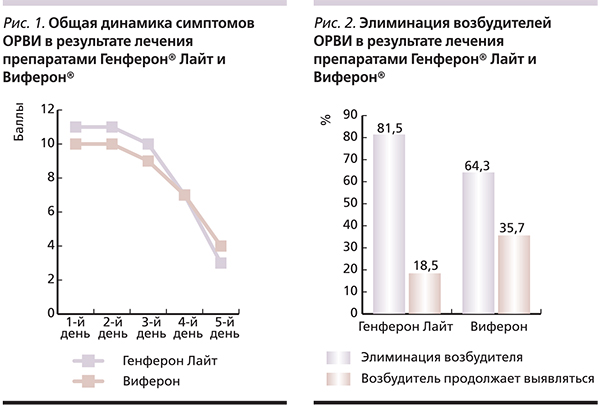
В конце лечения в основной группе полная элиминация возбудителей отмечена у 22 (81,5 %) из 27 больных, у 5 (18,5 %) больных возбудители продолжали выявляться (у 1 больного – респираторно-синтициальный и аденовирус, у 1 – риновирус, у 3 – вирус парагриппа). В группе сравнения элиминация достигнута у 18 (64,3 %) из 28; у 10 (35,7 %) детей вирус сохранялся (рис. 2). Таким образом, полная элиминация возбудителя чаще отмечалась в основной группе – в 81,5 % случаев, тогда как в группе сравнения возбудитель был элиминирован в 64 % (р = 0,07).
Заключение
Результаты открытого сравнительного рандомизированного проспективного исследования, выполненного в соответствии с разрешением Минздрава РФ и сравнивавшего эффективность и безопасность применения двух отечественных препаратов Генферона® Лайт (ЗАО БИОКАД, Россия) и Виферона® (ООО «Ферон», Россия) при лечении ОРВИ у 200 детей грудного, раннего детского и дошкольного возраста, свидетельствуют о сопоставимой клинико-лабораторной эффективности в отсутствие побочных и аллергических реакций.
Назначение препаратов Генферон® Лайт и Виферон® больным ОРВИ с сопутствующей патологией верхних и нижних дыхательных путей (ларинготрахеитом, бронхитом, пневмонией, отитом, гайморитом) способствует исчезновению симптомов интоксикации, включая лихорадку, положительная динамика которой в исследовании отмечена у 92–93 % детей младшего возраста и у 93–96 % детей старше 2 лет.
Катаральные признаки ОРВИ (заложенность носа, ринорея, гиперемия задней стенки глотки, отечность миндалин) к 6-му дню лечения детей, получавших препарат Генферон® Лайт, купировались достоверно чаще, чем у больных группы сравнения, что в итоге оказало влияние на интегральную оценку тяжести течения ОРВИ.
Элиминация возбудителей ОРВИ к концу лечения препаратами ИФН была достигнута в основной группе с большей частотой (67,5–81,5 %), чем в группе сравнения (64–65,4 %), без статистически достоверных различий.
Таким образом, препарат Генферон® Лайт, применяемый детьми различных возрастных групп в комплексной терапии ОРВИ, проявил себя как эффективный и хорошо переносимый препарат, обладающий широким спектром терапевтических свойств и подтвержденной безопасностью, позволяет снижать выраженность клинических проявлений заболевания, сокращать сроки его течения, ускорять элиминацию возбудителя, избегать возникновения осложнений и тяжелых форм респираторных инфекций.


