Определение
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) – хроническое рецидивирующее заболевание, обусловленное спонтанным, регулярно повторяющимся забросом в пищевод желудочного и/или дуоденального содержимого, что приводит к повреждению дистального отдела пищевода и появлению характерных симптомов (изжоги, ретростернальных болей, дисфагии).
ГЭРБ как самостоятельная нозологическая единица официально была утверждена международной рабочей группой по изучению ее диагностики и лечению в октябре 1997 г. (Генваль, Бельгия).
Эпидемиология
Истинная распространенность заболевания мало изучена. Это связано с большой вариабельностью клинических проявлений: от эпизодически возникающих изжог, из-за которых больные редко обращаются к врачу, до ярких признаков осложненного рефлюкс-эзофагита (РЭ), требующего госпитального лечения.
Среди взрослого населения Европы и США изжога, кардинальный симптом ГЭРБ, встречается в 20–40 % [1, 2]. В Италии проведено большое исследование по проекту LoianoMonghidoro (2004) и установлено, что распространенность ГЭРБ в популяции составляет 43,9 %, эрозивный РЭ выявлен в 13,4 %, неэрозивная рефлюксная болезнь – в 30,5 % случаев. Распределение по стадиям (по классификации Savary–Miller): I – 80,6 %; II–8,5%;III–2,3%;IV–0,8%;пищевод Барретта (ПБ) обнаружен в 7,8 % случаев.
В России распространенность ГЭРБ среди взрослого населения составляет 20–60 %. Так, в популяции взрослого населения Новосибирска, по данным эпидемиологического исследования, изжогу испытывают 61,7 % мужчин и 63,6 % женщин, причем соответственно у 10,3 и 15,1 % она отмечалась часто или постоянно [3]. О.Н. Минушкин и совт. при обследовании 530 пациентов, подвергшихся эзофагогастродуоденоскопии, обнаружили, что распространенность ГЭРБ составила 30 %, эрозивный эзофагит выявлен в 13 %, неэрозивная рефлюксная болезнь (НЭРБ) – в 16,7 % случаев [4].
Этиология и патогенез
ГЭРБ – многофакторное заболевание. Непосредственно РЭ вызывает длительный контакт желудочного (соляной кислоты, пепсина) или дуоденального (желчных кислот, лизолецитина) содержимого (последнее встречается существенно реже – в 7 % случаев) со слизистой оболочкой пищевода (СОП).
Выделяют следующие причины, приводящие к развитию заболевания [5, 6]:
- недостаточность запирательного механизма кардии;
- рефлюкс желудочного и дуоденального содержимого в пищевод;
- снижение пищеводного клиренса;
- уменьшение резистентности СОП.
Недостаточность запирательного механизма кардии
Поскольку давление в желудке выше, чем в пищеводе, рефлюкс желудочного содержимого в пищевод должен быть явлением постоянным. Однако благодаря запирательным механизмам кардии он возникает редко, на короткое время (менее 5 минут). Нормальные показатели рН в пищеводе – 5,5–7,0. Пищеводный рефлюкс следует считать патологическим, если общее число эпизодов рефлюксов в течение суток превышает 50 или если общее время снижения внутрипищеводного рН менее 4 в течение суток составляет более 4 часов.
Главную роль в запирательном механизме кардии отводят состоянию нижнего пищеводного сфинктера (НПС). У здоровых лиц давление в данной зоне составляет 20,8 ±3 мм рт. ст. У больных ГЭРБ эти цифры снижаются до 8,9 ± 2,3 мм рт. ст.
Другим важным элементом запирательного механизма кардии является угол Гиса. Он представляет собой угол перехода стенки пищевода в большую кривизну желудка. Воздушный пузырь желудка и внутрижелудочное давление способствуют тому, что складки слизистой оболочки, образующей угол Гиса, плотно прилегают к правой стенке, тем самым предотвращая забрасывание содержимого желудка в пищевод (клапан Губарева).
Часто ретроградное попадание желудочного содержимого в пищевод наблюдается среди пациентов с хиатальной грыжей. Дистопия желудка в грудную полость приводит к исчезновению угла Гиса и нарушению клапанного механизма кардии. Грыжа пищеводного отверстия диафрагмы служит достаточно частой причиной развития ГЭРБ. Хиатальная грыжа обнаруживается у 50 % обследуемых в возрасте старше 50 лет.
Роль рефлюкса желудочного содержимого при ГЭРБ Прослеживается положительная связь между вероятностью РЭ и уровнем закисления пищевода. Однако ведущая роль отводится не абсолютным показателям агрессивных компонентов желудочного содержимого, попадающих в пищевод, а снижению клиренса и резистентности СОП.
Пищеводный клиренс – скорость убывания химического раздражителя из полости пищевода. Эзофагеальный клиренс обеспечивается за счет активной перистальтики органа, а также ощелачивающего компонента слюны и слизи. При ГЭРБ происходит замедление пищеводного клиренса, связанного прежде всего с ослаблением перистальтики пищевода и с дисфункцией антирефлюксного барьера.
Резистентность СОП обусловлена преэпителиальным, эпителиальным и постэпителиальным факторами. Повреждение эпителия начинается, когда ионы водорода преодолевают водный слой, омывающий слизистую оболочку, преэпителиальный защитный слой слизи и активную бикарбонатную секрецию. Клеточная резистентность к ионам водорода зависит от нормального уровня внутриклеточной pH (7,3–7,4). Некроз возникает, когда этот механизм исчерпывается и происходит гибель клеток вследствие их резкого закисления. Противостоит образованию изъязвлений увеличение клеточного оборота за счет усиленного размножения базальных клеток СОП. Постэпителиальным эффективным защитным механизмом от кислотной агрессии является кровоснабжение слизистой оболочки.
Таким образом, длительное закисление пищевода относится к основным причинам развития ГЭРБ, а поэтому закономерно относить ГЭРБ к кислотозависимым заболеваниям.
Клиника
Среди симптомов ГЭРБ ведущее значение имеет изжога. Вторым по частоте проявлением данного заболевания является ретростернальная боль. Боль иррадиирует в межлопаточную область, нижнюю челюсть, левую половину грудной клетки и может имитировать стенокардию. Для дифференциальной диагностики генеза болей важно выявить факторы, провоцирующие и купирующие боли. Для эзофагеальных болей характерны их связь с приемом пищи, положением тела; купирование приемом щелочных минеральных вод и соды (“щелочной тест”) и появление их при перфузии пищевода 0,1 %-ным раствором соляной кислоты (“тест Бернштейна”) [7]. Дисфагия обычно служит признаком осложненного течения ГЭРБ – стенозирования дистального отдела пищевода.
В настоящее время большое внимание привлечено к внепищеводным проявлениям ГЭРБ [8, 9, 10].
Выделяют следующие синдромы экстрапищеводных проявлений ГЭРБ:
- Орофарингеальная симптоматика включает воспаление носоглотки, развитие эрозии эмали зубов, кариеса, периодонтита, фарингит, ощущение кома в горле.
- Отоларингологическая симптоматика проявляется ларингитом, изредка ларингеальным крупом, язвами, гранулемами и полипами голосовых складок, стенозированием гортани ниже голосовой щели, раком гортани, средним отитом, оталгиями и ринитом.
- Бронхолегочная симптоматика проявляется хроническим рецидивирующим бронхитом, развитием бронхоэктазов, аспирационной пневмонии, абсцессов легкого, кровохарканьем, ателектазом легкого или его долей, пароксизмальным ночным апноэ и приступами пароксизмального кашля, а также бронхиальной астмой.
- Боли в грудной клетке, связанные с заболеваниями сердца и/или их провоцирующие, проявляются рефлекторной стенокардией, развитием ишемии миокарда при рефлюксе содержимого желудка в пищевод. Боли могут сопровождаться появлением аритмии, подъемами артериального давления или развиваться самостоятельно.
- Боль в грудной клетке, не связанная с заболеваниями сердца (non-cаrdiac chest pain), – частое осложнение ГЭРБ, требующее адекватной терапии на основе проведения тщательного дифференциального диагноза с синдромом кардиальной боли. Широко дискутируется роль ГЭРБ как патогенетического фактора заболеваний бронхолегочной системы. ГЭРБ может служить триггером такого заболевания, как бронхиальная астма. Установление связи бронхиальной астмы с гастроэзофагеальным рефлюксом имеет большую клиническую ценность, поскольку позволяет по-новому подойти к их лечению [11].
Классификация
Согласно Международной классификации болезней 10-го пересмотра, ГЭРБ относится к рубрике К.21 и подразделяется на ГЭРБ с эзофагитом (К21.0) и без эзофагита (К21.1).
Для классификации ГЭРБ принципиальное значение имеет степень выраженности РЭ.
В 1994 г. в Лос-Анджелесе была принята классификация. Одним из преимуществ Лос-Анджелесской классификации является ее относительная простота при использовании в повседневной практике. Лос-Анджелесскую классификацию РЭ было рекомендовано использовать при формировании эндоскопического диагноза (табл. 1).
Наряду с Лос-Анджелесской классификацией сохранила свое значение классификация Savary–Miller (1978) в модификации Carisson и соавт. (1996), представленная в табл. 2.
Последние годы широко используется новая, принятая на IX Европейской гастроэнтерологической неделе в Амстердаме (2001) клиникоэндоскопическая классификация, которая подразделяет ГЭРБ на три группы:
- Неэрозивную наиболее частую форму (60 % ко всем случаям ГЭРБ), к которой относят ГЭРБ без признаков эзофагита и катаральный РЭ.
- Эрозивно-язвенную форму (34 %), ее осложнения: язва и стриктура пищевода.
- ПБ, 6 %, – метаплазию многослойного плоского эпителия в дистальном отделе пищевода в цилиндрический как следствие ГЭРБ. Выделение ПБ связано с тем, что цилиндрический эпителий специализированого кишечного типа является предраковым состоянием.
Диагностика
Диагностика ГЭРБ включает рентгенологическое исследование пищевода и желудка; внутрипищеводную суточную рН-метрию; эзофагогастроскопию и др.
Рентгенологическое исследование пищевода позволяет высказать предварительное суждение о состоянии кардиоэзофагеальной зоны. При его использовании удается зафиксировать попадание контраста из желудка в пищевод, обнаружить грыжу пищеводного отверстия диафрагмы, а также выявить язву, стриктуры, опухоль пищевода.
Суточная (24-часовая) рН-метрия пищевода является более надежным методом выявления гастроэзофагеального заброса, которая позволяет оценивать частоту, продолжительность и выраженность рефлюкса, влияние на него положения тела, приема пищи и лекарственных средств. Исследование суточной рН и пищеводного клиренса способствует выявлению случаев рефлюкса до развития эзофагита.
С помощью эндоскопии пищевода можно получить подтверждение наличия РЭ, оценить степень его тяжести и присутствие осложнений, провести контроль заживления повреждений СОП. Современные технологии и методики эндоскопических исследований (эндоскопия с высоким разрешением, хромоскопия, увеличительная эндоскопия, узкоспектральная эндоскопия) существенно улучшили диагностику ПБ и ранней формы аденокарциномы пищевода.
Биопсия пищевода с последующим гистологическим исследованием производится в основном с целью подтверждения наличия ПБ при характерной эндоскопической картине, поскольку верифицировать ПБ можно только гистологически.
Эзофагоманометрия – измерение давления в пищеводе с помощью специальных баллонных зондов – может дать ценные сведения о понижении давления в зоне НПС, нарушениях перистальтики и тонуса пищевода. В настоящее время стали использовать 24-часовое мониторирование моторики пищевода с использованием 7-F-катетера, несущего три миниатюрных электронных датчика давления. С использованием этого метода было показано, что неэффективная перистальтика приводит к увеличению времени контакта агрессивного содержимого желудка с СОП, способствуя развитию повреждений и появлению соответствующих симптомов [12].
Лечение
Цель лечения – купирование жалоб, улучшение качества жизни, борьба с рефлюксом, лечение эзофагита, предотвращение или устранение осложнений. Лечение ГЭРБ чаще бывает консервативным, реже – хирургическим.
Консервативное лечение включает:
- рекомендации больному по соблюдению определенного образа жизни и диете;
- антациды;
- альгинаты;
- антисекреторные препараты (Н2-блокаторы и ингибиторы протонной помпы);
- прокинетики, нормализующие расстройства моторики (однако клиническая практика показала недостаточную эффективность препаратов этой группы в лечении эрозивных РЭ).
1. Общие рекомендации по режиму и диете. Основные правила, которые больной должен соблюдать постоянно независимо от степени выраженности РЭ и стадии заболевания:
- после принятия пищи избегать наклонов вперед и не ложиться;
- спать с приподнятым головным концом кровати;
- не носить тесную одежду и тугие пояса, корсеты, бандажи, приводящие к повышению внутрибрюшного давления;
- избегать обильных приемов пищи; • не есть на ночь;
- ограничить потребление продуктов, вызывающих снижение давления НПС и обладающих раздражающим действием (жиры, алкоголь, кофе, шоколад, цитрусовые);
- отказаться от курения;
- снизить массу тела при ожирении;
- по возможности воздерживаться от приема лекарств, вызывающих рефлюкс (антихолинергические средства, спазмолитики, седативные и транквилизаторы, блокаторы кальциевых каналов, β-адреноблокаторы, теофиллин, простагландины, нитраты).
2. Антациды – лекарственные средства, уменьшающие кислотность желудочного содержимого за счет химического взаимодействия с соляной кислотой в полости желудка.
В настоящее время антациды применяют преимущественно в следующих ситуациях:
- для снятия симптомов РЭ при самолечении;
- как средство проведения дифференциального диагноза ex juvantibus между кардиальными и некардиальными загрудинными болями;
- для купирования симптомов ГЭРБ в первые дни обострений до назначения стандартизированного лечения;
- как лечебное средство, принимаемое пациентами по требованию (on demand) при изжоге.
3. Альгинаты – препараты, содержащие соли альгиновой кислоты, которые, взаимодействуя с соляной кислотой желудочного сока, образуют гель и формируют механический барьер-плато, тем самым создавая условия физиологического “покоя” для СОП. Альгинаты обычно используются “по требованию” при учащении изжоги у больных НЭРБ.
4. Антисекреторные препараты. Цель антисекреторной терапии ГЭРБ – уменьшить повреждающее действие кислого желудочного содержимого на СОП.
Н2-блокаторы (ранитидин, фамотидин) в свое время нашли широкое применение. Многочисленные клинические испытания блокаторов показали их эффективность. Однако следует учитывать, что через 2–3 недели применения эффективность Н2-блокаторов снижается, что делает необходимым или отменить препарат, или увеличить дозу. Кроме того, у 10–17 % популяции число Н2-рецепторов на обкладочных клетках небольшое, в связи с чем Н2-блокаторы в этих случаях малоэффективны или неэффективны вовсе. Н2-блокаторы совместно с прокинетиками используются в некоторых схемах лечения НЭРБ, что удешевляет лечение [12, 13].
В последние годы появились принципиально новые антисекреторные препараты – ингибиторы протонной помпы (ИПП). В семейство ИПП входят препараты пяти поколений: омепразол, лансопразол, пантопразол, рабепразол, эзомепразол.

Чтобы понять принцип действия и правильно выбрать препарат этой группы, необходимо знать процесс секреции соляной кислоты париетальными (обкладочными) клетками желудка и механизм действия ИПП [14–16]. Процесс секреции соляной кислоты основан на трансмембранном переносе протонов и осуществляется протонным насосом – Н+/К+-зависимой АТФазой.
В покое молекулы АТФазы диффузно распределены в цитоплазме. При активизации париетальных клеток (прием пищи) молекулы Н+/ К+-АТФазы встраиваются в мембрану секреторных канальцев и за счет энергии АТФ переносят ионы Н+ из клетки в просвет железы, обменивая их на ионы К+ из внеклеточного пространства. Этот процесс предваряет выход хлорид-ионов из цитозоля париетальной клетки. Так, в секреторных канальцах обкладочной клетки образуется соляная кислота, поступающая далее в просвет главных желез и полость желудка.

ИПП прочно блокируют молекулы Н+/К+-зависимой АТФазы, при этом полностью прекращается образование соляной кислоты. Для того чтобы клетка снова начала продуцировать кислоту, необходимо вновь синтезировать протонные помпы, свободные от связи с ингибитором. Продолжительность эффекта блокирования обусловлена скоростью обновления протонных помп. После отмены ИПП восстановление продукции соляной кислоты происходит на 4–5-й день в результате ресинтеза помп.
По своей химической структуре все ИПП относятся к классу бензимидазолов и различаются радикалами в пиридиновом и бензимидазольном кольцах. ИПП после прохождения желудка попадают в тонкую кишку, где растворяются, после чего по кровотоку поступают вначале в печень, а затем в канальцы париетальной клетки слизистой оболочки желудка. Здесь при кислом значении рН ИПП активируются и превращаются в тетрациклический сульфенамид, который не проходит через клеточные мембраны, а остается внутри канальцев. Скорость блокирования секреции, таким образом, определяется скоростью активации ингибитора протонной помпы, которая в свою очередь зависит от pKa – показателя pH, при котором половина протонных помп оказывается заблокированной. Среди всех ИПП рабепразол (Париет) имеет максимальный показатель pKa, поэтому он способен активироваться в наиболее широком диапазоне pH и блокировать максимальное количество протонных помп уже при первом приеме [17]. В активной форме он образует прочные ковалентные связи с цистеиновыми остатками Н+/К+-АТФазы, которая становится необратимо исключенной из процесса секреции соляной кислоты. В равных условиях ИПП блокируют протонные помпы при разной концентрации действующего вещества (К50). Так, рабепразол достигает полумаксимального ингибирующего эффекта при меньшей концентрации (0,07 мкМ) действующего вещества по сравнению с омепразолом/эзомепразолом (0,47 мкМ), что определяет большую у рабепразола способность подавлять секрецию кислоты [18, 19].
Метаболизм ИПП происходит в печени при участии двух изоформ цитохрома Р450: CYP2C19 и CYP3A4, обеспечивающих окисление СН3-группы до гидроксисульфонов. Некоторые ИПП (рабепразол) преимущественно метаболизируются неферментным путем. Метаболиты выводятся из организма главным образом почками, в меньшей степени – кишечником.
ИПП обеспечивают выраженное и продолжительное подавление кислой желудочной секреции. ИПП отличаются особой эффективностью при эрозивно-язвенном эзофагите, обеспечивая после 6–8 недель лечения заживление пораженных участков в 90–96 % случаев. Антисекреторное действие Париета (рабепразола) наступает быстрее по сравнению с другими ИПП, что является его несомненным преимуществом и позволяет купировать симптомы уже в первый день терапии. Кроме того, рабепразол обладает максимальным среди всех ИПП потенциалом кислотосупрессии. Париет назначается в дозе 10–20 мг однократно в сутки [20].
Выбор тактики лечения
В настоящее время подробно разработаны правила медикаментозного лечения обострения ГЭРБ в зависимости от степени выраженности РЭ (см. рисунок).
На первом этапе ИПП назначают однократно за 30 минут до завтрака в полной дозе (20 мг омепразола, 30 мг лансопразола, 40 мг пантопразола, 20 мг рабепразола или 40 мг эзомепразола). Предпочтение следует отдавать Париету, действие которого по сравнению с другими ИПП наступает быстрее и держится более продолжительное время, что является несомненным преимуществом препарата. Лечение продолжают 4 недели при НЭРБ и 8 недель – при эрозивной ГЭРБ. Если после 8-й недели терапии повреждения СОП сохраняются, следует исключить факторы, влияющие на эффективность терапии, приведенные ниже. Последующую поддерживающую терапию проводят ИПП в полной или половинной дозе “по требованию” или в режиме “выходного дня”.
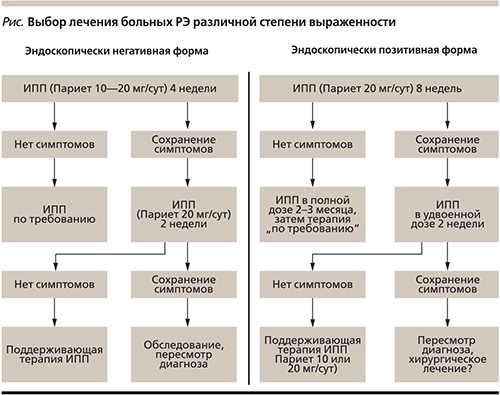
При недостаточно быстрой динамике заживления эрозий или наличии внепищеводных проявлений ГЭРБ следует назначать удвоенную дозу ИПП и увеличивать продолжительность лечения (до 12 недель и более). Критерий эффективности лечения – стойкое устранение симптомов.
Подводя итог консервативному лечению ГЭРБ, следует заметить, что первоначальный энтузиазм в отношении возможности терапии все более мощными антисекреторными препаратами на сегодняшний день уменьшился. Частота клинической неэффективности лечения при ГЭРБ составляет 10–40 % [21].
Причины неэффективности лечения больных ГЭРБ:
- Недостаточная приверженность больных лечению вследствие длительности схем лечения: по данным A.F. Barrison и соавт. (2001), только 55 % пациентов принимали ИПП в течение рекомендуемых 4 недель, а для 37 % этот срок составил 12 дней.
- Неправильное применение ИПП. лучше принимать ИПП за 30 минут до завтрака: по данным A.F. Barrison и соавт. (2001), более 70 % врачей первичного звена не знают этого [22].
- Несостоятельность кислотосупрессии ИПП для ряда больных (не удается поддерживать уровень рН в пищеводе выше 4,0 в течение 16–22 часов); “ночной кислотный прорыв”; “быстрые метаболизаторы” – генетический полиморфизм изофермента 2С19 системы цитохрома Р450, определяющего способность метаболизировать ИПП быстро и медленно. Следует отметить, что Париет обеспечивает круглосуточный контроль секреции, а способность Париета поддерживать pH > 4 в ночное время выше таковой у эзомепразола [23]. Кроме того, эффект Париета не зависит от генетического полиморфизма изоферментов цитохрома P450 [24].
- Эффективность лечения повреждений СОП значительно превышает способность ИПП избавлять от изжоги (больные с “гиперсенситивным пищеводом”, “функциональная изжога”).
- Рефлюктант не кислый, а щелочной (“желчный”) – 10–12 % [21].
При возникновении проблемы резистентности к проводимой терапии в первую очередь необходимо исключить влияние субъективных факторов, таких как несоблюдение больным рекомендаций по изменению образа жизни и приему лекарств, а также неадекватное назначение препаратов лечащим врачом.
Возможности по преодолению резистентности к терапии пациентов ГЭРБ:
- Немедикаментозные методы: соблюдение общего режима и диеты; правильный прием ИПП строго за 30 минут до завтрака (ИПП наиболее эффективны в период активации париетальных клеток пищей); ИПП не следует сочетать по времени с приемом Н2-блокаторов.
- Лечение пациентов с резистентной НЭРБ: при сохранении симптомов на фоне однократного приема ИПП рекомендуется добавлять антациды и альгинаты.
- Лечение пациентов с резистентным эрозивным РЭ: если использовались ИПП первого поколения (омепразол, лансопразол), целесообразно переходить на ИПП последующих поколений (эзомепразол, рабепразол); переходить на двукратный прием (перед завтраком и ужином); при “ночном кислотном прорыве” добавлять к терапии ИПП на ночь Н2-блокаторы, которые лучше действуют в ночное время.
Хирургическое лечение
Отсутствие эффекта от консервативной терапии, осложнения РЭ требуют принятия решения о целесообразности оперативного лечения.
Показания к оперативному лечению:
- безуспешность консервативного лечения;
- осложнения ГЭРБ (стриктуры, повторные кровотечения);
- частые аспирационные пневмонии;
- ПБ с наличием дисплазии эпителия высокой степени (из-за опасности малигнизации);
- необходимость долгосрочной антирефлюксной терапии молодых пациентов с ГЭРБ.
Основным типом операции при РЭ является фундопликация по Ниссену. В настоящее время разрабатываются и внедряются методы фундопликации, проводимой через лапароскоп.
Заключение
Таким образом, развитие ГЭРБ тесно связано с длительным закислением пищевода вследствие рефлюкса содержимого желудка в пищевод. Современная стратегия лечения ГЭРБ предусматривает применение антисекреторных препаратов, прежде всего ИПП. Наиболее эффективный и безопасный из них – Париет. Он обеспечивает быстрое (с первых суток) наступление стойкого и длительного антисекреторного эффекта, способствует наступлению стойкой клинической и эндоскопической ремиссии болезни. Именно поэтому Париет считается “золотым стандартом” лечения всех форм ГЭРБ.



