Желчнокаменная болезнь (ЖКБ) – одно из наиболее распространенных заболеваний человека, занимающее третье место после сердечнососудистых заболеваний и сахарного диабета [1]. В России среди различных контингентов обследованных лиц распространенность ЖКБ колеблется в пределах 3–12 % и выявляется в среднем у каждой пятой женщины и у каждого десятого мужчины. Заболеваемость как среди мужчин, так и среди женщин увеличивается с возрастом постепенно, достигая максимума к 60 годам. В настоящее время по числу оперативных вмешательств холецистэктомия вышла на второе место в мире после аппендэктомии [2, 3].
ЖКБ в настоящее время рассматривается как многофакторное и многостадийное заболевание. К факторам риска ЖКБ относят наследственную предрасположенность, аномалии развития билиарного тракта, неадекватное питание, ожирение, нарушение обмена холестерина, сахарный диабет, гипотиреоз, применение лекарственных препаратов (пероральные контрацептивы, клофибрат, никотиновая кислота, цефтриаксон, производные сандостатина и др ), беременность, воспалительные заболевания кишечника, хронические запоры, гиподинамию и др. Как показали исследования, в патогенезе формирования камней и прогрессирования заболевания необходимым условием является одновременное существование трех факторов: перенасыщение желчи холестерином, нарушение баланса между пронуклеирующими и антинуклеирующими факторами, снижение эвакуаторной функции желчного пузыря (ЖП). Значительная роль в патогенезе ЖКБ отводится воспалению в билиарной системе.
Прогресс в изучении патогенеза камнеобразования, внедрение в широкую практику современных методов ультразвуковой диагностики послужили основой для новой классификации ЖКБ, предложенной профессором А.А Ильченко [4]. Классификация была обсуждена на III съезде гастроэнтерологов России и рекомендована для использования в клинической практике.
Классификация желчнокаменной болезни:
I. Стадия начальная или предкаменная:
а) густая неоднородная желчь;
б) формирование билиарного сладжа (БC): с наличием микролитов, замазкообразной желчи; сочетание замазкообразной желчи с микролитами.
II. Стадия формирования желчных камней.
а) по локализации: в ЖП, общем желчном протоке, в печеночных протоках;
б) по количеству конкрементов: одиночные, множественные;
в) по составу: холестериновые, пигментные, смешанные;
г) по клиническому течению:
1) латентное течение,
2) с наличием клинических симптомов: болевая форма с типичными желчными коликами; диспепсическая форма; под маской других заболеваний.
III. Стадия хронического калькулезного холецистита.
IV. Стадия осложнений.
Диагностическая тактика при ЖКБ включает установление факта наличия камней в ЖП, их размеров, количества и состава; уточнение состояния сократительной функции ЖП (функционирующий или нефункционирующий); определение состояния холедоха, фатерова сосочка, поджелудочной железы; выявление сопутствующих заболеваний органов пищеварения, а также других органов и систем. В зависимости от результатов обследования и клинической ситуации определяется выбор лечебной тактики у больных ЖКБ.
Холецистэктомия до настоящего времени считается “золотым стандартом” лечения ЖКБ. Однако показания к ее проведению за исключением осложнений ЖКБ четко не определены. Мнения хирургов и терапевтов в отношении сроков плановой холецистэктомии часто не совпадают. С одной стороны, целесообразно направлять пациентов на операцию до развития осложнений и прогрессирования сопутствующих заболеваний. С другой – удаление функционирующего ЖП часто приводит к развитию постхолецистэктомического синдрома (ПХЭС), в основе которого лежит гипертонус сфинктера Одди (СФО) с формированием болевого синдрома, нередко приносящего пациенту большее страдание, чем до операции.
Руководством для направления больных ЖКБ на оперативное лечение могут быть международные рекомендации Euricterus по отбору пациентов с холелитиазом для хирургического лечения, принятые на съезде хирургов в 1997 г. (см. таблицу). Наиболее важными факторами, используемыми в системе Euricterus для направления на оперативное лечение, являются наличие клинической симптоматики (билиарной боли, желчной колики); сопутствующий хронический панкреатит; выраженное снижение сократительной функции ЖП; наличие осложнений ЖКБ.
Таблица.Международные рекомендации по отбору пациентов с ЖКБ для хирургического лечения (Программа Euricterus).
К альтернативным способам лечения ЖКБ относятся преоральная литолитическая терапия, ударноволновая литотрипсия, ударноволновая лититрипсия в сочетании с преоральной литолитической терапией, чрескожная, чреспеченочная литолитическая терапия.
Однако в связи с внедрением в практику лапароскопической холецисэктомии консервативные методы в настоящее время используются реже. Наиболее часто из этих видов консервативного лечения используется пероральная литолитическая терапия.
Литолитическая терапия может быть назначена при наличии БС; конкрементов, содержащих в своем составе преимущественно холестерин; больным, у которых клинические проявления заболевания не требуют срочного хирургического вмешательства или имеется повышенный риск операции; при отказе от хирургического лечения; при наличии функционирующего ЖП.
БС в настоящее время рассматривается в качестве начальной (I стадии) формирования желчных камней. Одним из важных аргументов в пользу этого положения является тот факт, что со временем у 8–20 % больных с БС образуются конкременты. С другой стороны, в 30–60 % случаев наблюдается персистенция БС, когда он исчезает и появляется вновь, что позволяет предполагать обратимость ЖКБ на ранних стадиях [5]. На этой стадии ЖКБ благодаря комплексу мероприятий, направленных на нормализацию обмена холестерина и восстановление сократительной функции ЖП, возможно ликвидировать БС [6]. Патогенетически обоснованным является применение препаратов урсодезоксихолевой кислоты (УДХК) – урсотерапия. УДХК тормозит всасывание холестерина в кишечнике, оказывает ингибирующее влияние на ГМГ-КоА-редуктазу и тем самым тормозит синтез холестерина, образует жидкие кристаллы с холестерином, содержащиеся в перенасыщенной желчи. УДХК назначается в дозе 10–15 мг/кг массы тела, вся доза принимается однократно вечером, через час после ужина или на ночь. Длительность приема зависит от клинической ситуации. Для БС в виде гиперэхогенных частиц обычно требуется месячный курс лечения. При других формах БС курс более длительный и составляет чаще 3, реже 6 месяцев [5]. УДХК помимо выраженного литолитического эффекта обладает гепатопротективным действием, которое следует учитывать при наличии сопутствующего поражения печени (стеатоз или стеатогепатит).
При наличии сформировавшихся конкрементов критерии отбора больных для пероральной литолитической терапии основываются на данных ультразвукового исследования (УЗИ) и пероральной холецистографии. Одним из главных условий, определяющих эффективность литолитической терапии, является подтверждение преимущественно холестериновой природы конкрементов. По данным УЗИ, конкременты холестеринового состава характеризуются гомогенной, низкоэхогенной структурой; округлой или овальной формой; с поверхностью конкремента, близкой к ровной или в виде тутовой ягоды; наличием неинтенсивной, плохо заметной акустической тени позади конкремента; медленным его падением при изменении положения больного во время проведения исследования. Состав конкрементов может быть уточнен при компьютерной томографии (КТ). По данным КТ, более вероятно растворение камней с коэффициентом ослабления ниже 70–100 ЕД по Хаунсфилду. Успех терапии зависит от размера конкремента (при одиночном – не более 10 мм) и их количества: при множественном камненосительстве объем конкрементов не должен занимать более 25 % объема ЖП [7]. Обязательным условием являются отсутствие препятствий в билиарной системе и сохраненная сократительная функция ЖП. Для растворения камней назначают препараты УДХК из расчета 15 мг на 1 кг веса, всю дозу принимают однократно вечером перед сном. Результаты терапии зависят от многих причин: соблюдения режима и регулярности приема препарата, длительности терапии, правильного отбора пациента для этого вида терапии. Эффективность лечения контролируется УЗИ каждые 3–6 месяцев. В отсутствие эффекта в течение 6 месяцев терапию отменяют и рассматривают целесообразность оперативного лечения. После успешного растворения рецидив камнеобразования (до 50 % в течение последующих 5 лет после растворения) может потребоваться повторение курсов литолитической терапии [1, 7].
Клиническая картина у пациентов с ЖКБ может отсутствовать или проявляться диспепсией, болями преимущественно билиарного и/или панкреатического типа. Для купирования болевого синдрома и коррекции моторных нарушений билиарной системы у этой группы больных чаще используются миотропные спазмолитики. Природа билиарной боли может быть функциональной и/или органической. Наибольшее значение в плане тактики лечения при ЖКБ имеет дифференциальный диагноз механизма возникновения боли – разграничение соматической и висцеральной боли [8, 9].
Соматическая боль обусловлена наличием патологических процессов в париетальной брюшине и тканях, имеющих окончания чувствительных спинномозговых нервов, и ее возникновение связано с патологическими процессами, сопровождающимися повреждением брюшной стенки и/ или брюшины. В отличие от висцеральной боли она имеет длительный, постоянный и интенсивный характер. Боль отчетливо локализована в соответствии с пораженной зоной, имеет характерную иррадиацию. При пальпации живота определяются локальная болезненность и признаки вовлечения в патологический процесс брюшинного покрова. Как правило, отмечаются лихорадка и лейкоцитоз. Причины развития париетальной боли при ЖКБ – наличие воспаления, отека, деструкции тканей, механическая травматизация тканей конкрементом (острый калькулезный холецистит, холангит). Введение спазмолитиков для купирования соматической боли является неэффективным и противопоказанным. Подавляющему большинству больных с наличием соматических болей, как правило, требуется хирургическое лечение.
Висцеральная боль при патологии билиарной системы возникает в ответ на быстрое увеличение внутрипротокового давления и растяжения стенки ЖП, а также желчевыводящих путей в результате раздражения болевых рецепторов, расположенных в мышечной оболочке этих органов. При этом интенсивность боли прямо пропорциональна скорости нарастания внутрипросветного давления в органе и его диаметру. Классическим примером висцеральной боли при патологии билиарной системы является желчная колика. Желчная колика характеризуется схваткообразными болями в правом верхнем квадранте живота и/ или эпигастральной области, которые носят быстронарастающий и интенсивный характер. На высоте болей пациенты с желчной коликой часто вынуждены принимать вынужденную позу. Висцеральная боль не имеет четкой локализации и носит разлитой характер. Нередко наблюдается характерная иррадиация в правое надплечье, правую лопатку (иррадиирующие боли). Повышение внутрипротокового давления может сопровождаться рефлекторной тошнотой, рвотой, не приносящей облегчения. При осмотре пациента определяется неотчетливо локализованная болезненность в эпигастральной области и правом подреберье. Причины развития желчной гипертензии и желчной колики весьма разнообразны. При ЖКБ спазм мускулатуры желчевыводящих путей может быть обусловлен ущемлением конкремента в шейке ЖП или в протоках, функциональным спазмом СФО, наличием холангита, развитием синдрома Мириззи. Таким образом, основной причиной возникновения билиарной боли при ЖКБ чаще всего является спазм гладкой мускулатуры, в основе развития которого могут лежать как функциональные, так и органические изменения [10]. В качестве провоцирующих внешних воздействий при возникновении висцеральной боли могут выступать нарушение диеты, тряская езда, эмоциональное перенапряжение.
В качестве критериев диагностики билиарной боли могут использоваться Римские критерии-III. В них функциональная билиарная патология подразделяется на E1 – Функциональное расстройство ЖП (ФРЖП); Е2 – Функциональное билиарное расстройство сфинктера Одди (билиарное ФРСО); Е3 – Функциональное панкреатическое расстройство сфинктера Одди (панкреатическое ФРСО) [11, 12].
К общим диагностическим критериям функциональных расстройств ЖП и СФО относятся эпизоды болей продолжительностью не менее 6 месяцев до установления диагноза и проявляющиеся не менее 3 месяцев, локализованных в эпигастрии/или в правом верхнем квадранте живота и все критерии из нижеследующих:
1) эпизоды болей длительностью 30 минут и более;
2) рецидивирование эпизодов с различными интервалами (не ежедневно);
3) боли достигают постоянного уровня;
4) боли умеренные или сильные (боль определяется как умеренная, когда она нарушает ежедневную деятельность пациента, и как тяжелая, когда требует незамедлительной медицинской консультации или медикаментозного купирования);
5) боли не уменьшаются после стула, при перемене положения тела, после приема антацидов;
6) исключены другие структурные заболевания, которые могли бы объяснить симптомы.
Подтверждающие критерии: боли могут сочетаться с одним или более из нижеследующих симптомов: а) боли ассоциированы с тошнотой или рвотой; б) боли иррадиируют в спину и/ или правую подлопаточную область; в) боли возникают в ночное время.
Диагностические критерии ФРЖП включают симптомы, свойственные функциональным расстройствам ЖП и СФО и нормальные показатели печеночных ферментов, конъюгированного билирубина и амилазы/липазы. Дополнительными тестами являются фиброгастродуоденоскопия и оценка состояния функции ЖП. Опорожнение ЖП выражается как фракция выброса, измеряется в процентах.
Тип дифункции СФО определятся его сложной анатомической структурой, состоящей из сфинктера общего желчного протока, сфинктера панкреатического протока и сфинктера их общей ампулы, которая открывается в двенадцатиперстную кишку большим дуоденальным сосочком. При спазме преимущественно сфинктера холедоха развивается билиарное, при спазме панкреатического сфинктера – панкреатическое ФРСО.
Диагностические критерии ФРСО билиарного типа включают оба следующих признака: общие симптомы, свойственные функциональным расстройствам ЖП и СФО; нормальный уровень амилазы/липазы. Подтверждающими критериями считаются подъем уровня сывороточных трансаминаз щелочной фосфатазы или конъюгированного билирубина, связанных по времени по крайней мере с двумя эпизодами болей.
Диагностические критерии ФРСО панкреатического типа включают оба следующих признака: общие симптомы, свойственные функциональным расстройствам ЖП и СФО; повышенный уровень амилазы и/или липазы во время приступа. Для дифференциального диагноза функционального и органического генеза болевого синдрома в билиарной системе рекомендуется использовать определенный набор инструментальных исследований и лабораторных тестов.
Диагностические тесты при заболеваниях билиарного тракта
Скрининговые:
- функциональные пробы печени, панкреатические ферменты в крови и моче;
- УЗИ;
- эзофагогастродуоденоскопия с детальным осмотром зоны большого дуоденального сосочка. Уточняющие:
- УЗИ с оценкой функции ЖП и СФО;
- эндоскопическое УЗИ;
- гепатобилисцинтиграфия с 99 mTc;
- медикоментозные тесты (с холецистокинином);
- микроскопия желчи;
- магнитно-резонансная холангиопанкреатография (МРХПГ) – наиболее точный неинвазивный метод оценки состояния билиарной системы;
- эндоскопическая ретроградная холангиопанкреатография с манометрией СФО.
Для купирования билиарной боли в настоящее время используются релаксанты гладкой мускулатуры нескольких групп: холинолитики (М1-, М2и М3-холиноблокаторы) и миотропные спазмолитики прямого действия [13]. Использование холинолитиков (атропин, платифилин, бускопан) патогенетически оправданно, и они достаточно эффективны, в т. ч. и при спазме СФО, но их курсовое длительное применение ограничено большим числом хорошо известных побочных эффектов. Холинолитики обычно применяются кратковременно для купирования острого болевого приступа, вызванного спазмом.
Миотропные спазмолитики представлены тремя группами препаратов с разными механизмами действия: неселективные спазмолитики – папаверин и дротаверин являются блокаторами фосфодиэстеразы цАМФ и цГМФ; пиноверия бромид и отилония бромид – блокаторы кальциевых каналов, селективно воздействующие на гладкие мышцы желудочно-кишечного тракта (ЖКТ), и мебеверин – селективный блокатор натриевых каналов гладких мышц ЖКТ. Конечный этап механизма действия этих спазмолитиков – это уменьшение концентрации ионов кальция в миоците и гладкомышечная релаксация [14, 15].
Применение неселективных миотропных спазмолитиков (папаверин и дротаверин), особенно длительное, приводит к развитию гипомоторной дискинезии и гипотонии сфинктерного аппарата ЖКТ и вызывает вазодилатирующий системный эффект. Кроме того, при использовании миотропных спазмолитиков, как и М-холиноблокаторов, необходимо учитывать существенные индивидуальные различия в эффективности и снижение ее в процессе лечения. Поэтому данные препараты используются кратковременно для купирования спастических болей, но не в курсовом лечении.
Препараты с селективным действием на гладкие мышцы пищеварительной системы (мебеверин, отилония бромид, пиноверия бромид) являются более предпочтительными. Однако при патологии билиарной системы и особенно при спазме СФО препаратом выбора следует считать мебеверин (Дюспаталин). Препарат используется в клинической практике с 1965 г. По сравнению с селективными блокаторами кальциевых каналов у Дюспаталина есть значительные преимущества, т. к. он в отличие от других препаратов обладает высоким сродством к мышечному аппарату СФО. Спазмолитический эффект Дюспаталина выше по сравнению с другими известными препаратами и примерно в 30 раз превышает таковой при применении платифиллина, что оправдывает его назначение больным ЖКБ и ПХЭС. Кроме того, препарат оказывает не только антиспастическое, но и нормализующее действие на моторику ЖКТ, не подавляя полностью мышечные сокращения после гипермоторики, т. е. не вызывает рефлекторной гипотонии. Этот механизм обусловлен тем, что Дюспаталин препятствует восполнению депо кальция на мембране миоцита после стимуляции α1-адреноцепторов. Отсутствие рефлекторной гипотонии является существенным преимуществом препарата и позволяет применять его среди больных при смешанных нарушениях моторики: при гипертонусе СФО и одновременной гипотонии ЖП, что часто встречается у больных ЖКБ. При этом дополнительного снижения тонуса стенки ЖП не происходит. Эффект после приема Дюспаталина возникает быстро (через 20–30 минут) и продолжается в пределах 12 часов, что делает возможным его двукратный прием в сутки – это тоже является его преимуществом по сравнению с другими спазмолитиками. Пролонгированное действие Дюспаталина объясняется современной формой выпуска препарата: капсула содержит 200 мг мебеверина в микросферах с двуслойным покрытием, внешний слой которого кислотоустойчив, а внутренний содержит препарат пролонгированного действия [16]. Механизм действия Дюспаталина не затрагивает автономную нервную систему и поэтому не имеет типичных антихолинергических побочных эффектов, что дает возможность применять препарат больными с такими сопутствующими заболеваниями, как гипертрофия предстательной железы, задержка мочи или глаукома.
Применение Дюспаталина при физико-химической стадии ЖКБ в короткие сроки восстанавливает моторную активность СФО и ЖП, улучшает желчеотделение и реологические свойства желчи, а также купирует боль и диспепсические симптомы[17]. Благодаря снятию спазма СФО и восстановлению желчеоттока препарат оказывает прокинетическое действие на моторику двенадцатиперстной кишки и устраняет симптомы функциональной дуоденальной гипертензии [18]. Включение Дюспаталина в комплекс лечения больных в хирургических отделениях с острым обструктивным калькулезным холециститом и после холецистэктомии также сопровождалось положительным эффектом – приводило к более быстрому купированию болевого синдрома [19]. У больных с дисфункцией СФО, перенесших холецистэктомию, на фоне монотерапии Дюспаталином не только исчезал болевой синдром, но и уменьшался диаметр холедоха. Полученные результаты доказывают целесообразность назначения Дюспаталина сразу после холецистэктомии для профилактики дисфункции СФО [18, 20]. Эффекты дюспаталина на билиарную систему представлены на рисунке.
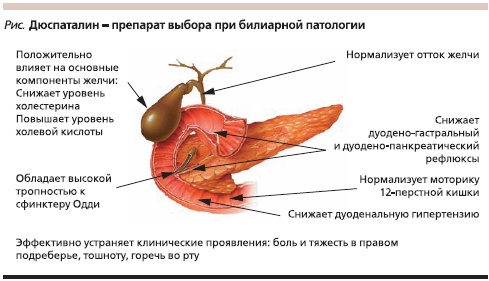
Достоинством Дюспаталина является его нормализующее действие и на моторику толстой кишки, изменения которой часто отмечаются у больных с функциональными нарушениями билиарной системы, в т. ч. при ЖКБ. Этот эффект доказан многочисленными исследованиями Дюспаталина у пациентов с синдромом раздраженной кишки [21, 22]. Данные по безопасности и переносимости препарата получены в клинических исследованиях с участием более 3500 пациентов, принимавших Дюспаталин. Препарат практически не всасывается, не попадает в общий кровоток и поэтому не оказывает побочных эффектов. Он всегда хорошо переносился больными, даже при использовании доз, превышающих терапевтические. Гематологические и биохимические показатели оставались неизменными на протяжении курса лечения. В анализе исследований препаратов, обычно используемых при лечении функциональных нарушений СФО, Дюспаталин занимал первое место по отсутствию побочных эффектов [23, 24].
Таким образом, назначение Дюспаталина больным ЖКБ при наличии конкрементов или БС показано в качестве патогенетического лечения (устранения функциональных расстройств СФО и ЖП) в комплексе с литолитической терапией, при подготовке к операции, а также в качестве симптоматической терапии для купирования болей билиарного типа на любой стадии ЖКБ и при ПХЭС.
Для купирования синдрома диспепсии и нормализации процессов пищеварения больным ЖКБ назначаются панкреатические ферменты: например Креон 10000; доза подбирается индивидуально с учетом сопутствующего панкреатита (25000–40000 ЕД). По показаниям проводятся курсы деконтаминационной терапии. Деконтаминация двенадцатиперстной кишки предотвращает преждевременную деконъюгацию желчных кислот и разрушение ферментов бактериальной флорой, тем самым уменьшает билиарную и ферментативную недостаточность и улучшает процессы пищеварения у больных ЖКБ. Курс деконтаминационной терапии включает спазмолитик, антибактериальные препараты, пре-и пробиотики.
Примерная схема лечения больных ЖКБ с функциональными расстройствами ЖП и/или СФО и синдром диспепсии:
- Дюспаталин 200 мг 2 раза в день, 4–6 недель.
- По показаниям терапия, направленная на деконтаминацию двенадцатиперстной кишки, включающая 7–10-дневный прием одного из антибактериальных препаратов в общепринятых суточных дозах: рифаксимин, или нифуроксазид или ципрофлоксацин с последующим назначением пробиотиков, содержащих тонкокишечную микрофлору (Бифиформ) и/или пребиотиков (Дюфалак) в обычных дозах не менее 2 недель.
- Препараты УДХК 15 мг на 1 кг массы тела (пероральная литолитическая терапия по показаниям).
- Ферменты (Креон 10000) 2–3 раза в день при наличии показаний.
- При наличии воспаления в билиарной системе назначаются антибактериальные препараты, включенные в энтерогепатическую циркуляцию (ципрофлоксацин, доксициклин, гентамицин и др.), курс – 7–10 дней в общепринятых терапевтических дозах.
Примерная схема лечения хронического калькулезного холецистита в фазе обострения:
- Антибактериальные препараты (ципрофлоксацин 500–1000 мг/сут или гентамицин 3 мг/кг/сут, или доксициклин 100–200 мг/сут, или ко-тримоксазол 960 мг/сут и др.) 7–14 дней.
- Дюспаталин 200 мг – 2 раза в сутки, 14 дней.
- Дезинтоксикационная терапия (по показаниям).
Информация об авторах:
Агафонова Наталья Анатольевна – доцент кафедры гастроэнтерологии Российского государственного
медицинского университета им. Н.И. Пирогова. Тел. 8 (499) 464-39-63;
Яковенко Эмилия Прохоровна – профессор, заведующая кафедрой гастроэнтерологии Российского
государственного медицинского университета им. Н.И. Пирогова;
Прянишникова Антонина Семеновна – доцент кафедры гастроэнтерологии Российского
государственного медицинского университета им. Н.И. Пирогова;
Яковенко Андрей Владиславович – доцент кафедры гастроэнтерологии Российского государственного
медицинского университета им. Н.И. Пирогова;
Иванов Александр Николаевич – доцент кафедры гастроэнтерологии Российского государственного
медицинского университета им. Н.И. Пирогова



