Биологическая терапия заняла прочные позиции в лечении иммуновоспалительных заболеваний. В равной мере это относится и к воспалительным заболеваниям кишечника (ВЗК), в частности к язвенному колиту (ЯК). Среди обширного спектра биологических препаратов для лечения ЯК пока зарегистрирован лишь один – инфликсимаб (Ремикейд®). В России Ремикейд® используется при ЯК с 2006 г., и уже накоплен определенный опыт его применения, хотя не столь значительный, как за рубежом. В реальной клинической практике врачи часто боятся назначать инфликсимаб, не располагают такой возможностью или не знают показаний к его назначению. Поэтому мы сочли целесообразным рассмотреть в этой статье ряд основополагающих исследований по оценке эффективности инфликсимаба при ЯК и поделиться собственным опытом применения препарата.
Цели лечения ЯК:
• купирование атаки и индукция ремиссии;
• поддержание ремиссии без применения глюкокортикостероидов (ГКС);
• профилактика осложнений и операций;
• улучшение качества жизни.
Частота стероидрефрактерных и стероидзависимых форм ЯК во всем мире суммарно составляет 40–50 %; по России точные данные пока отсутствуют, по Московской области эта величина составляет около 40 %. Часть больных также не отвечают на лечение традиционными иммуносупрессорами (азатиоприном и циклоспорином). К важнейшим целям лечения ВЗК относятся преодоление резистентности к лечению и отказ от ГКС при стероидзависимых формах заболеваний, поддержание ремиссии без их использования. Именно на это направлено лечение инфликсимабом. Показаниями к назначению этого препарата, согласно Европейскому кон-сенсусу (ЕССО), являются резистентные ко всем видам базисной терапии формы ВЗК, включая стероидзависимость и стероидрезистентность [1]. На экспертном совете по разработке новых стандартов применения инфликсимаба в странах ЕС и США, состоявшемся в октябре 2005 г. (UC and CD: Treating to New Standards Expert Round Table),
было предложено включить в показания к лечению не только стероидрефрактерные формы болезни Крона и ЯК, но и тяжелые формы этих заболеваний (в качестве препарата первой линии).
Эффективность инфликсимаба
Систематические обзоры по оценке инфликсимаба при среднетяжелом и тяжелом ЯК, рефрактерном к стероидам и иммуносупрессорам, свидетельствуют, что препарат эффективен с точки зрения достижения клинического ответа, индукции клинической ремиссии, ускоряет заживление слизистой оболочки толстой кишки (СОТК) и снижает частоту срочных колэктомий [2, 3]. В рандомизированных клинических исследованиях инфликсимаб, назначенных в виде трех инфузий (исходной, 2-я и 6-я недели), превосходил стандартную терапию по индукции клинической и эндоскопической ремиссии и клиническому ответу на 8-й неделе [4–7]. В двойном слепом плацебо-контролируемом исследовании
G. Janerot и соавт., включившем 45 пациентов с тяжелым или среднетяжелым стероидорезистентным ЯК, частота колэктомий в течение трех месяцев после единичной инфузии инфликсимаба была в 2 раза ниже, чем в группе стандартной терапии [8].
Ключевыми в изучении эффективности и безопасности инфликсимаба при ЯК были два рандомизированных двойных слепых плацебоконтролируемых исследования: АСТ I и АСТ II. Они были сходными по дизайну, отличаясь лишь длительностью активного лечения и сроками наблюдения [4]. В исследование АСТ I были включены 364 пациента с тяжелым или среднетяжелым ЯК (6–12 баллов по индексу активности Мэйо), получавших ГКС и/или тиопурины, или рефрактерных к пероральному приему этих препаратов. В исследование АСТ II были также включены 364 пациента, рефрактерных хотя бы к одному из базисных препаратов – ГКС (в виде монотерапии или в комбинации), аминосалицилатам и тиопуринам. В обоих исследованиях пациенты получали инфузии инфликсимаба в дозе 5 или 10 мг/кг в виде индукционного курса (исходно, 2-я и 6-я недели) и затем регулярно каждые 8 недель или стандартную терапию: в АСТ I в течение одного года (последняя инфузия – на 46-й неделе), в АСТ II
последняя инфузия проводилась на 22-й неделе. Результаты оценивали на 8-й, 30-й и 54-й неделях в АСТ I и на 8-й и 30-й неделях в АСТ II.
Критерии оценки:
• частота достижения клинического ответа (снижение индекса Мэйо минимум на три пункта по сравнению с исходным и исчезновение или значительное уменьшение видимой крови в стуле);
• частота достижения клинической ремиссии (индекс Мэйо не более двух баллов);
• степень заживления СОТК (эндоскопический индекс 0–1 балла, что практически соответствует эндоскопической ремиссии);
• возможность отказа от приема ГКС к 30-й и 54-й неделям при наличии ремиссии;
• частота госпитализаций и доля госпитализированных больных.
Результаты показали достоверно более высокую частоту клинического и эндоскопического ответа (более 60 %), равно как и выхода в ремиссию, среди больных, получавших инфликсимаб, по сравнению с группой стандартной терапии. Как и при болезни Крона, оптимальной оказалась доза инфликсимаба 5 мг/кг/сут. В исследовании АСТ I клинический ответ на 8-й неделе был достигнут у 69,6, 61,5 и 37,2 % пациентов в группах, получавших 5, 10 мг/кг и стандартную терапию соответственно. Доли больных, достигших в тот же срок клинической ремиссии, составили в соответствующих группах 38,8; 32,0 и 14,9 %, а заживление СОТК тмечено у 62,0; 59,0 и 33,9 % больных. Почти идентичные результаты в указанный срок были получены в АСТ II (табл. 1). Аналогичная тенденция достижения клинического ответа отмечена на 30-й неделе: 52,1; 50,8 и 29,8 % больных в указанных группах в АСТ I, 47,1; 60,0 и 26,0 % – в АСТ II.
Таблица 1. Эффективность инфликсимаба (% больных) при ЯК (АСТ I и II).
В исследованиях АСТ I и АСТ II были получены впечатляющие результаты в отношении достижения эндоскопической ремиссии, существенно превы сившие эффект в группе стандартной терапии. Наиболее значимая разница (в 2 и более раз) в обоих исследованиях отмечена на 8-й неделе, несколько меньшая, но также достоверная – на 30-й неделе (табл. 1). Все три показателя (клинический ответ, клиническая ремиссия и заживление СОТК) в группах, получавших Ремикейд®, сохранили позитивную динамику на 54-й неделе, более чем в 2 раза превзойдя показатели в группе стандартной терапии.
Доли больных, отметивших нежелательные явления, были сходными во всех трех группах в АСТ I и АСТ II. У больных в группе стандартной терапии чаще отмечали нарастание тяжести ЯК и анемию.
На основании приведенных исследований можно сделать следующие выводы:
• инфликсимаб эффективен в лечении ЯК и характеризуется высоким коэффициентом польза/риск;
• инфликсимаб способен индуцировать и поддерживать при ЯК полную (клиническую и эндоскопическую) ремиссию;
• на фоне стойкой ремиссии инфликсимаб позволяет отказаться от приема ГКС у значительного числа пациентов.
Одна из последних работ также подтвердила возможность поддержания ремиссии и полного отказа от ГКС у 17 больных стероидзависимым ЯК при двухлетнем лечении инфликсимабом [9].
Действие инфликсимаба развивается быстро: уже через одну неделю можно наблюдать начало клинического эффекта. Через 8–12 недель концентрация препарата в сыворотке снижается, поэтому у больных с наиболее упорной формой заболевания рекомендуются повторные инфузии каждые 8 недель для поддержания клинического ответа.
Клинико-экономические аспекты
Раннее начало болезни, госпитализации и операции определяют экономические затраты при ЯК. Целью исследования R.D. Cohen соавт. (2010) был систематический обзор литературы по стоимости ведения больных ЯК в западных странах. Ежегодные медицинские расходы на одного пациента с ЯК составляют 6200–11 500 долл. в США и 8900–10 400 евро в Европе, причем стоимость госпитализаций составляет 40–55 % всех прямых медицинских затрат. Непрямые затраты составляют 30 % всех расходов в США и 54–68 % в Европе [10].
В исследованиях АСТ I и АСТ II был проведен анализ частоты госпитализаций больных ЯК. Всего в двух исследованиях участвовали 728 человек, из которых 484 пациента получали Ремикейд® в разных дозах (5 и 10 мг/кг/сут). Общая частота госпитализаций в течение 30 недель, в т. ч. повторных, была вдвое ниже в группе, получавшей Ремикейд®, по сравнению с группой стандартной терапии (9 против 18 %). Доля госпитализированных пациентов составила соответственно 8 и 14 % [11]. Поскольку стационарное лечение является наиболее затратной частью ведения больных ЯК; можно сделать вывод, что применение Ремикейда обеспечивает существенный экономический эффект для национальных систем здравоохранения.
Собственный опыт применения Ремикейда при ЯК
В отделении гастроэнтерологии МОНИКИ имеется опыт применения Ремикейда у больных ВЗК: 20 пациентов с болезнью Крона, 40 – с ЯК, из них 3 пациента после субтотальной резекции толстой кишки с активностью в культе сигмовидной и прямой кишки.
Задачи настоящего исследования:
• оценка эффективности индукционного курса терапии инфликсимабом у больных ЯК, рефрактерных к другим методам лечения;
• оценка возможности достижения и поддержания клинико-эндоскопической ремиссии ЯК при терапии инфликсимабом;
• поддержание ремиссии ЯК без ГКС на фоне терапии инфликсимабом.
Задачи исследования были сформулированы с целью сравнения эффективности биологической терапии инфликсимабом в России (на примере популяции больных Московской области), Европе и в других странах.
Материал и методы
В открытое проспективное исследование были включены 37 неоперированных больных ЯК, наблюдавшихся с января 2008-го по декабрь 2010 г. Диагноз ЯК был подтвержден эндоскопически и гистологически. Все больные проходили обследование на наличие скрытых форм туберкулеза.
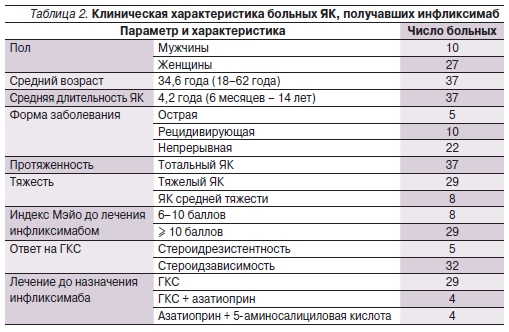
Клиническая характеристика больных представлена в табл. 2. Стероидрезистентность развилась у 5 пациентов с острой формой (первой атакой) заболевания, у остальных 32 больных сформировалась стероидзависимость. Исходную тяжесть атаки ЯК оценивали по индексу активности критериев Truelove и Witts [12–14]. Мониторинг эффективности терапии проведен по индексу Мэйо. До начала терапии инфликсимабом ГКС в виде монотерапии (преднизолон или метилпреднизолон) применяли у 29 пациентов. Из них 5 человек с острой тяжелой формой заболевания впервые получали 250–500 мг метилпреднизолона внутривенно с последующим снижением дозы и переходом на пероральный прием преднизолона из расчета 1 мг/кг массы тела в сутки; 24 пациента с очередной атакой рецидивирующей формы ЯК получали преднизолон перорально в той же дозе – 1 мг/кг массы тела.
Комбинацию пероральных ГКС в дозе 30–40 мг и азатиоприна в дозе 100–150 мг (не менее 2 мг/кг ) использовали 4 больных со стероидзависимой непрерывной формой ЯК. Комбинацию азатиоприна в той же дозе и 5-аминосалициловой кислоты получали 4 пациента со стероидзависимой формой ЯК и выраженными побочными эффектами ГКС. Таким образом, до назначения Ремикейда ГКС получали в общей сложности 33 больных, азатиоприн АЗА – 8 пациентов.
Больным назначали инфликсимаб (Ремикейд®) по программе ДЛО Московской области из расчета 5 мг/кг массы тела в сутки в виде индукционного курса (3 инфузии на исходной, 2-й и 6-й неделях) и затем каждые 8 недель. Мониторинг эффективности лечения проведен по индексу Мэйо. Индукционный курс (не менее 3 инфузий) получили 35 из 37 пациентов. Его эффективность оценена по аналогии с исследованиями АСТ I и II на 8-й неделе после начала лечения (через 2 недели после 3-й инфузии). В табл. 3 приведено количество инфузий Ремикейда у наблюдаемых нами больных ЯК включительно по декабрь 2010 г.
Таблица 3. Количество инфузий инфликсимаба у больных ЯК.
Результаты и обсуждение
Клиническое улучшение разной степени выраженности у 22 (59,5 %) больных наступило уже через 4–7 дней после первой инфузии инфликсимаба, у 6 (16,2 %) – после второй и у 9 (24,3 %) – после третьей инфузии препарата. На 8-й неделе оценили эффективность индукционного курса инфликсимаба у 35 пациентов (табл. 4). Положительный ответ был отмечен у 33 из них (94,3 %). Индекс Мэйо у этих больных уменьшился в 1,7–3,0 раза (снижение на 3–5 баллов по сравнению с исходным показателем). Самая низкая активность на 8-й неделе (2–3 балла) отмечена у 7 пациентов с исходным индексом 6–8 баллов, но полной ремиссии на этом этапе достигнуто не было. У 26 пациентов клинический и эндоскопический ответы были менее выраженными, хотя отмечена положительная динамика со снижением индекса Мэйо на 3 балла, при этом больные переходили из зоны высокой активности в зону умеренной активности.
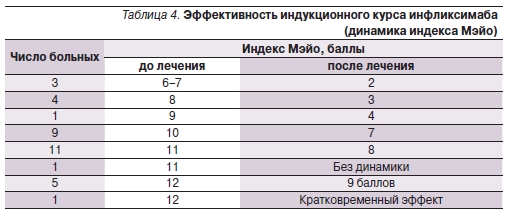
В дальнейшем 27 пациентов получали поддерживающую терапию инфликсимабом и у 26 из них на разных сроках лечения, но не позднее 6-й инфузии (30-я неделя) была достигнута полная клинико-эндоскопическая ремиссия или отмечено значительное улучшение (индекс Мэйо – не более 2–3 баллов), сохранившиеся по настоящее время. Улучшение морфологической картины СОТК, исчезновение язв и криптабсцессов отмечены у подавляющего большинства больных при достижении эндоскопической ремиссии, однако даже при длительных сроках лечения сохранялась плотная воспалительная инфильтрация собственной пластинки, т. е. морфологической ремиссии достигнуто не было.
В двух (6,1 %) случаях Ремикейд® был малоэффективным. У одной пациентки с острой формой ЯК и исходным индексом активности 11 баллов улучшение после 1-й инфузии сохранялось недолго и активность вновь стала нарастать, достигнув исходных показателей. После 3-й инфузии Ремикейда в связи с отсутствием положительной динамики больной была проведена субтотальная резекция толстой кишки с наложением илеостомы. Вторая пациентка с непрерывным стероидзависимым течением ЯК получила 6 инфузий препарата, причем две последние инфузии проводились в увеличенной дозе – 7,5 мг/кг, а интервалы между введениями были сокращены с 8 до 6 недель. После каждой инфузии у больной наступало улучшение, однако его длительность составила не более 4 недель. Попытки комбинировать инфликсимаб с иммуносупрессорами (азатиоприн, циклоспорин) не повысили эффективность лечения. Больная готовится к колэктомии.
Прием ГКС с постепенным снижением дозы больные продолжали до наступления стойкой клинической ремиссии на фоне терапии инфликсимабом. Полностью отменить ГКС удалось у 22 из 27 пациентов, получивших более трех инфузий Ремикейда (81,5 %) не позднее 30-й недели (после 6-й инфузии), при этом нарастания активности ЯК не отмечено.
Что касается азатиоприна, то пациенты, принимавшие его изначально, продолжили прием и на фоне Ремикейда в прежней дозе. Большей части больных, не получавших азатиоприн ранее, препарат назначали параллельно с Ремикейдом. Азатиоприн использован по двум причинам.
Во-первых, нет гарантии в регулярном поступлении Ремикейда по программе ДЛО и больные не должны оста-ваться без поддерживающей терапии. Во-вторых, мы опирались на результаты последнего исследования SONIC при болезни Крона, в котором показано, что комбинация инфликсимаба и азатиоприна с точки зрения поддержания ремиссии более эффективна, чем каждый из препаратов в отдельности [15]. Таким образом, 7 больных получали в качестве поддерживающего лечения только инфликсимаб, а 26 пациентов – инфликсимаб в комбинации с азатиоприном.
Нежелательные явления при лечении Ремикейдом отмечены у 3 (8,6 %) больных. У одной пациентки во время 1-й инфузии развился бронхоспазм, купированный внутривенным введением преднизолона. Эффект от инфликсимаба был хорошим, поэтому назначена вторая инфузия, однако бронхоспазм повторился, несмотря на предварительное введение преднизолона. В результате инфликсимаб был отменен. У второй больной после 4-й инфузии Ремикейда на фоне приема азатиоприна развился острый лекарственный гепатит. Отмена азатиоприна как основного токсичного препарата привела к нормализации функциональных проб печени, после чего в срок была проведена 5-я плановая инфузия Ремикейда. Однако через 4 дня после нее уровни печеночных ферментов вновь повысились. Таким образом, токсическое влияние на печень связано непосредственно с инфликсимабом. Больше этот препарат не вводился. Следует отметить, что, несмотря на короткий курс Ремикейда (2 и 5 инфузий), у указанных больных изменилось течение заболевания. В настоящее время у первой пациентки достигнута клинико-эндоскопическая ремиссия при приеме азатиоприна и месалазина, у второй – стойкая клиническая и неполная эндоскопическая ремиссия поддерживается препаратами 5-аминосалициловой кислоты.
У третьей больной после 5-й инфузии появились кашель, лихорадка, рентгенологически диагностирована диссеминированная форма туберкулеза легких (предварительно больная пациентка обследована на наличие туберкулеза). Ремикейд® был отменен, проводится лечение туберкулостатическими препаратами. Сохраняется активность ЯК от умеренной до высокой, больная получает 4 г месалазина и 30 мг преднизолона (преднизолон длительно принимала самостоятельно до назначения Ремикейда, пока полностью отменить не удается из-за нарастания активности ЯК).
Таким образом, при проведении данного исследования мы ответили на вопросы, поставленные в его задачах.
Первый вопрос: какова эффективность индукционного курса терапии инфликсимабом в российской популяции больных ЯК, рефрактерных к другим методам лечения?
Ответ: эффективность индукционного курса терапии инфликсимабом высокая, положительная клиническая и эндоскопическая динамика наблюдалась более чем у 90 % больных, получавших препарат. Снижение индекса Мэйо по сравнению с исходными значениями составило 3–5 баллов, т. е. индекс уменьшился в 1,7–3,0 раза.
Второй вопрос: возможно ли достижение и поддержание клинико-эндоскопической ремиссии ЯК при терапии инфликсимабом?
Ответ: поддерживающую терапию в количестве более 3 инфузий (максимально 13 инфузий) каждые 8 недель получали 27 из 37 пациентов, леченных инфликсимабом. У 26 из них (96,3 %) в разные сроки, но не позднее 6-й инфузии (30-я неделя лечения) была достигнута клинико-эндоскопическая
ремиссия или наблюдалось значительное улучшение (индекс Мэйо – не более 2 баллов).
Третий вопрос: возможна ли отмена ГКС на фоне инфликсимаба?
Ответ: ГКС отменены более чем у 80 % пациентов, получавших более 3 инфузий инфликсимаба.
Итак, в проведенном исследовании мы получили очень хорошие результаты, в ряде случаев превзошедшие результаты исследований АСТ I и АСТ II [4]. Мы связываем это с применением у части больных эффективной комбинации двух препаратов – инфликсимаба и азатиоприна. Отметим, что
эти пациенты не ответили на предварительную терапию ГКС, ГКС в сочетании с азатиоприном или на монотерапию азатиоприном. В то же время 7 пациентов получали длительную монотерапию инфликсимабом, и до настоящего времени у них сохраняется полная ремиссия. Мы не можем пока определенно высказаться о преимуществе монотерапии Ремикейдом или его комбинации с азатиоприном для поддержания ремиссии ЯК.
С нашей точки зрения, следует обратить особое внимание на сроки достижения эффекта в начале лечения инфликсимабом. Результаты одной инфузии не всегда показательны. Не рекомендуется прекращать лечение, если после первых двух инфузий эффекта не отмечено. Результат следует оценивать позднее – после 3-й инфузии на 8-й неделе лечения, как это было сделано в исследованиях АСТ. Набор пациентов и наблюдение за ними продолжаются.



