Введение
Одной из первостепенных задач при развитии прогрессирующего стеатогепатита в рамках неалкогольной жировой болезни печени (НАЖБП) является подбор терапии, позволяющей стабилизировать процесс и запустить репаративные процессы в ткани печени. НАЖБП – заболевание со сложным патогенезом, компоненты которого («толчки») тесно взаимосвязаны, подчас образовывая своеобразные «порочные круги» [1].
Центральное место в патогенезе НАЖБП имеет нарушение чувствительности тканей к инсулину. Инсулинорезистентность приводит к развитию липолиза в жировой ткани и увеличивает продукцию свободных жирных кислот (СЖК), большая часть которых попадает в печень. Избыток СЖК в клетках печени запускает каскад гормональной и метаболической адаптации к их избытку путем стимуляции митохондриального и пероксисомального окисления СЖК. В результате наблюдается повышение уровня АТФ, расходующегося преимущественно для липогенеза и глюконеогенеза («порочный круг») [2]. Возникают митохондриальная дисфункция, следом – энергетический дефицит внутри клетки, гипоксия и как следствие – развитие стеатоза и стеатогепатита.
В связи с этим для терапии неалкогольного стеатогепатита необходим не просто нормализующий клинико-диагностические показатели симптоматический препарат с оптимальным профилем безопасности. Важно комплексное влияние на патогенез процесса. Выбор лекарственных препаратов здесь невелик: большое число гепатопротекторов противопоказано при наличии прогрессирующего цитолиза.
В данной ситуации вариантом терапии НАЖБП может стать комбинированный оригинальный инфузионный полиионный сукцинат-метиониновый комплекс под названием Ремаксол®. Многокомпонентный состав препарата включает янтарную кислоту, рибоксин, никотинамид, метионин. Это инфузионный гепатопротектор комплексного действия, стимулятор синтеза эндогенного адеметионина (аденозил-метионинового комплекса), который повышает синтез глутатиона, полиаминов, фосфотидилхолина и усиливает регенеративные процессы в печени [1, 3].
Входящая в состав янтарная кислота – активное вещество, действующее на клеточный метаболизм, которое стимулирует процесс аэробного гликолиза, выступая в роли антиоксиданта и восстанавливая нормальную деятельность митохондрий [4].
Метионин – аминокислота, обладающая выраженным гепатопротективным действием. Под влиянием фермента метионинаденозилтрансферазы метионин трансформируется в S-аденозилметионин, участвующий в синтезе холина, лецитина и других фосфолипидов [5].
Другими активными компонентами комбинированного препарата являются N-метилглюкамин (меглюмин), инозин (рибоксин), никотинамид и электролиты – натрия хлорид, магния хлорид, калия хлорид. Согласно литературным данным, меглюмин оказывает влияние на активность иммунного ответа [6]. Инозин участвует в метаболизме пировиноградной кислоты, способствует активации ксантиндегидрогеназы и ингибированию ксантиноксидазы, снижает активность процесса перекисного окисления липидов, определяя антиоксидантное действие препарата Ремаксол и восстанавливая тканевое дыхание [7]. Никотинамид − субстрат для синтеза НАД и никотин-аденин-динуклеотидфосфата, регулирующих репарацию гепатоцитов и их энергообеспечение [8].
Таким образом, Ремаксол − универсальный гепатопротектор, имеющий показания к применению при различных печеночных патологиях [9]. Но действие оригинального комплекса, направленное на коррекцию дисметаболических расстройств, можно справедливо назвать уникальным в комплексной терапии НАЖБП, в частности на стадии стеатогепатита [10, 11].
В подтверждение приведем клинический случай ведения пациента с неалкогольным стеатогепатитом с использованием препарата Ремаксол.
Клинический случай
Больной А. 1993 г.р. при обращении 30.01.2020 на амбулаторный прием предъявлял жалобы на слабость, быструю утомляемость. Из анамнеза заболевания: в рамках ежегодной диспансеризации в общем анализе крови от 18.01.2020 выявлен лейкоцитоз (12,5×109/мл), сохраняющийся в динамике (10,7×109/мл) (01.02.2020). При более детальном обследовании: индекс массы тела пациента (ИМТ) – 29,8 кг/м2, окружность талии – 93 см, в биохимическом анализе крови наблюдался синдром цитолиза: аланиаминотрансфераза (АЛТ) – 188 ЕД/л, аспартатаминотрансфераза (АСТ) – 153 ЕД/л, глюкоза сыворотки крови натощак – 6,0 ммоль/л, уровень гликозилированного гемоглобина – 5,5%. Мазок по результатам полимеразной цепной реакции (ПЦР), антитела по результатам иммуноферментного анализа (ИФА) к новой коронавирусной инфекции отрицательные. При компьютерной томографии легких патологических изменений выявлено не было. По данным ультразвукового исследования (УЗИ) органов брюшной полости от 15.02.2020: перегиб желчного пузыря, вторичные изменения поджелудочной железы. Исследование крови на маркеры вирусные гепатитов (ИФА, ПЦР) двухкратно − отрицательные результаты.
В липидограмме от 15.02.2020: холестерин − 6,1 ммоль/л, триглицериды − 2,34 ммоль/л, липопротеиды низкой плотности (ЛПНП) − 4,05 ммоль/л.
По данным фиброгастродуоденоскопии от 15.02.2020 − катаральный рефлюкс-эзофагит, диффузный гастродуоденит, результат быстрого уреазного теста на наличие хеликобактерной инфекции отрицательный. Пациенту был выставлен предварительный диагноз «стеатогепатит. Нарушение толерантности к глюкозе». Назначена низкоуглеводная, низкожировая диета с ограничением суточного калоража, рекомендовано увеличить уровень двигательной активности и интенсивность физических нагрузок, проведен курс инфузионной терапии адеметионином, далее продолжен пероральный прием данного гепатопротектора в течение 2 месяцев.
По данным биохимического иссле-дования крови от 15.04.2020: АЛТ − 149,3 ЕД/л, АСТ − 109,8 ЕД/л, глюкоза – 5,6 ммоль/л, в гемограмме лейкоцитоз (11,4×109/мл) сохраняется. Показатели биохимического анализа крови от 29.04.2020: АЛТ − 173,6 ЕД/л, АСТ − 143,3 ЕД/л, γ-глютамилтрансфераза (ГГТП) − 63,7 ЕД/л, щелочная фосфатаза (ЩФ) – 349,5 ЕД/л, в гемограмме лейкоциты – 12,2×109/мл. Согласно заключению транзиентной эластографии печени от 29.04.2020, установлен фиброз печени F3 (по МЕТАVIR). Учтя негативную динамику, 02.06.2020 было решено перевести пациента на стационарное лечение с диагнозом «стеатогепатит, биохимическая активность 2-й степени, ПН 0 степени, F3 (по МЕТАVIR)».
В рамках стационарного лечения была назначена следующая терапия: диета № 5; инфузионная терапия: Ремаксол 400 мл 2 раза в сутки №10 внутривенно капельно (медленно); внутрь перорально: препарат урсодезоксихолевой кислоты, викасол, тримебутин‚ эзомепразол курсами в стандартных дозировках.
По данным биохимического анализа крови от 03.06.2020: АЛТ – 127 ЕД/л, АСТ – 82 ЕД/л, ЩФ – 429 ЕД/л, ГГТП – 63 ЕД/л; от 08.06.2020: АЛТ − 77,3 ЕД/л, АСТ − 57,5 ЕД/л, ЩФ – 474 ЕД/л; от 12.06.2020: АЛТ − 66,6 ЕД/л, АСТ − 57,6 ЕД/л, ЩФ – 377 ЕД/л, ГГТП – норма; уровень лейкоцитов нормализовался (рис. 1, 2).
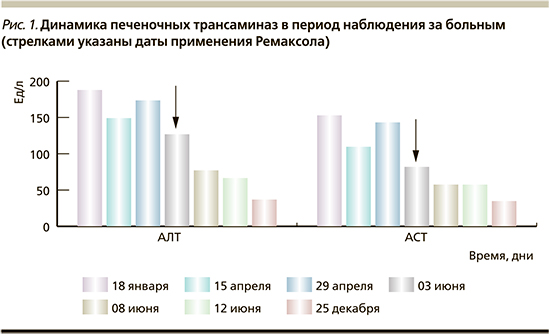
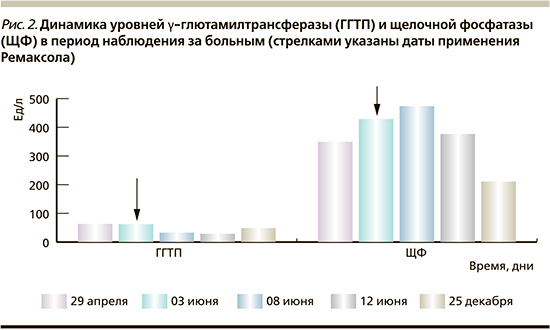
Результаты лапароскопической биопсии печени от 08.06.2020: «хронический гепатит с минимальной активностью (1 балл по Knodell, А0 по МЕТАVIR) и неравномерно выраженным фиброзом (МЕТАVIR F2-3)».
Учитывая жалобы, анамнез заболевания и жизни пациента, данные объективного осмотра, а также результаты лабораторных и инструментальных исследований, был выставлен следующий окончательный диагноз: «Неалкогольный стеатогепатит, биохимическая активность 1 степени, фиброз F2-3 по МЕТАVIR‚ по данным транзиентной эластографии печени (от 29.04.2020) – F3 по МЕТАVIR, индекс гистологической активности по Knodell – 1 балл, А0 по МЕТАVIR (по данным гепатобиопсии от 08.06.2020). Шифр по МКБ: [К73.2] Хронический активный гепатит, не классифицированный в других рубриках». Пациент был выписан на 14-й день от момента госпитализации с улучшением, рекомендовано продолжение пероральной медикаментозной терапии, модификация образа жизни. Показатели от 25.12.2020: ИМТ – 24,7 кг/м2, окружность талии – 82 см, АЛТ – 37 ЕД/л, АСТ – 35 ЕД/л, ЩФ – 211 ЕД/л, ГГТП – 49 ЕД/л, холестерин – 4,1 ммоль/л, ЛПНП – 2,5 ммоль/л. Заключение по результатам транзиентной эластографии печени от 12.01.2021: фиброз печени F1 (по МЕТАVIR). Субъективно жалоб не предъявляет.
На данный момент отмечается устойчивая положительная динамика состояния пациента. Нормализация клинико-диагностических показателей, снижение степени фиброза на 2 пункта – отличный показатель эффективности проведенной терапии. Справедливо отметить, что «переломным моментом» в данной истории болезни явился курс препарата Ремаксол.
Клинически действие препарата проявилось купированием астеновегетативного синдрома, лабораторно – снижением выраженности биохимических проявлений цитолитического и холестатического синдромов. Отмечена нормализация липидного состава крови.
Заключение
Ремаксол − уникальный препарат, весьма успешно применяемый при лечении дисметаболических расстройств и незаменимый в комплексной терапии метаболического синдрома и НАЖБП, в т.ч. на стадии стеатогепатита.



