Введение
Инсульт остается важнейшей медико-социальной проблемой ввиду высокого уровня заболеваемости и смертности в большинстве развитых стран мира (В.И. Скворцова и соавт., 2006), а также служит одной из причин нетрудоспособности населения.
Стойкое нарушение функции верхней конечности отмечают 75% пациентов, выживших после ишемического инсульта, даже после продолжительного курса реабилитации [1, 2]. Только 25% пациентов возвращаются к уровню повседневной активности, сравнимой с таковой до инсульта. Важным аспектом качества жизни, возможности самообслуживания и самоэффективности пациентов, перенесших инсульт, считается сохранность функции руки, прежде всего тонкой моторики кисти [3].
Возможность раннего прогнозирования клинического и функционального восстановления пациентов после мозгового инсульта – важная составляющая реабилитационного процесса. Раннее прогнозирование позволяет обеспечивать индивидуальное планирование, ставить реалистичные, оптимальные и, что немаловажно, понятные для пациента цели и задачи на реабилитационный период, осуществлять более целенаправленное воздействие на поврежденные вследствие мозговой катастрофы структуры путем применения адекватных средств, методов и форм реабилитации, а также наиболее эффективно распределять ресурсы. Все это повышает приверженность пациента, способствует вовлечению ближайшего окружения (родственников) в реабилитационный процесс. Данный подход способствует скорейшему возвращению пациента к его социальной роли в обществе как конечной цели реабилитации пациентов с любой патологией.
Одной из главных целей определения реабилитационного прогноза пациентов после инсульта является обеспечение реалистической направленности реабилитационных мероприятий на ранней стадии восстановления. Коллектив авторов [4] разработал алгоритм оценки предикторов восстановления функции верхней конечности после инсульта – PREP (Predict Recovery Potential algorithm), который состоит из трех этапов. На первом этапе оценивается мышечная сила верхней конечности: SAFE (Shoulder Abduction Flexor Extension) через 72 часа после дебюта инсульта (MRCWS – Британская шкала оценки мышечной силы), если сумма баллов >8, то прогноз по восстановлению функции верхней конечности в течение первых 3 месяцев достаточно высокий (1-я реабилитационная группа – РГ). Если сумма баллов <8, то далее с целью оценки функциональной целостности нисходящих моторных путей к поврежденной верхней конечности рекомендуется проведение транскраниальной магнитной стимуляции (ТМС) на 5–7-й день от дебюта заболевания. При наличии вызванных моторных ответов (ВМО) от собственных мышц кисти (первая межкостная тыльная мышца) прогноз на восстановление функции верхней конечности в течение первых 3 месяцев благоприятный (2-я РГ). В случае отсутствия ВМО от собственных мышц кисти рекомендуется на 10-й день от дебюта инсульта проведение диффузно-взвешенной МРТ для оценки структурной целостности заднего бедра внутренней капсулы (фракционная анизотропия) и рассчитывается индекс асимметрии. Если индекс асимметрии составляет <0,15, то пациент имеет ограниченный потенциал для восстановления утраченных функций (3-я РГ). В случае когда индекс асимметрии >0,15, то прогноз отрицательный (4-я РГ). В зависимости от прогноза пациент попадает в определенные РГ, различные по целям, задачам и реабилитационному воздействию. Задачи реабилитации для пациентов 1-й РГ сводятся к активному вовлечению пораженной руки в процесс жизнедеятельности, а также минимизации развития компенсаций со стороны здоровой руки. Задачи 2-й РГ с благоприятным прогнозом заключаются в восстановлении нормальных параметров мышечной силы и координации при выполнении необходимых действий, а также минимизации развития компенсаций со стороны здоровой руки. Третья РГ с ограниченным (лимитированным) прогнозом также занимается восстановлением утраченной мышечной силы, объема пассивных/активных движений и формированием адаптаций и компенсаций в повседневной деятельности. Четвертая РГ с отрицательным прогнозом занимается профилактикой вторичных осложнений, таких как развитие «болевого плеча», нестабильность плечевого сустава, спастичность, а также формирование компенсации со стороны здоровой руки. Данный алгоритм имел предсказательную силу (88%), высокую специфичность (88%) и чувствительность (73%).
Клинический случай
В декабре 2018 г. в клинику обратился пациент Г. 46 лет в позднем восстановительном периоде (6 меяцев) после перенесенного ишемического инсульта с синдромом правой средней мозговой артерии.
Из анамнеза: заболел 03.06.2018, когда на фоне повышения артериального давления (АД) до 220/100 мм. рт.ст. ослабели левые конечности и нарушилась речь. Бригадой Скорой медицинской помощи был доставлен в ГКБ-15 им. О.М. Филатова Москвы. В неврологическом статусе отмечены сглаженность левой носогубной складки, девиация языка влево, левосторонний пирамидный синдром до плегии в руке, в ноге мышечная сила проксимально 3 балла, дистально 2 балла, болевая гемигипестезия левых конечностей. Мультиспиральная компьютерная томография (МСКТ) головного мозга от 03.06.2018: на момент обследования свежих зон ишемии и кровоизлияний не выявлено; КТ-признаки кистозной трансформации в мосту; кистозно-глиозная трансформация в области базальных ядер слева. Ангиография головного мозга 03.06.2018: данных на наличие аневризм, окклюзий и мальформаций не выявлено. Дуплексное сканирование брахиоцефальных артерий (ДС БЦА) от 04.06.2018: атеросклеротические изменения БЦА – уплотнение стенок артерий; стенозы внутренних сонных артерий до 45% справа, 40% слева.
На основании проведенных клинических, инструментальных и лабораторных исследований диагностирован инфаркт головного мозга от 03.06.2018. Синдром правой средней мозговой артерии. Неуточненный подтип по TOAST (Trial of Org 10172 in Acute Stroke Treatment). Фоновое заболевание: гипертоническая болезнь с преимущественным поражением почек 3-й стадии, 3-я степень. Риск сердечно-сосудистых осложнений (ССО) – 4. Сопутствующий диагноз: нефроангиосклероз. Нарушение функции почек (скорость клубочковой фильтрации [СКФ] –70,0 мл/мин). Дислипидемия.
Тромболитическая терапия проведена 03.06.2018 с минимальным положительным эффектом. Далее проводилась инфузионная, антиоксидантная, нейропротекторная, гастропротекторная, антикоагулянтная и дезагрегантная терапия.
МСКТ головного мозга от 08.06.2018: КТ-признаки подострой ишемии в области базальных ядер справа с переходом в кистозную трансформацию.
Реабилитационный потенциал пациента не оценивался. Восстановительные мероприятия включали ЛФК при заболеваниях центральной нервной системы (ЦНС). При выписке состояние с незначительной положительной динамикой. Очаговый неврологический дефицит регрессировал частично. Сохранялись умеренная дизартрия и асимметрия оскала, плегия левой верхней конечности; мышечная сила в левой нижней конечности проксимально наросла до 4 баллов, дистально – до 3. Достигнута двигательная активность: пациент стал самостоятельно присаживаться в кровати, уверенно сидел, самостоятельно вставал и ходил с посторонней помощью. Оценка по шкале NIHSS – 6 баллов, модифицированной шкале Рэнкина (МШР) – 4, индекс Бартел – 50, индекс мобильности Ривермид – 6.
Далее с 22.06 по 06.07.2018 пациент находился на реабилитации в отделении медицинской реабилитации для больных с нарушением функции ЦНС. Реабилитационный потенциал не оценивался. На фоне проводимых восстановительных мероприятий (электростимуляция мышц левых конечностей, переменное электромагнитное поле – [ПЕМП] на область левых конечностей, лечебной гимнастики при синдроме гемипареза механотерапия) у пациента наблюдалась положительная динамика в виде увеличения мышечной силы в левой верхней конечности проксимально до 2 баллов, дистально – 1 балл; левая нижняя конечность проксимально – 4 балла, дистально – 3 балла.
Оценка по МШР – 4 балла, индекс мобильности Ривермид – 6.
В нашу клинику пациент поступил на плановую госпитализацию17.12.2018.
Жалобы на момент осмотра: отсутствие функциональной активности левой кисти.
В неврологическом статусе общемозговых, менингеальных и когнитивных нарушений нет. Сохраняется умеренная дизартрия, сглаженность левой носогубной складки. Симптомы орального автоматизма (Маринеску–Радовичи). Левосторонний гемипарез со снижением мышечной силы в верхней конечности проксимально до 3, дистально до 2 баллов, нижней конечности проксимально до 4, дистально до 3 баллов. Объем пассивных движений левой верхней конечности: в плечевом суставе ограничение отведения (до 100°), сгибания (до 150°) и разгибания (до 40°), ограничение супинации предплечья и тыльного сгибания в лучезапястном суставе, мышечный тонус повышен слева по спастическому типу. Сухожильные и периостальные рефлексы также повышены слева. Симптом Бабинского слева. Чувствительность сохранена. Координаторные пробы левой верхней конечностью в рамках пареза, правыми выполняет удовлетворительно. В позе Ромберга пошатывание без четкой латерализации. Оценка по МШР – 3 балла, индекс Бартел – 85, индекс мобильности Ривермид – 11.
Пациенту доступны лишь глобальные движения левой верхней конечностью. Подъем согнутой в локтевом суставе левой верхней конечности до 50–60° через отведение в плечевом суставе. Доступные функции: включение/выключение выключателя света на уровне груди путем надавливания тыльной стороной ладони, удержание левой прямой рукой с приоткрытой кистью (ладонной стороной) в отсутствие тыльного сгибания запястья предметов на столе при приготовлении пищи. У пациента имеется нижний кистевой захват, соответствующий 2А по классификации кистевых захватов по E.A. Zancolli [5]. Минимальная манипулятивная и хватательная функции кисти.
Оценка двигательной и функциональной активности верхней конечности проведена с использованием шкал: ARAT (Action Research Arm Test) 19 (max 57): шаровой захват – 8, цилиндрический – 5, щипковый – 1, крупные движения – 4. FMA (Fugl-Meyer Assessment) 34 (max 66).
Общий анализ крови, мочи без патологии. В биохимическом анализе крови: белок общий – 60,1 г/л, креатинин – 146,4 мкмоль/л, щелочная фосфатаза – 70,9 ЕД/л, в остальном без патологии.
Компьютерная томография головного мозга от 17.12.2018: признаки лакунарных кист в области базальных ядер с обеих сторон и в области моста.
В соответствии с алгоритмом оценки предикторов восстановления функции верхней конечности после инсульта (PREP), а также с целью определения пациента в РГ проведено нейрофизиологическое обследование с помощью электромиографа Viking Select (Nicolet Biomedical, США) и магнитного стимулятора Magstim (Великобритания). Кортикоспинальное (надсегментарное моторное) проведение оценивалось методом ТМС. ВМО с m. abductor pollicis brevis с двух сторон записаны на магнитную стимуляцию двигательной коры и корешков срединных нервов. Состояние проведения по периферическим нервам (сегментарное моторное проведение) оценивалось методом электронейромиографии (ЭНМГ): исследовали М-ответы и скорость распространения возбуждения (СРВ) по n. medianus с двух сторон, а также поздние моторные ответы – F-волны и Н-рефлексы в m. abductor pollicis brevis на стимуляцию n. medianus.

По данным ТМС (см. таблицу), у пациента выявлены грубые нарушения кортикоспинального (надсегментарного моторного) проведения для мышц левой руки (рис. 1). ВМО на магнитную стимуляцию двигательной коры с мышцы левой кисти получены лишь при использовании приема фасилитации. Латентность кортикального ВМО увеличена слева, амплитуда ответа значительно снижена. Время центрального моторного проведения (ВЦМП) для мышцы левой кисти увеличено. Амплитуда корешкового ВМО справа снижена.
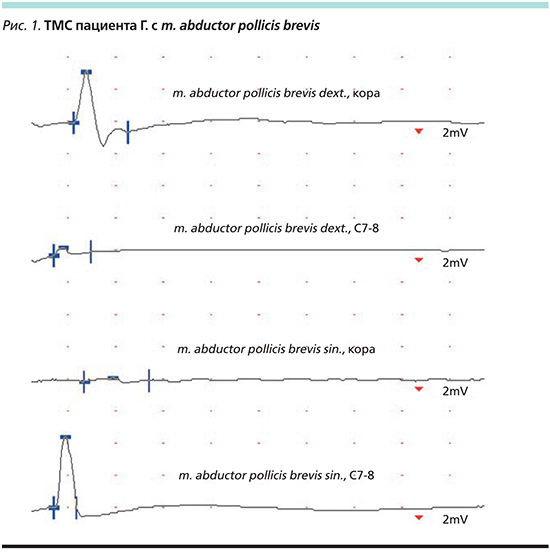
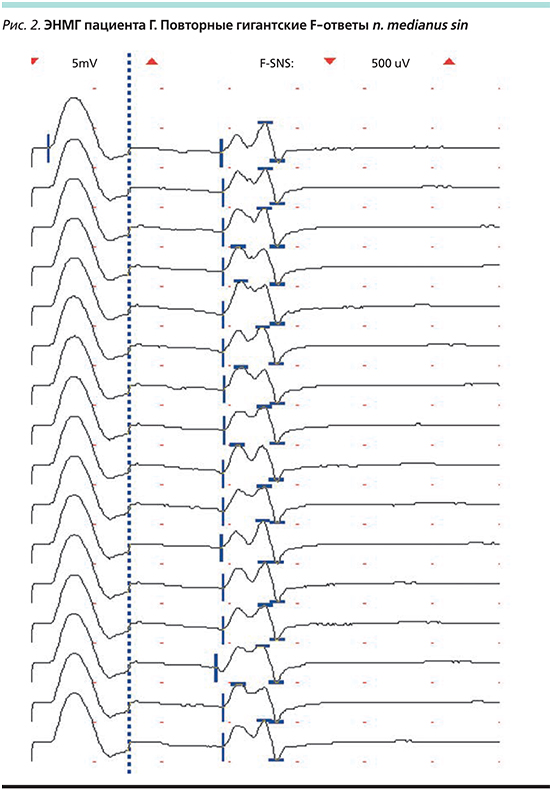
По данным ЭНМГ нарушений проведения по периферическим нервам (сегментарного моторного) не обнаружено. Амплитуда М-ответа n. medianus и скорость проведения возбуждения соответствовали норме, но М-ответ был выраженно ниже слева. Выявлены патологические изменения параметров поздних моторных ответов слева, указывающие на повышение возбудимости спинального мотонейронного пула для мышц левой кисти (рис. 2). При исследовании F-волн n. medianus sin получены повторные гигантские ответы с нормативными латентностями, СРВ по F-волне max оказалась несколько ниже слева. В m. abductor pollicis brevis sin. при стимуляции n. medianus sin. получен Н-рефлекс (в норме в данной мышце отсутствует): появляется при «нулевом» М-ответе, постепенно затухая, переходит в F-волну, Hmax/Mmax=69% (рис. 3).
На основании данных клинического осмотра, инструментальных и лабораторных методов исследования выставлен основной диагноз: хроническая ишемическая болезнь головного мозга с недостаточностью кровообращения в бассейне правой средней мозговой артерии. Поздний восстановительный период ишемического инсульта в бассейне правой средней мозговой артерии (от 03.06.2018). Тромболизис от 03.06.2018. Фоновое заболевание: гипертоническая болезнь 3-й стадии, 3-я степень. Риск ССО – 4. Сопутствующие заболевания: нефроангиосклероз. Нарушение функции почек (СКФ – 75,0 мл/мин).

Опираясь на предложенный алгоритм PREP (ретроспективно в т.ч.) и с учетом полученных данных клинического, нейрофизиологического осмотров, анализа сохранных двигательных функций, пациент был отнесен во 2-ю РГ, в приоритетные задачи в которой входят восстановление нормальных параметров мышечной силы и координации при выполнении необходимых действий, а также минимизация развития компенсаций со стороны здоровой руки. Немаловажное значение в постановке ближайшей цели имела и ориентированность пациента на восстановление функции кисти (желаемая двигательная активность – удержание черенка лопаты для уборки снега). Была сформулирована цель: постановка/формирование эффективного кистевого захвата. Исходя из поставленной цели, на данный реабилитационный период была определена программа воздействия:
- Стандартизированная методика реабилитации больных после инсульта (ООКТ), 1–4-я ступени, PNF (Proprioceptive Neuromuscular Facilitation)-терапия, тренировки на кардиотренажере «Мotomed») [6].
- Тренировки на тренажере Нейроинтерфейс–мозг–компьютер–экзоскелет (НМКЭ) кисти с визуальной и кинестетической обратной связью. Достоинствами данной технологии является возможность повышения эффективности реабилитационных мероприятий в восстановлении утраченных в результате инсульта двигательных функций у больных посредством качественной идеомоторной тренировки, а также реализации мультисенсорной обратной связи. Применение данной технологии показало свою эффективность [7–9]. Методика проведения занятий на НМКЭ кисти с мультисенсорной обратной связью, а также ее нейрофизиологические механизмы реализации опубликованы ранее [7, 8, 10–12].
- Мануальная терапия для улучшения функции кисти. Реализуется через последовательное воздействие на трех уровнях: А. Работа со структурой: подавление патологических синкинезий при сгибании верхней конечности (отведение в плечевом суставе, сгибание в локтевом, пронация предплечья), подавление патологического мышечного тонуса, ограничивающего реализацию нормального двигательного стереотипа верхней конечности. В. Реализация мероприятий, направленных на коррекцию/улучшение постурального контроля при выполнении определенного двигательного действия верхней конечностью. Формирование у пациента сознательного опережающего постурального контроля, включившего мобилизацию грудного отдела позвоночника, выведение в правильную позицию лопатки, плечевой кости и предплечья. При освоении данных этапов можно приступать к формированию активности. С. Создание облегченных положений для мобилизации дистального отдела верхней конечности и тренировки необходимых функций. Реализация описанных блоков облегчает старт двигательных реакций в дистальном отделе верхней конечности. Так, для каждого эффективного активного двигательного действия существует определенная «двигательная цепочка», подразумевающая реализацию механизмов реципрокной координации и постурального контроля.
Результаты
В результате проведенного восстановительного лечения в двигательном статусе была отмечена положительная динамика в виде увеличения объема движений левой верхней конечностью, улучшения хватательной и манипулятивной функций кисти. Улучшение функции кисти произошло за счет появления возможности супинации предплечья и формирования тыльного сгибания в лучезапястном суставе. По классификации спастической кисти по E.A. Zancolli [5] пациент перешел из захватов группы 2А в группу 1, т.е. из нижнего захвата перешел в верхний. Динамика восстановления двигательной и функциональной активности верхней конечности отражена в шкалах ARAT 31 (max 57): шаровой захват – 15, цилиндрический – 8, щипковый – 4, крупные движения – 4. FMA – 38 (max 66). Оценка по МШР – 3 балла, индекс Бартела – 90, индекс мобильности Ривермид – 11.
Обсуждение
Нейрофизиологическое исследование пациента не было проведено в остром периоде инсульта (по протоколу PREP это рекомендуется сделать в первые 5–7 дней), однако наличие кортикального ВМО в мышце кисти паретичной руки, несмотря на значительное снижение мышечной силы, в ней указывает на относительно сохранный реабилитационный потенциал, но выраженные ТМС-изменения (получение ВМО только при использовании приема фасилитации, удлинение ВЦМП, увеличение латентности и снижение амплитуды кортикального ВМО) показывают его ограниченность.
Применение протокола PREP позволило нам рационализировать стратегию и индивидуализировать план реабилитационных мероприятий. Это в свою очередь позволило реализовать реабилитационный потенциал в рамках задач-ориентированного подхода.
Таким образом, клинические (плегия в левой руке в остром периоде инсульта, парез до 2–3 баллов в позднем восстановительном периоде инсульта) и нейрофизиологические (регистрация ВМО с мышц паретичной левой кисти) данные позволили отнести пациента к группе с относительно благоприятным реабилитационным прогнозом и сформировать программу восстановительного лечения, показавшую свою эффективность. Тем не менее считаем, что улучшение функции кисти паретичной верхней конечности произошло не за счет регресса неврологического дефицита (сохраняются прежняя глубина пареза и спастичность в левой руке), а за счет более правильного и эффективного использования сохранных возможностей паретичной конечности.
Заключение
Данное наблюдение подтверждает важность постановки оптимальных целей на реабилитационный период, применения специфичных повреждению средств и методов восстановительного лечения для решения поставленных задач, а также демонстрирует взаимодополняемость клинических и нейрофизиологических данных в оценке предикторов восстановления.



