Введение
Лицевые боли непароксизмального характера могут быть обусловленными дисфункцией височно-нижнечелюстного сустава и миофасциальным болевым синдромом (МБС), клинически проявляющимися изменениями в жевательной мускулатуре (ЖМ), в частности мышечным спазмом, ограничивающим движения нижней челюсти. В клинической картине этого синдрома выделяют два периода – дисфункции и болезненного спазма ЖМ. В спазмированных мышцах возникают болезненные участки – “курковые”, или “триггерные”, мышечные зоны, из которых боль иррадиирует в соседние области лица и шеи.
Характерными диагностическими признаками МБС лица в настоящее время считаются боль в ЖМ, усиливающаяся при движениях нижней челюсти; ограничение подвижности нижней челюсти (вместо нормального открывания рта до 46–56 мм между резцами рот открывается только в пределах 15–25 мм); щелканье и крепитация в суставе; S-образное отклонение нижней челюсти в сторону или вперед при открывании рта; боль при пальпации мышц, поднимающих нижнюю челюсть.
В ЖМ таких больных обнаруживаются (при бимануальном исследовании) болезненные уплотнения, в толще которых имеются участки гиперчувствительности – мышечные триггерные точки (МТТ). Растяжение или сдавливание участка ЖМ с расположенной в ней МТТ приводит к боли, распространяющейся на соседние зоны лица, головы, шеи, что обозначается как “болевой паттерн мышцы”. Характерно, что болевой паттерн соответствует не невральной иннервации, а лишь определенной части склеротома. Дисфункциональный МБС развивается как осложнение длительного напряжения ЖМ без их последующей релаксации. У лиц среднего возраста с асимметричной адентией это может быть связано с вредными привычками – сжиманием челюстей в стрессовых ситуациях, выдвижением нижней челюсти и т. д. Вначале в мышце возникает остаточное напряжение, а затем в межклеточном пространстве формируются локальные мышечные уплотнения, связанные с трансформацией межклеточной жидкости в миогеллоидные уплотнения (МТТ), являющиеся источником патологической импульсации в вышележащие отделы центральной нервной системы. Наиболее часто МТТ образуются в крыловидных мышцах ввиду их анатомо-функциональных особенностей.
Часто МБС лица в значительной степени обусловлен психологическими причинами, депрессией, ипохондрией, неврозами, ввиду чего такие болевые синдромы можно обозначать как психопатологические. Лечебные мероприятия включают блокады локальными анестетиками или “сухой иглой”, назначение антидепрессантов и миорелаксантов. В последние годы все большее значение при МБС приобретают нестероидные противовоспалительные средства (НПВС). В патологическом каскаде, который запускает мышечный спазм с формированием ММТ, решающее значение имеет асептическое воспаление, в значительной степени опосредуемое двумя изоформами циклооксигеназы (ЦОГ). Согласно современным представлениям, мишенью большинства НПВС является главным образом ЦОГ2, с угнетением активности которой и связано их противоболевое действие. С учетом риска развития нежелательных явлений при системном применении НПВС понятен повышенный интерес к применению при МБС их местных (топических) лекарственных форм. Существуют определенные требования, предъявляемые к таким препаратам. Это эффективность, безопасность, отсутствие местных токсических и аллергических реакций, низкая системная биодоступность, обеспечение высокой концентрации активного вещества в скелетной мускулатуре.
Целью настоящего исследования являлось изучение эффективности и безопасности при МБС лица местных препаратов НПВС (Нурофен гель, Кетонал гель и Фастум гель) в сочетании с традиционным лечением (без пероральных форм НПВС).
Материал и методы
В исследование были включены 39 больных, страдающих МБС лица интенсивностью не менее 6 баллов по визуально-аналоговой шкале (ВАШ). Средний возраст пациентов составлял 45,7 ± 5,5 года, длительность заболевания в среднем составляла 3,2 года.
Критериями исключения были кожные аллергические реакции на тестируемые препараты.
Больные были разделены на 3 группы по 13 человек, местную терапию в которых проводили с использованием препаратов Кетонал гель (кетопрофен; 1-я группа), Фастум гель (кетопрофен; 2-я группа) и Нурофен гель (ибупрофен; 3-я группа) соответственно. Пациенты применяли топические препараты НПВС 2 раза в сутки в течение 7 дней на фоне стандартной терапии (блокады анестетиками, применения антидепрессантов, миорелаксантов). Лечение проводилось стационарно в условиях неврологического отделения.
Оценка интенсивности боли по ВАШ и степень ее уменьшения по 10-балльной шкале проводились в течение первого часа, через 1, 2, 3, 4, 5 и 6 часов после использования первой дозы тестируемых препаратов, а также на 2-й, 3-й, 4-й, 5-й, 6-й и 7-й дни их применения. У больных ежедневно оценивали также степень ограничения повседневной активности в стационаре из-за болевого синдрома (по данным субъективной оценки пациентом).
Результаты и обсуждение
Достоверное снижение интенсивности боли после первой дозы в группе, получавшей Кетонал гель (с 5,70 до 1,96 балла по ВАШ), отмечено к 15-й минуте; в группе, получавшей Фастум гель (с 5,40 до 1,94 балла по ВАШ), – к 18-й минуте; в группе, получавшей Нурофен гель (с 5,8 до 2,2 балла по ВАШ), – к 11-й минуте. При этом длительность противоболевого эффекта составила в группе Кетонала геля 40,0 ± 3,5 минуты, в группе Фастума геля – 48,5 ± 3,2 и в группе Нурофена геля – 51,0 ± 4,1 минуты.
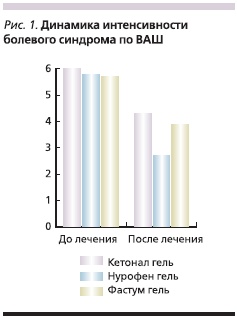
Динамика интенсивности болевого синдрома в результате проведенного лечения представлена на рис. 1. Наибольший эффект был зарегистрирован в группе больных, получавших Нурофен гель, у которых показатель боли уменьшился в 2 раза.
Общая эффективность лечения, по мнению пациентов, представлена на рис. 2. Наибольшая доля пациентов, отметивших значительное улучшение (72 %), была отмечена в группе, получавшей Нурофен гель.
Рисунок 2. Общая эффективность лечения, по мнению пациентов, препаратами, представленными на диаграмме.
В ходе исследования 4 пациента отметили нежелательные побочные явления в период лечения: чувство жжения – 1 больной в группе Фастума геля, чувство стянутости кожи – 2 пациента в группе Кетонала геля, неприятный привкус во рту – 1 больной в группе Кетонала геля. Все нежелательные явления разрешились к моменту завершения исследования самостоятельно и не потребовали отмены применявшихся топических НПВС.
Полученные в нашей работе результаты подтвердили эффективность и безопасность применения трансдермальных форм НПВС для местного лечения МБС лица. Достоверное анальгетическое действие препаратов отмечено уже через 11–18 минут после их первого применения. Наиболее быстро обезболивающее действие, чтоочень важно при наличии острой боли, достигалось у больных, применявших Нурофен гель. В той же группе регистрировалась наибольшая продолжительность анальгетического эффекта.
К концу проведенного лечения клиническое улучшение (уменьшение болевого синдрома ограничения повседневной активности) наблюдалось во всех группах, но максимальный эффект был зарегистрирован среди больных, которым проводилось лечение Нурофеном гелем. Важно подчеркнуть, что именно в этой группе наибольшее число пациентов (почти 3/4.) оценили достигнутый эффект как значительный.
Нурофен гель характеризовался и высокой степенью безопасности: побочные явления отмечены только у больных, получавших кетопрофенсодержащие препараты. В целом данный факт не отразился на профиле безопасности препаратов.
Заключение
Проведенное исследование подтвердило возможность применения трансдермальных форм НПВП при МБС лица. Наиболее эффективным и безопасным препаратом оказался Нурофен гель (ибупрофен), превосходящий в этом отношении кетопрофенсодержащие препараты по скорости наступления обезболивающего действия. Можно рассчитывать, что комбинированная терапия, включающая трансдермальные формы НПВС, позволит существенно повысить эффективность лечения МБС лица и других локализаций.
Информация об авторах:
Шаров Михаил Николаевич – доктор медицинских наук, профессор кафедры нервных болезней стоматологическогофакультета МГМСУ, заведующий нейростоматологическим отделением ГКБ № 50.
Тел. 8 (495) 611-22-86; e-mail: 6112286@mail.ru;
Фищенко Ольга Николаевна – ассистент кафедры нервных болезней стоматологического факультета МГМСУ
Тел. 8 (495) 611-73-78; e-mail: of177@bk. ru



