ВРоссии болезни опорно-двигательного аппарата являются социально отягощающим фактором, занимая второе место по дням и третье по случаям временной нетрудоспособности среди всех классов болезней. В практике терапевта пациенты с заболеваниями опорно-двигательного аппарата встречаются достаточно часто. Кроме того, в настоящее время участковые врачи-терапевты, врачи общей практики (семейные врачи) осуществляют оказание медицинской помощи пациентам с ревматическими заболеваниями с учетом рекомендаций врачей-ревматологов (приказ Минздравсоцразвития РФ № 315н от 04.05.2010).
Наиболее универсальными патологическими механизмами, лежащими в основе ревматических болезней, являются боль и воспаление. При отдельных нозологических формах воспалительный процесс в разной степени связан с факторами невоспалительного характера. Все известные типы боли – ноцицептивная, нейрогенная, психосоматическая и др. – могут принимать участие в формировании болевого синдрома.
К одной из основных групп лекарственных средств, влияющих как на процесс воспаления, так и на механизмы боли, относятся нестероидные противовоспалительные средства (НПВС). Противовоспалительное действие НПВС обусловлено ингибированием циклооксигеназы (ЦОГ). Важную роль в противовоспалительном действии НПВС играет их влияние на метаболизм и биоэффекты кининов. Снижение образования брадикинина приводит к уменьшению синтеза арахидоновой кислоты и как следствие – к действию продуктов ее метаболизма. Не менее важной представляется способность НПВС блокировать взаимодействие брадикинина с тканевыми рецепторами, что приводит к восстановлению нарушенной микроциркуляции, уменьшению перерастяжения капилляров, снижению выхода жидкой части плазмы, ее белков, провоспалительных факторов и форменных элементов, что опосредованно влияет на развитие других фаз воспалительного процесса.
Анальгезирующий эффект НПВС в большей степени проявляется при болях слабой и средней интенсивности, которые локализуются в мышцах, суставах, сухожилиях, нервных стволах, а также при головной или зубной боли. При интенсивных висцеральных болях, связанных с травмой, оперативным вмешательством, опухолью, большинство НПВС уступают по силе анальгезирующего действия наркотическим анальгетикам.
В то же время в ряде контролируемых исследований показана достаточно высокая анальгетическая активность диклофенака, кеторолака, кетопрофена при почечной колике и послеоперационной боли. Основным фактором, ограничивающим использование НПВС, являются побочные эффекты со стороны желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы, в большей или меньшей степени характерные для всех представителей этой лекарственной группы.
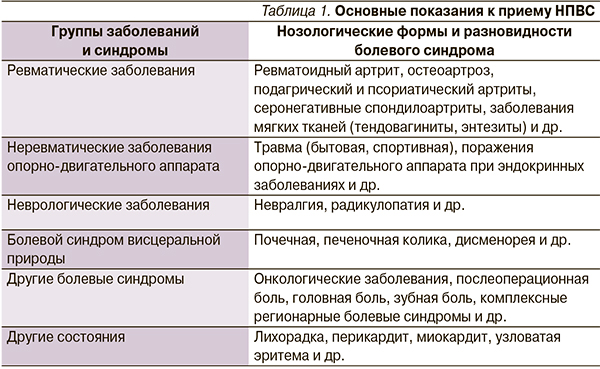
Основной спектр показаний к приему НПВС представлен в табл. 1.
С клинической точки зрения всем НПВС свойствен ряд общих черт:
- Неспецифичность противовоспалительного эффекта, т. е. тормозящее влияние на любой воспалительный процесс независимо от его этиологических и нозологических особенностей.
- Сочетание противовоспалительного, болеутоляющего и жаропонижающего действий.
- Хорошая переносимость.
- Тормозящее влияние на агрегацию тромбоцитов.
Индивидуальный ответ больного на различные НПВС может колебаться в широких пределах. Выбор эффективного препарата зависит от особенностей заболевания или болевого синдрома и во многом определяется активностью болезни, лабораторными показателями и распространенностью процесса. При выборе НПВС необходимо принимать во внимание селективность в отношении изоформ ЦОГ, фармакодинамические свойства, совместимость с другими лекарственными средствами, наличие хондропозитивного/хондронегативного эффектов. Для обеспечения безопасности длительного лечения НПВС перед началом терапии необходимо проводить стандартное лабораторное обследование – клинический анализ крови, биохимический анализ крови (уровни креатинина, аспартатаминотрансферазы, аланинаминотрансферазы), затем через 8 недель проводить повторное обследование. При сочетанном приеме НПВС и ингибиторов ангиотензинпревращающего фермента (ИАПФ) уровень сывороточного креатинина необходимо определять каждые 3 недели [1].
Большое значение в комплексном лечении болевых синдромов уделяется использованию аппликационной терапии. Применение локальных форм НПВС показано при моно‐ и олигоартикулярном поражении, при местной патологии околосуставных мягких тканей (тендинитах, тендовагинитах, бурситах), а также как дополнение при системном использовании этих лекарств. Локальные формы НПВС могут быть использованы пациентами с высоким риском осложнений при наличии ограничений в отношении системного применения этих лекарств (уровень доказательности А). Локальные формы НПВС являются эффективным самостоятельным симптоматическим средством при остеоартрозе коленных суставов и мелких суставов кистей (уровень доказательности А) [2–4].

Аппликационная терапия подразумевает применение различных лекарственных веществ с созданием в месте нанесения терапевтической концентрации препарата в тканях, что обусловливает противовоспалительный и обезболивающий эффекты. Препараты, используемые для данного вида терапии, можно разделить на три основные группы (табл. 2).
Практический опыт показывает, что, собственно, для купирования субъективных болевых проявлений наиболее часто используются НПВС местного применения. Локальная терапия с применением НПВС служит альтернативой пероральному и парентеральному использованию НПВС, а также важным вспомогательным компонентом комплексного лечения болевого синдрома. Рекомендуются к применению мазевые, кремовые и гелевые формы НПВС, способные глубоко проникать в кожу и подкожную клетчатку, блокируя болевые рецепторы. Кроме наиболее часто используемого диклофенака в России зарегистрированы локальные препараты на основе ибупрофена, кетопрофена, индометацина, бутадиона, пироксикама, кеторолака трометамина.
Известно, что выраженность и скорость наступления лечебного эффекта зависят от действующего вещества. Большое значение имеет также лекарственная форма. Наиболее удачной формой для локальной терапии является гель, в состав которого в качестве растворителя входит спирт, обеспечивающий быстрое всасывание действующего вещества в поверхностно расположенные структуры сустава. Поэтому применение геля более эффективно по сравнению с мазями или кремами и к тому же более эконо-мично [5, 6].
Из современных НПВС, представленных на российском рынке, наиболее мощным и быстрым обезболивающим действием обладает кеторолака трометамин, применение которого среди представителей данной фармакологической группы, предназначенных для купирования болей, наиболее предпочтительно. Для оптимизации проницаемости лекарственная композиция включает усиливающие агенты и рН-системы. По результатам сравнительных тестов различных агентов – усилителей всасывания – было обнаружено, что диметилсульфоксид (ДМСО), олеиновая и лимонная кислоты значительно повышают проницаемость кеторолака в кожу. Разработанная лекарственная форма предназначена для купирования болевого синдрома, вызванного воспалительными процессами, при этом отсутствует риск развития побочных эффектов со стороны ЖКТ, характерных для перорального приема кеторолака.
С целью изучения сравнительной эффективности и безопасности препарата Кеторол® гель (кеторолак, Д-р Реддиʹс Лабораторис Лтд, Индия) в качестве локального болеутоляющего средства при заболеваниях опорно-двигательного аппарата, в частности при болях в спине и гонартрозе, было иницировано настоящее исследование.
Материал и методы
На кафедре факультетской терапии им. акад. А.И. Нестерова совместно с кафедрой терапии и эндокринологии Ивановской государственной медицинской академии (зав. кафедрой – проф. С.Е. Мясоедова) проведено открытое многоцентровое проспективное рандомизированное сравнительное исследование в параллельных группах по оценке эффективности и безопасности использования в амбулаторных условиях лекарственных препаратов наружного применения Кеторол® гель 2,0 % и Фастум® гель 2,5 % (кетопрофен, А. Менарини Мэнюфекчеринг Лоджистикс энд Сервисиз С.р.Л., Италия). Проведение исследования одобрено Этическим комитетом РНИМУ им. Н.И. Пирогова. Положительное влияние НПВС на течение остеоартроза определяется их отчетливым анальгетическим действием и противовоспалительным эффектом, что позволяет существенно влиять на выраженность боли в суставах и способствовать восстановлению объема движений, т. е. воздействовать на наиболее значимые субъективные и объективные симптомы заболевания. В свою очередь боль в спине также занимает лидирующее положение среди всех болевых синдромов, являясь одной из основных и наиболее частых причин использования болеутоляющих средств.

В исследование были включены пациенты с умеренным болевым синдромом при гонартрозе и болью в нижней части спины (БНС). Всего в исследовании приняли участие 240 пациентов.
Размер выборки был рассчитан для основной переменной эффективности – среднее значение интенсивности боли по визуальной аналоговой шкале (ВАШ) через 10 дней терапии.
Пациенты, подлежащие включению в исследование и подписавшие информированное согласие, распределили в группы исследования в зависимости от установленного диагноза: группа «Гонартроз» и группа «БНС». Внутри этих групп в соответствии с назначенным лекарственным препаратом проведена рандомизация в одну из групп лечения таким образом, чтобы 50 % пациентов в группах «Гонартроз» и «БНС» получали Кеторол® или Фастум®.
Критерии включения в группу больных гонартрозом:
Пациенты обоего пола в возрасте от 40 до 70 лет с манифестным гонартрозом.
Интенсивность боли в коленном суставе по ВАШ в покое ≥ 40 мм, при движении ≥ 50 мм.
Рентгенологически подтвержденный диагноз «гонартроз» (наличие рентгенологических признаков остеофитов и сужения суставной щели и/или соответствующий критериям Клинической классификации артритов коленного сустава – ACR (R. Altman и соавт., 1986) на момент включения в исследование.
Критерии включения в группу больных БНС:
- Пациенты обоего пола в возрасте от 20 до 65 лет с острым болевым синдромом в нижней части спины (менее 12 недель) или обострением хронической боли в спине (более 12 недель);
- Интенсивность боли в спине по ВАШ в покое ≥ 40 мм при движении ≥ 50 мм.
Согласно проведенной рандомизации, пациенты использовали один из исследуемых препаратов в течение 10 дней путем нанесения геля тонким слоем на область максимальной болезненности 3 (Кеторол® гель) или 2 (Фастум® гель) раза в сутки, согласно инструкциям по применению препаратов. Параметрами эффективности в обеих группах служили интенсивность болевых ощущений по ВАШ в покое (мм); интенсивность боли по ВАШ при движении (мм); суммарная оценка состояния здоровья пациента, данная врачом и пациентом (ВАШ, мм); субъективная оценка эффективности проводимой терапии врачом, приверженность пациентов к проводимой терапии. Во время исследования всем больным было запрещено применение других средств локальной терапии (НПВС гели, мази, кремы), кроме исследуемых, а также глю-кокортикостероидов, как для системного, так и для местного применения, НПВС для системного применения в группе пациентов с гонартро-зом.
Мощность исследования планировалась для тестирования гипотезы о не меньшей эффективности (non-inferiority) исследуемого препарата по сравнению с препаратом сравнения. На основании данных литературы граница «не меньшей эффективности» была принята 15 мм, стандартное отклонение – 40 мм.
H0: -15 ≥ µкеторол – µфастум ≤ 15
Ha: -15 < µкеторол – µфастум > 15
Результаты и обсуждение
В анализ эффективности вошли данные 238 пациентов, завершивших исследование. Двое пациентов выбыли из исследования по причинам, не связанным с применением исследуемых препаратов. Согласно результатам, полученным в ходе статистической обработки, значимых различий в группах Кеторол® и Фастум® по возрасту, индексу массы тела (ИМТ), стадии гонартроза, длительности болезни, выраженности заболевания по ВАШ в мм, оцененных врачом и пациентом, а также оценки боли в покое и при движении по ВАШ в мм не выявлено (табл. 3).
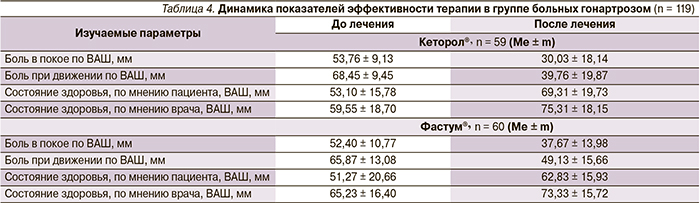
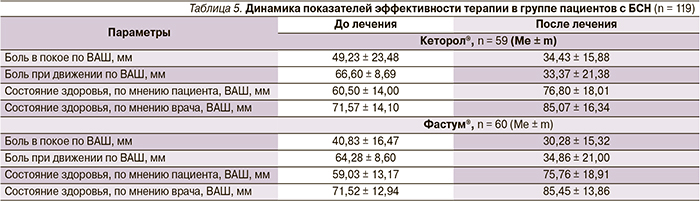
В ходе сравнительной оценки эффективности лекарственных препаратов для наружного применения Кеторол® гель и Фастум® гель пациентами с гонартрозом и первичным БСН отмечена статистически значимая динамика интенсивности боли по ВАШ как при движении, так и в покое, а также положительная динамика в оценке состояния здоровья, по мнению врача и пациента, в обеих группах больных (p < 0,05), (табл. 4, 5).
Достоверных статистических различий по основным показателям эффективности терапии между группами Кеторол® и Фастум® не выявлено. Доказательство сопоставимой эффективности препаратов основывается на расчете 95 % доверительного интервала для разности средних значений шкалы ВАШ боли в покое на последнем визите.
Эффективность проводимой терапии препаратом Кеторол® гель, по мнению врача, в группах пациентов с БНС и гонартрозом в большинстве (95 %) случаев оценена как «значительное улучшение» и «улучшение». По мнению пациентов, переносимость проводимой терапии отмечена как «отличная» и «хорошая» у подавляющего числа больных (98 %).
В ходе исследования выполнялись промежуточный и итоговый анализы переносимости препаратов каждым пациентом. Оба препарата – Кеторол® гель и Фастум® гель – продемонстрировали одинаково благоприятный профиль безопасности для пациентов с БНС и гонартрозом. Всего было зарегистрировано 2 нежелательных явления легкой степени тяжести в изучаемых группах больных (дерматит в месте нанесения), не потребовавших отмены препарата.
Выводы
Таким образом, проведенное исследование позволяет положительно оценивать применение геля Кеторол® больными остеоартрозом коленного сустава и болью в нижней части спины. Препарат Кеторол® в лекарственной форме гель для наружного применения, по нашим данным, обладает высокой клинической эффективностью, отчетливым анальгетическим эффектом, хорошим профилем безопасности, что делает актуальным его использование в лечении костно-мышечных заболеваний в амбулаторной практике.



