Острые респираторные вирусные инфекции (ОРВИ) и грипп в настоящее время являются самыми частыми заболеваниями в мире, которые охватывают все возрастные группы населения. Достаточно сказать, что в периоды ежегодных эпидемий заболевают до 10 % населения земного шара, во время пандемий число заболевших увеличивается в 4–5 раз [1]. В России ежегодно регистрируется около 50 млн случаев инфекционных заболеваний, из которых ОРВИ и грипп составляют до 90 % [2]. По данным МЧС, в период эпидемии 2003 г. ОРВИ и гриппом переболели около 30 млн человек, а экономические затраты составили 50 млрд руб. В настоящее время отмечается рост на 12 % по сравнению с предыдущим десятилетием т. н. простудных заболеваний, вызываемых различными представителями вирусов гриппа, парагриппа, адено-, рино-, коронавирусов и др. [3].
По данным Федерального центра Госсанэпиднадзора Минздравсоцразвития России, число заболевших гриппом в РФ с января по май 2008 г. составило 317 319 человек [4]. Очевидно, что вышеприведенные цифры заболеваемости ОРВИ и гриппом явно занижены, т. к. мы можем оперировать только данными по зарегистрированной заболеваемости, опираясь на количество извещений, поступающих из амбулаторно-поликлинических лечебных учреждений и число выданных листков нетрудоспособности. Для сравнения: в США число заболевших достигает 30 млн человек в год (табл. 1) [5].
Таблица 1. Статистика годовой заболеваемости и смертности от гриппа в мире [5].
Столь высокая заболеваемость обусловливает значительные социальные и экономические последствия. Известно, что на лечение гриппа и его осложнений ежегодно в мире расходуется около 14,6 млрд долл. При этом основная сумма затрат приходится на косвенные издержки, связанные с потерей трудоспособности. В частности, в США косвенные потери от гриппа составляют порядка 10–15 млрд долл. в год [5, 6]. В России ежегодный суммарный экономический ущерб от гриппа в среднем оценивается в 10 млрд руб. [5].
Смертность от гриппа и его осложнений занимает первое место среди всех инфекционных заболеваний. В структуре смертности ведущее место принадлежит пациентам старше 65 лет (80–90 %) – лицам пожилого возраста с отягощенным анамнезом, страдающим рядом тяжелых хронических заболеваний сердечно-сосудистой системы, органов дыхания. В то же время среди пациентов 45–64 лет без сопутствующей патологии смертность составляет примерно 2 случая на 100 тыс. человек [7]. В табл. 1 приведены сведения о годовой смертности от гриппа в ряде стран.
По расчетам британских пульмонологов, клинически значимые случаи ОРВИ возникают с частотой 2–3 эпизода в год на 1 взрослого человека и 7–10 эпизодов на 1 ребенка школьного возраста в год [8]. Если принимать в среднем 2 эпизода в год на 1 жителя Великобритании (население страны – примерно 60 млн человек), это составит 120 млн эпизодов ОРВИ в год [9].
ОРВИ обычно характеризуется симптомокомплексом, включающим воспалительные изменения в носоглотке (затруднение носового дыхания, выделения из носа, гиперемию зева, болезненность при глотании), кашель, явления интоксикации (лихорадку, ознобы, одышку, слабость, мышечные боли). Заболевания, вызванные разными вирусами, отличаются степенью выраженности отдельных симптомов, продолжительностью их течения. Причем явления интоксикации более выражены при гриппе (табл. 2) [10]. Как правило, заболевание протекает в течение относительно короткого времени (10–14 дней). Т
Таблица 2. Сравнительная частота развития симптомов ОРВИ и гриппа [10].
олько часть ОРВИ (40–50 %) сопровождается развитием острого кашля, что составляет 45–48 млн случаев в год [9]. Нередко кашель, его тяжесть, выраженность и продолжительность требуют использования лекарственных средств.
По статистике, ОРВИ является причиной наиболее частого обращения к врачу – примерно 20 % всех заболевших. Эти обращения обусловлены преимущественно резистентностью кашляк купленным и/или домашним средствам, употребляемым пациентами, а также значительной длительностью кашля, по времени заметно превышающей ожидаемую продолжительность заболевания [9]. Что касается числа госпитализаций, то их число не поддается учету. У практически здоровых людей, заболевших ОРВИ, кашель не требует обязательного направления в стационар. В то же время пациенты групп риска, например страдающие хронической обструктивной болезнью легких (ХОБЛ) или бронхиальной астмой (БА), у которых ОРВИ является триггером обострения заболевания, а также больные с тяжелыми хроническими интеркуррентными заболеваниями нередко подлежат госпитализации.
Кашель принадлежит к числу симптомов, часто встречающихся во врачебной практике, и является пятой по частоте причиной, заставляющей амбулаторных больных обращаться к врачу. Среди симптомов, обусловленных патологией респираторной системы, кашель занимает первое место [11]. Кашель (tussis) – рефлекторный акт, играющий большую роль в самоочищении дыхательных путей как от инородных тел, попавших извне, так и от эндогенно образовавшихся продуктов (слизи, крови, гноя, продуктов тканевого распада) [12]. В клинической практике часто приходится классифицировать кашель в зависимости от причинного фактора. Поэтому большое диагностическое значение имеет информация о времени возникновения кашля, его продуктивности, а также сопутствующих симптомах.
При определении этиологии кашля важно установить его продолжительность. По длительности существования кашля выделяют острый кашель (табл. 3) продолжительностью до 3 недель и хронический – продолжительностью более 8 недель [13–16].
Таблица 3. Основные причины острого и хронического кашля (адаптировано из Чучалина А.Г., Абросимова В.Н., 2000 [5]).
Эти две категории кашля не являются взаимоисключающими, и деление это в большой мере условно. Например, при ОРВИ острый кашель может продолжаться значительно дольше 3 недель. Так называемый постинфекционный кашель связан с тем, что воспаление на фоне вирусной инфекции способствует гиперреактивности бронхов, вследствие чего развивается затянувшийся кашель.
Продуктивность кашля определяется не только и не столько экспекторацией мокроты. Определяющим моментом является гиперпродукция бронхиальной слизи в дыхательных путях при их поражении. Соответственно, непродуктивный кашель развивается при заболеваниях, не связанных с развитием воспалительного процесса в дыхательных путях и не сопровождается гиперсекрецией бронхиальной слизи. Так, кашель при простудных заболеваниях (ОРВИ) развивается в основном в результате механического раздражения рецепторных зон секретом из верхних дыхательных путей и/или гортани (постназальным затеком) или чихания, или обеих причин и, по сути, является непродуктивным (табл. 3).
Особо следует выделить одну из групп риска – курильщиков, выкуривающих большое количество сигарет в течение длительного периода. Табакокурение относится к одному из агрессивных факторов риска, приводящих к развитию и прогрессированию болезней, имеющих большое социальное значение, таких как заболевания легких, артериальная гипертензия и ишемическая болезнь сердца, язвенная болезнь желудка, разнообразные эндокринологические заболевания и многие другие формы патологии [17]. Эти пациенты страдают хроническим бронхитом, в просторечии называемым “кашель курильщика”. В то же время эпизоды обострения хронического бронхита могут продолжаться более короткое время – до 3 недель при корректном лечении. Эти эпизоды могут повторяться достаточно часто в течение года (по определению хронического бронхита – кашель более 3 месяцев в году на протяжении 2 последовательных лет и более). Короткие эпизоды обострений хронического бронхита нередко расцениваются как повторные эпизоды острого бронхита, что может приводить к гиподиагностике хронического бронхита.
К сожалению, курильщики, которые кашляют и отделяют мокроту, не считают себя больными, не обращают внимания лечащих врачей на эту особенность своей жизни. Таким образом, заболевание ОРВИ (гриппом) расценивается у этой категории пациентов как эпизод острого кашля. Тем не менее в отличие от случаев заболевания практически здоровых лиц в данной ситуации мы имеем дело с развитием продуктивного кашля, что в целом нехарактерно для ОРВИ (гриппа). Следует отметить, что курильщики значительно чаще болеют инфекционными заболеваниями (в т. ч. ОРВИ), чем некурящие [18]. Известно, что табакокурение является основной экзогенной причиной развития ХОБЛ. В патогенезе ХОБЛ важное место отводится нарушению мукоцилиарного клиренса – гиперсекреции бронхиальной слизи и угнетению активности реснитчатых клеток.
Табачный дым содержит значительное количество свободных радикалов, ингаляционно проникающих в дыхательные пути и нарушающих баланс в системе оксиданты–антиоксиданты. Thatcher T.H. и соавт. (2007), Yang S.R. и соавт. (2007) [19], Rahman I. и соавт. (2006) [20] установили, что в табачном дыме одной затяжки сигареты, проникшем в дыхательные пути человека, содержится около 1015 свободных радикалов и около 4700 различных химических соединений. В процессе формирования этого дисбаланса, охарактеризованного как окислительный (оксидативный) стресс, происходит повреждение биологических мембран клеток, входящих в структуру легочной ткани. Острое повреждение легочной ткани при хроническом курении трансформируется в хронический воспалительный процесс дыхательных путей, результатом которого является медленное, но прогрессирующее снижение вентиляционной функции легких. Клиническая картина этого патологического процесса известна, как ХОБЛ [21].
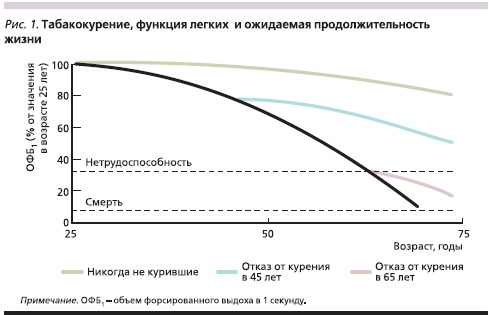
Табакокурение приводит к редукции вентиляционной функции легких; преждевременно снижаются параметры функции внешнего дыхания, ускоренными темпами нарастает дыхательная недостаточность [22]. Необходимо подчеркнуть, что в условиях холодного климата и напряженной физической работы ингаляция табачного дыма провоцирует раннее развитие эмфиземы легких. Fletcher C. и соавт. (1977) смогли продемонстрировать негативное влияние табачного дыма наожидаемую продолжительность жизни курящего человека (рис. 1). Итак, к группам риска при заболевании ОРВИ относятся люди, длительно курящие табак, а также пожилые пациенты, особенно страдающие хроническими заболеваниями.
Симптоматическое лечение при ОРВИ (гриппе) должно быть направлено на уменьшение лихорадки, болевого синдрома и дегидратации, а также на редукцию воспалительных изменений в носоглотке. Острый непродуктивный кашель при ОРВИ, как правило, протекает доброкачественно. Лечение его в целом не является серьезной проблемой. Рекомендуется увлажнение воздуха в помещении, применение паровых ингаляций, домашних средств (например, меда, лимона), растительных настоев или отваров. В случаях изнурительного кашля возможно применение противокашлевых лекарственных средств – препаратов, подавляющих кашель (седативных, антигистаминных, декстрометорфана, ментола). Опиатные противокашлевые средства (например, кодеин) обладают значительными побочными эффектами, вследствие чего не могут быть рекомендованными.
Проблема возникает обычно при необходимости лечения острого кашля у заболевших ОРВИ курильщиков. Как мы уже говорили, у этой группы лиц острый кашель чаще всего продуктивный. Гиперпродукция вязкой бронхиальной слизи требует применения серьезных муколитических средств, а гиперреактивность дыхательных путей и нередко бронхиальная обструкция – бронхолитических препаратов. Для исключения полипрагмазии – назначения одновременно нескольких препаратов, направленных на отдельные звенья патогенеза острого кашля при ОРВИ у курильщиков, желательно применение комбинированных препаратов.
Одним из таких препаратов является препарат Аскорил экспекторант (Гленмарк, Индия), в состав которого входят сальбутамол, бромгексин и гвайфенезин:
- сальбутамол – β-адреномиметик с избирательной активностью. Селективно стимулирует β2-адренорецепторы, локализующиеся, в частности, в бронхах. Обладает выраженными бронхолитическими свойствами: предупреждает и купирует бронхоспазм; снижает сопротивление в дыхательных путях, увеличивает жизненную емкость легких. Бронхолитический эффект обусловлен расслаблением гладкой мускулатуры бронхов. Тормозит выброс медиаторов воспаления из тучных клеток и базофилов, анти-IgE-индуцированный выброс гистамина, предупреждает развитие бронхоспазма, обусловленного антигеном. Устраняет антигензависимое подавление мукоцилиарного транспорта, улучшает мукоцилиарный клиренс и выделение факторов хемотаксиса нейтрофилов, умеренно стимулирует секрецию слизи, активирует функции мерцательного эпителия, стимулирует восстановление реснитчатого эпителия дыхательных путей;
- бромгексин оказывает муколитическое и отхаркивающее действия в результате деполимеризации и разрушения мукопротеидов и мукополисахаридов, входящих в состав мокроты. Кроме того, стимулирует деятельность секреторных клеток слизистой оболочки бронхов, продуцирующих сурфактант, который обеспечивает стабильность альвеол в процессе дыхания, защиту от неблагоприятных факторов, а также улучшает реологические свойства бронхиальной слизи (снижает адгезию, обеспечивает формирование двух фаз бронхиальной слизи – золя и геля), что способствует лучшей ее экспекторации. При приеме внутрь полное (99 %) всасывание происходит в течение 30 минут. Биодоступность при пероральном приеме составляет 80 % вследствие эффекта “первого прохождения” через печень. В плазме бромгексин связывается с белками. Проникает через гематоэнцефалический и плацентарный барьеры. В печени подвергается деметилированию и окислению. Часть образующихся метаболитов сохраняет активность. Период полувыведения достигает 15 часов вследствие медленной обратной диффузии из тканей. В виде метаболитов экскретируется почками 99 % препарата, в неизмененном виде – 1 %;
- гвайфенезин – отхаркивающее средство. Стимулирует секрецию жидких частей бронхиальной слизи, повышает активность цилиарного эпителия бронхов и трахеи. Уменьшает поверхностное натяжение и адгезивные свойства мокроты, что снижает ее вязкость и облегчает эвакуацию из дыхательных путей. Всасывается в желудочно-кишечном тракте, быстро метаболизируется и выводится с мочой. Период полувыведения – 1 час. Основной метаболит – β-(2-метоксифенокси) молочная кислота.
По данным исследований эффективности и безопасности Аскорила у пациентов с различными заболеваниями органов дыхания (острым и хроническим бронхитом, БА, ХОБЛ, пневмонией), проведенных в России и за рубежом, отмечена высокая эффективность терапии этим препаратом (78–96 %) [22–24], особенно у пациентов с хроническими бронхообструктивными заболеваниями [24], что выражается достоверным улучшением бронхиальной проходимости [24], уменьшением интенсивности кашля, облегчением экспекторации мокроты. Начало действия препарата зарегистрировано уже к концу первых суток лечения. Как правило, серьезных побочных эффектов не отмечено, однако у 6–8 % пациентов возникали кратковременное сердцебиение и тремор рук при приеме дозы 30 мл/сут [23, 24], при снижении дозы препарата эти явления проходили. К тому же была отмечена фармакоэкономическая выгода при использовании Аскорила по сравнению с применением комбинации муколитика и бронхолитика [24].
Таким образом, Аскорил одновременно воздействует практически на все звенья патогенеза острых и хронических бронхолегочных заболеваний, сопровождающихся образованием трудноотделяемого вязкого секрета: БА, трахеобронхита, обструктивного бронхита, пневмонии, эмфиземы легких, коклюша, пневмокониоза, туберкулеза легких и др. Применение комбинированного препарата позволяет снизить кратность приема, уменьшить количество лекарственных средств и риск побочных эффектов. Это приобретает особую актуальность в условиях, когда невозможно осуществить ингаляционную терапию.
Целью проведенного сравнительного исследования была оценка клинической эффективности и безопасности применения препарата Аскорил экспекторант, а также стандартного лечения ОРВИ с явлениями бронхиальной обструкции и кашля у курильщиков.
Материал и методы
Открытое сравнительное рандомизированное исследование было проведено в марте–мае 2008 г. В исследование включали пациентов, отобранных согласно критериям включения и исключения.
Критерии включения в исследование:
- наличие письменного согласия пациента на участие в исследовании;
- возможность лечения в амбулаторных условиях;
- обязательное наличие у больного двух основных симптомов простуды (затруднение носового дыхания, выделения из носа) и минимум двух дополнительных симптомов из следующих: слабость, недомогание, повышение температуры, озноб, мышечные боли, болезненность при глотании, гиперемия зева);
- наличие/усиление кашля с отделением мокроты или без нее;
- стаж курения;
- отсутствие показаний к назначению антибиотиков (возраст > 75 лет при наличии лихорадки, сердечная недостаточность, инсулинозависимый сахарный диабет, серьезные неврологические нарушения – инсульт).
Критерии исключения:
- состояние, требующее направления в отделение реанимации и интенсивной терапии;
- подтвержденная или предполагаемая непереносимость компонентов препарата Аскорил;
- диагностированные/установленные ранее заболевания органов дыхания (ХОБЛ, БА, туберкулез, саркоидоз, рак легкого, аллергические заболевания и др.);
- пациенты, принимающие теофиллин, ингибиторы моноаминоксидазы, β-адреноблокаторы, диуретики, системные глюкокортикостероиды, противокашлевые препараты.
Всего в исследование были включены 60 пациентов (46 мужчин, 14 женщин) в возрасте от 23 до 72 лет (средний возраст – 41,2 ± 11,8 года). Все больные получали лекарственные препараты стандартной терапии ОРВИ (гриппа) – жаропонижающие, противовоспалительные средства, деконгестанты и т. д. Для применения муколитических препаратов пациенты были рандомизированы методом случайной выборки в 2 группы: группа А (31 пациент) получала исследуемый препарат Аскорил, группа Ст (29 пациентов) получала стандартную терапию ОРВИ + муколитик (бромгексин, ацетилцистеин, амброксол, растительные отхаркивающие средства).
Было запланировано 4 визита: 1-й – в первые сутки на приеме врача (осмотр, рандомизация, выдача дневника, заполнение индивидуальной регистрационной карты), 2-й – на вторые сутки (по телефону) уточнение переносимости препаратов, 3-й – напятые сутки лечения (решение вопроса об эффективности терапии и продолжении/завершении выбранного лечения), 4-й – на десятые сутки лечения – завершающий. В течение всего исследования все пациенты вели ежедневный дневник, отвечая на вопросы и оценивая свое состояние в баллах соответственно шкалам оценки симптомов.
Результаты
Обе группы оказались сопоставимыми по демографическим показателям, наличию сопутствующих заболеваний, статусу курения (табл. 4, 5), выраженности симптомов заболевания.
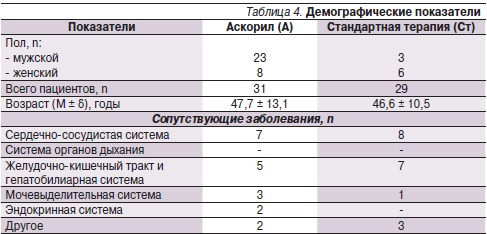
Оценка интенсивности дневного и ночного кашля проводилась по 6-балльной шкале БОК (табл. 6) [25]. На тяжелый кашель (3–4 балла) жаловались 28 (87,1 %) больных группы А и 28 (96,6 %) больных группы Ст. Достоверные различия степени интенсивности дневного кашля (p < 0,01) отмечены к 5-м суткам лечения у группы пациентов, получавших Аскорил, по сравнению с группой получавших стандартную терапию. Данные различия сохранялись в течение 5–8 суток лечения, и эффективность терапии дневного кашля в обеих группах сравнялась только к 9–10-м суткам лечения. Динамика тяжелого дневного кашля отражена на рис. 2. Степень интенсивности ночного кашля начала достоверно уменьшаться в группе А по сравнению с группой Ст начиная с 1-го дня терапии (p < 0,01). Это преимущество больных, принимавших Аскорил (p < 0,01, p < 0,05), сохранялось до 9-х суток лечения (рис. 3).
Таблица 6. Оценка дневного и ночного кашля (шкала БОК).

Количество мокроты оценивали по следующей шкале: мокроты нет – 0 баллов, незначительное количество (до 5 мл) – 1 балл, немного (15 мл) – 2 балла, умеренное количество (30 мл и более) – 3 балла, много (150 мл и более) – 4 балла. Кроме того, для оценки цвета мокроты использовали следующую шкалу: мокроты нет – 0, бесцветная – 1 балл, бледно-желтая – 2, светло-желтая – 3, светло-желтая/ зеленая – 4, темно-желтая/зеленая – 5 баллов.
На протяжении первых 5 суток лечения только у 9 больных из обеих групп отделялоcь умеренное количество мокроты (> 30 мл/сут). На 2-е сутки лечения число пациентов, у которых стала отделяться мокрота, увеличилось до 96,7 % в группе А, а в группе Ст только на 3-е сутки лечения отделение мокроты было зарегистрировано у 100 % пациентов. При этом достоверно более выраженная динамика уменьшения количества гнойной мокроты была зарегистрирована в группе А начиная с 3-го дня заболевания (р < 0,07). Равенство показателей в обеих группах сохранялось до 6-х суток (рис. 4). Затем тенденция к уменьшению количества мокроты стала четко прослеживаться в группе А, а на 7-е сутки различие между группами стало статистически достоверным (p < 0,01). На 6–7-е сутки лечения число больных, отделяющих зеленую мокроту в группе получавших Аскорил, достоверно уменьшилось по сравнению с группой Ст (p < 0,02).

Вопрос о прекращении/продолжении терапии решался на 5–6-е сутки лечения, что определялось рабочим графиком лечащих врачей. Нередко прекращали лечение самостоятельно в связи со значительным улучшением состояния/самочувствия. На 6–8-е сутки таких больных из группы Аскорила было больше, чем из группы стандартной терапии.
Заключение
Таким образом, результаты исследования показали эффективность и безопасность обеих схем терапии. Однако эффективность лечения препаратом Аскорил была выше по сравнению со стандартной терапией, т. к. на его фоне период выраженности симптомов заболевания и длительность лечения ОРВИ были короче.
Информация об авторе:
Клячкина Ирина Львовна – кандидат медицинских наук, доцент кафедры пульмонологии
с курсом фтизиатрии ГИУВ МО РФ



