Ревматоидный артрит (РА) сохраняет свое значение как одна из наиболее важных проблем научной и практической ревматологии. Заболевание характеризуется широкой распространенностью (около 1 % населения), упорным прогрессирующим течением, сложными патогенетическими механизмами, гетерогенностью клинико-иммунологических форм. В отсутствие адекватного лечения инвалидизация пациентов может наступить в первые годы заболевания. За счет потенциально опасных системных проявлений и осложнений (васкулит, амилоидоз и др.), а также ускоренного развития атеросклероза и высокой частоты тяжелой кардиоваскулярной патологии у больных РА наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [1, 2]. Все эти факторы делают терапию РА серьезной задачей.
Долгое время РА считался неуклонно прогрессирующим заболеванием, контролировать течение которого чрезвычайно сложно. С середины 1990-х гг. в подходах к лечению РА наблюдаются существенные перемены, приведшие к значительному улучшению прогноза.
Были обоснованы следующие стратегически важные концепции [3, 4]:
- Представление о наличии ранней стадии болезни, когда терапевтические воздействия принципиально более эффективны, чем на более поздних этапах.
- Концепция ранней агрессивной терапии и тщательного контроля, которая говорит о необходимости активного лечения сразу после установления диагноза и частого (не реже 1 раза в 3 месяца) регулярного мониторирования показателей активности болезни с целью своевременной модификации терапии при ее недостаточной эффективности.
- Понятие о ключевых механизмах патогенеза РА, которое обосновывает развитие принципиально новых методов терапии.
Настоящую революцию в лечении РА и других воспалительных ревматических заболеваний, таких как болезнь Бехтерева, псориатический артрит и др., совершило появление генноинженерных биологических препаратов (ГИБП), представляющих собой специально созданные иммуноглобулины или другие белковые молекулы. Создание ГИБП непосредственно связано с представлением о ключевых механизмах патогенеза, на которые они оказывают блокирующее или модулирующее действие. В ревматологии ГИБП занимают место, аналогичное таргетной терапии в современной онкологии.
ГИБП радикально улучшили результаты лечения ранее некурабельных пациентов. Хорошо известно [5], что на стандартную терапию базисными противовоспалительными препаратами (БПВП), такими как метотрексат, лефлуномид, сульфасалазин, в т. ч. при сочетании с глюкокортикоидами, удовлетворительно отвечают только 50–60 % больных (при раннем РА, когда длительность болезни не превышает одного года, результаты могут быть лучше). Таким образом, около половины пациентов оказываются резистентными к БПВП. Поэтому еще 10–15 лет назад 20 %-ное улучшение состояния больного РА (по таким показателям, как число припухших и болезненных суставов) могло считаться терапевтическим успехом. В клинической практике в 1980–1990 гг. частота достижения клинической ремиссии составляла менее 10 % [6]. В случае, когда целью лечения является не просто улучшение, а достижение устойчивой низкой активности болезни, как это было в известном шведском исследовании SWEFOT [7], оказывается, что около 2/3 больных нуждаются в комбинированной терапии.
После внедрения ГИБП в клиническую практику помимо купирования симптомов заболевания в настоящее время ставятся такие задачи, как торможение эрозивного процесса в суставах, нормализация функционального статуса и качества жизни пациента, потенциальное увеличение продолжительности жизни до популяционного уровня [8, 9]. При этом частота клинической ремиссии на фоне комбинированной терапии даже у тяжелых больных в рандомизированных клинических (РКИ) и наблюдательных исследованиях достигает 30–40 % и более [6]. В связи с этим на последних международных ревматологических конгрессах в Копенгагене (июнь, 2009) и Филадельфии (октябрь, 2009) уже прямо говорилось о достижении клинической ремиссии как основной цели лечения РА.
Проблемы терапии РА
Первой и поэтому наиболее распространенной группой ГИБП были ингибиторы фактора некроза опухоли α (ФНО-α), к которым относятся инфликсимаб, этанерцепт и адалимумаб. ФНО-α представляет собой регуляторную молекулу, ответственную за продукцию других противовоспалительных цитокинов, экспрессию молекул адгезии эндотелиальными клетками и транспорт лейкоцитов в воспаленный сустав, повышение синтеза металлопротеиназ и активности остеокластов. Таким образом, ФНО является медиатором развития хронического синовита и деструктивного компонента ревматоидного воспаления. РКИ, и особенно результаты известного исследования BeST (Behandel-Strategieёn) [10, 11], убедительно продемонстрировали, что комбинация метотрексата и ингибитора ФНО-α улучшает клинический ответ на лечение, замедляет рентгенологическое прогрессирование, улучшает исход в отношении функции суставов и существенно повышает частоту клинической ремиссии по сравнению с монотерапией метотрексатом.
К сожалению, 10 лет применения ингибиторов ФНО-α выявили ряд проблем, из которых важнейшими являются следующие:
- Недостаточный ответ на лечение у значительной (порядка 30 %) части пациентов [12]. Первичное отсутствие ответа (отсутствие значимого улучшения после начала терапии ингибиторами ФНО-α) встречается редко, однако характерным является развитие вторичной неэффективности, т. е. снижение терапевтического действия при продолжающейся терапии. Существуют особые иммунные механизмы, объясняющие этот феномен [13].
- Вероятность развития либо активации инфекций [14], особенно в мягких тканях и суставах. Наиболее серьезным является риск туберкулезной инфекции [15–17], обусловливающий необходимость специального скрининга до назначения и в процессе лечения ингибиторами ФНО.
- Повышение риска возникновения лимфом и некоторых злокачественных новообразований, в частности кожи [14, 18], хотя этот риск относительно невелик и сильно зависит от отбора пациентов [19].
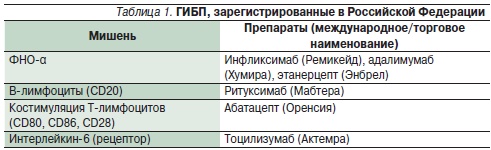
Суммарно, по данным национальных регистров биологических препаратов и других наблюдательных исследований [20–22], первичная или вторичная неэффективность либо непереносимость ингибиторов ФНО заставляла менять схему лечения у 30–50 % больных. Поэтому в последнее время все большее внимание привлекают ГИБП с иными механизмами действия. В настоящее время в России зарегистрировано 6 препаратов этой группы: три ингибитора ФНО и три препарата, имеющих другие мишени для воздействия (табл. 1). Среди ГИБП особенно выделяется ритуксимаб (Мабтера®).
Ритуксимаб – механизмы действия при РА
Ритуксимаб в настоящее время занимает важное место в терапии РА, хотя его применение для лечения этого заболевания зарегистрировано только в 2006 г., а первоначально его применяли в гематологии при неходжкинских лимфомах (1997) [23]. Ритуксимаб относится к группе химерных моноклональных антител, т. е. представляет собой генно-инженерный иммуноглобулин, содержащий как человеческий, так и мышиный иммуноглобулин. Препарат специфически соединяется с молекулой CD20 – трансмембранным белком, находящимся на поверхности В-лимфоцитов. CD20 выполняет определенные функции как регулятор ранних стадий клеточного цикла и, вероятно, участвует в транспорте ионов кальция [24].
Связываясь с CD20, ритуксимаб оказывает на В-лимфоциты ряд эффектов [23], вызывающих их гибель, среди которых выделяют:
- антителозависимую клеточную цитотоксичность;
- цитотоксичность, связанную с активацией комплемента;
- стимуляцию апоптоза В-клеток.
Таким образом, под воздействием ритуксимаба происходит подавление (деплеция) В-лимфоцитов. Поскольку CD20 отсутствует на стволовых клетках и других предшественниках В-лимфоцитов, а также на плазматических клетках, выраженного угнетения костного мозга и нарушения продукции нормальных антител не происходит [23–25].
В-лимфоциты играют важнейшую роль в патогенезе РА. Они могут выполнять антиген-презентирующие функции и тем самым участвовать в запуске иммунной реакции, регулируют активность Т-лимфоцитов, являются источником ряда цитокинов и предшественниками плазматических клеток, отвечающих за продукцию аутоантител [23, 28]. Поэтому деплеция В-клеток оказывает многогранное терапевтическое воздействие на иммунное воспаление при РА.
После введения ритуксимаба число В-лимфоцитов в периферической крови существенно уменьшается [26]. Это приводит к снижению пролиферации Т-лимфоцитов и синтеза ими цитокинов CD4+; уменьшению образования аутоантиген-специфичных В-клеток памяти, плазматических клеток; подавлению синтеза антител и образования иммунных комплексов; активации Т-регуляторных клеток (CD4+, CD25+) и модуляции активности ряда других иммунокомпетентных клеток [27].
В ревматологии ритуксимаб зарегистрирован для применения при активном РА взрослых в комбинации с метотрексатом при непереносимости или неадекватном ответе на текущие режимы терапии, включающие один или более ингибиторов ФНО-α. В настоящее время стандартным методом лечения РА является применение ритуксимаба курсами внутривенно по 1000 мг дважды (с промежутком в 2 недели). В связи с возможностью инфузионных реакций в качестве премедикации рекомендуется вводить 100 мг метилпреднизолона. Клиническое улучшение обычно наступает через 8–16 недель [26, 29, 30]. В связи с выраженным подавлением В-лимфоцитов и медленным восстановлением их числа после проведения одного курса терапии эффект сохраняется длительно (6 месяцев и более).
Поскольку патологическая активность В-лимфоцитов является универсальным иммунологическим феноменом [31], играющим важную роль при ряде заболеваний, применение ритуксимаба является перспективным методом лечения при таких состояниях, как системная красная волчанка, синдром и болезнь Шегрена, системная склеродермия, идиопатические воспалительные миопатии, системные васкулиты [31–35], хотя официально эти показания пока не зарегистрированы.
Клинический опыт применения ритуксимаба при РА
Наиболее широко изучено применение ритуксимаба у больных РА с резистентностью к предшествующей терапии БПВП и другими ГИБП, преимущественно ингибиторами ФНО-α. В РКИ DANCER (Doseranging Assessment International Clinical Evaluation of Rituximab in RA) [36] были включены 465 больных РА с недостаточным ответом на применявшуюся ранее терапию БПВП, из них 29 % также получали ГИБП (большинство – ингибиторы ФНО-α). Больные были распределены в три группы, две из которых получали метотрексат и ритуксимаб в дозе 500 либо 1000 мг на введение, а третья – метотрексат и плацебо.
Ответ на лечение оценивали по критериям Американской коллегии ревматологов (АКР), которые включают улучшение на 20 % (АКР20), 50 % (АКР50) и 70 % (АКР70) по числу припухших и болезненных суставов, а также по трем из следующих пяти критериев:
- общая оценка своего состояния больным;
- общая оценка состояния больного врачом;
- оценка боли;
- оценка функциональной способности больного по специальной шкале HAQ;
- уровень СОЭ или С-реактивного белка.
Ответ также оценивали по критериям Европейской лиги против ревматизма (EULAR – European League against Rheumatism), основанным на динамике индекса активности РА по шкале DAS28 (Disease activity scale). В двух группах больных, получавших ритуксимаб, ответ через 6 месяцев лечения по критериям АКР50 был вдвое выше (33 и 34 % против 13 %), а по критериям АКР70 в несколько раз выше (13 и 20 % против 5 %) по сравнению с группой, получавшей метотрексат + плацебо. Ответ по критериям EULAR при применении ритуксимаба также достигался в 2 раза чаще (73 и 67 % против 37 %).
В исследовании REFLEX (Randomised Evaluation oF Long-term Efficacy of rituXimab in RA) участвовали 512 больных РА, рефрактерных к ингибиторам ФНО-α [37]. Ритуксимаб продемонстрировал существенное преимущество над плацебо: через 6 месяцев наблюдения ответ на АКР50 составил 27 и 5 % соответственно, на АКР70 – 12 против 1 %. В продленной открытой фазе исследований [38] 1039 больным РА (из них 59 % ранее получали блокаторы ФНО-α, 41 % – нет) проводили повторные курсы лечения ритуксимабом по мере необходимости в течение нескольких лет. Было показано повышение числа пациентов с хорошим ответом на фоне длительной терапии ритуксимабом, при этом частота инфузионных реакций снижалась.
Помимо РКИ высокая эффективность ритуксимаба в клинической практике была показана в 28 наблюдательных исследованиях [39].
В рамках РКИ для ритуксимаба была доказана способность вызывать торможение эрозивного процесса в суставах. В исследовании REFLEX, в котором для количественной оценки рентгенологического прогрессирования использовался адаптированный модифицированный метод Шарпа–Генанта, у пациентов, получавших комбинацию ритуксимаба и метотрексата, по сравнению с группой метотрексата в сочетании с плацебо за 56 недель счет эрозий составил 0,50 и 1,32 балла; оценка сужения суставной щели – 0,41 и 0,99; общий счет – 1,0 и 2,31 балла соответственно.
В нашей стране ритуксимаб зарегистрирован с 2006 г. Данные собственных наблюдений, в т. ч. в рамках Российского регистра ритуксимаба [26, 40], подтвердили высокую эффективность препарата, включая значительное улучшение показателей качества жизни, у разных групп больных РА [41]. Разработан алгоритм применения ритуксимаба при РА [42].
Ритуксимаб как препарат первого ряда биологической терапии ревматоидного артрита
В последнее время особое внимание уделяется вопросу о возможности и целесообразности использования ритуксимаба в качестве препарата 1-го ряда биологической терапии РА. McGonagle и соавт. [43] сообщили об успешном использовании ритуксимаба в клинической практике у 39 больных РА в качестве первого биологического препарата. Отбирали пациентов с недостаточной эффективностью терапии БПВП и невозможностью по тем или иным причинам использовать ингибиторы ФНО-α. К 12-му месяцу наблюдения ответ на лечение ритуксимабом отмечен у 76,7 % больных, что позволило авторам сделать вывод о хорошем эффекте кратковременного применения этого препарата в качестве первого средства биологической терапии.
В исследовании SERENE (Study Evaluating Rituximab’s Efficacy in methotrexate iNadequate rEsponders) лечение ритуксимабом в дозах 500 или1000 мг либо плацебо назначали 509 пациентам, неадекватно отвечающим на метотрексат и никогда не получавшим ГИБП [44]. Результаты показали (рис. 1), что комбинация ритуксимаба и метотрексата у этих пациентов достоверно эффективнее метотрексата и плацебо по параметрам АКР20, АКР50, частоте и качеству ответа на терапию, а также частоте развития клинической ремиссии по критериям EULAR к 24-й неделе наблюдения.

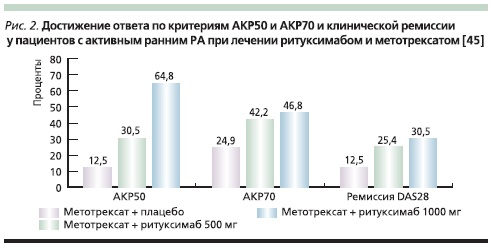
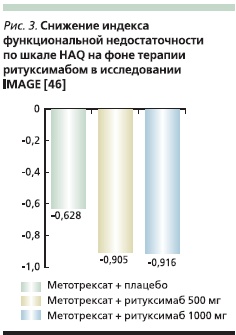
Ритуксимаб назначили 755 больным активным ранним РА в РКИ IMAGE [45, 46]. Исследование показало преимущество комбинации ритуксимаба и метотрексата над монотерапией метотрексатом на ранней стадии болезни в отношении ответа на терапию и частоты развития клинической ремиссии (рис. 2), а также улучшения функциональных способностей пациентов (рис. 3).
По данным наблюдения за больными РА на фоне терапии ритуксимабом в рамках Российского регистра ARBITER [26, 40, 47], применение ритуксимаба в качестве первого ГИБП высокоэффективно у больных РА с разной длительностью заболевания. Таким образом, современные исследования обосновывают применение ритуксимаба в качестве препарата первой линии биологической терапии РА.
Сравнительный анализ результатов применения ритуксимаба и других ГИБП
В 2009 г. опубликован обзор Кокрановского сотрудничества (www. cochrane.org), посвященный сравнению разных биологических препаратов для лечения РА [48, 49]. Сравнение характеристик зарегистрированных в России ГИБП – ингибиторов ФНО, абатацепта и ритуксимаба – в качестве препаратов патогенетической терапии РА представлено в табл. 2.
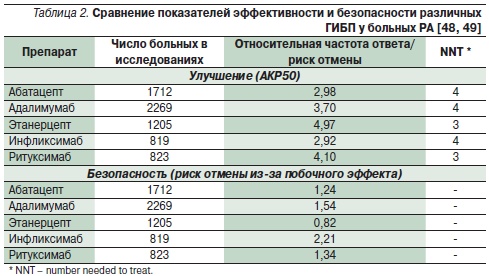
В качестве показателя эффективности авторы мета-анализа проведенных исследований использовали относительную частоту достижения ответа на лечение по критериям АКР50 по сравнению с таковой в контрольных группах. Кроме того, был проведен NNT (number needed to treat) анализ, который показывает, сколько больных должны получать препарат, чтобы у одного из них был достигнут избранный уровень ответа на лечение. Можно видеть, что по эффективности ритуксимаб находится на одном уровне с этанерцептом, превосходя адалимумаб, абатацепт и инфликсимаб.
Множество ранее проведенных исследований продемонстрировало хорошую переносимость терапии ритуксимабом [23, 25, 28, 47]. Несмотря на имеющийся определенный риск инфузионных реакций (который существенно снижается за счет применения премедикации) и наличие инфекций, в целом частота этих нежелательных реакций невелика. Такое серьезное осложнение, как активация или развитие туберкулезной инфекции, характерное для ингибиторов ФНО-α, полностью отсутствует при применении ритуксимаба. Кокрановский метаанализ показывает (табл. 2), что риск отмены ритуксимаба из-за побочного эффекта достаточно мал (повышение в 1,34 раза) и соответствует картине, наблюдаемой при других методах биологической терапии.
Другой мета-анализ, проведенный французскими авторами [50], включает 12 РКИ препаратов, не являющихся ингибиторами ФНО (ритуксимаб, абатацепт и анакинра), и анализирует данные, касающиеся возникновения серьезных инфекционных осложнений. В целом 745 пациентов получали ритуксимаб, 1960 – абатацепт, 2062 – анакинру и 2112 – плацебо. Не было выявлено статистически достоверного повышения частоты серьезных инфекций на фоне использования ритуксимаба и абатацепта. Суммарные данные по сопоставлению ритуксимаба и наиболее распространенной группы ГИБП – ингибиторов ФНО-α – представлены в табл. 3.
Таблица 3. Сравнительная характеристика ритуксимаба и ингибиторов ФНО-α при лечении РА.
Ритуксимаб характеризуется особым методом применения: препарат назначают в виде достаточно редких (не чаще одного раза в 6 месяцев) повторных курсов, состоящих из 2 последовательных внутривенных вливаний. Такая методика лечения может быть удобной пациентам, которые не хотят быть привязанными к клинике постоянными процедурами, как это наблюдается при лечении другими препаратами. Для ритуксимаба в целом не характерно развитие вторичной неэффективности; наоборот, показана возможность улучшения результатов при повторных введениях препарата. В большинстве случаев ритуксимаб позволяет добиться хорошего ответа на лечение у пациентов с неэффективностью или непереносимостью ингибиторов ФНО. Риск развития постинфузионных/постинъекционных осложнений, а также инфекций существует для всех групп ГИБП, однако для ритуксимаба в целом характерно отсутствие риска туберкулезной инфекции, что существенно расширяет целевую аудиторию препарата.
Таким образом, если год назад на основании данных литературы можно было говорить об отсутствии достаточных оснований, для того чтобы считать ритуксимаб препаратом первого выбора для больных активным РА [50, 51], то сейчас накоплены сведения, которые позволяют рассматривать ритуксимаб именно как препарат, заслуживающий широкого практического применения, активно конкурирующий с ингибиторами ФНО-α.
Информация об авторе:
Каратеев Дмитрий Евгеньевич – доктор медицинских наук, заведующий отделом
ранних артритов НИИ ревматологии РАМН, Москва.
Тел. 8 (499) 614-71-37


