Введение
Современные тенденции здравоохранения и концепция персонализированной медицины диктуют необходимость индивидуализированных подходов к диагностике и лечению различных заболеваний с учетом разнообразных факторов, оказывающих влияние на их течение.
Наличие коморбидной патологии у больных ишемической болезнью сердца (ИБС) является одним из наиболее значимых факторов течения заболевания, в ряде случаев приводящим к ухудшению прогноза основного заболевания [1]. Так, наличие сахарного диабета (СД) у больных ИБС сопровождается повышением летальности в 2 раза, а при хронической обструктивной болезни легких (ХОБЛ) у больных ИБС летальность может увеличиваться в 3 раза [2, 3]. Вынужденная полипрагмазия вследствие коморбидности, число лекарственных назначений при которой может достигать 10 и более, практически в 100% случаев приводит к появлению неблагоприятных побочных эффектов, что сопровождается повышением летальности [1, 4]. По данным зарубежных исследований, при наличии 6 сопутствующих заболеваний фармакотерапия включает 5 и более лекарственных препаратов у 45% пациентов, что существенно повышает риск межлекарственных взаимодействий и неблагоприятных побочных эффектов [5].
Больные ИБС, подвергающиеся кардиохирургическим операциям, имеют ряд сопутствующих заболеваний: по данным отечественных регистров, более 80% страдают сопутствующей артериальной гипертензией (АГ), более 12% - ХОБЛ, более 10% имеют ряд эрозивноязвенных поражений желудочно-кишечного тракта, более 17% страдают СД 2 типа [6]. Известно, что наличие коморбидности помимо влияния на прогноз ИБС также может осложнять течение послеоперационного периода после кардиохирургических операций. Цирроз печени ассоциирован с более низкой 10-летней выживаемостью больных после кардиохирургических операций, а риск летальности в послеоперационном периоде у больных ожирением возрастает в 1,57 раза, при этом стоимость лечения таких пациентов в условиях кардиохирургического отделения на 17,2% выше, чем пациентов с индексом массы тела в пределах нормы [7, 8]. Кроме того, известно, что частота и тяжесть сопутствующих заболеваний может зависеть от гендерных факторов, что также необходимо учитывать при тактике ведения коморбидного пациента [9].
Выполнение кардиохирургических операций путем срединной стернотомии сопровождается наличием боли в области послеоперационной раны, которая сохраняется в течение полугода у 37% пациентов и у 17% спустя 2 года с момента операции, что может существенно затруднять период реабилитации и активизацию пациента [10].
При этом коморбидность также может оказывать влияние на интенсивность болевого синдрома. Так, наличие заболеваний печени, сердечно-сосудистых заболеваний связано с более высокой интенсивностью болевого синдрома по визуально-аналоговой шкале у пациентов с остеоартрозом, а по другим данным, более чем у половины женщин, страдающих болью в спине, отмечается наличие двух и более сопутствующих заболеваний, при этом риск наличия боли в спине напрямую зависит от числа сопутствующих заболеваний [11, 12].
Цель данного исследования: оценка эффективности и переносимости кетопрофена у пациентов с ИБС в послеоперационном периоде после кардиохирургических вмешательств в зависимости от коморбидного статуса.
Методы
Исследование выполнялось на базе кардиохирургического отделения Университетской клинической больницы № 1 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава РФ (Сеченовский Университет). Протокол исследования был рассмотрен и одобрен локальным этическим комитетом (протокола № 17-19 от 11.12.2019). Критерии включения: мужчины и женщины старше 18 лет, установленный диагноз ИБС, послеоперационный период после кардиохирургических операций (с применением стернотомного доступа: аорто/маммарокоронарное шунтирование, протезирование клапанов, комбинированные операции). Критерии невключения: декомпенсированная хроническая сердечная недостаточность, язвенная болезнь желудка в стадии обострения, выраженные нарушения функции почек (скорость клубочковой фильтрации менее 30 мл/мин), беременность, период лактации, постоянный прием анальгетиков, транквилизаторов и других психотропных препаратов по поводу сопутствующих заболеваний (для исключения дополнительного влияния лекарственных препаратов, обладающих анальгетическим эффектом, на интенсивность болевого синдрома).
В исследование были включены 90 больных ИБС, отвечавших критериям включения/невключения: 76,7% мужчин и 23,3% женщин в возрасте от 37 до 87 лет (средний возраст - 63±7 лет).
Формы ИБС у включенных в исследование больных представлены в табл. 1.

Кардиохирургические операции выполнялись по следующим показаниям: клинически значимые стенозы коронарного русла, клапанная болезнь сердца (стеноз и/или недостаточность аортального, митрального, трикуспидального клапанов), аневризма аорты.
Из кардиохирургических вмешательств выполнены: аорто- и маммарокоронарное шунтирование у 64 (71,1%) пациентов, протезирование клапанов у 12 (13,3%), протезирование аорты у 2 (2,3%), комбинированные операции у 12 (13,3%) пациентов.
Послеоперационная анальгезия у пациентов кардиохирургического профиля проводилась в течение 5 дней с применением кетопрофена 100 мг внутримышечно 2 раза в сутки в соответствии с клиническими рекомендациями по послеоперационному обезболиванию после кардиохирургических операций [13].
Оценка эффективности послеоперационного обезболивания кетопрофеном по интенсивности болевого синдрома проводилась ежедневно с помощью цифровой рейтинговой шкалы (ЦРШ) в баллах от 0 до 10 в течение 5 суток послеоперационного периода [13].
Оценка переносимости послеоперационного обезболивания кетопрофеном проводилась в соответствии с клиническими рекомендациями по рациональному применению нестероидных противовоспалительных средств (НПВС) в клинической практике на основе регистрации частоты неблагоприятных побочных эффектов [14].
Эпизоды острого почечного повреждения (ОПП) в послеоперационном периоде регистрировались в соответствии с международными критериями при увеличении уровня сывороточного креатинина в 1,5 раза от исходного в течение периода наблюдения или увеличении на 0,3 мг/дл за 48 часов [15]. Гепатотоксические реакции регистрировались при элевации уровня печеночных трансаминаз свыше 2 верхних границ нормы [16]. Признаки НПВС-ассоциированной диспепсии определялись при выявлении более 15 баллов по данным русскоязычной версии опросника GSRS (Gastrointestinal Symptom Rating Scale) [17].
Для количественной оценки коморбидного статуса применялся индекс Чарльсон в виде суммы баллов с учетом тяжести, числа сопутствовавших заболеваний и возраста пациента [18].
Анализ сопутствовавшей фармакотерапии проводился в виде количественной оценки одновременно принимаемых лекарственных препаратов в периоперационном периоде у больных ИБС после кардиохирургических вмешательств, а также с применением оценки числа одновременно принимаемых лекарственных препаратов в зависимости от степени коморбидности, согласно индексу Чарльсон.
Статистическую обработку проводили с применением программного обеспечения StatSoft Statistica 12. Данные представлены как среднее значение±стандартное отклонение (M±SD) и медиана с интерквартильным размахом 25-75 квартиль (Me [Q1; Q3]). Критерии Шапиро-Уилка и Колмогорова-Смирнова применяли для оценки нормальности распределения. Критерий Манна-Уитни для двух независимых групп применяли ввиду ненормальности распределения количественных данных. Точный критерий Фишера (в случае значений ожидаемого явления менее 5) и х2-критерий Пирсона применяли для сравнения качественных частотных показателей. Статистическая значимость установлена на уровне p<0,05.
Результаты
Анализ сопутствовавшей патологии у больных ИБС после кардиохирургических вмешательств, которым были проведены кардиохирургические операции, показал, что у 36 (38,8%) больных имела место хроническая сердечная недостаточность, у 32 (35,5%) АГ, у 25 (27,8%) ожирение 1-2-й ст., у 23 (25,5%) СД 2 типа, у 16 (14,4%) хронический гастрит и/ или язвенная болезнь желудка, у 13 (14,4%) хроническая болезнь почек, у 13 (14,4%) фибрилляция предсердий, у 11 (12,2%) хронический бронхит и/или ХОБЛ, у 2 (4,44%) доброкачественная гиперплазия предстательной железы, у 2 (4,44%) желчнокаменная болезнь, у 2 (4,44%) мочекаменная болезнь, у 1 (1,11%) хронический гломерулонефрит, у 1 (1,11%) рак мочевого пузыря, у 1 (1,11%) рак предстательной железы.
Анализ гендерных различий сопутствовавшей патологии не выявил достоверных различий частоты встречаемости сопутствовавшей патологии у мужчин и женщин (р>0,05) (табл. 2).
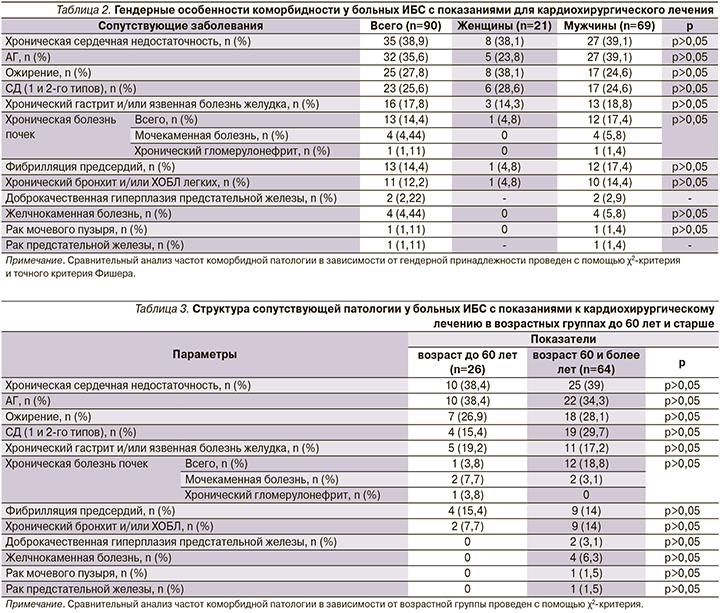
Также был проведен анализ структуры коморбидности и частоты встречаемости сопутствовавших заболеваний у мужчин и женщин в возрастных группах до 60 лет и старше. Достоверных различий выявлено не было (табл. 3).
В соответствии с выявленными значениями индекса коморбидности Чарлсона выделены следующие подгруппы: низкой коморбидности (0-1 балл), умеренной коморбидности (2-3 балла), высокой коморбидности (4 и более баллов).
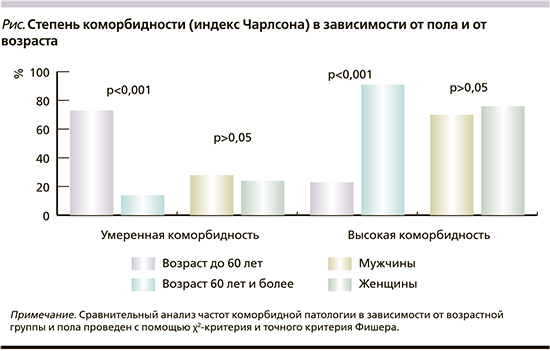
Все включенные в исследование пациенты имели высокую или умеренную коморбидность, кроме одного пациента с низкой коморбидностью, исключенного из данного анализа. Высокая коморбидность отмечена у 65 (72,3%) больных, умеренная у 24 (26,7%). Индекс коморбидности Чарлсона в исследуемой группе колебался от 2 до 8 баллов и в среднем составил 4,4±1,4 балла. Достоверных различий степени коморбидности у мужчин и женщин выявлено не было. Анализ возрастных групп по степени коморбидности показал достоверно большую частоту умеренной коморбидности у пациентов в возрасте до 60 лет по сравнению с пациентами старше 60 лет: 19 (73%) и 9 (14%; p<0,001), соответственно. А высокая коморбидность отмечалась достоверно чаще в более старшей возрастной группе: более лет и до 60 лет соответственно 58 (90,6%) и 6 (23%) в группах 60 и (p<0,001) (см. рисунок).
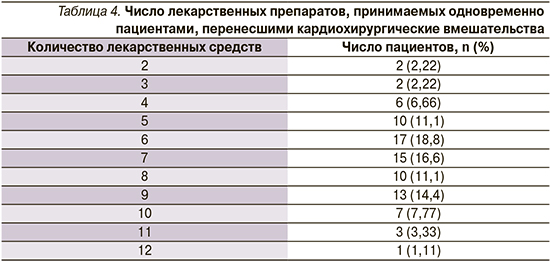
Число одновременно принимаемых лекарственных препаратов пациентами кардиохирургического профиля в периоперационном периоде и их зависимость от степени коморбидности представлены в табл. 4, 5. Среднее число одновременных медикаментозных назначений составило 7 (от 2 до 12) лекарственных препаратов. Среди лекарственных назначений в периоперационном периоде присутствовали следующие группы лекарственных препаратов: ингибиторы ангиотензинпревращающего фермента (30%), вг-адреноблокаторы (76,7%), антиагреганты (51,1%), антиаритмические препараты (7,7%), ингибиторы протонной помпы (71,1%), калийсберегающие диуретики (41,1%), блокаторы рецепторов ангиотензина II (11,1%), пероральные гипогликемические препараты (18,9%), блокаторы кальциевых каналов (36,7%), статины (42,2%).
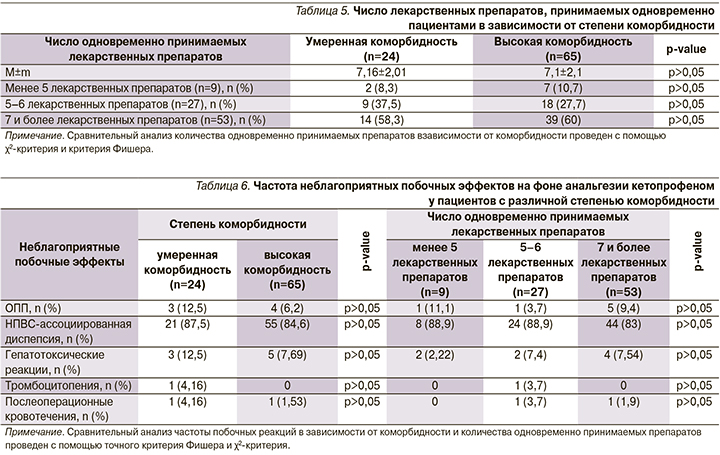
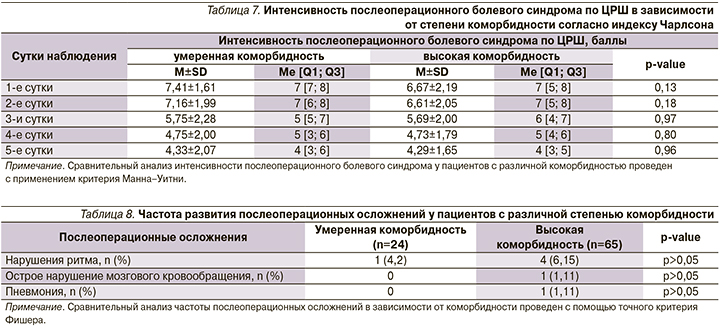
Анализ неблагоприятных побочных эффектов на фоне обезболивания кетопрофеном показал высокую распространенность диспепсии (по данным опросника GSRS) в послеоперационном периоде (85,4%). Также были зафиксированы эпизоды ОПП, гепатотоксических реакций, НПВС-ассоциированной диспепсии, тромбоцитопении и послеоперационных кровотечений. Два зарегистрированных эпизода кровотечения являлись носовыми, самостоятельно купируемыми, не требующими специализированной медицинской помощи (табл. 6). Достоверных различий, выявленных неблагоприятных побочных эффектов на фоне обезболивания кетопрофеном в зависимости от степени коморбидности и числа одновременно принимаемых препаратов, выявлено не было (табл. 6).
Достоверных различий интенсивности болевого синдрома в зависимости от степени коморбидности также выявлено не было (табл. 7).
Обсуждение
Анализ коморбидной патологии продемонстрировал значительную распространенность различных сопутствующих заболеваний у больных ИБС с показаниями к кардиохирургическому лечению. Существенную долю коморбидности составляли заболевания, являвшиеся ведущим звеном метаболического синдрома: ожирение 1-2-й ст. и СД: 27,8 и 25,5%, при этом данные заболевания чаще встречались среди женщин. Однако установленный диагноз АГ чаще встречался среди мужчин, что согласуется с эпидемиологическими данными в российской популяции [19].
Несмотря на отсутствие статистической значимости различий частоты встречаемости сопутствовавших заболеваний между исследованными возрастными группами, наличие хронической болезни почек чаще отмечалось в возрастной группе старше 60 лет, что также сопоставимо с данными российских исследований, по данным которых частота встречаемости этой патологии в этой возрастной группе может достигать 36% [20]. В целом в нашем исследовании выявлено достоверное увеличение степени коморбидности по индексу Чарльсон у лиц старшей возрастной группы, старше 60 лет, что также согласуется с данными других исследователей [21].
Наибольшее число (72,2%) больных получали от 5 до 9 лекарственных препаратов, что может существенно повышать риск межлекарственных взаимодействий и требует мониторинга безопасности периоперационной фармакотерапии. Однако проведенный анализ не выявил взаимосвязи числа одновременно принимаемых препаратов со степенью коморбидности и частотой неблагоприятных побочных эффектов на фоне обезболивания кетопрофеном. Несмотря на более высокую частоту приема 7 и более лекарственных препаратов в группе высокой коморбидности, в исследовании не было выявлено достоверных различий числа принимаемых лекарственных препаратов в зависимости от степени коморбидности (табл. 5), что, вероятно, связано с небольшим объемом выборки в данном исследовании.
На текущий момент данные о взаимосвязи коморбидности и интенсивности болевого синдрома у пациентов различного профиля ограниченны. В исследовании F. Wolfe et al. продемонстрировано, что наличие одного и более сопутствующего заболевания у пациентов ревматологического профиля с фибромиалгией ассоциировано с увеличением индекса распространенной боли в 1,8 раза [22]. А по данным исследования M. Ferguson et al. выявлено, что пациенты с высокой коморбидностью чаще предъявляли жалобы на хронический болевой синдром в зависимости от основного заболевания (отношение рисков [ОР]=1,08, 95% доверительный интервал [ДИ]: 1,07-1,08; p<0,001) [23]. В другом исследовании, O. Melkevik et al., выявлена статистически значимая корреляция между выраженностью симптомов депрессии и числом участков локализации боли у пациентов с различным скелетно-мышечным болевым синдромом (r=0,24; p<0,001) [24]. По данным W. Athar et al., наличие обструктивного ночного апноэ служит фактором риска болевого синдрома умеренной и высокой степеней выраженности (ОР=1,09, 95% ДИ: 1,08-1,11; p<0,001) [25].
В нашем исследовании достоверных различий интенсивности послеоперационного болевого синдрома в зависимости от степени коморбидности по индексу Чарльсон выявлено не было. Вероятно, для выявления достоверных различий интенсивности болевого синдрома требуется проведение дальнейших более объемных исследований для детальной оценки болевого синдрома у пациентов с низкой и высокой коморбидностью.
В нашем исследовании не было выявлено эпизодов тромбозов глубоких вен, а также тромбоэмболии легочной артерии, что согласуется с данными зарубежных систематических обзоров, по данным которых частота фатальных тромбоэмболических событий после кардиохирургических операций не превышает 0,3%, что обусловлено активной тактикой периоперационной антикоагулянтной профилактики [26].
Заключение
Проведенный анализ показал значительную вариабельность коморбидной патологии у больных ИБС с показаниями к кардиохирургическому лечению, отражающую тяжесть ведения пациентов данной категории. Выявлены достоверные различия степени коморбидности в зависимости от возрастной группы: умеренная коморбидность достоверно чаще встречалась у пациентов до 60 лет (p<0,001), высокая коморбидность - у больных старше 60 лет (p<0,001). Анализ гендерных различий не выявил статистически значимых различий сопутствовавшей патологии у мужчин и женщин. В исследовании не выявлено различий эффективности и частоты неблагоприятных побочных эффектов кетопрофена у больных ИБС после кардиохирургических вмешательств с различной степенью коморбидности.
Таким образом, наличие множественной коморбидной патологии не оказывает негативного влияния на выраженность послеоперационного болевого синдрома и не снижает эффективности анальгезии кетопрофеном, а также не повышает риска развития неблагоприятных побочных эффектов, что имеет большое значение для клинической практики.
В дальнейших исследованиях представляется актуальным применение более многочисленных выборок исследуемых пациентов, а также использование дополнительных индексов оценки коморбидного статуса.
Финансирование. Исследование выполнено при финансовой поддержке Гранта Президента РФ для научных школ № НШ-2698.2020.7.



