Актуальность проблемы
Сахарный диабет (СД) является неинфекционным заболеванием, принимающим характер эпидемии в современном мире. В связи с развитием технологий и медицины продолжительность жизни людей увеличивается, население Земли неуклонно стареет, что в свою очередь сказывается на численности пациентов с СД 2 типа (СД2), который по праву считается возраст- ассоциированным.
По данным Международной федерации диабета, численность пациентов с СД в мире достигла 463 млн в 2019 г., а к 2045 г. ожидается увеличение на 51% – до 700 млн человек, при этом 1 из 5 пациентов с СД находится в старшей возрастной группе >65 лет (136 млн) [1]. В России распространенность СД, по данным регистра 2020 г., составила 3,23% населения (4,8 млн), при этом более половины всех пациентов с СД старше 65 лет – 2,7 млн [2].
СД поражает множество органов, включая кожу. По данным литературы, кожное осложнение СД встречается у 30–70% пациентов в течение жизни [3]. В основе формирования различных высыпаний на коже лежат разнообразные патоморфологические процессы, происходящие в эпидермисе, дерме, гиподерме, совокупность которых может быть специфичной для того или иного дерматоза.
Актуальным представляется изучение дерматозов у пациентов с СД в пожилом возрасте и эффективных методов воздействия на них. Такие пациенты требуют особого диагностического и лечебного подхода. Терапия пожилых – сложная задача для врачей многих специальностей из-за сопутствующих заболеваний, полипрагмазии, особенностей функционального и психосоциального статуса пациентов. Больные старческого возраста нередко одиноки, социально изолированы и беспомощны, часто маломобильны и «не доходят» до узких специалистов (врачей-дерматологов) для определения тактики лечения тех или иных поражений кожи при СД. Поэтому особенности протекания и лечения основных поражений кожи при СД важно знать и уметь диагностировать врачам первичного звена в плане оказания своевременной медицинской помощи.
Основную роль в развитии дерматозов у пожилых при СД отводят глюкозотоксичности, инсулинорезистентости, повышению окислительного стресса и хронического воспаления, как следствие – возникновению сосудистых и трофических изменений [4], что приводит к структурным изменениям в дерме, эпидермисе, фолликулах и потовых железах. В течение заболевания накапливаются конечные продукты гликирования, ускоряется химическое старение белков ткани кожи (коллагена, кристаллина, эластина и др.), изменяется проницаемость стенок сосудов и микроциркуляция [5]. Сочетание диабетической нейропатии, микро- и макроангиопатий, нарушений местного и общего иммунитета приводит к появлению различных видов сыпи, пигментных пятен, изъязвлений, а также к гнойно-септическим осложнениям. Как правило, поражения кожи при СД характеризуются длительным хроническим течением, наличием обострений и трудностями медикаментозного лечения.
У лиц пожилого и старческого возраста с СД также существуют дополнительные факторы, способствующие росту инсулинорезистентости: употребление в пищу более калорийной пищи, полуфабрикатов, проблемы с пережевыванием, снижение физической активности, мышечной массы и ее силы, развитие саркопении, прием лекарственных препаратов, негативно влияющих на метаболизм. При этом течение СД у лиц пожилого возраста часто осложняется гериатрическим синдромом, включающим совокупность когнитивных нарушений, старческой слабости, депрессии, функциональных расстройств и падений, полиморбидности [6].
В литературе описано более 30 видов дерматозов при СД [7], которые ряд авторов условно разделяют на 3 и более групп. В основе классификаций лежат клиническая характеристика и некоторые аспекты патогенеза кожных изменений, среди которых выделяют:
- Первичные дерматозы, возникшие вследствие развития диабетических ангиопатий и метаболических нарушений (черный акантоз, липоидный некробиоз, диабетические дерматопатии, диабетический ксантоматоз, диабетические пузыри и др.);
- Вторичные – при присоединении бактериальной или грибковой инфекции;
- Дерматозы, возникающие на фоне лечения медикаментозными препаратами (экзематозные, аллергические, побочные реакции, в т.ч. крапивница, токсикодермия, постинъекционные липодистрофии) [8].
Другие авторы условно разбивают большой пул дерматозов первой группы на дерматозы, связанные с СД и инсулинорезистентностью, и отдельно выносят дерматозы, ассоциированные с хроническими осложнениями СД (микро-, макроангиопатиями, нейропатией) [9, 10].
Поражения кожи при СД
Черный акантоз (ЧА – acanthosis nigricans) – это состояние кожи, при котором один или несколько участков становятся темнее и толще, появляется гиперпигментация с гиперкератозом (рис. 1). Это классическое дерматологическое проявление СД, внешне похожее на «грязную» кожу. Он проявляется в виде множественных, плохо разграниченных бляшек с гиперпигментацией от серого до темно-коричневого цвета и утолщенной бархатистой или бородавчатой текстурой. ЧА встречается у 1% представителей европеоидной расы одинаково часто у мужчин и женщин всех возрастов, при этом значительно чаще встречается у лиц с более темным цветом кожи (широко представлен у афро- и латиноамериканцев) [11].
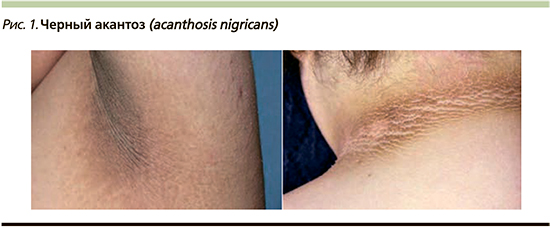
Первый зарегистрированный случай ЧА был описан P.G. Unna и S. Pollitzer в 1889 г. в Германии. К 1909 г. были описаны приблизительно 50 пациентов с таким диагнозом. В 1976 г. C.R. Kahn et al. опубликовали свое знаменитое исследование, в котором впервые была выявлена связь резистентности к инсулину и данным состоянием кожи [12].
ЧА не самостоятельное заболевание, а симптом эндокринопатий с развитием инсулинорезистентности: акромегалии, синдрома Кушинга, ожирения, синдрома поликистозных яичников и дисфункции щитовидной железы. Семейное ожирение, определенные злокачественные опухоли, в основном аденокарциномы органов желудочно-кишечного тракта и другие карциномы, могут сами по себе вырабатывать инсулиноподобные факторы роста и таким образом вызывать развитие ЧА [13].
Патогенез ЧА до конца не изучен. Основная теория заключается в том, что в условиях инсулинорезистентности стимулируется пролиферация эпидермальных кератиноцитов и дермальных фибробластов инсулиноподобным фактором роста-1 (ИФР-1) [13].
Классически ЧА симметрично расположен на участках кожи, которые подвергаются регулярному трению в естественных складках, таких как подмышечные впадины, локти, складки под грудью, а также на задней части шеи, около пупка и в области паха. Пораженные участки обычно не беспокоят пациентов, однако может возникать зуд и неприятный запах. Особенность данного дерматоза у пациентов пожилого возраста заключается в диагностике нарушения углеводного обмена при появлении ЧА, что важно знать врачам первичного звена.
При микроскопии кожи выявляется утолщение шиповатого слоя в результате повышения скорости пролиферации кератиноцитов базального и супрабазальных слоев эпидермиса с повышением в них энергетического обмена и митотической активности, формируется гиперкератоз и эпидермальный папилломатоз с акантозом. Изменения пигментации кожи являются следствием гиперкератоза и не связаны с синтезом меланина, как правило, появляются медленно – в течение нескольких месяцев или лет.
При лечении ЧА основная цель состоит в снижении инсулинорезистентности, компенсации углеводного обмена при СД, изменении образа жизни, привычек питания, повышении физической активности и снижении массы тела. На этом фоне изменения кожи могут регрессировать. Первичная дерматологическая терапия обычно неэффективна, особенно у пациентов с генерализованным поражением. Однако у пациентов с утолщенными или мацерированными участками кожи для облегчения симптомов можно использовать пероральные ретиноиды или местные кератолитики, такие как лактат аммония, ретиноевая или салициловая кислоты, применение лечения лазером [14].
Липоидный некробиоз (ЛН) – хронический дерматоз, в основе которого лежат метаболические и микроциркуляторные нарушения, характеризующиеся дегенерацией коллагена (рис. 2) [15]. Он характеризуется отложением липоидов в участках дермы, где имеется дегенерация или некробиоз коллагена. Это не осложнение СД как таковое, но состояние, прочно с ним ассоциированное.
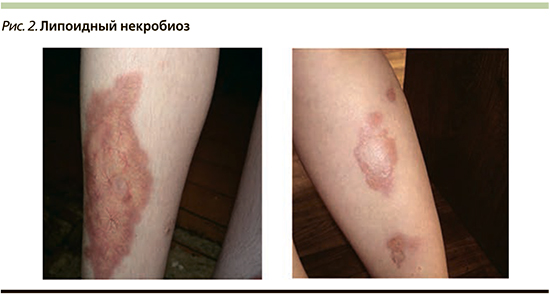
Заболевание было описано М. Оппенгеймом в 1929 г. и названо «dermatitis atrophicans lipoidica diabetica». При дальнейшем изучении стало очевидно, что данный дерматоз может развиваться и у пациентов без СД. Распространенность ЛН среди взрослых пациентов с СД составляет от 0,1 до 3%, по разным данным, у женщин встречается в 3 раза чаще, чем у мужчин, дебют наблюдается в возрасте от 20 до 60 лет, при этом может развиваться как у детей, так и у лиц старшего возраста.
Этиология ЛН недостаточно изучена, патогенез многофакторный. На данный момент основной причиной признается нарушение экспрессии транспортера глюкозы ГЛЮТ-1 в фибробластах [16]. Это приводит к дегенерации коллагена, потере чувствительности клеток к инсулину, структурным изменениям дермы. Без травмирования или изъязвления ЛН не вызывает никаких субъективных ощущений у пациентов.
ЛН характеризуется ограниченными очагами некробиоза соединительной ткани, дегенерацией коллагена и эластина, гранулематозным воспалением нижних слоев дермы, утолщением стенок мелких сосудов кожи, что приводит к тканевой гипоксии. Подобная трансформация стенок сосудов напоминает такие же изменения при других диабетических микроангиопатиях.
Основные элементы при ЛН представлены в виде пятен, бляшек 2–10 см в диаметре красно-коричневого цвета, возвышающихся над поверхностью здоровой кожи, склонных к росту по периферии и слиянию друг с другом. Типичные очаги локализуются на передней поверхности голеней, имеют четкие границы, при этом поражение чаще билатеральное и симметричное, но очаги могут быть и на любых других участках тела. На поверхности может наблюдаться легкое шелушение, в основании при пальпации определяется небольшая инфильтрация. Очаги ЛН при травматическом повреждении могут изъязвляться. После эпителизации язв кожа приобретает бугристый вид с признаками рубцовой атрофии.
Диагноз ЛН базируется на результатах биопсии, а также клинического, биохимического и гистологического обследования пациента. Все более широкое распространение в дерматологии в последние годы получает метод ультразвукового сканирования кожи.
Среди всех дерматозов, ассоциированных с СД, именно ЛН при наличии хронических раневых дефектов чаще всего вызывает трудности у врачей различных специальностей (эндокринологов, хирургов, дерматологов) в дифференциальной диагностике и выборе терапевтической тактики [15]. Наиболее сложна дифференциальная диагностика ЛН и диссеминированной кольцевидной гранулемы у лиц старше 50 лет.
На сегодняшний день не существует методов лечения ЛН, эффективность которых была бы доказана. Направления терапии включают коррекцию нарушений углеводного обмена, реологических свойств крови, нормализацию показателей микроциркуляции, противовоспалительную терапию. Для симптоматического лечения активных поражений ЛН, как правило, местно применяются препараты глюкокортикоидов в виде мазей. В литературе описано успешное применение циклоспорина, инфликсимаба, пентоксифиллина, противомалярийных средств (например, гидроксихлорохина), дипиридамола и низкодозированного аспирина [17]. При язвенных поражениях важен надлежащий уход за раной, это часто включает местные антибиотики, защиту уязвимых участков кожи, смягчающие средства и компрессионные повязки. В тяжелых случаях (например, при изъязвлении, инфицировании) применяется хирургическое лечение. Некоторые язвенные поражения можно лечить с помощью пересадки кожи.
Диабетическая дермопатия (ДД) проявляется множественными гиперпигментными пятнами округлой формы на разгибательной поверхности нижних конечностей размером 0,5–2 см (рис. 3). Это наиболее часто встречающееся кожное заболевание при СД. Данный дерматоз еще называют «пятнистая голень». Он впервые был описан и предложен в качестве маркера СД в 1964 г. [18].
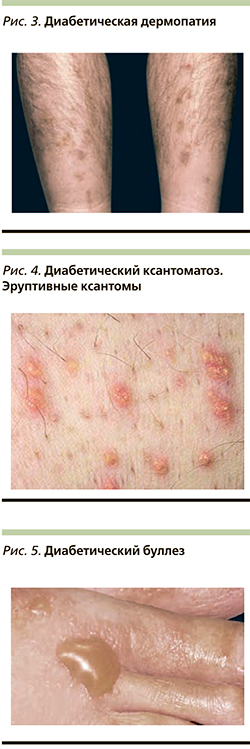
ДД начинается с папулезных высыпаний. Далее формируются множественные округлые атрофические красновато-коричневые пятна на передней поверхности голеней в местах небольших поверхностных травм, пятна могут шелушиться [19]. ДД чаще встречается у мужчин и лиц старше 50 лет. Элементы имеют бессимптомное течение и исчезают через 1–2 года, оставляя после себя небольшую атрофию или гипопигментацию.
ДД – это клинический диагноз, который не требует биопсии кожи. Гистологически ДД довольно неспеци-фична, характеризуется лимфоцитарными инфильтратами, окружающими сосудистую сеть, переполненными кровеносными сосудами в сосочковом слое дермы и дисперсными отложениями гемосидерина. Существует прямая корреляционная связь между выраженностью ДД и тяжестью микроангиопатий, таких как диабетические ретинопатия и нефропатия. Также была выявлена связь с сердечно-сосудистыми заболеваниями.
Особенностью данного дерматоза у пожилых является то, что при проявлении характерных пятен на голени лечащий врач должен рекомендовать внеочередное офтальмологическое обследование пациента, чтобы не пропустить прогрессирование диабетической ретинопатии. А в динамике контролировать статус диабетической нефропатии, уровень креатинина сыворотки крови с расчетом скорости клубочковой фильтрации и альбуминурию.
Лечения обычно не требуется из-за бессимптомного и саморазрешающегося характера высыпаний. В связи с тем, что ДД часто возникает в контексте микрососудистых осложнений СД и длительной персистенции нейропатии, пациенты нуждаются в обследовании и более тщательном наблюдении за этими осложнениями.
Эруптивные ксантомы — это клиническое проявление гипертриглицеридемии, обычно связанное с уровнем триглицеридов в сыворотке выше 2,0 мг/дл [20]. В связи с тем, что при СД2 у большинства пациентов (75% и более), имеется нарушение липидного обмена [21], развитие данного дерматоза распространено среди пожилых пациентов этой когорты, по некоторым данным, до 2% пациентов с СД имеют характерные поражения кожи, которые иногда служат первым признаком СД. Аналогичные высыпания также характерны для заболеваний, ассоциированных с гиперлипидемиями, такими как желчнокаменная болезнь, билиарный цирроз, новообразования печени, хроническая почечная недостаточность, алкоголизм, гипотиреоз.
У пациентов с СД ксантоматоз чаще представлен множественной узелковой формой (эруптивные ксантомы), мелкими красновато-желтыми папулами размером 1–4 мм с четкими границами (рис. 4). Преимущественная локализация – кожа сгибательных и разгибательных поверхностей конечностей, груди, лица, шеи. Гистологически в дерме обнаруживается скопление ксантомных (пенистых) клеток, макрофагов, лимфоцитов и нейтрофилов.
В дальнейшем фиброзная ткань замещает пенистые клетки. Ксантоматоз обычно протекает бессимптомно, но может быть зудящим или болезненным.
Лечение дерматоза направлено на коррекцию гиперлипидемии. Клиническая значимость ксантом при СД у пожилых пациентов состоит в том, чтобы побудить врача любой специальности обратить внимание на уровень триглицеридов сыворотки, назначить необходимое лечение.
Диабетический буллез – невоспалительное поражение кожи, субэпидермальный буллезный дерматоз (рис. 5), который проявляется у людей с СД. Впервые пузыри в качестве одного из вариантов поражений кожи при СД наблюдал D. Kramer в 1930 г. [22]. Данный дерматоз преимущественно возникает при длительном течении СД у пожилых людей на фоне других диабетических осложнений (нейропатии, нефропатии и ретинопатии) [23]. Значительно чаще встречается у пациентов мужского пола, начинается в возрасте от 50 до 70 лет.
Характерно быстрое возникновение дерматоза вследствие акантолиза на фоне микроангиопатий, после формирования пузыри увеличиваются в размерах от 0,5 до 5 см и более. Они безболезненны, заживают без рубцевания самопроизвольно через 2–6 недель.
В отсутствие инфицирования специфического лечения не требуется. У пожилых пациентов очень важно защищать пораженные участки кожи от вторичной бактериальной инфекции. Диабетические пузыри следует дифференцировать с группой пузырных дерматозов и потертостями.
Диабетическая склередема – это заболевание соединительной ткани, связанное с СД, впервые описанное A. Buschke в 1900 г. [24]. Склередема развивается на коже в верхней части спины, плеч и шеи (рис. 6), встречается у пациентов с длительным анамнезом СД в сочетании с ожирением. Распространенность при СД составляет 2,5–14% [22]. Данный дерматоз характеризуется диффузными симметричными индуративными изменениями кожи (утолщением), без четких границ поражения. В патогенезе описывают утолщение пучков коллагена и повышение отложения гликозаминогликанов, гистологически выявляют утолщенную ретикулярную дерму с окружающим муцинозным инфильтратом, без отека или склероза.Пожилые пациенты с СД могут испытывать снижение чувствительности в области пораженных участков кожи, при прогрессировании заболевания появляются затруднения движений верхних конечностей и шеи.
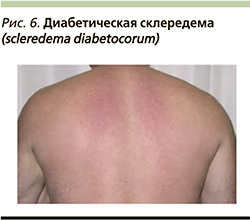
Описано множество терапевтических вариантов лечения склередемы с разной эффективностью. Некоторые из этих методов лечения включают фототерапию, иммунодепрессанты, глюкокортикостероиды, внутривенное введение иммуноглобулина и электронно-лучевую терапию [25]. Независимо от других методов лечения физиотерапия является одним из основных терапевтических методов для пожилых пациентов со склередемой и ограниченной подвижностью.
Другим проявлением изменений кожи при СД, подобным склеродермии, является ограниченная подвижность суставов из-за диабетического утолщение кожи. Развивается приблизительно у 8–36% пациентов с СД [3]. Гистологически при этом определяются повышение активности фибробластов, утолщение коллагеновых волокон, их дезорганизация и расслоение. Это состояние, несомненно, оказывает влияние на качество жизни, т.к. ограничивает подвижность рук. Целесообразно рекомендовать пациентам необходимость строгого гликемического контроля.
Другие поражения кожи при СД
Очень часто у пожилых пациентов с СД (до 40%) наблюдается бессимптомное изменение цвета кожи или ногтей на желтый цвет. Эти доброкачественные изменения обычно затрагивают ладони, подошвы, лицо или ноготь первого пальца ноги. Патогенез остается спорным, но основное объяснение механизма пожелтения заключается в накоплении конечных продуктов нарушенного метаболизма (каротина, гликозилированных белков) [3]. Следует подчеркнуть, что желтый цвет ногтей при СД необходимо дифференцировать с такими заболеваниями, как онихомикозы, при которых тактика ведения пациентов будет совершенно разной.
Пожилым пациентам важно поддерживать целостности кожи, ее эластичность. Избыточную сухость кожи, обусловленную как возрастными изменениями, так и диабетологическими, необходимо устранять с помощью увлажняющих кремов с высоким содержанием мочевины.
На фоне СД у пожилых пациентов наблюдается высокая частота (до 45%) грибковых инфекций. Развитию и прогрессированию заболевания сопутствуют такие факторы, как нарушение микроциркуляции, гипергликемия, снижение иммунного статуса, сухость кожи, трофические изменения в связи со старением организма в целом. Следует отметить, что 80% регистрируемого кандидоза кожи приходится на пациентов с СД [26]. Пациенты с рецидивами кандидоза должны быть обследованы на наличие у них нарушений углеводного обмена. Очаги кандидоза локализуются преимущественно в складках кожи, межпальцевых промежутках, на слизистых оболочках, гениталиях, часто поражается кожа стоп, выявляются онихомикозы.
Диагноз микоза должен основываться на данных клинического исследования и результатах бактериологического исследования соскоба пораженной кожи.
На фоне СД тяжелее протекают такие дерматологические заболевания, как псориаз, красный плоский лишай, кожные бактериальные инфекции. Стафилококковый фолликулит или кожные абсцессы у пациентов данной когорты подробно описаны и лечатся с помощью антибиотиков и хирургического дренажа абсцессов. Большой пул пожилых пациентов с длительным анамнезом СД страдают от синдрома диабетической стопы с нарушениями целостности кожи. Поздние стадии диабетической нейропатии с полной или частичной потерей чувствительности препятствует распознаванию повреждения.
Заключение
Численность пожилых пациентов с СД непреклонно увеличивается вследствие старения населения. Увеличивается и распространенность кожных заболеваний у пациентов данной когорты, т.к. метаболические нарушения служат пусковым механизмом развития многих дерматозов. С учетом разнообразие кожной патологии при СД важно отличать заболевания, прямо связанные с СД, от тех, которые могут встречаться и при другой патологии.
Поражения кожи при СД у людей старшей возрастной группы способны вызывать определенные трудности в диагностике и выборе терапевтической тактики. Основная задача лечения поражений кожи при СД в старости – это комплексная оценка состояния пациента, нутритивного статуса, компенсация углеводного обмена, коррекция сопутствующих заболеваний. Положительные результаты у пожилых людей обеспечивают командный подход не только медицинского персонала, но также членов семьи и общества. Необходимо объединение усилий для достижения цели лечения команды врачей различных специальностей (терапевта, эндокринолога, дерматолога, геронтолога, хирурга, невропатолога и др.).
Вклад авторов. Все авторы внесли равнозначный вклад в написание текста статьи.



