Возможности врачей-дерматологов по неинвазивной диагностике воспалительных и опухолевых заболеваний кожи существенно увеличились за счет внедрения таких методик, как дерматоскопия (эпилюминисцентная микроскопия), оптическая когерентная томография, ультразвуковое сканирование и конфокальная лазерная сканирующая микроскопия [1, 2]. Наиболее простым и доступным для практикующего специалиста является метод дерматоскопии, позволяющий оценивать изменения кожи при 10-кратном увеличении. Ценность и практическое значение дерматоскопии не только в диагностике опухолей кожи, но и в клинической дерматологии неоднократно подчеркивались профессором Ю.В. Сергеевым [3, 4]. В первую очередь осмотр пораженного участка кожи с увеличением позволяет определить структуру эпидермиса, сохранность придатков кожи (особенно волосяных фолликулов) и их функциональную активность. Не менее важным аспектом является возможность правильной оценки морфологических элементов формирующихся высыпаний, позволяющая поставить диагноз на начальном этапе заболевания, когда клиническая картина еще недостаточно выражена. Правильная интерпретация дерматоскопической картины существенно облегчает проведение различных лечебно-диагностических процедур (выявление специфических симптомов, выбор места для забора материала для цитологического или гистологического исследования и др.). Проведение фотодокументирования дерматоскопической картины высыпаний позволяет брать под тщательный контроль динамику лечебного процесса, оценивать регресс высыпаний или их резистентность к лечебным мероприятиям. Дополнительным перспективным направлением диагностики является возможность проведения телеконсультаций полученных изображений, однако этот аспект более активно развивается в отношении новообразований кожи [5]. Широкое применение дерматоскопии при различных неопухолевых дерматозах привело к формированию отдельных направлений в неинвазивной диагностике: инфламматоскопии (осмотр воспалительных заболеваний), трихоскопии (осмотр заболеваний волос и волосистой части головы), энтодерматоскопии (осмотр инфекционных заболеваний кожи) и капилляроскопии (осмотр капиллярного русла околоногтевых валиков при системных заболеваниях соединительной ткани) [6].
Для интерпретации дерматоскопической картины воспалительных заболеваний кожи предложен последовательный алгоритм, включающий:
- морфологическую оценку сосудистых структур;
- оценку распределения сосудистых структур в пределах высыпаний;
- оценку цвета определяемых структур;
- оценку сохранности волосяных фолликулов [7].
Как видно из предложенного алгоритма, основной акцент в дерматоскопической диагностике дерматозов делается на сосудистый компонент высыпаний. К сожалению, большое разнообразие морфологических типов сосудов, а также зависимость их правильного определения от степени давления контактной платы дерматоскопа на высыпания делают дерматоскопию воспалительных дерматозов менее специфичной по сравнению с осмотром новообразований кожи. Также необходимо понимать, что перечисленных характеристик может быть недостаточно для постановки диагноза и должны использоваться дополнительные, возможно более специфичные признаки.
Наиболее подробно описаны дерматоскопические проявления таких папуло-сквамозных дерматозов, как псориаз, экзема, красный плоский лишай и розовый лишай Жибера.
В некоторых случаях проведение клинической дифференциальной диагностики между этими нозологиями является затруднительной задачей и знание дерматоскопических проявлений этих заболеваний может помочь определиться с окончательным диагнозом. Отсутствие типичных дерматоскопических признаков перечисленных заболеваний может послужить поводом для проведения более углубленной диагностики, например гистологического исследования для исключения лимфопролиферативных заболеваний, нередко имеющих схожую с дерматозами клиническую картину.

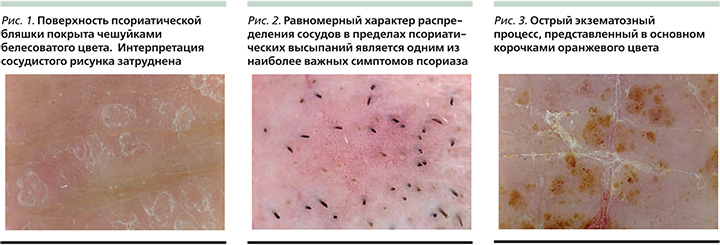
Дерматоскопическая картина псориатических высыпаний состоит из сочетания равномерно распределенных по очагу сосудистых структур и чешуек белесоватого цвета [6–10]. Для оценки сосудистого компонента требуется нанесение иммерсионной жидкости на поверхность высыпаний, учитывая выраженные гиперкератотические наслоения на поверхности папул и бляшек (рис. 1). В большинстве литературных источников преобладающий тип сосудистого рисунка указывается как точечный, однако использование техники с бóльшим увеличением позволяет однозначно трактовать сосудистый рисунок в пределах псориатических высыпаний как сосуды в виде шпильки (рис. 2). Акцент в трактовке сосудистого рисунка смещается в сторону равномерного распределения сосудов в пределах высыпаний, что является одним из наиболее специфичных дерматоскопических признаков этого заболевания. Осмотр высыпаний в процессе выявления симптомов псориатической триады позволяет более четко выявить классические симптомы.
Дерматоскопическая картина экземы характеризуется сочетанием очагово-распределенных в пределах высыпаний сосудов в виде точек и чешуек-корок желтого цвета [6, 7, 11, 12]. Отличительной особенностью экзематозных высыпаний является эволюционный полиморфизм, четко определяемый при дерматоскопии. Острый процесс характеризуется наличием корочек желтоватого цвета, располагающихся на эритематозном фоне, также возможно обнаружение «серозных колодцев» без эритемы в дебюте заболевания (рис. 3, 4). Хронически протекающая экзема проявляется точечными сосудами, имеющими очаговое расположение в пределах высыпаний, также возможно обнаружение трещин и чешуек белого цвета (рис. 5).
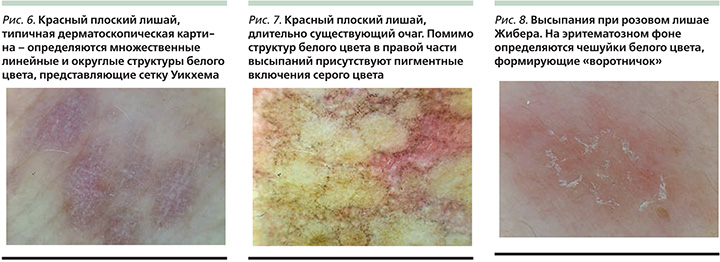
Дерматоскопическая картина красного плоского лишая характеризуется в первую очередь наличием структур белого цвета (сетка Уикхема), которые имеют различные внешние проявления в виде линейных, округлых, сетчатых или кольцевидных структур (рис. 6) [6–8, 11–14]. По периферии сетки Уикхема возможно обнаружение сосудов в виде точек или линейно-извитых сосудов. В более длительно существующих очагах красного плоского лишая менее выражен сосудистый компонент, зато возможно обнаружение пигментных включений серого цвета, аналогичных структурам регресса, определяемым в пигментных новообразованиях кожи [15] (рис. 7).
Дерматоскопические проявления розового лишая Жибера менее информативны и представлены в основном чешуйками белого цвета, формирующими «воротничок» по периферии высыпаний (рис. 8). Дополнительно возможно обнаружение единичных точечных сосудов [6–8, 11].
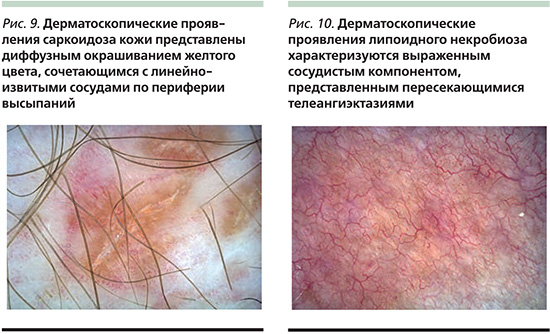
Достаточно редким для дерматоскопии желтым цветом проявляются такие гранулематозные заболевания кожи, как саркоидоз, липоидный некробиоз, кольцевидная гранулема, гранулематозная форма розацеа и др. Дерматоскопическая картина перечисленных нозологий может перекликаться, что обусловливает необходимость проведения гистологического исследования, однако выявление структур желтого цвета при дерматоскопии позволит сузить круг диагностического поиска [8, 16]. Типичным проявлением саркоидоза кожи считается обнаружение диффузного желтовато-коричневого окрашивания всего элемента сыпи (симптом яблочного желе) или отдельных структур желтого цвета, сочетающихся с линейно-извитыми сосудами в периферической части образования (рис. 9) [6, 8, 16–18]. Дерматоскопические проявления липоидного некробиоза отличаются в первую очередь выраженным сосудистым компонентом, представленным диффузной сетью пересекающихся друг с другом телеангиэктазий, определяемых во всем очаге поражения. Также возможно наличие бесструктурного окрашивания фона высыпаний в белый или желто-оранжевый цвет (рис. 10) [6, 8, 19].
В литературе можно встретить описания дерматоскопической картины еще многих дерматозов (красная волчанка, кольцевидная гранулема, эозинофильная гранулема, крапивница, уртикарный ангиит, мастоцитоз, болезнь Дарье, грибковые инфекции и др.) и инфестаций (чесотка, вшивость, миаз и др.) [6, 8, 20, 21]. Проявления большинства перечисленных дерматозов (за исключением инфестаций) при дерматоскопии, на наш взгляд, достаточно субъективны. Более информативна дерматоскопическая картина таких заболеваний, как склероатрофический лихен, хроническая пигментная пурпура, фиксированная токсикодермия.
Наиболее характерными дерматоскопическими проявлениями склероатрофического лихена являются комедоноподобные структуры, располагающиеся в расширенных устьях волосяных фолликулов, и диффузные бесструктурные зоны белого цвета (рис. 11). Необходимо учитывать, что внешние проявления очагов склероатрофического лихена зависят от длительности существования очагов. Свежие высыпания характеризуются комедоно-подобными структурами и периферическим эритематозным венчиком, а более старые очаги проявляются преимущественно бесструктурными зонами белого цвета [6, 8, 20, 22].
Дерматоскопическая картина хронической пигментной пурпуры проявляется множественными точками и глыбками красного цвета, расположенными на красновато-коричневом фоне и иногда определяемыми совместно с пигментной сетью (рис. 12) [6, 8, 20].
Дерматоскопические проявления фиксированной токсикодермии являются достаточно специфичными среди других дерматозов, однако имеют общие черты с меланоцитарными образованиями, подвергшимися полному регрессу. В пределах всех высыпаний определяются точечные структуры серого цвета, формирующие кольцевидные структуры вокруг устьев волосяных фолликулов (рис. 13) [20].

Таким образом, проведение дерматоскопического исследования в рамках амбулаторного приема помогает врачу-дерматологу подтвердить предполагаемый клинический диагноз, сузить круг дифференциально-диагностического поиска, исключить инфекционную природу высыпаний и перейти к подбору терапии.
Длительное время помощь людям, страдающим воспалительными заболеваниями кожи, сводилась к подбору и изготовлению сложных рецептурных прописей на основе соединений цинка, серы, салициловой кислоты, нафталана и других «традиционных» дерматологических компонентов [23]. Революцию в дерматологии совершили M.B. Sulzberger, V.H. Witten и C.C. Smith, впервые применившие в 1952 г. гидрокортизон в лечении атопического дерматита, лишая Видаля, аногенитального зуда и контактного дерматита [24]. С тех пор подходы к лечению дерматозов претерпели значительные изменения: помимо усовершенствования молекулы гидрокортизона и синтеза более активных глюкокортистероидов активнее стала использоваться фототерапия, появились системные препараты для лечения как тяжело протекающих дерматозов (атопический дерматит, псориаз), так и дерматозов, угрожающих жизни человека (обыкновенная пузырчатка). Однако основными и наиболее часто назначающимися препаратами в дерматологической практике остаются наружные глюкокортикостероиды.
Топические глюкокортикостероидные препараты (ТГКС) оказывают неоценимую помощь врачу-дерматологу в лечении пациентов с острыми и хроническими дерматозами. В большинстве клинических ситуаций эти препараты считаются первой линией терапии, они быстро и эффективно устраняют симптомы заболеваний, уменьшают сроки лечения. Основными механизмами действия ТГКС при кожных заболеваниях являются противовоспалительный, противозудный, сосудосуживающий и антипролиферативный [25].

Однако ТГКС при большом их разнообразии не равноценны. Выбор препарата в каждом конкретном случае должен зависеть как от свойств самого препарата, так и от особенностей заболевания. Врачу необходимо учитывать степень активности лекарства, риск развития как местных, так и системных побочных эффектов, возраст пациента. Важен и индивидуальный подбор лекарственной формы (раствор, мазь, крем, гель, лосьон и др.) в зависимости от клинических проявлений, остроты процесса, локализации высыпаний и площади поражения. Особое значение имеет терапевтический индекс, который отражает соотношение эффективности и безопасности лекарственных средств. Вопреки распространенному мнению, усиление активности действующего вещества не всегда сопровождается повышением риска развития побочных эффектов. Так, препараты последних поколений высокоактивны, при этом их профиль безопасности сопоставим и даже превосходит таковой у ряда значительно более слабых ТГКС предыдущих поколений – они обладают высоким терапевтическим индексом (табл. 1).
Из ТГКС последних поколений наиболее высокий терапевтический индекс имеют мометазона фуроат, метилпреднизолона ацепонат и флутиказона пропионат [26]. Среди них метилпреднизолона ацепонат (МПА) занимает особое место, поскольку он является пролекарством и действует сугубо локально в очаге воспаления [27]. МПА является глюкокортикостероидом четвертого поколения и не имеет в своей структуре галогенов (хлор, фтор). Благодаря двойной этерификации молекула МПА является липофильной, что облегчает ее быстрое проникновение в роговой слой и распределение в очаге воспаления. Попав в кожу, МПА под воздействием эстераз гидролизируется в активный метаболит – метилпреднизолона 17-пропионат (МПП). Процесс гидролиза МПА активнее происходит в пределах воспаленной кожи за счет содержания более высоких концентраций эстераз по сравнению со здоровой кожей. Аффинность молекул МПА и МПП к глюкокортикостероидным рецепторам в 2, 4 и 6,1 раза соответственно превосходит таковую гидрокортизона. После абсорбции МПП быстро и полностью инактивируется благодаря конъюгации с глюкуроновой кислотой и выводится преимущественно с мочой, не оказывая таким образом каких-либо системных эффектов [28].
Одной из проблем при применении ТГКС является риск развития побочных эффектов и связанный с этим страх использования препарата (т.н. стероидофобия). Наиболее частым осложнением длительного, бесконтрольного применения ТГКС является атрофия кожи. По данным R.P. Zaumseil и соавт., признаки атрофии кожи при лечении МПА были выявлены только у 2 пациентов из 1900, причем в обоих случаях, по мнению авторов, явления атрофии присутствовали и до начала терапии [29]. Применение МПА в течение 4 и 6 месяцев, по данным литературы, не приводит к подавлению гипоталамо-гипофизарно-надпочечниковой системы и изменению циркадного ритма секреции кортизола, что очень важно в лечении торпидно-протекающих дерматозов [30, 31].
Благодаря низкому риску развития побочных эффектов МПА можно применять в отношении детей с раннего возраста. О.Н. Тарасова и соавт. описали опыт использования МПА (Адвантан, Bayer) у детей от 6 месяцев до 16 лет в лечении атопического дерматита и псориаза. Высокая эффективность препарата (95,7%) отражалась в уменьшении мокнутия на 2–3-й день лечения и практически полном разрешении высыпаний на 6–7-й день лечения [32]. Н.Г. Короткий и соавт. показали высокую эффективность монотерапии мазью МПА (Адвантан) различных форм атопического дерматита у детей от 6 месяцев до 15 лет. В процессе лечения отмечено значительное снижение индекса SCORAD с 48,5 в группе детей с тяжелым течением атопического дерматита до 3,1 к концу третьей недели терапии [33]. И.В. Хамаганова и соавт. также описали опыт использования МПА (Адвантан) в лечении атопического дерматита у детей от 4 месяцев до 15 лет. Эффект от наружной терапии отмечен уже на второй день лечения, а к 12–14-му дню лечения регистрировалось значительного улучшение кожного процесса [34].
В зарубежных исследованиях результаты эффективности и безопасности МПА при использовании на протяжении 2–4 недель сопоставимы с данными отечественных публикаций [35, 36].
МПА широко используется у взрослых для лечения экземы кистей, в т.ч. профессиональной, контактного дерматита, солнечных ожогов, псориаза и других стероид-чувствительных дерматозов [26–28, 37]. Препарат выпускается в четырех лекарственных формах (эмульсия, крем, мазь, жирная мазь), что позволяет удобно наносить его на кожу особых локализаций (лицо, волосистая часть головы, крупные складки) и использовать в разные стадии воспалительного процесса. В период 4-недельного лечения МПА 575 пациентов с дерматозами, располагающимися на лице (атопический дерматит, контактный дерматит, себорейная экзема и фотодерматит), не было зарегистрировано случаев развития атрофии кожи или периорального дерматита [38]. Высокая эффективность и безопасность МПА в лечении дерматозов лица и волосистой части головы была также показана при лечении 1744 пациентов [39]. Известны работы по применению МПА на протяжении 8 и 20 недель в терапии генитального склероатрофического лихена у мужчин и женщин без развития местных побочных эффектов [40, 41]. Помимо удобства нанесения лекарственного препарата на приверженность пациентов лечению влияет и кратность использования средства в течение дня. Отличительной особенностью МПА (Адвантан) является его высокая эффективность при однократном использовании [28, 31, 35, 36].
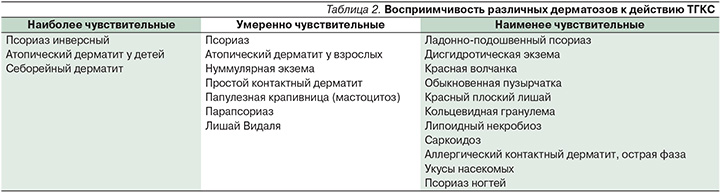
Еще один очень важный фактор – т.н. стероидчувствительность различных дерматозов. Именно этот фактор определяет выбор ТГКС с точки зрения их активности. Например, такие заболевания, как ладонно-подошвенный псориаз и дисгидротическая экзема, надо сразу начинать лечить сильными или очень сильными кортикостероидными препаратами, от слабых препаратов эффекта не будет. Восприимчивость наиболее часто встречающихся воспалительных заболеваний кожи, в т.ч. аллергического характера, отражена в табл. 2 [42].
Актуальным вопросом в лечении большинства дерматозов является продолжительность ремиссии после очередного обострения заболевания. В некоторых случаях скорое обострение экзематозного процесса может быть обусловлено краткосрочностью терапии и сохранением воспалительных элементов у пациента. В таких ситуациях целесообразно проводить дерматоскопический контроль излеченности пациентов. Суть методики заключается в тщательном осмотре участков предшествовавшего воспаления при помощи дерматоскопа для оценки регресса патологического сосудистого компонента, купирования явлений ксероза, отсутствия формирующихся элементов сыпи и полного восстановления естественной структуры кожи.
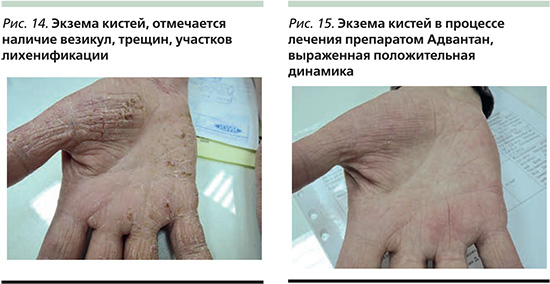
Наибольшее количество работ, использующих дерматоскопический контроль излеченности, посвящено нехирургическим методам лечения базальноклеточного рака кожи [43, 44]. Российские авторы описали опыт видеодерматоскопической оценки регресса угревых высыпаний [45]. Наш практический опыт показывает значимость дерматоскопии и при других дерматозах, например при экземе кистей (рис. 14). После двухнедельного курса лечения препаратом Адвантан у пациентки наблюдалась выраженная положительная динамика по результатам клинического осмотра (рис. 15). Дерматоскопический осмотр выявил наличие мелких везикул (рис. 4), что послужило поводом для продолжения лечения ТГКС, но уже в другом режиме дозирования.
Резюмируя все вышеизложенное, следует подчеркнуть, что врачу-дерматологу очень важно использовать в своей клинической практике достижения оптической диагностики кожи для более эффективной постановки диагноза, что в первую очередь определяет выбор тактики лекарственной терапии. Стероидчувствительность дерматозов сильно различается, и недооценка этого фактора замедляет процесс выздоровления. Так называемая стероидорезистентность может на деле означать как неправильную постановку диагноза, так и неверно подобранную терапию. Например, применение слабого кортикостероидного препарата при низкой восприимчивости заболевания к ТГКС приводит к малой эффективности лечения, увеличению продолжительности его течения и повышает в конечном итоге стоимость терапии. Выбирая препарат из доступных ТГКС высокой активности, необходимо учитывать его терапевтический индекс, который наиболее благоприятен для препаратов последних поколений.



