Введение
В настоящее время тревожно-депрессивные расстройства (ТДР) особенно актуальны для больных, находящихся на программном гемодиализе (ПГД) [1–4]. Это связано с неуклонным ростом числа диализных больных, а также с высокой распространенностью самого ПГД. В связи с этим депрессия получила название «самое частое осложнение гемодиализа» (А.К. De-Nour и соавт., 1968). Несмотря на современные подходы к ведению и лечению больных на ПГД, исследователи P.L. Kimmel, R.A. Реterson (2005) определяют депрессию как самое частое психическое расстройство у диализных пациентов. По данным литературы, распространенность клинически выраженной депрессии на ПГД варьируется от 5 до 60% и более [5–8]. Исследователями выявлена сильная зависимость между прогрессированием депрессии и ее тяжестью в популяции диализных больных (K.L. Johanson и соавт., 2000). Логично заметить, что выраженность депрессии у больных, начавших получать лечение ПГД, служит независимым прогностическим фактором выживаемости [9–13].
В ходе диализного процесса тревога также довольно часто сопровождает больных, находящихся на ПГД. Это можно объяснить тем, что диализные пациенты кроме влияния основной патологии испытывают массу зависимостей: непосредственно от процедуры ПГД, медицинского оборудования, персонала, регламентации диеты, соблюдения питьевого режима, постоянного приема медикаментов, потери работы и свободы передвижения, возникновения половой дисфункции [14]. Все эти обстоятельства, бесспорно, являются мощным стрессогенным фактором, который беспокоит пациентов на ПГД (И.А. Васильева, 1992; J.A. Gurklis, Е.М. Menke, 1995; S.C. Yeh, H.C. Chou, 2007; A. Rahimi и соавт., 2008). Повышенный уровень депрессии в свою очередь ведет к снижению показателей качества жизни диализных пациентов [15].
ТДР у больных, находящихся на ПГД, бесспорно, требует квалифицированной психотерапевтической помощи, но, к сожалению, в условиях существующей системы здравоохранения она остается не всегда доступной. С учетом этого возрастает роль медикаментозной коррекции ТДР [16]. Однако в доступной литературе этот вопрос к настоящему времени остается мало разработанным. Можно назвать лишь единичную работу (Н.В. Агранович, Ю.П. Редько, 2009), в которой авторы применили анксиолитик фабомотизол с целью коррекции ТДР у больных, находившихся на лечении ПГД, но отдаленные результаты лечения ТДР у указанных лиц ни в одной из публикаций не рассматривались.
Цель исследования: оценить наличие и выраженность ТДР у больных, находящихся на лечении ПГД, а также проследить его динамику после фармакотерапии селективным анксиолитиком фабомотизолом, а также спустя 1 и 2 месяца.
Материал и методы
В исследование включена группа из 90 пациентов, находившихся на лечении ПГД (33 мужчины и 57 женщин). Средний возраст больных составил 61 [56; 68] год. Длительность ПГД, по данным анамнеза, составила 4 [3; 7] года. С целью выявления наличия ТДР у больных на ПГД было проведено психологическое тестирование с помощью общепринятых опросников: госпитальная шкала тревоги и депрессии HADS (The hospital Anxiety and Depression Scale), шкала Гамильтона для оценки тревоги и депрессии, шкала депрессий Центра эпидемиологических исследований CES-D (The center for Epidemiologic Studies Depression Scale), шкалы Спилберга, включившая личностную и ситуационную тревожность.
С целью коррекции состояния пациентам с установленными тревогой и депрессией (78/84,4%) был назначен фабомотизол, селективный анксиолитик небензодиазепинового ряда, в дозировке 5 мг 3 раза в сутки в течение 4 недель. Механизм действия данного препарата основан на способности препятствовать развитию мембранно-зависимых изменений, которые наблюдаются при формировании стрессовой реакции [17, 18]. Фабомотизол не оказывает стимулирующего действия на бензодиазепиновые рецепторы, но имеет способность воздействовать на сигма-1-рецепторы головного мозга, находящиеся в зонах, которые отвечают за сенсорное восприятие, тонкую моторику, память и эмоции. Фабомотизол относится к классу «короткоживущих» лекарственных средств (период полувыведения – 0,82±0,54 часа) с высоким клиренсом. Безусловно это имеет большое практическое значение при назначении лекарственного средства пациентам с терминальной хронической почечной недостаточностью [19]. Препарат хорошо адсорбируется из желудочно-кишечного тракта, достаточно быстро экскретируется из организма с мочой и калом в виде 0,1% неизмененного соединения и 42,1% метаболитов (А.О. Вигшинская, 2007). Достоверный клинический эффект развивается с 3–7-го дня терапии [20]. В целом фабомотизол обладает анксиолитическим, мягким стимулирующим и вегетостабилизирующим действиями в отсутствие седативного и миорелаксирующего эффектов. В ходе проведенного ранее исследования было подтверждено положительное влияние препарата на ассоциированные с тревожностью когнитивные расстройства [21]. Также в лабораторных условиях была доказана способность фабомотизола связываться с рецепторами моноаминоксидазы А (МАО-А). Таким образом, препарат обладает свойствами, сходными с антидепрессантами [22].
До и после проведенной терапии мы оценивали показатели наличия и выраженности ТДР у больных, находившихся на ПГД. Статистическая обработка данных проведена с помощью пакета прикладных программ Statistica 10.0 с использованием непараметрических методов (сопоставление независимых групп с использованием критериев Манна–Уитни. При p<0,05 различия считались достоверными.
Результаты и обсуждение
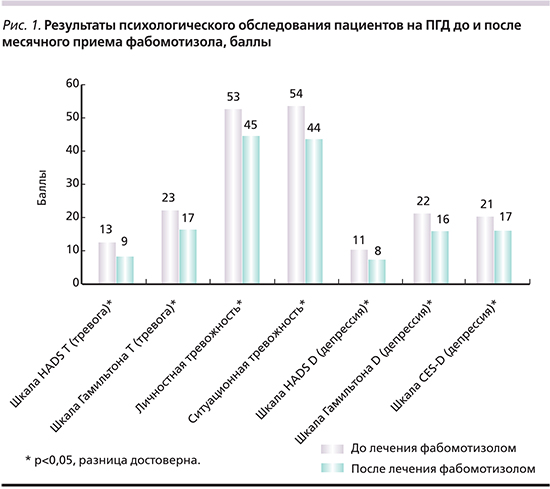
В результате проведенного психологического тестирования по опросникам HADS, Гамильтона, CES-D, личностной и ситуационной тревожности у 78 из 90 пациентов были выявлены ТДР. С целью коррекции состояния данные больные в течение месяца получали фабомотизол в дозировке 5 мг 3 раза в сутки. Динамика психологического статуса представлена на рис. 1, из которого видно, что у диализных больных выявлена достоверная положительная динамика в виде уменьшения выраженности ТДР по данным снижения медиан числа баллов по шкалам всех используемых опросников. Стоит отметить, что по опроснику HADS уровни тревоги и депрессии после проведенной терапии фабомотизолом из клинически выраженной (р<0,007 и р<0,03 соответственно) достоверно перешли в субклинически выраженную. По шкале Гамильтона уровень тревоги из тяжелой достоверно значимо трансформировался в легкую (р<0,004), депрессии – из средней степени тяжести в легкую (р<0,009). По другим опросникам после лечения фабомотизолом также фиксировалась достоверно значимая положительная динамика в виде уменьшения проявления ТДР: по шкалам личностной и ситуационной тревожности выраженная тревожность достоверно (р<0,04 и р<0,02 соответственно) перешла в умеренную, а по опроснику CES-D легкое депрессивное расстройство – в состояние отсутствия депрессии, что статистически достоверно (р<0,03).
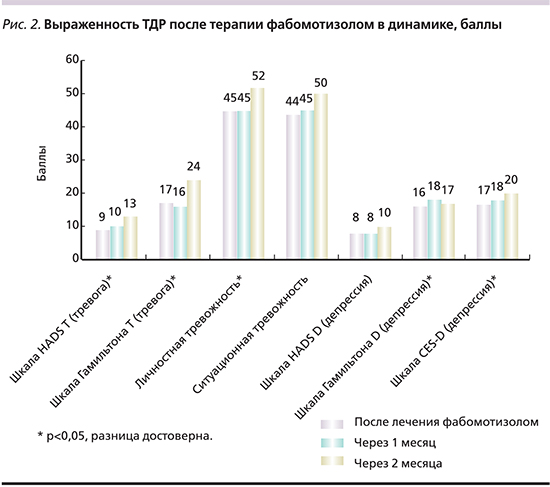
С целью определения срока, в течение которого длится эффект от проведенного лечения фабомотизолом, больным, находившимся на ПГД, у которых ранее диагносцированы ТДР, вновь была проведена оценка психологического статуса в динамике, через 1 и 2 месяца. Результаты представлены на рис. 2, из которого следует, что через месяц после терапии фабомотизолом существенной динамики у диализных больных ни по одному из использованных опросников зафиксировано не было. Однако уже через 2 месяца вновь установлены признаки ТДР, а именно: по шкале HADS-Т достоверно (р<0,04) диагносцирована клинически выраженная тревога, по шкале Гамильтона слабовыраженная тревога достоверно (р<0,006) перешла в разряд субклинически выраженной тревоги, по шкалам личностной и ситуационной тревожности умеренная тревожность – в выраженную. По шкалам, определяющим наличие депрессии, наблюдалась следующая динамика: по шкале HADS-D состояние субклинически выраженной тревоги в динамике и через месяц, и через 2 осталось прежним, по шкале Гамильтона легкая депрессия также осталась на прежнем уровне, по шкале CES-D, по которой после проведенного курса фабомотизолом депрессия отсутствовала, было зафиксировано легкое депрессивное расстройство, что статистически достоверно (р<0,05).
Полученные данные наводят на мысль о рекомендации провести повторный курс фабомотизола через 2 месяца. При наличии показаний, выявленных по результатам психологического тестирования, можно рекомендовать и более ранний прием препарата. Больных на ПГД с признаками ТДР стоит также направлять на консультацию психотерапевта или психолога с целью коррекции состояния.
Выводы
- По результатам проведенного исследования у подавляющего большинства (84,4%) больных, находившихся на ПГД, выявлены ТДР.
- Включение в комплексную терапию диализных больных анксиолитика фабомотизола способствует снижению выраженности ТДР.
- Через 2 месяца после проведенной терапии фабомотизолом вновь диагносцированы признаки ТДР.
- При наличии показаний следует рекомендовать повторный курс фабомотизола через 2 месяца, а также по показаниям, выявленным в ходе психологического тестирования.



