Выраженность сахароснижающего эффекта того или иного антидиабетического препарата является одним из важнейших факторов, которые определяют возможность его регистрации и использования в реальной клинической практике. В клинических рекомендациях EASD (European Association for Study of Diabetes) и ADA (American Diabetes Assosiation) можно найти подразделение всех неинсулиновых классов антидиабетических препаратов по их сахароснижающему потенциалу на две категории – умеренного и выраженного действия [1]. К препаратам с умеренной сахароснижающей эффективностью относят меглитиниды, ингибиторы дипептидилпептидазы-4 (иДПП-4), ингибиторы α-глюкозидаз. Сахароснижающая активность этой первой группы при монотерапии находится в условном диапазоне уровня гликированного гемоглобина (HbA1c) 0,5–1,0%. К препаратам с выраженным сахароснижающим действием относятся метформин, производные сульфонилмочевины (СМ), тиазолидиндионы (ТЗД) и агонисты рецепторов глюкагоноподобного пептида-1 (аГПП-1), чья условная сахароснижающая эффективность была условно определена диапазоном HbA1c 1,0–1,5%. При этом следует отметить, что данные значения носят условный характер с учетом нескольких факторов. Прежде всего сила сахаро-снижающего эффекта почти любого неинсулинового сахароснижающего препарата напрямую зависит от исходного уровня HbA1c у конкретного пациента: чем выше исходный уровень HbA1c, тем более существенна итоговая динамика снижения. Важно также отметить, что данные по прямым сравнительным исследованиям носят ограниченный характер. Как правило, речь идет о сравнительных исследованиях иДПП-4 с метформином, где показана полная сопоставимость сахароснижающего действия.
В большинстве прямых сравнительных исследований речь идет о комбинированной терапии с бигуанидами и в качестве препарата сравнения чаще всего выступают препараты СМ. Сравнительные исследования внутри класса препаратов проводятся не так часто, однако в ряде случаев показаны существенные различия. Так, репаглинид в прямых сравнительных исследованиях показал существенное преимущество по снижению уровня HbA1c над натеглинидом (-1,57 и -1,04%; p=0,002) в монотерапии [2] и -1,28 и -0,67% (p<0,001) при добавлении к метформину [3]), или в прямом сравнительном исследовании LEAD-6 лираглутид в суточной дозе 1,8 мг значимо превзошел эксенатид, вводимый два раза в сутки (-1,12 и -0,79%; p<0,0001) [4]. Мета-анализ исследований по сравнительной эффективности метформина и СМ не показал каких-либо значимых различий по выраженности снижения уровня HbA1c в монотерапии (разница +0,06% в пользу метформина, 95% доверительный интервал [ДИ] – 0,16–0,26) [5], так же как пиоглитазон в прямом сравнительном исследовании с СМ (монотерапия и добавление к метформину), которое длилось год, также не показал статистически значимого преимущества по снижению уровня HbA1c по сравнению с СМ [6], хотя при долгосрочном исследовании глитазоны проявили преимущество и по отношению к метформину, и СМ по удержанию достигнутого контроля гликемии, в частности, в исследовании RECORD. Прямые сравнительные исследования иДПП-4 с СМ в комбинированной терапии с метформином показали полную идентичность в отношении динамики снижения уровня HbA1c в течение первого года терапии [7–12] и 2-летнего года лечения [13–17], за исключением препарата алоглиптин, где через два года было отмечено преимущество иДПП-4 по сравнению с глипизидом (исследование ENDURE). Однако следует отметить, что к концу второго года терапии доза глипизида у большинства пациентов не превышала 10 мг при максимально возможной дозе 20 мг, что было связано с повышением частоты гипогликемических состояний в группе пациентов на СМ и ограничением возможности дальнейшей титрации дозы. Таким образом, при сравнительных исследованиях с СМ всегда следует уделять внимание не только показателям динамики гликемии, но возможности титрации дозы СМ и сопутствующим рискам развития гипогликемических эпизодов, ограничивающих такую возможность. Тем не менее у большинства клиницистов имеется устойчивое мнение о хорошем сахароснижающем потенциале препаратов СМ, основанное, как правило, на «историческом» опыте, зачастую связанном с назначением препаратов СМ пациентам с выраженной гипергликемией.
Как уже было сказано ранее, чем выше исходный уровень гликемии, тем более существенным ожидается его динамика. В настоящее время, когда принята концепция раннего вмешательства с целью достижения и поддержания целевого уровня HbA1c максимально безопасным способом, становится очевидным, что понятие «антидиабетический эффект» приобретает более широкий смысл и не ограничивается только гипогликемизирующим действием препарата, но возможностью долгосрочного действия, влиянием на риск гипогликемий, динамики массы тела и аспектами безопасности.
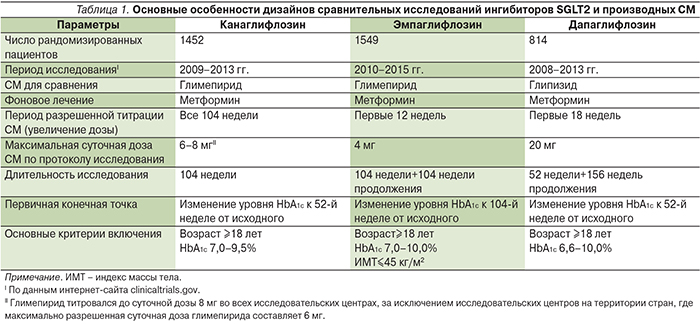
Появление нового класса препаратов ингибиторов натрий-глюкозного транспортера 2 типа (SGLT2 – Sodium dependent GLucose Transport) вызвало большой интерес среди клиницистов и по-прежнему традиционно в аспекте сравнительного и гипогликимизирующего эффектов с теми же препаратами СМ. Все три ингибитора SGLT2, зарегистрированные в России, прошли клинические испытания, где продемонстрировали преимущество в снижении уровня HbA1c над СМ в среднесрочной перспективе. В табл. 1 приведены основные сведения о дизайнах этих трех исследований [18], из которой видно, что все три исследования изначально были спланированы на достаточно длительный срок, не менее 2 лет, с достаточно большой выборкой пациентов.
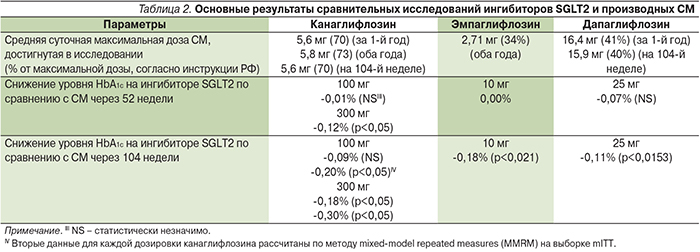
Два из трех ингибиторов SGLT2 (канаглифлозин и эмпаглифлозин) избрали в качестве СМ сравнения хорошо известный и хорошо зарекомендовавший себя в России глимепирид – препарат длительного действия, имеющий один из самых благоприятных среди препаратов СМ профиль эффективности и безопасности, что определяет и относительно высокую его стоимость. Дапаглифлозин сравнивался с глипизидом, препаратом СМ, наиболее часто назначаемым в США. Во всех трех исследованиях ингибиторы SGLT2 сравнивались с СМ в наиболее ожидаемой комбинации – в двойной терапии при добавлении к стабильной максимально переносимой дозе метформина. Дизайн трех исследований несколько различался по возможности титрации дозы препаратов СМ, в частности в исследовании, где в качестве основного препарата использовался канаглифлозин в группе сравнения, у исследователей была возможность максимальной титрации дозы глимепирида при ускользании эффекта терапии на протяжении всего периода наблюдения. В то время как в двух других сравнительных исследованиях исследователи имели ограничение с точки зрения титрации дозы препарата СМ до среднетерапевтических или субмаксимальных значений. В итоге, как видно из табл. 1, среднесуточная доза препаратов СМ варьировалась в разных исследованиях (табл. 1, 2), средняя суточная доза СМ в исследовании на канаглифлозине была выше по сравнению с остальными двумя исследованиями. Как видно из табл. 2, все три препарата, ингибитора SGLT2 (а не только канаглифлозин), имели достоверно более выраженное снижение и поддержание уровня HbA1c на долгосрочной основе.
Конечно, с точки зрения клинической значимости данное статистическое преимущество может показаться незначимым. Однако с учетом дополнительных преимуществ в виде снижения массы тела и низкого риска гипогликемий, а также умеренного, но достоверного снижения систолического артериального давления без увеличения частоты сердечных сокращений, зарегистрированных во всех трех исследованиях, где пациенты получали ингибитор SGLT2, преимущество над СМ становится очевидным и клинически значимым (табл. 3). Особенно если иметь в виду тот факт, что на препаратах СМ имеет место тенденция к нарастанию массы тела и снижению сахароснижающего ответа с течением времени.

Таким образом, ингибиторы SGLT2 – это новый стандарт эффективности гликемического контроля, обладающий рядом дополнительных преимуществ в отношении профиля безопасности, которые в полной мере проявятся скорее всего в долгосрочных исследованиях по сердечно-сосудистой безопасности EMPAREG, CANVAS и DECLARE. Исследование сравнительной эффективности ингибитора SGLT2 канаглифлозина оказалось наиболее демонстративным с точки зрения преимуществ ингибитора SGLT2 по сравнению с препаратом СМ, поскольку, согласно дизайну, прямое сравнительное исследование осуществлялось против максимальной, свободно титруемой дозы препарата СМ. Канаглифлозин достиг преимущества в снижении уровня HbA1c уже через год терапии, в то время как для эмпаглифлозина и дапаглифлозина это стало возможным через 2 года исследования. Вместе с этим для выявления тех или иных преимуществ сахароснижающих препаратов внутри класса требуются прямые сравнительные исследования, которые на данный момент отсутствуют, следовательно, делать вывод о преимуществе того или иного препарата преждевременно.



