Введение
Псориаз – хронический дерматоз многофакторной природы с доминирующим значением в развитии генетических факторов и иммуноопосредованной направленностью, характеризующийся гиперпролиферацией клеток в эпидермисе с формированием кератинизации, различной степени выраженности воспалительной реакции в эпидермисе и дерме, изменениями в различных органах и системах [1–3]. Псориаз распространен на значительной части земного шара, данным дерматозом страдают около 2% населения России, Западной Европы и США [4, 5].
В последнее время в литературе все чаще обсуждается ассоциация псориаза с различными коморбидными состояниями [6, 7]. Под термином «коморбидность» понимают наличие дополнительной клинической картины, которая уже существует или может появиться самостоятельно помимо текущего заболевания и всегда отличается от него [8]. Среди основных коморбидностей, ассоциированных с псориазом, выделяют псориатический артрит, сахарный диабет (СД) 2 типа, сердечно-сосудистые заболевания, метаболический синдром и депрессивные расстройства [7, 9, 10]. Существует мнение, будто развитие коморбидностей, скорее всего, основано на общности патогенеза сочетающихся заболеваний и не зависит от экономических или средовых факторов [11].
При псориазе установлена генетическая детерминация нарушений липидного и углеводного обменов, в связи с чем метаболический синдром, СД и гиперлипидемию у больных данным дерматозом выявляют значительно чаще, чем в общей популяции [2].
У пациентов с псориазом отмечена положительная корреляция с развитием инсулинорезистентности и нарушением толерантности к глюкозе, что ведет к частому сочетанию псориаза и СД. Устойчивость к инсулину, имеющаяся при СД 2 типа (псориаз не имеет отношения к СД 1 типа), – ответная реакция на воспаление [12, 13].
По данным проведенных исследований, больные псориазом средней тяжести имеют риск развития СД в 1,5 раза выше, чем в общей популяции, для больных тяжелым псориазом риск выше в 2 раза. В исследованиях, оценивавших распространенность псориаза, риск развития диабета был выше на 27% по сравнению с общей популяцией [12–14].
Псориаз, протекающий на фоне сопутствующего СД, чаще всего имеет тяжелое течение, может осложняться вторичной инфекцией [15]. Наблюдаются такие формы, как экссудативный псориаз, псориатический полиартрит, псориаз крупных складок. Кроме того, лечение больных псориазом всегда представляет определенные трудности при назначении терапии, особенно больным с отягощенным коморбидным статусом [10, 12, 14].
Как при псориазе, так и при СД 2 типа хроническое воспаление сосудистой стенки служит одним из важных звеньев патогенеза заболевания. Развитие эндотелиальной дисфункции имеет сходную природу: поврежденный эндотелий активирует систему сосудисто-тромбоцитарного звена гемостаза, что сопровождается изменением реологических свойств крови, склонностью к тромбообразованию и стимуляцией процессов свертывания крови [16, 17]. В основе поражения сосудов как при псориазе, так и при СД лежит хроническое воспаление эндотелия сосудистой стенки, возникающее на фоне снижения вазодилататора оксида азота и повышения мощного вазоконстриктора эндотелина-1, а также тромбоцитарной гиперагрегации. При обоих заболеваниях наблюдается локальное усиление ангиогенеза в связи с повышенной выработкой ростовых факторов, в частности фактора роста эндотелия сосудов [18, 19].
За последние годы появилось множество сообщений о применении в лечении васкулярных патологий, в т.ч. и при псориазе, препарата сулодексид группы гликозаминогликанов. Активным веществом лекарственного средства является экстракт, получаемый из слизистой оболочки тонкого отдела кишечника животных. Это естественная смесь гепариноподобной фракции и дерматансульфата. Обладая антитромботическим, фибринолитическим и ангиопротективным действиями, сулодексид способен оказывать комплексное влияние на стенки сосудов [19, 20]. Фармакологические свойства сулодексида и наличие успешных результатов его применения больными СД позволили сделать предположение о возможности использования данного препарата пациентами с псориазом, сопровождающимся эндотелиальной дисфункцией сосудов кожи и усиленным ангиогенезом.
Целью данного исследования стало изучение влияния комбинированной цитостатической терапии и сулодексида на течение дерматоза и показатели эндотелиальной дисфункции у больных псориазом с учетом коморбидных состояний.
Материал и методы
В исследование были включены 125 больных различными формами псориаза, 54 женщины и 71 мужчина, их средний возраст составил 64,8±1,9 года. У большинства пациентов наблюдалась экссудативная форма дерматоза – 79 (63,2%) человек, вульгарной формой страдали 38 (30,1%) больных, интертригинозной – 8 (6,4%). У всех пациентов отмечен распространенный характер патологического процесса на коже в стадии прогрессирования. Индекс PASI (Psoriasis Area and Severity Index) для всех участников исследования в среднем был равен 38,7.
В зависимости от наличия сопутствующей патологии испытуемые были разделены на 2 основные группы: в I были включены больные псориазом в сочетании с СД 2 типа – всего 40 человек. Пациенты получали стандартное лечение псориаза с применением цитостатических препаратов (метотрексат по схеме Weinstein и Frost). Дополнительно к проводимой терапии 18 больным был назначен сулодексид. Лечение начиналось с ежедневного внутривенного введения содержимого 1 ампулы препарата (2 мл 600 ЛЕ) в течение 15 дней. Затем пациенты продолжали терапию, принимая препарат внутрь по 1 капсуле (250 ЛЕ) 2 раза в сутки в перерыве между приемами пищи на протяжении 30 дней.
Вторую группу составили больные псориазом без СД (всего – 85 человек), соответствующие больным I группы по возрасту, конституциональным особенностям и клинической картине псориаза. Пациенты II группы также получали стандартное лечение псориаза с применением цитостатиков, 35 больным дополнительно в курс терапии был включен сулодексид, схема приема препарата была аналогичной с пациентами I группы.
Клиническая эффективность проводимой терапии оценивалась с учетом динамики индекса PASI. Уменьшение значений индекса PASI на 90% расценивали как клиническое разрешение; на 75% – как значительное улучшение; на 50% – как улучшение.
Для лабораторной оценки эффективности проводимого лечения методом иммуноферментного анализа в сыворотке крови определяли маркеры эндотелиальной дисфункции и ангиогенеза – оксид азота (NO), эндотелин-1 (Et-1) и фактор роста эндотелия сосудов (VEGF) до (исходно) и после терапии.
Контрольную группу для сравнения лабораторных показателей составили 30 практически здоровых лиц в возрасте от 30 до 48 лет.
Для статистического анализа полученных результатов использовались пакеты компьютерных программ Statistica 6.0 (StatSoftInc.), SPSS 13.0 for Windows (SPSS Inc.), Microsoft Office Excel 2007. Достоверность полученных данных устанавливали с помощью непараметрического критерия Манна–Уитни. Различие оценивалось как статистически значимое при p<0,05. При значении p<0,001 достоверность считалась высокой.
Результаты
До начала терапии среди больных обеих групп было выявлено достоверное снижение NO и повышение Et-1 и VEGF в сыворотке крови по сравнению с контрольной группой. Причем у больных псориазом и СД 2 типа наблюдался более выраженный сдвиг данных показателей, что, скорее всего, обусловлено наличием коморбидного статуса.
После окончания курса лечения (на 45-й день терапии) среди больных обеих групп, получавших только цитостатическую терапию (суммарная доза метотрексата составила 100 мг), клиническое разрешение наблюдалось у 32 (44,5%) человек, значительное улучшение – у 12 (16,7%), улучшение – у 28 (39%) пациентов. Среди пациентов I и II групп, получавших в комплексе с метотрексатом (суммарная доза препарата составила 40 мг) сулодексид, клиническое разрешение отмечено у 37 (69,8%) человек, значительное улучшение – у 7 (13,2%), улучшение – у 9 (17%) человек. Все пациенты хорошо переносили проводимую терапию, побочных эффектов на фоне приема сулодексида не было.
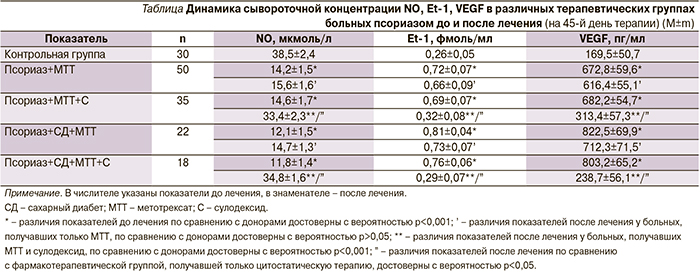
У больных псориазом обеих групп, получавших только цитостатическую терапию без применения сулодексида, тенденции к нормализации маркеров эндотелиальной дисфункции не отмечено или она была выражена слабо. Среди пациентов I и II групп, получавших в комбинации с метотрексатом сулодексид, было зафиксировано достоверное повышение NO, снижение Et-1 и VEGF (см. таблицу).
Обсуждение
Таким образом, результаты проведенного нами исследования демонстрируют общность механизма развития дисфункции эндотелия при псориазе и СД 2 типа. Включение в терапию гепариноидов позволяет снижать лекарственную нагрузку пациентов, уменьшать курсовую дозу и длительность применения метотрексата. Исходя из данных лабораторных показателей, сулодексид оказывает нормализующее влияние на уровень маркеров эндотелиальной дисфункции и ангиогенеза. Сулодексид также снижает риск развития осложнений СД, который является час-той коморбидностью для больных псориазом.
Выводы
Нормализация сосудистого звена патогенеза представляет важную задачу в терапии пациентов с псориазом, особенно имеющих отягощенный коморбидный статус. Применение цитостатической терапии в сочетании с сулодексидом оказывает нормализующее действие на эндотелиальную дисфункцию, улучшает лабораторные показатели, способствуя более быстрому улучшению или разрешению патологического процесса. Включение в комплексную терапию сулодексида помогает уменьшить риск развития нежелательных побочных эффектов цитостатиков и приводит к достижению более раннего и стойкого терапевтического эффекта.


