По данным Всемирной организации здравоохранения, за последние годы регистрируется неуклонный рост хронических заболеваний печени как вирусной, так и невирусной этиологии. Наибольшее распространение получила неалкогольная жировая болезнь печени (НАЖБП). Так, частота встречаемости НАЖБП только в России достигает 27%, причем из них стеатоз составляет 80,3%, стеатогепатит – 16,8%, а цирроз печени – 2,9%. Что касается жителей европейских стран, то распространенность НАЖБП достигает 35%, в США – 34, в Японии – 29%. Необходимо также отметить, что НАЖБП выявляется как у детей, так и у взрослых. А вот среди больных, страдающих ожирением, распространенность НАЖБП значительно выше, нежели в общей популяции, и по данным различных исследований, достигает 62–93%. Так, на стадии стеатогепатита НАЖБП диагностируется у 18,5–26,0%, на стадии фиброза – у 20–37%, на стадии цирроза печени – у 10% больных. Частота встречаемости НАЖБП при морбидном ожирении уже возрастает до 95–100%. Но в одном из исследований было показано, что среди пациентов НАЖБП, не страдающих сахарным диабетом, 22% были худыми, 64% не соответствовали минимальным критериям метаболического синдрома (МС), а у 12% не было выявлено ни одного критерия МС. Другое исследование продемонстрировало, что стеатоз печени может развиваться при повышении массы тела, не сопровождающимся повышением индекса массы тела (Y. Chang, S. Ryu, E. Sung et al., 2006). Существует мнение, будто стеатоз формируется при увеличении веса независимо от того, превышает ли он нормальные значения индекса массы тела. Оказалось, что даже незначительное увеличение массы тела способствует перераспределению содержания липидов в тканях и нарушению их нормального метаболизма. Так, при изучении особенностей метаболизма холестерина при НАЖБП было установлено, что независимо от веса синтез его повышен, а всасывание в кишечнике снижено, что может быть связано с нарушением кишечного микробиоценоза, который, по различным данным, встречается в 100% случаев у больных хроническими заболеваниями печени.
С одной стороны, НАЖБП – это самостоятельная нозологическая единица, представляющая собой патогенетически связанную группу поражений печени, включающую стеатоз, неалкогольный стеатогепатит, фиброз и цирроз печени. С другой стороны, НАЖБП служит фактором риска сердечно-сосудистых заболеваний, рассматривается как печеночный компонент МС и ассоциирована с абдоминально-висцеральным ожирением, периферической инсулинорезистентностью, артериальной гипертензией и дислипидемией.
В настоящее время в МКБ-10 отсутствует единый код НАЖБП, в полной мере отражающий полноту диагноза, равно как и общепринятые российские стандарты по диагностике и лечению этого заболевания. НАЖБП (синонимы: «жирная» печень, жировая дистрофия печени, жировая дегенерация печени, стеатоз печени) – это хроническое заболевание, объединяющее клинико-морфологические изменения в органе у лиц, не употребляющих алкоголь в чрезмерном количестве. В основе стеатоза лежит дисбаланс между потреблением и утилизацией липидов. Накопление жира в клетках печени может быть следствием повышения поступления свободных жирных кислот в печень; снижения скорости β-окисления свободных жирных кислот в митохондриях; избыточного их синтеза; снижения синтеза или секреции липопротеинов очень низкой плотности.
Механизмами трансформации стеатоза в стеатогепатит являются повышение продукции TNF-a жировой тканью, увеличение концентрации свободных жирных кислот, которые оказывают прямой повреждающий эффект на мембраны гепатоцитов; активация цитохрома Р450, повышение перекисного окисления липидов, накопление реактивных форм кислорода (оксидативный стресс) с образованием избыточного количества высокотоксичных ксенобиотиков, а также эндотоксемия на фоне кишечного дисбиоза.

Выделяют первичные и вторичные факторы, способствующие прогрессированию НАЖБП. К первичным факторам относят малоподвижный образ жизни, сниженную физическую активность, МС, сахарный диабет, висцеральное ожирение, дислипидемию. Среди вторичных выделяют применение лекарственных препаратов (глюкокортикоиды, амиодарон, эстрогены, тамоксифен, тетрациклин, ацетилсалициловая кислота, индометацин, бруфен, антибиотики); нарушение питания (голодание, резкое сокращение или увеличение калорийности пищи, чрезмерное потребление углеводов, парентеральное питание, недостаток белков, витаминов и микроэлементов); нарушение процессов пищеварения и всасывания (хронические заболевания органов желудочно-кишечного тракта с секреторной недостаточностью пищеварительных ферментов); болезни обмена (Вильсона–Коновалова, Вебера–Крисчена, подагра); гипотиреоз; беременность; кислородную недостаточность (на фоне анемии, хронической сердечной и дыхательной недостаточности); нарушение микробиоценозов кишечника.
Клиническая картина НАЖБП характеризуется бессимптомным течением. Зачастую пациенты обращаются к врачу по поводу жалоб, не связанных с заболеванием печени, а именно по поводу артериальной гипертензии, ишемической болезни сердца, заболеваний периферических сосудов, ожирения, сахарного диабета 2 типа и др. На стадии стеатоза, как правило, пациенты жалоб не предъявляют или они носят неспецифический характер. На стадии стеатогепатита возможно наличие слабости, утомляемости, дискомфорта и тяжести в правом подреберье без четкой связи с приемом пищи. Необходимо учитывать, что интенсивность предъявляемых жалоб не коррелирует со степенью активности процесса. Клинические проявления на стадии фиброза опосредованы возникновением спленомегалии (анемии, лейкопении, тромбоцитопении), развитием портальной гипертензии, что затрудняет диагностику. Периодически возможны кровотечения из варикозно расширенных вен пищевода и желудка. Подобные состояния рассматривают как проявление цирроза печени. На стадии цирроза появляются характерные симптомы, указывающие на развитие печеночно-клеточной недостаточности, портальной гипертензии. И проявляются они увеличением живота в размерах, отеками, расширением вен пищевода и желудка, умеренной желтухой, повышенной кровоточивостью.
Что касается методов лабораторной диагностики, то показатели биохимического анализа крови у пациентов на стадии стеатоза печени зачастую не превышают границ нормы. Но нормальные показатели трансаминаз не исключают вероятности существования некротически воспалительных изменений в печени. На стадии стеатогепатита отмечается повышение показателей, характеризующих функциональное состояние печени: аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), гамма-глутамилтранспептидазы (ГГТП), щелочной фосфатазы (ЩФ), гамма-глобулинов; при этом активность АЛТ и АСТ не превышает верхнюю границу нормы более чем в 4–5 раз, а уровень АЛТ доминирует над таковым АСТ. Наличие фиброза характеризуется изменением сывороточных маркеров: гиалуроновой кислоты, проколлагена III типа, N-терминального пептида проколлагена III, ламинина и др. Также отмечается повышение активности ЩФ, ГГТП и билирубина, но не более чем в 2 раза. При трансформации фиброза в цирроз печени наблюдается преобладание АСТ над АЛТ, и это соотношение составляет менее 2, снижение уровня общего белка, альбумина, холестерина, холинэстеразы и протромбинового индекса, повышение уровня билирубина и тромбоцитопения. Для больных НАЖБП также характерно наличие дислипидемии. Для установления степени выраженности некровоспалительных изменений и стадии фиброза печени для больных НАЖБП разработан неинвазивный диагностический тест ФиброМакс. ФиброМакс включает определение активности процесса – Актитест, стадию фиброза – Фибротест, отражает тяжесть заболевания стеатозом – Стеатотест – и отражает тяжесть заболевания стеатогепатитом – Нэштест. По ряду биохимических показателей с учетом пола, возраста, роста и веса пациента, на основании математического анализа производится расчет индекса, соответствующего той или иной шкале.
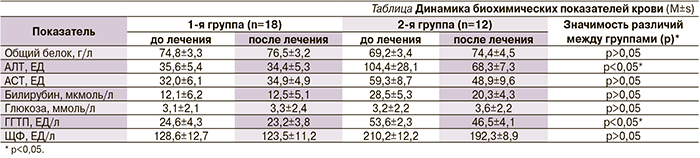
Среди визуальных методов диагностики НАЖБП наибольшее распространение ввиду своей доступности получило ультразвуковое исследование, которое может быть единственным методом, позволяющим заподозрить стеатоз печени, особенно при наличии у больного факторов риска. Ультразвуковая картина гепатоза характеризуется дистальным затуханием эхосигнала; диффузной гиперэхогенностью печени; увеличением эхогенности печени по сравнению с почками; нечеткостью сосудистого рисунка. Для выявления фиброза используется также эластометрия. Недостатком этого метода служит отсутствие возможности оценки выраженности некровоспалительного процесса; неинформативность пациентов с избыточной массой тела; искажение значения результатов пациентов в стадии биохимической ремиссии, с острым воспалением и с острым гепатитом; невозможность оценки состояния печени на стадиях стеатоза, стеатогепатита и ранних стадиях фиброза. При компьютерной томографии определяется снижение рентгеноплотности печени; визуализация внутрипеченочных сосудов, воротной и нижней полой вен как более плотных структур по сравнению с печеночной тканью; пересечение нормальными кровеносными сосудами печени зон пониженной Rh-контрастности, что является характерным признаком для очаговой жировой дистрофии.
Если ни одно из перечисленных исследований не дает возможности определиться с диагнозом, рекомендуется назначать биопсию печени для подтверждения или исключения неалкогольного стеатогепатита, фиброза или цирроза, поскольку о прогрессировании НАЖБП нельзя в полной мере судить лишь на основании жалоб, результатов лабораторных исследований и данных методов лучевой диагностики.
Основной целью терапии служит профилактика прогрессирования болезни: уменьшение выраженности стеатоза и предотвращение прогрессирования заболевания в стеатогепатит, фиброз и цирроз, а также снижение риска сердечно-сосудистых осложнений. Для чего необходимо контролировать массу тела, соблюдать диетические рекомендации, вести активный образ жизни, отказываться от вредных привычек, контролировать уровень глюкозы в крови, корректировать липидный профиль и кишечный микробиоценоз, а также важна адекватная терапия сопутствующих заболеваний и отмена гепатотоксичных препаратов. В ряде исследований показано, что комплексные меры по изменению образа жизни пациентов с НАЖБП способствуют снижению смертности от сердечно-сосудистых заболеваний на 40%, что сопоставимо с эффективностью медикаментозной коррекции.
Основу патогенетической терапии больных заболеваниями печени составляют гепатопротекторы (греч. hepar – печень, лат. protector – страж, охранитель) – препараты, повышающие устойчивость гепатоцитов к патологическим воздействиям, усиливающие антитоксическую функцию, способствующие восстановлению их функционального состояния. Действие их направлено на восстановление гомеостаза, повышение устойчивости к воздействию патогенных факторов, нормализацию функциональной активности и стимуляции репаративно-регенерационных процессов (нормализация синтеза и тока желчи). До сих пор в литературе отсутствует единое мнение относительно эффективности гепатопротекторов. Подавляющее большинство из используемых в медицинской практике гепатопротекторов в полной мере не удовлетворяет этим требованиям. В то же время в последние годы арсенал современных гепатотропных средств существенно расширился за счет появления новых как синтетических, так и природных средств. До настоящего времени клиническая эффективность многих известных и давно применяющихся гепатопротекторов не доказана, что побуждает исследователей на совершенствование доказательной базы и поиск новых препаратов для лечения больных хроническими заболеваниями печени. Несмотря на очевидную актуальность проблемы жировой болезни печени, до сегодняшнего дня в России отсутствуют общепринятые стандарты диагностики и лечения НАЖБП.
С учетом всего вышеизложенного нами на кафедре внутренних болезней и нефрологии СЗГМУ им. И.И. Мечникова было проведено исследование по применению препарата Прогепар больными НАЖБП. Основной целью исследования было выявление новых и/или констатация известных эффектов препарата Прогепар, в составе которого содержится экстракт печени крупного рогатого скота, цианокобаламин, холин, цистеин и мио-инозитол, для больных НАЖБП. В исследовании приняли участие 30 пациентов, средний возраст которых составил 46,3±12,3 года. Критерии включения в исследование: возраст 18 лет и старше, наличие верифицированной неалкогольной жировой инфильтрации печени. Все пациенты были разделены на две группы в зависимости от активности печеночных ферментов (АСТ и АЛТ). Так, в 1-ю группу вошли 18 пациентов с признаками стеатоза и уровнем трансаминаз в пределах референтных значений, во 2-ю были включены пациенты с признаками неалкогольного стеатогепатита и уровнем трансаминаз, превышающих нормальные значения. Препарат назначался всем пациентам по 2 таблетки 3 раза в день во время еды в течение трех месяцев.
Методы исследования: до и после курса терапии исследуемым препаратом обследование пациентов включало расспрос (использовался стандартизированный опросник), оценку качества жизни (опросник SF-36), клинический и биохимический анализы крови, проведение теста ФиброМакс, бактериологическое исследование содержимого толстой кишки (методом ПЦР диагностики), биоимпедансный анализ компонентного состава организма, ультразвуковое исследование органов брюшной полости. Оценка эффективности лечения проводилась по следующим показателям: быстрота исчезновения субъективных клинических симптомов, динамика показателей качества жизни, клинического и биохимического анализов крови, теста ФиброМакс, ультразвукового исследования и результатов биоимпедансного анализа состава организма. Оценка безопасности проводилась посредством мониторирования субъективного состояния пациентов в течение периода наблюдения и оценки динамики физикальных данных, клинических и биохимических показателей крови.
На фоне проводимой терапии препаратом Прогепар одним из наиболее важных результатов было выявление его положительного влияния на субъективные клинические проявления заболевания печени. Основными жалобами, которые предъявляли пациенты до лечения, были дискомфорт и тяжесть в правом подреберье, тошнота, нарушение стула с преобладанием запоров, слабость и утомляемость. После курса терапии была отмечена отчетливая положительная динамика по частоте выявления вышеперечисленных жалоб (рис. 1). Полученные данные свидетельствовали об эффективности воздействия препарата на субъективные признаки заболеваний печени.
В обеих группах данные клинического анализа крови (гемоглобин, лейкоциты, эритроциты, тромбоциты, СОЭ) как до, так и после лечения были в пределах нормальных значений.
В 1-й группе в пределах нормальных значений также оставались данные биохимического анализа крови (общий белок, амилаза, общий билирубин, глюкоза, АЛТ, АСТ, ГГТП, ЩФ). Во 2-й на фоне проводимой терапии отмечена отчетливая тенденция к снижению активности ферментов АЛТ, АСТ, ГГТП и показателя общего билирубина, что свидетельствует о восстановлении функции печени и снижении активности процесса. Динамика биохимических показателей крови у всех находящихся под наблюдением пациентов и результаты статистического анализа представлены в таблице.
На фоне проводимой терапии во всех группах отмечена тенденция к снижению показателей липидограммы, что свидетельствует о нормализации липидного спектра и снижении риска развития сердечно-сосудистых осложнений. Статистически значимым было отмечено снижение уровня общего холестерина (р<0,05, рис. 2). На фоне проводимой терапии препаратом Прогепар, по данным теста ФиброМакс, включающего оценку активности процесса, фиброза, стеатоза, метаболических нарушений, отмечена положительная динамика по всем показателям, что свидетельствует о снижении выраженности активности процесса и степени стеатоза. Подобные изменения вносят существенный вклад в профилактику прогрессирования заболевания. Для констатации более достоверных результатов рекомендовано продолжить наблюдения за пациентами до 6 месяцев (рис. 3).
При исследовании кишечного микробиоценоза методом ПЦР с количественным определением основных бактериальных представителей у большинства пациентов имел место микробный дисбаланс (дисбиоз кишечника), который выражался в значительном снижении доли бактероидов (бактериальной группы с высокоразвитым гликобиомом). Как известно, уменьшение доли бактероидов в микробиоте толстой кишки является характерным признаком для пациентов с избыточной массой тела и ожирением. После курса терапии у всех пациентов отмечена тенденция к нормализации кишечного микробиоценоза, в т.ч. за счет повышения доли бактероидов, а именно одного из важнейших представителей Faecalibacterium prausnitzii и Bacteroides fragilis. Такие изменения свидетельствуют о способности препарата регулировать кишечный микробиоценоз, связанный с избыточной массой тела, вследствие чего улучшается регуляция энергетического обмена, что способствует снижению риска развития МС (рис. 4).
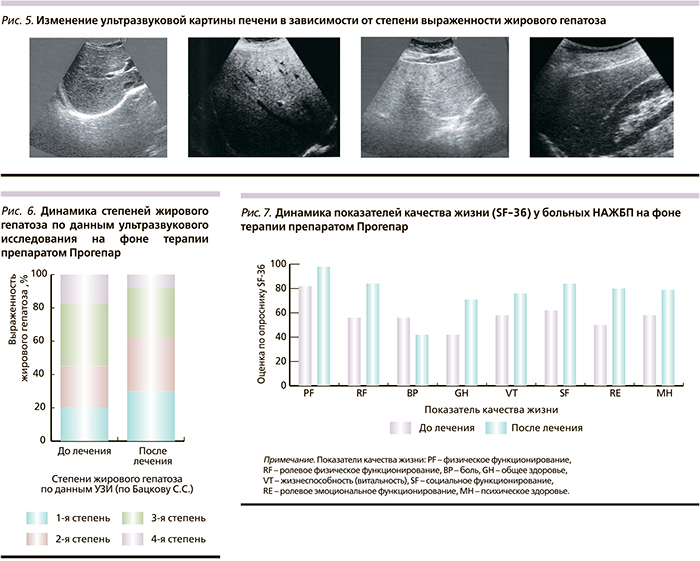
На основании результатов, полученных в ходе биоимпедансного анализа компонентного состава организма, выявлена тенденция к снижению индекса массы тела в среднем на 2,7% и количество жировой ткани в организме пациентов на 2,6%, что косвенно свидетельствует о нормализации метаболической функции печени. По результатам данных ультразвукового исследования гепатобилиарной системы отмечена положительная динамика за счет нормализации размеров печени у пациентов с гепатомегалией и регрессированием признаков жировой инфильтрации печени, согласно методике ультразвуковых критериев жирового гепатоза, предложенной С.С. Бацковым в 2005 г. (рис. 5), что является признаком гепатопротективного эффекта исследуемого препарата (рис. 6). При оценке качества жизни с помощью опросника SF-36 до лечения у всех пациентов (100%) отмечалось снижение показателей, характеризующих физический и психологический компоненты здоровья. После проведенного лечения выявлено достоверное (р<0,05) улучшение показателей, характеризующих физический компонент здоровья (рис. 7).
В процессе наблюдения и по результатам лабораторно-инструментальных методов обследования серьезных нежелательных явлений у пациентов, находившихся под наблюдением, зарегистрировано не было. Приверженность пациентов к лечению в среднем составила 97% за 90 дней приема.
Результаты проведенного исследования свидетельствуют об эффективности и безопасности препарата Прогепар в терапии больных НАЖБП, назначаемого в течение 3 месяцев по 2 таблетки 3 раза в день во время еды в качестве монотерапии. Терапия препаратом Прогепар способствует положительной динамике симптомов заболевания, улучшая состояние гепатобилиарного тракта, нормализации липидного спектра, повышению качества жизни пациентов и профилактике прогрессирования НАЖБП.
Полученные результаты позволяют заключить следующее: препарат Прогепар оказывает положительное влияние на клиническую картину заболевания у пациентов с НАЖБП; обладает гепатопротективным и гиполипидемическим действиями; способствует уменьшению эндоинтоксикации за счет нормализации микробиоценоза кишечника; способствует профилактике прогрессирования НАЖБП и снижению риска сердечно-сосудистых осложнений; улучшает показатели качества жизни. Прогепар имеет хорошую переносимость, безопасен, может быть рекомендован для применения больными НАЖБП в дозе по 2 таблетки 3 раза в день с едой в течение трех месяцев.



