Введение
Сердечно-сосудистые заболевания (ССЗ) являются основной причиной смертности в России, и летальность от ишемической болезни сердца (ИБС) составляет около 25 % в структуре общей смертности [1].
Применение статинов – ингибиторов ГМГ (гидрокси-метилглутарил)-КоА(коэнзим-А)-редуктазы позволило снизить риск смерти от ИБС, при этом наибольшую пользу от их приема получают пациенты с высоким и очень высоким риском [2, 3], которым показаны статины в максимально переносимой дозе для достижения целевых значений уровня холестерина липопротеидов низкой плотности (ЛПНП). До недавнего времени не было четких данных об эффективности статинов при их использовании в первичной профилактике. Более того, в мета-анализе 11 рандомизированных исследований, включивших более 65 тыс. участников, не было получено достоверного снижения общей смертности [4]. Тем не менее в течение последних лет появились данные, позволившие по-новому взглянуть на пользу статинов при их применении с целью первичной профилактики. Так, результаты регистра Cochrane Central Register of Controlled Trials, включившего 9 исследований с 56 934 участниками, подтвердили, что применение статинов с целью первичной профилактики ассоциировано со снижением общей смертности, частоты сердечно-сосудистых осложнений (ССО) и необходимости в реваскуляризации [6]. Также появились уточненные данные о безусловной пользе статинов и для пациентов с низким сердечно-сосудистым риском. Было показано, что снижение уровня ЛПНП сопровождается достоверным снижением частоты ССО – таким же, как и у пациентов с высоким риском. Эти данные были получены в результате мета-анализа клинических исследований с участием 170 тыс. пациентов, проведенного объединенной группой исследователей по лечению гиперхолестеринемии (CTT – Cholesterol Treatment Trialists Collaborators). Результаты исследования показали, что снижение уровня ЛПНП при применении статинов с целью первичной профилактики на 1 ммоль/л сопровождается уменьшением уровня сердечно-сосудистой смертности на 15 % и общей смертности на 9 % [5]. Таким образом, результаты перечисленных исследований подтвердили реальную возможность статинов снижать частоту ССО примерно в равной степени при применении препаратов с целью вторичной или первичной профилактики. Поскольку для решения этой задачи целесообразно использование наиболее эффективных современных гиполипидемических препаратов, мы планировали данное исследование с целью оценки гиполипидемической эффективности и безопасности розувастатина при его приеме в разных дозах – от 5 до 40 мг/сут.
Материал и методы
 Исследование проводилось как открытое многоцентровое наблюдательное, в котором участвовали 184 поликлиники из 70 городов Российской Федерации. В рамках исследования был изучен липидный профиль амбулаторных пациентов, получавших статины. Решение о назначении розувастатина (препарата Мертенил, компании «Гедеон Рихтер») и выборе его дозы принималось лечащими врачами самостоятельно.
Исследование проводилось как открытое многоцентровое наблюдательное, в котором участвовали 184 поликлиники из 70 городов Российской Федерации. В рамках исследования был изучен липидный профиль амбулаторных пациентов, получавших статины. Решение о назначении розувастатина (препарата Мертенил, компании «Гедеон Рихтер») и выборе его дозы принималось лечащими врачами самостоятельно.
После скрининга в исследование был включен 3591 пациент (1581 мужчина, 2010 женщин). Средний возраст пациентов составил 59,0 ± 19,2 года. В исследование включали пациентов с умеренным, высоким и очень высоким риском ССЗ и первичной гиперлипидемией IIа- и IIб-типов, не достигших целевых уровней ЛПНП на монотерапии статинами в течение 3 месяцев и более. В исследование не включили лиц, принимавших розувастатин, имеющих повышенные более чем в 2 раза уровни ферментов аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), креатинкиназы (КК), а также больных, принимающих участие в других исследованиях и страдающих заболеваниями, при которых участие в исследовании исключалось.
Врачи поликлиник были приглашены к участию в исследовании на основе случайных выборок.
Результаты исследования были подвергнуты статистической обработке с использованием пакета статистических программ Statistica 6.0. Результаты представлены в виде среднего и стандартного отклонений (Mean ± SD). При сравнении групп по количественному признаку использовались параметрический (t-критерий Стьюдента, однофакторный ANOVA) и непараметрический (критерий Манна–Уитни, ранговый анализ по Краскелу–Уоллису) методы. Статистически достоверными считали различия при p < 0,05.
Результаты
Клиническая характеристика больных и их исходные данные представлены в табл. 1. Из всех пациентов, включенных в исследование, ИБС была выявлена у 44 % пациентов, при этом более 90 % больных страдали АГ и 14 % СД. У 33 % больных был выявлен субклинический атеросклероз периферических артерий и у 1,5 % – клинически значимый атеросклероз периферических артерий.
Часть (785 человек) пациентов до включения в исследование принимали статины: симвастатин (45,6 %) и аторвастатин (54,4 %), при этом большинство из них принимали статины в низких дозах (табл. 2).
На этом фоне средний уровень ЛПНП в группе больных, получавших статины до включения в исследование, исходно составлял в среднем 3,42 ± 0,80 ммоль/л (табл. 3).
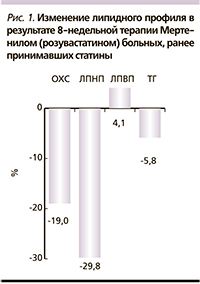
В рамках данного исследования этим пациентам был назначен Мертенил (розувастатин) в основном в дозах 10 и 20 мг/сут (табл. 4). Терапия Мертенилом в течение 8 недель привела к дополнительному снижению уровня ЛПНП на 29,8 % и ОХС – на 19 % (p < 0,01) при этом уровень ТГ снизился на 5,8 % (p < 0,01; рис. 1). Повышение уровня ЛПВП на 4,1 % было статистически незначимым. Показатели активности АСТ, АЛТ и КК при терапии Мертенилом в течение 8 недель достоверно не отличались от исходных значений. У 7 пациентов была повышена активность АЛТ и АСТ, однако их значения не превышали 2 верхних пределов нормальных значений (ВПН) и были клинически незначимыми.
Другой группе в количестве 2806 больных, ранее не получавших статины, Мертенил назначался по решению лечащего врача в дозах от 5 до 40 мг/сут. Наиболее часто Мертенил назначали в дозах 10 (57 % больных) и 20 мг/сут (28 % больных). Несколько реже Мертенил назначали в дозе 5 мг/сут (13 % больных) и довольно редко – в дозе 40 мг/сут (только 2 % больных).
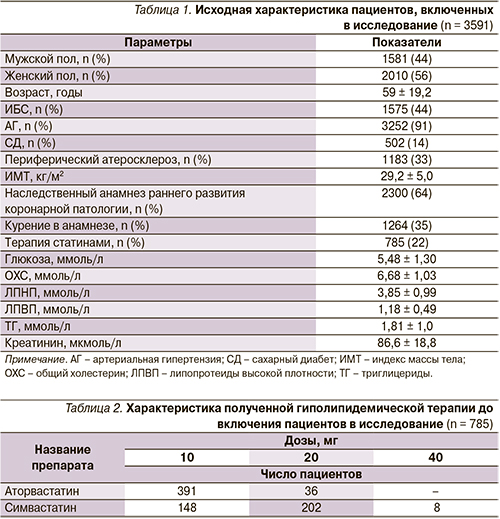
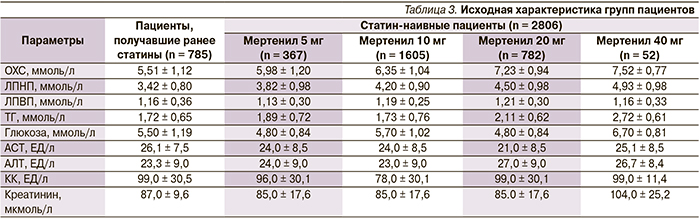
Лечение больных препаратом Мертенил в дозе 5 мг/сут проводилось преимущественно с целью первичной профилактики. В эту группу были отобраны 367 пациентов с исходно более умеренным нарушением липидного обмена (табл. 3), не имеющих клинических признаков атеросклероза периферических артерий. Терапия Мертенилом в течение 8 недель привела к снижению уровня ЛПНП на 35 % (рис. 2) и ОХС на 27,4 % (p < 0,01 для обоих показателей) (рис. 3).
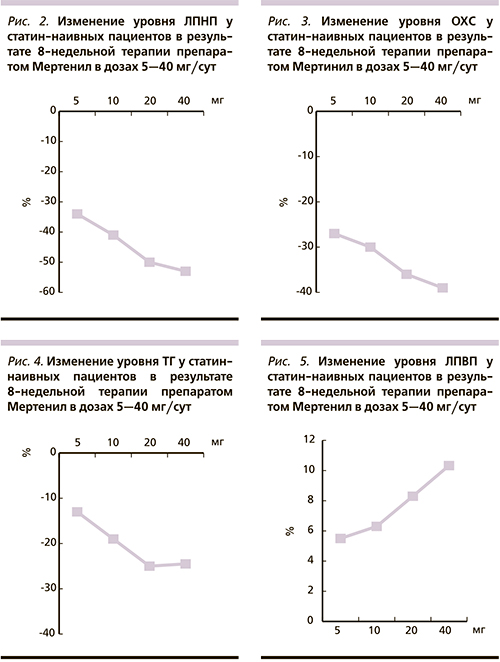
Кроме этого было отмечено достоверное снижение уровня ТГ на 14,3 % (p < 0,01) (рис. 4) и повышение уровня ЛПВП на 5,3 % (p < 0,05) (рис. 5).
Показатели безопасности АСТ, АЛТ и КК при терапии Мертенилом достоверно не отличались от исходных значений. У 19 пациентов исходно отмечено повышение активности АЛТ и АСТ, обусловленное наличием неалкогольного стеатогепатоза. На фоне терапии розувастатином их значения не превышали 2 ВПН и были клинически незначимыми.
Лечение больных Мертенилом в дозе 10 мг/сут привело к снижению уровня ЛПНП на 41,4 %, ОХС – на 30,0 % и ТГ – на 19,1 % (p < 0,01 для всех показателей), к повышению уровня ЛПВП на 6,3 % (p < 0,05).
Показатели безопасности АСТ, АЛТ и КК для этой группы также достоверно не отличались от исходных значений.
Дозы 20 и 40 мг/сут применялись для лечения больных с высоким и очень высоким риском ССО, для больных с клиническими проявлениями атеросклероза периферических артерий и страдающих СД. Применение розувастатина в дозе 20 мг/сут позволило добиться достоверного снижения уровней ЛПНП на 50,9 %, ОХС – на 36,5 % и ТГ – на 24,8 % (p < 0,01 для всех показателей) и повышения уровня ЛПВП на 8,3 % (p < 0,01). Максимальная доза Мертенила (40 мг/сут) оказала наибольшее воздействие на липидный профиль, снизив уровни ЛПНП на 53,3 %, ОХС – на 38,6 % и ТГ – на 23,9 % (p < 0,05 для всех показателей), а также на повышение уровня ЛПВП на 10,3 % (p < 0,05).
Переносимость и безопасность препарата были удовлетворительными. Побочные эффекты в виде повышения уровней АЛТ и АСТ выше 2 ВПН, но ниже 3 ВПН отмечены у 11 пациентов, получавших розувастатин в дозе 20 мг/сут, и у 1 пациента, принимавшего 40 мг/сут розувастатина, что не потребовало отмены препарата. Появление артралгии имело место у 4 больных, получавших розувастатин в дозе 20 мг/сут, и у 1 пациента, принимавшего 40 мг/сут розувастатина, что не потребовало отмены препарата. Возникновение миалгии без повышения уровня КК выше 5 ВПН отмечали 3 пациента, получавших розувастатин в дозе 20 мг/сут, при этом один из них отметил появление тендовагинита, в связи с чем препарат был отменен.
Прием любой указанной дозы розувастатина не сопровождался повышением уровня креатинина крови и значимым повышением уровня глюкозы крови.
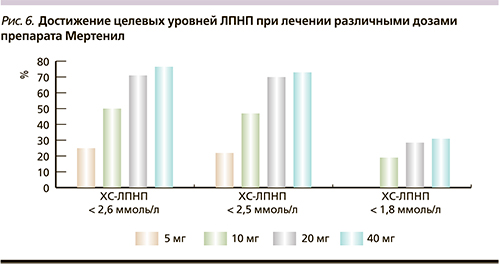
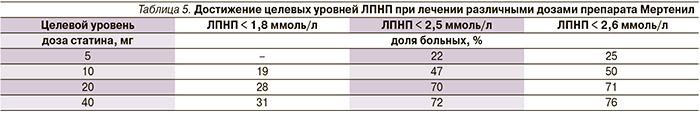
В данном исследовании анализировалось достижение целевого уровня ЛПНП, который, согласно рекомендациям Национального общества по изучению проблем атеросклероза (2012), должен быть ниже 2,5 ммоль/л у больных высокого риска и ниже 1,8 ммоль/л у больных очень высокого риска. Начальная доза Мертенила 5 мг/сут позволила добиться снижения уровня ЛПНП ниже 2,5 ммоль/л 22 % больных, при этом применение максимальной дозы Мертенила (40 мг/сут) способствовало достижению целевого уровня уже 72 % больных (табл. 5, рис. 6).
Достижение целевого уровня ЛПНП ниже 1,8 ммоль/л наблюдалось у меньшего числа пациентов. Оно отмечено у 19 % больных, принимавших 10 мг/сут розувастатина, при этом максимальное число достигших этих значений (31 %) принимали максимально высокую дозу – 40 мг/сут.
Обсуждение
Результаты исследования «от 5 до 40» показали, что часть пациентов, получающих статины, принимают их в довольно низких дозах. Это было отмечено на этапе скрининга при анализе группы больных, получавших статины до включения в исследование. Уровень ЛПНП у них в среднем составлял 3,42 ± 0,80 ммоль/л, несмотря на то что более 50 % пациентов данной группы относились к группе высокого риска. Аналогичные результаты были получены в исследовании DYSIS-RUSSIA, в котором было показано, что существует большой разрыв между рекомендациями профессиональных обществ по диагностике и лечению дислипидемий у больных ИБС и повседневной клинической практикой, а ~3/4 пациентов, получающих статины, имеют резидуальный риск, несмотря на проводимое лечение. «Долечивание» таких пациентов в исследовании «от 5 до 40» привело к дополнительному снижению уровня ЛПНП на 29,8 %, хотя лишь незначительное число больных (около 1,4 %) принимали максимальную дозу розувастатина 40 мг/сут, в то время как основная часть пациентов принимали его в дозах 10 и 20 мг/сут.
Дизайн исследования «от 5 до 40» предполагал врачам поликлиник самостоятельно определять дозы препарата Мертенил. Его результаты показали, что в широкой амбулаторной практике используется полный спектр доз розувастатина. Доза 5 мг/сут применялась преимущественно с целью первичной профилактики больных с умеренным нарушением липидного обмена, не страдающих СД и периферическим атеросклерозом. Несмотря на то что розувастатин уже достаточно долго используется в клинической практике, в настоящее время существует ограниченное число исследований по его применению в дозе 5 мг/сут. Результаты первых 5 небольших плацебо-контролируемых исследований, объединенных в мета-анализ, показали возможность розувастатина в дозе 5 мг/сут снижать уровень ЛПНП на 41,9 % [9]. Последними современными работами являются исследования S. Takagi и соавт. [8] и C. Meek и соавт. [7]. В исследовании S. Takagi и соавт. [8] розувастатин применяли в дозах 2,5–5,0 мг/сут, что позволило снизить содержание ЛПНП на 26,5 %, ОХС – на 18,3 % и ТГ – на 8,9 % и добиться повышения уровня ЛПВП на 12,8 %. В работе C. Meek и соавт. [7] не использовали дозу 2,5 мг, а применение 5 мг/сут розувастатина позволило в большей степени воздействовать на липидный профиль, снизив содержание ЛПНП на 43 %, ОХС – на 31 % и ТГ – на 15 %.

В исследовании «от 5 до 40» мы наблюдали аналогичное снижение уровня ТГ на 14,3 %, и, несмотря на несколько бóльшую степень снижения уровней ЛПНП и ОХС в работе C. Meek и соавт. [7], эти результаты в общем сопоставимы с данными нашего исследования. Имеющиеся различия в степени воздействия на уровни ЛПНП и ОХС, вероятно, связаны с довольно небольшим числом наблюдаемых пациентов в работе C. Meek и соавт. и более высокими уровнями ЛПНП и ОХС исходно. Возможно, определенную роль играет и то, что в исследовании «от 5 до 40» Мертенил в дозе 5 мг/сут назначали с целью первичной профилактики в отличие от исследования C. Meek и соавт., где 41 % больных страдали ИБС и 15 % болели СД. По-видимому, отсутствие «тяжелого заболевания», по мнению пациентов этой группы, и стало причиной того, что около 25 % из них указали в анкете, что не полностью следуют диетическим рекомендациям. Несколько иная картина наблюдалась в других группах пациентов, принимавших Мертенил в дозах 10–40 мг/сут. Из этих пациентов около 8 % не всегда следовали рекомендациям. Прием препарата Мертенил в дозе 10 мг/сут сопровождался снижением уровней ЛПНП на 41,4 %, ОХС – на 30 % и ТГ – на 19,1 %, что сопоставимо с данными, полученными в исследовании STELLAR [10, 11] и работе А. Catapano и соавт., проведенной несколько позже [12]. Гиполипидемическая эффективность доз 20 и 40 мг/сут в исследовании «от 5 до 40» также оказалась сопоставимой с данными, полученными в ранее проведенных исследованиях с аналогичными дозами розувастатина [10–12]. Важным аспектом в лечении больных дислипидемией и ИБС является достижение целевых уровней ЛПНП. В исследовании STELLAR было отмечено преимущество розувастатина перед другими статинами (симвастатином, правастатином и аторвастатином) в достижении целевого уровня ЛПНП ниже 2,6 ммоль/л.
В исследовании «от 5 до 40» нами было проанализировано достижение больными данного целевого уровня ЛПНП и выявлено, что по числу больных, достигших снижения уровня ЛПНП ниже 2,6 ммоль/л, оба эти исследования сопоставимы. Однако спустя некоторое время с момента проведения исследования STELLAR был проведен пересмотр рекомендаций по лечению пациентов с дислипидемиями европейских обществ кардиологов и атеросклероза [14], а также появились рекомендации Российского национального общества по изучению атеросклероза (НОА, 2012) [15]. Учтя этот факт, нами был проведен анализ достижения и других целевых уровней ЛПНП в соответствии с последними рекомендациями НОА. Проведенный анализ показал, что прием препарата Мертенил даже в начальной дозе 5 мг/сут позволяет достигать уровня ЛПНП ниже 2,5 ммоль/л 22 % больных при его исходном уровне около 3,8 ммоль/л. Увеличение дозы Мертенила сопровождалось увеличением числа пациентов, достигших уровня ЛПНП ниже 2,5 ммоль/л, а применение максимальной дозы Мертенила (40 мг/сут) привело к достижению целевого уровня уже 72 % больных при его исходном уровне около 4,93 ммоль/л. Следует отметить, что для больных очень высокого риска в последних рекомендациях медицинских профессиональных сообществ сделан следующий шаг к уменьшению целевого уровня ЛПНП ниже 1,8 ммоль/л. Это произошло после изучения результатов клинических исследований, показавших несомненную пользу такой активной гиполипидемической терапии. Наиболее яркими из них были исследования ASTEROID и SATURN. В исследовании ASTEROID [13] больные атеросклерозом коронарных артерий принимали розувастатин в дозе 40 мг/сут в течение 2 лет. Результаты исследования показали, что снижение уровня ЛПНП менее 1,8 ммоль/л при терапии розувастатином привело к статистически значимому регрессу атеросклеротической бляшки. Аналогичные результаты были получены и в исследовании SATURN [16], в котором терапия розувастатином в дозе 40 мг/сут в течение 2 лет также способствовала уменьшению объема атеросклеротического поражения коронарных артерий. Довольно важным моментом является то, что применение такой интенсивной гиполипидемической терапии в обоих исследованиях на протяжении 2 лет сочеталось с вполне приемлемым профилем безопасности. В исследовании «от 5 до 40» нами были также получены данные, свидетельствующие о хорошей переносимости и безопасности розувастатина для всех используемых доз.
Таким образом, применение препарата Мертенил (розувастатин) компании «Гедеон Рихтер» в исследовании «от 5 до 40» с целью первичной и вторичной профилактики сопровождалось дополнительным снижением уровня ЛПНП у пациентов, находившихся ранее на терапии другими статинами. Терапия Мертенилом в средних и максимальных дозах обладает хорошим профилем безопасности и сопровождается высокой частотой достижения целевых уровней ЛПНП больными очень высокого риска с более выраженным нарушением липидного обмена, что в итоге приводит к уменьшению риска ССО.



