Актуальность адекватного лечения стабильной стенокардии можно проиллюстрировать двумя положениями:
Словами, сказанными Д.Д. Плетневым в сентябре 1932 г. в Берлинском медицинском обществе: «Сущность грудной жабы как клинического синдрома сводится к двум основным пунктам: боль и смерть… Правилом можно считать положение, что каждый припадок грудной жабы может быть последним. Грозность и сплошь и рядом внезапность припадка, его распространенность во всех странах в достаточной мере объясняют тот интерес к этому синдрому, который существует во всем мире».
Данными Göteborg Primary Pre-vention Study: наличие болей в грудной клетке значимо увеличивает риск смертельных осложнений, особенно если они носят характер типичных стенокардических и если они имеют место у пациентов, ранее перенесших инфаркт миокарда (ИМ) [1].
В соответствии с современными рекомендациями [2, 3] по ведению пациентов со стабильной ишемической болезнью сердца (ИБС) выделяют два новых, равных по своей значимости направления лечения:
- Мероприятия, направленные на улучшение прогноза.
- Мероприятия, направленные на уменьшение частоты и выраженности приступов стенокардии и/или эпизодов ишемии, на улучшение качества жизни.
Подходы к решению этих задач хорошо отработаны:
- меры, направленные на коррекцию образа жизни;
- своевременное и соответствующее хирургическое лечение;
- назначение четырех групп препаратов, снижающих сердечно-сосудистую заболеваемость и смертность (антиагреганты, статины, ингибиторы ангиотензинпревращающего фермента [иАПФ] и β-адреноблокаторы [БАБ] лицам, перенесшим ИМ);
- адекватное назначение антиангинальных и противоишемических препаратов (БАБ, ивабрадин, антагонисты кальция [AK], нитраты, миокардиальные цитопротекторы и др.).
Немедикаментозные мероприятия, направленные на изменение образа жизни пациента:
- прекращение курения самим пациентом и всемерное уменьшение воздействия дыма из окружающего воздуха (пассивное курение);
- физическая нагрузка: следует рекомендовать пациентам умеренные аэробные физические нагрузки (ходьба, бег или плавание) не менее 30 минут 7 дней (минимум 5 дней) в неделю;
- правильное питание: рекомендована диета, содержащая много фруктов, овощей, продуктов с низким содержанием животных жиров, увеличение употребления омега-3 ненасыщенных жирных кислот;
- поддержание нормального веса (индекс массы тела – 18,5–24,9 кг/м2) и окружности талии.
Хирургические методы лечения
Для улучшения прогноза пациентам проводят аортокоронарное шунтирование (АКШ). С целью снижения выраженности ишемии, стенокардии выполняют АКШ и операции чрескожной транслюминальной ангиопластики (ЧТКА). При этом АКШ рекомендовано при неэффективности максимальной медикаментозной терапии. Следует также помнить, что, поскольку ЧТКА не улучшает прогноз, а лишь в большей степени, чем медикаментозная терапия, в течение первых трех лет снижает частоту приступов стенокардии и улучшает качество жизни, пациенту должна быть предоставлена вся информация о риске и возможной пользе для самостоятельного выбора типа лечения.
Медикаментозные подходы, направленные на улучшение прогноза
Дезагреганты – ацетилсалициловая кислота 75–165 мг, либо двойная дезагрегантная терапия – ацетилсалициловая кислота + клопидогрел 75 мг, либо тикагрелор или прасугрел в течение 12 месяцев после острого коронарного синдрома. При мерцательной аритмии – антикоагулянт варфарин (до достижения МНО 2–3).
Статины – на неопределенно долгий срок (целевые значения общего холестерина < 4 ммоль/л, липопротеидов низкой плотности < 2 ммоль/л).
ИАПФ – при артериальной гипертензии, низкой фракции выброса (менее 40 %), сахарном диабете, а также всем другим пациентам, страдающим ИБС (периндоприл 10 мг и рамиприл 10 мг – основанием являются результаты исследований EUROPE и HOPE [4, 5].
БАБ – в основном липофильные, назначаемые перенесшим ИМ (до трех лет).
Необходим также контроль состояний, способствующих прогрессированию атеросклеротического процесса:
- контроль нарушений углеводного обмена – снижение уровня гликированного гемоглобина < 7 ммоль/л, не допуская эпизодов гипогликемии;
- контроль уровня артериального давления (АД) от 140/90 до 130/80 мм рт. ст. Антигипертензивными препаратами первого выбора являются используемые также с целью антиангинальной терапии БАБ, АК и т. д.
Мероприятия, направленные на уменьшение частоты и выраженности ишемии и стенокардии
Цель антиангинальной терапии – уменьшение частоты и тяжести приступов стенокардии, возвращение к нормальной двигательной активности (в идеале снижение тяжести стенокардии до 1 функционального класса) при сохранении высокого качества жизни.
Таким образом, эффективность антиангинальной терапии следует оценивать по снижению количества приступов болей и принятых таблеток короткодействующего нитроглицерина, а также с помощью объективных методов оценки ишемических изменений, к которым относят регистрацию ЭКГ, локальной сократимости миокарда или его перфузии при нагрузочных тестах. Противоишемическую эффективность лечения можно также оценивать по выраженности возникающих ишемических изменений (депрессий сегмента ST на ЭКГ) или увеличению времени нагрузки, при которой возникают эти изменения.
В настоящее время рассматривают три основных похода к уменьшению выраженности ишемии миокарда и стенокардии, используя при решении этих задач различные хирургические и медикаментозные подходы:
- увеличение доставки кислорода с кровью (хирургическая коррекция, вазодилататоры – нитраты и АК);
- снижение потребности миокарда в кислороде (БАБ, АК, ивабрадин, иАПФ);
- защита миокарда с помощью препаратов, предотвращающих метаболические последствия ишемии (главным образом речь идет о триметазидине).
Медикаментозные подходы, направленные на увеличение кровотока
В первую очередь речь идет о нитратах.
Действие нитратов при стенокардии обусловлено следующими механизмами:
Влияние на коронарные сосуды, сопротивление которых снижается, в т. ч. и в стенозированнной области. Оксид азота (NO), донатором которого являются нитраты, стимулирует гуанилатциклазу и увеличивает уровень цГМФ, что в конечном итоге приводит к снижению внутриклеточной концентрации свободных ионов кальция. Это приводит к дополнительному снижению тонуса сосудов. Тем самым обеспечивается увеличение коронарного кровотока, коллатерального кровотока, улучшение перфузии субэндокардиальных слоев миокарда.
Расширение посткапиллярных емкостных сосудов, снижение венозного возврата (уменьшение преднагрузки). Это приводит к уменьшению конечно-диастолического и конечно-систолического давления в левом желудочке и улучшению насосной функции сердца. Кроме того, снижается тонус артериол, что уменьшает постнагрузку.
Снижение потребности миокарда в кислороде.
Положительные свойства нитратов не ограничиваются их сосудорасширяющими свойствами: было показано, что NO может оказывать антиагрегантный эффект, предотвращать адгезию лейкоцитов на поверхности эндотелиальных клеток за счет ингибирования адгезионных молекул и тем самым уменьшать окислительный стресс, повреждающий эндотелий сосудов. NO ингибирует пролиферацию гладкомышечных клеток, что играет ключевую роль в поддержании величины просвета артерий при ИБС.
Для купирования приступов стенокардии используют короткодействующие формы нитратов, в основном нитроглицерин в виде таблеток, растворов, мази, аэрозоля, пластыря.
Препараты для профилактики приступов стенокардии и ишемии содержат пролонгированные формы нитроглицерина, изосорбида динитрат и изосорбида мононитрат.
При длительном назначении нитратов к одной из основных проблем относится развитие толерантности к ним, что требует строгого соблюдения следующих правил:
- короткодействующие нитраты применяют только для купирования болей;
- препараты со средней и большой продолжительностью действия используют для профилактики приступов стенокардии, возникающих многократно в течение дня;
- динитраты назначают 1–3 раза в день, оставляя «свободный» от нитратов период времени в течение 6–8 часов;
- пролонгированные мононитраты чаще назначают 1 раз в день; при необходимости их назначения 2 раза в день должен быть соблюден принцип «асимметричного» или «эксцентрического» приема – утром и днем или днем и вечером.
Медикаментозные подходы, направленные на снижение потребности миокарда в кислороде
Наряду со снижением АД достижение целевых значений частоты сердечных сокращений (ЧСС; 50–60 ударов в 1 минуту) является одной из наиболее важных составляющих успешного лечения пациентов со стенокардией.
С этой целью используют три группы препаратов: БАБ, недигидропиридиновые АК (верапамил, дилтиазем) и блокаторы f-каналов (ивабрадин) [6].
Механизм антиангинального действия БАБ при стенокардии включает:
- уменьшение ЧСС и АД в покое и при нагрузке;
- уменьшение сократимости миокарда;
- уменьшение возбудимости миокарда;
- уменьшение потребности миокарда в кислороде.
БАБ являются препаратом выбора при сочетании стенокардии с артериальной гипертензией, суправентрикулярными нарушениями ритма, нагрузочными желудочковыми нарушениями ритма, постинфарктным кардиосклерозом, мигренями, тремором. Четыре БАБ рекомендовано в качестве лечения больных с сердечной недостаточностью: метопролола сукцинат пролонгированного действия, бисопролол, карведилол, небиволол.
Механизм антиангинального действия АК обусловлен снижением транспорта ионов кальция через кальциевые каналы L-типа и уменьшением содержания внутриклеточного Са2+. Это приводит к снижению тонуса артериол, общего периферического сопротивления сосудов и как следствие – к уменьшению постнагрузки, снижению АД. За счет вазодилатирующего действия увеличивается коронарный кровоток, уменьшается спазм коронарных артерий при вариантной стенокардии. АК усиливают продукцию NO, улучшают эндотелиальную функцию, уменьшают агрегацию тромбоцитов, клеточную пролиферацию, кальцификацию и атерогенез сосудов. Кроме того, верапамил и дилтиазем уменьшают ЧСС, замедляют проведение в атриовентрикулярном узле и возбудимость миокарда, тем самым снижая потребность миокарда в кислороде.
В исследовании APSIS [7] показано, что лица, перенесшие ИМ, при лечении верапамилом пролонгированного действия имеют такой же прогноз, как при терапии метопролола сукцинатом.
Ивабрадин является первым препаратом блокаторов f-каналов – нового класса лекарственных средств лечения стенокардии. Механизм его отрицательного хронотропного действия обусловлен ингибированием f-каналов, которые находятся в основном в пейсмекерных клетках синусного узла. Вследствие этого уменьшается угол наклона спонтанной диастолической деполяризации, очередной потенциал действия возникает позднее и тем самым уменьшается ЧСС. Антиангинальный и противоишемический эффекты ивабрадина сравнимы с таковыми БАБ и АК.
Принципиальное отличие ивабрадина от других антиангинальных препаратов с отрицательным хронотропным эффектом заключено в отсутствии влияния на центральную гемодинамику, т. е. он может быть с успехом использован в тех ситуациях, когда назначение БАБ и АК невозможно, например, пациентам с гипотонией, бронхиальной астмой или перемежающейся хромотой.
Антиангинальный эффект ивабрадина обусловлен не только снижением ЧСС. В отличие от БАБ, при использовании которых на нагрузке происходит сужение просвета коронарных артерий за счет относительной β-агонистической активности, ивабрадин сохраняет коронарный кровоток и поддерживает нормальную реакцию коронарных сосудов (вазодилатацию) в ответ на физическую нагрузку.
Таким образом, антиангинальный эффект ивабрадина обеспечивается двумя механизмами: с одной стороны, он обусловлен снижением ЧСС и, следовательно, уменьшением потребности в кислороде, с другой – поддержанием коронарного кровотока во время нагрузки.
Начиная терапию ивабрадином с приема препарата по 5 мг 2 раза в сутки, необходимо своевременно титровать дозу до 7,5 мг 2 раза в сутки.
Частичные ингибиторы окисления жирных кислот (цитопротекторы)
Еще одним направлением в лечении пациентов со стабильной стенокардией является применение цитопротекторов [8]. К настоящему времени по этому показанию, по сути, используют лишь один препарат – триметазидин, который в множестве исследований продемонстрировал достоверный антиангинальный эффект. Мета-анализ, проведенный N. Danchin и соавт. [9], свидетельствует, что триметазидин по антиангинальной и противоишемической эффективности не отличается от других препаратов, используемых при стенокардии.
В июне 2012 г. Европейское агентство по контролю за применением лекарственных препаратов (EMEA), рассмотрев полное досье на триметазидин, пришло к заключению, что преимущества этого препарата существенно превышают возможный риск. Его применение рекомендовано к лечению стенокардии в монотерапии или в комбинации с любыми другими антиангинальными препаратами. Триметазидин не влияет на гемодинамические параметры, может быть с успехом использован в тех случаях, когда применение традиционных препаратов с гемодинамическим действием ограниченно, например при исходной брадикардии, нарушениях атриовентрикулярного проведения, низких значениях АД, а также при гемодинамически значимых стенозах клапанов, хронической обструктивной болезни легких, перемежающейся хромоте и т. д.
Антиишемическое и, соответственно, антиангинальное действия триметазидина [10–12] обусловлены частичным ингибированием окисления длинноцепочечных жирных кислот в митохондриях за счет селективного подавления конечного фермента в цикле β-окисления – длинноцепочечной 3-кетоацил-КоА-тиолазы, и восстановлением нарушенного ишемией сопряжения гликолиза и окисления пирувата в митохондриях. Это позволяет сердцу лучше (оптимальнее) использовать недостаточное в условиях ишемии количество кислорода и продолжать синтезировать АТФ, необходый для нормального функционирования клетки. Именно этот механизм препятствует возникновению клеточного ацидоза и накоплению недоокисленных жирных кислот, лактата и кислых эквивалентов, которые и являются отчасти причиной возникновения ангинозной боли. Таким образом, предотвращение боли (самого позднего в ишемическом каскаде проявления) происходит при использовании триметазидина на самых первых этапах ишемии – на уровне нарушения метаболизма, что не позволяет развиваться и более поздним изменениям: нарушениям сократимости миокарда, ишемическим изменениям на ЭКГ, боли.
Кроме того, положительное действие препарата может быть обусловлено подавлением агрегации тромбоцитов, улучшением реологических свойств крови. Триметазидин ингибирует движение нейтрофилов к очагу воспаления в зоне некроза кардио-миоцитов. Это предупреждает образование чрезмерного количества радикалов кислорода, способных увеличивать зону поражения за счет индукции апоптоза и/или некроза кардиомиоцитов. Другой механизм, с помощью которого триметазидин предотвращает гибель клеток, заключен в способности препарата закрывать мегапору, формирующуюся в митохондриях при ишемии/реперфузии [13].
Другие антиангинальные препараты
Механизм антиангинального действия препарата никорандил обусловлен главным образом его способностью открывать АТФ-зависимые калиевые каналы. Возникающая при этом гиперполяризация плазматической мембраны приводит к торможению открытия потенциал-регулируемых медленных кальциевых каналов, что сопровождается снижением поступления кальция в цитоплазму гладкомышечных клеток и выхода кальция из саркоплазматического ретикулума. В результате уменьшается тонус сосудов. Никорандил является донором NO, вследствие чего также оказывает нитратоподобное действие. Препарат практически не изменяет ЧСС, сократимость миокарда, но может вызывать некоторое снижение АД, особенно в ортостатическом положении. В целом никорандил хорошо сочетается с любыми другими антиангинальными препаратами. Важной его особенностью является способность не только предупреждать приступы стенокардии (в дозе 10–20 мг 1–3 раза в сутки), но и купировать приступы стенокардии (в течение 4–17 минут) при приеме под язык.
Никорандил в сочетании с любыми антиангинальными средствами улучшает прогноз пациентов с ИБС и стабильной стенокардией (исследование IONA): на 17 % снижает риск смерти от ИБС, нефатального ИМ и внеплановой госпитализации в связи с сердечной болью, на 21 % снижает риск возникновения острого коронарного синдрома (смерть от ИБС, нефатальный ИМ, нестабильная стенокардия) [14].
В качестве антиангинального средства к применению разрешен и препарат ранолазин. Показано, что помимо частичного ингибирования окисления жирных кислот в митохондриях ранолазин обладает способностью блокировать поздний натриевый ток. Препарат удлиняет интервал QT, в связи с чем необходимы контроль ЭКГ и определенная осторожность при применении.
Комбинированное назначение антиангинальных препаратов
Как показывают исследования, проведенные в последние годы в России, около 75 % пациентов со стенокардией получают комбинированную антиангинальную терапию. Несмотря на это, частота приступов болей у них остается высокой – в среднем до 7–10 в неделю [15, 16]. По данным исследования TIBBS [17], пациенты с частотой приступов стенокардии более 2 раз в неделю имеют значимо худший прогноз, чем при их меньшей частоте. Установлено, что приступы стенокардии с частотой ≥ 1 в неделю ассоциированы с увеличением 5-летнего риска наступления смерти на 27 %, развития ИМ – на 21 % [18]. Несомненными причинами столь неадекватного лечения является, с одной стороны, отсутствие должного контроля АД и ЧСС, с другой – нерациональное комбинирование антиангинальных препаратов.
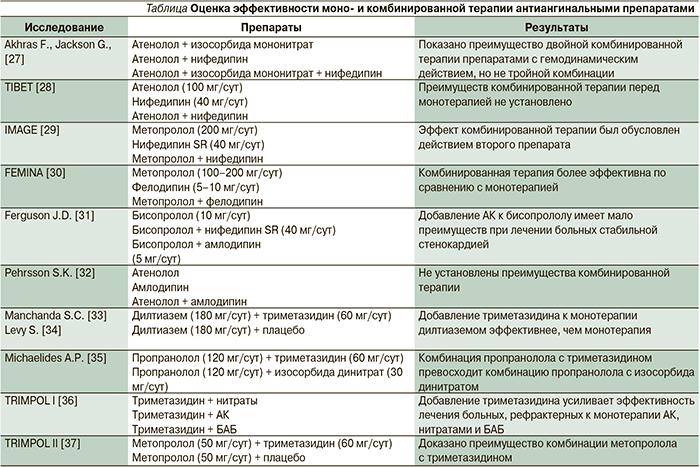
В то же время результаты исследования ПРЕМЬЕРА отчетливо свидетельствуют, что коррекция АД приводит к значимому снижению частоты приступов стенокардии [20]. В исследовании ЛИНКОР [21] также показано, что коррекция АД и ЧСС приводит к значимому снижению частоты приступов стенокардии (рис. 1).
Таким образом, для улучшения ситуации с лечением больных стабильной стенокардией должны быть предприняты усилия по достижению в ходе терапии целевых значений АД и ЧСС. Следует подчеркнуть, что повышенная ЧСС отчетливо связана с частотой и тяжестью приступов стенокардии и является независимым предиктором неблагоприятных исходов для различных категорий пациентов, страдающих ИБС [22].
С целью достижения целевой ЧСС необходимо использовать адекватные дозы препаратов с отрицательным хронотропным эффектом и шире использовать комбинацию БАБ с ивабрадином. В настоящее время имеется достаточно большое число исследований, свидетельствующих о том, что именно эта комбинация обеспечивает более выраженный антиангинальный и противоишемический эффекты.
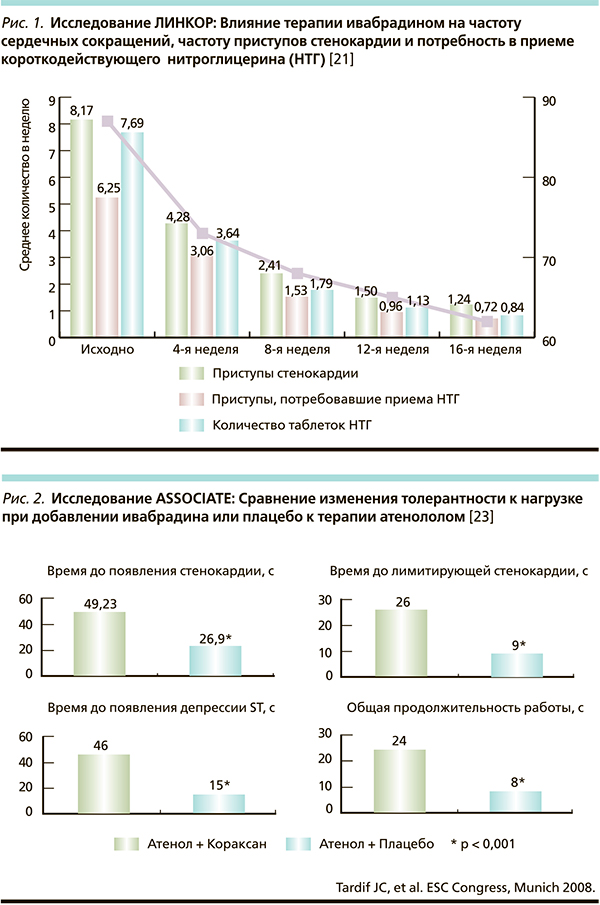
Так, в исследовании ASSOCIATE [23] показано, что при проведении комбинированной терапии атенололом и ивабрадином в 2 раза по сравнению с применением одного БАБ увеличивалось время до появления стенокардии во время физической нагрузки и в 3 раза – время до появления лимитирующей стенокарлии, до появления депрессий ST и общее время нагрузки (рис. 2).
В исследовании КОНТРОЛЬ [24] добавление ивабрадина к терапии БАБ приводило к 56 %-ному уменьшению числа пациентов, имевших 3 приступа стенокардии и более в неделю.
В программе ЛИНКОР показано, что добавление ивабрадина к терапии пациентов, перенесших ИМ менее 12 месяцев назад, значимо увеличивало число больных, которые переставали испытывать приступы стенокардии, и уменьшало число пациентов, вызывавших скорую медицинскую помощи (с 35,6 до 1,5 %) и госпитализированных (с 15,4 до 1,2 %) [21].
Аналогичные данные были получены в исследовании ADDITIONS (2330 пациентов со стабильной стенокардией), в котором добавление ивабрадина к БАБ не только значимо снижало частоту приступов стенокардии и улучшало качество жизни пациентов, но и в 2,4 раза увеличивало число больных с I функциональным классом стенокардии [25].
Несомненно, что рациональность комбинирования любых классов препаратов определяется эффективностью и безопасностью выбранной комбинации, а также конкретной клинической ситуацией. Принципиально разный механизм действия ивабрадина и БАБ позволяет сочетать эти препараты с высокой эффективностью. Ивабрадин напрямую связывается с белком f-канала и закрывает его, как «пробка закрывает горлышко бутылки», в то время как БАБ снижают уровень сАМР и его модифицирующее влияние на структуру белка f-канала [6].
С точки зрения безопасности комбинация также является рациональной, т. к. ивабрадин с высокой избирательностью действует на f-каналы, не влияя на другие виды ионных каналов, и не оказывает в терапевтических дозах влияния на сократимость и проводимость миокарда [6]. В исследовании КОНТРОЛЬ-2 показано, что добавление ивабрадина к терапии БАБ позволяет достигать более выраженного антиангинального эффекта, чем при титрации доз БАБ [26].
В то же время, как показывает большинство исследований (см. таблицу), при комбинировании БАБ с АК дигидропиридинового ряда антиангинальная и противоишемическая эффективность не меняется или увеличивается по сравнению с монотерапией лишь незначительно [27–32]. Комбинация БАБ с АК недигидропиридинового ряда нецелесообразна из-за возможного увеличения числа нежелательных реакций в виде чрезмерного замедления атриовентрикулярной проводимости и снижения сократимости миокарда.
Следующим вариантом рациональных комбинаций является добавление к терапии препаратами с гемодинамическим действием лекарственных средств, оказывающих влияние на метаболизм миокарда, т. к. подобное сочетание дает более выраженный антиангинальный эффект. При недостаточной эффективности БАБ в монотерапии или в комбинации с ивабрадином или АК целесообразно добавлять к лечению триметазидин, т. к. получение более выраженного антиангинального эффекта обусловлено влиянием на разные звенья патогенеза ишемического повреждения миокарда. Целесообразность таких комбинаций доказана во многих исследованиях [33–37], в т. ч. и российских (ПЕРСПЕКТИВА, ПАРАЛЛЕЛЬ, ПРИМА) [16, 38, 39]. Так, в исследовании ПАРАЛЛЕЛЬ [38] показано, что добавление триметазидина в большей степени, чем добавление ивабрадина, снижает частоту приступов стенокардии и потребность в нитроглицерине. При этом почти в 2 раза больше пациентов улучшили функциональный класс стенокардии (33 против 19 %) и в 3 раза больше больных достигли ее I функционального класса.
Аналогичные данные по положительному антиангинальному действию триметазидина получены в исследовании ПЕРСПЕКТИВА [16]. Следует подчеркнуть, что у пациентов, получающих комбинированную терапию БАБ с триметазидином, в достоверно большей степени улучшается качество жизни, в т. ч. и удовлетворенность качеством терапии, чем у больных, получающих комбинированную терапию БАБ с нитратом [38]. Следует отметить, что улучшение качества жизни может обеспечивать пациентам и лучший прогноз [40], меньшие частоту госпитализаций и смертность в течение ближайшего года.
К сожалению, большинство российских врачей продолжают использовать в качестве комбинированной терапии комбинации нескольких препаратов с гемодинамическим действием, несмотря на то что многие исследования показывают малую эффективность таких комбинаций. Так, по данным исследования ПЕРСПЕКТИВА [16], при двойной комбинации в 71 % случаев используется комбинация БАБ с нитратами и лишь в 1 % случаев – комбинация БАБ с ивабрадином, а в 4 % – БАБ с метаболическими цитопротекторами. При тройной комбинации в 55 % случаев комбинируют БАБ с нитратами и АК, нитраты присутствуют в терапии в 94 % случаев, тогда как ивабрадин – в 9 % и метаболическая терапия – в 37 %.
Таким образом, в реальной практике существуют много высокоэффективных антиангинальных препаратов и возможность их комбинированного использования. Для повышения эффективности лечения следует лишь более четко следовать существующим рекомендациям и шире внедрять в свою практическую деятельность подходы, разработанные благодаря проведенным качественным научным исследованиям.


