При назначении психотропных препаратов (ПТП) кормящим грудью женщинам следует тщательно взвешивать пользу и потенциальные риски. Польза грудного вскармливания (ГВ) для детей первых месяцев жизни доказана. У детей, находящихся на ГВ, ниже риск заболеваемости (снижение риска желудочнокишечных, респираторных и мочевых инфекций, сепсиса, менингита, некротизирующего энтероколита, улучшение нейрокогнитивного развития) и смертности. Кроме того, дети и подростки, получавшие кормление грудью, реже страдают бронхиальной астмой, воспалительными заболеваниями кишечника, сахарным диабетом, злокачественными заболеваниями крови и ожирением [1]. ГВ также полезно для здоровья матери. Кроме того, тесный контакт между матерью и ребенком в момент кормления способствует установлению их взаимной привязанности. ВОЗ рекомендует ГВ в течение 6 месяцев всем детям, которые могут получать его [2]. Кормящих грудью женщин необходимо подробно проинформировать о пользе и рисках, связанных с фармакотерапией и нелеченым заболеванием. На начальной стадии фармакотерапии необходим тщательный мониторинг симптомов заболевания у матери. Детей нужно обследовать до назначения лекарственных средств (ЛС) матери. В период лечения они должны находиться под наблюдением педиатра, которому следует тщательно следить за ростом и весом ребенка. Терапию рекомендуется начинать с минимальной эффективной дозы препарата с последующим ее постепенным повышением. Предпочтение следует отдавать монотерапии. Для снижения риска развития нежелательных эффектов у ребенка (снижения концентраций в момент очередного кормления) принимать ПТП рекомендуется сразу после кормления [3].
При выборе конкретного ЛС необходимо учитывать опыт его применения в индивидуальном и семейном анамнезе, наличие других заболеваний у женщины и прием других ЛС, наличие у нее аллергий, побочные эффекты ПТП и пожелания самой женщины. Если женщина принимала препарат во время гестации, его смена в послеродовом периоде в связи с высоким риском рецидива и развития послеродового психоза не желательна. Предпочтение следует по возможности отдавать наиболее хорошо изученным препаратам. ПТП, профиль безопасности которых в период ГВ не определен, указаны в табл. 1.

Безопасной для ребенка принято считать суточную дозу (рассчитанную на основании дозы матери и уровня препарата в молоке), составляющую не более 10 % от терапевтической дозы, рекомендуемой детям, или от взрослой дозы, стандартизованной на кг массы тела [5]. Следует помнить, что наряду с физико-химическими свойствами препарата на выделение ЛС с молоком матери могут повлиять полиморфизм изоферментов печени, гипоальбуминемия у матери и прием других ЛС, включая растительные.
Безопасность антидепрессантов
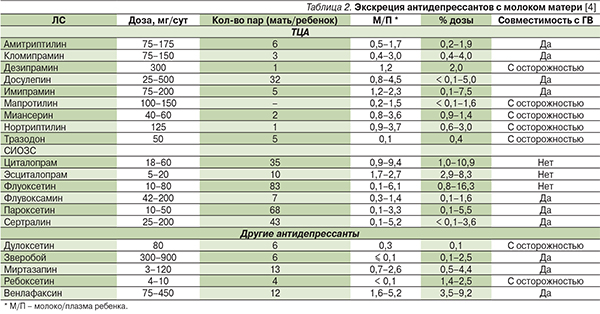
Большинство антидепрессантов выделяется с молоком матери в небольших количествах [6]. Среди селективных ингибиторов обратного захвата серотонина (СИОЗС) наиболее высокие концентрации в молоке создает флуоксетин (5–9 % от дозы, получаемой матерью) [6]. Цитолапрам может создавать высокие концентрации в крови у отдельных детей, особенно в случае приема матерью высокой дозы или потребления ребенком большого количества молока [7]. Сертралин, пароксетин и флувоксамин создают очень низкие или неопределяемые концентрации в молоке. Доза, поступающая в организм ребенка при приеме кормящей матерью сертралина, пароксетина и флувоксамина, составляет 0,3–0,5 от материнской дозы, флуоксетина и циталопрама – 1–6 [8]. Сертралин определяется в молоке только в случае, если суточная доза препарата у матери составляет 100 мг или более [9]. Максимальные концентрации сертралина и его метаболита десметилсертралина в молоке определяются через 8–9 часов после приема препарата матерью [9]. Небольшие исследования показали, что низкие концентрации в молоке и очень низкие в сыворотке крови детей создаются при применении флувоксамина [8]. Концентрации венлафаксина и его метаболита, создаваемые в молоке и сыворотке крови ребенка, подвержены значительным вариациям [10, 11]. В большинстве исследований они были низкими, однако в одном исследовании уровень венлафаксина и его метаболита в молоке составил 9,2 % от дозы, принятой матерью [11]. Данные о проникновении в грудное молоко других антидепрессантов представлены в табл. 2.
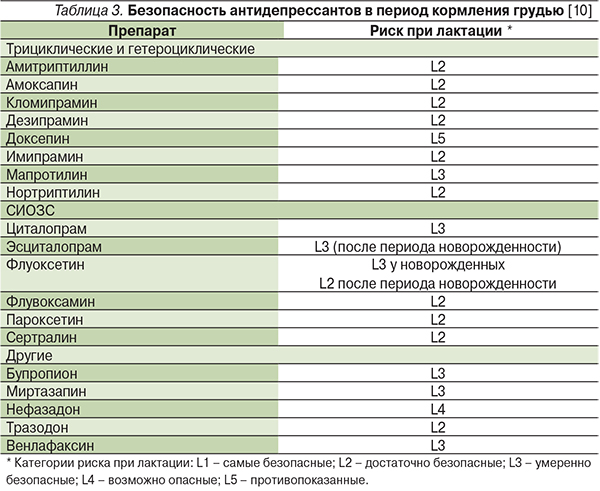
Распределение антидепрессантов по категориям риска при лактации (США) представлено в табл. 3.
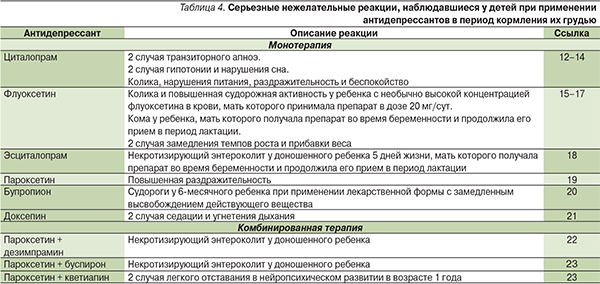
Побочные эффекты СИОЗС у ребенка, находящегося на ГВ, развиваются редко и, как правило, носят нетяжелый характер. Единичные случаи серьезных нежелательных реакций, описанные при их применении, суммированы в табл. 4. Сообщений о развитии серьезных реакций у ребенка при лечении кормящих грудью женщин сертралином и широко применяемыми трициклическими антидепрессантами (ТЦА; имипрамин, нортриптилин, дезипрамин и кломипрамин) нет. Безопасность венлафаксина в период лактации изучена недостаточно. В трех исследованиях, суммарно включивших 12 грудных детей, побочных реакций отмечено не было [11].
В целом большой опыт применения антидепрессантов из групп ТЦА и СИОЗС кормящими грудью женщинкми свидетельствует об их хорошей переносимости детьми и достаточно высокой безопасности. Однако данные недавно проведенного исследования, в котором 8 женщин принимали СИОЗС, позволяют предположить, что препараты этой группы могут способствовать задержке лактации. Этот риск при приеме СИОЗС оказался в 2 раза выше, чем у родильниц, не принимавших их. Среднее время появления молока у женщин, получавших СИОЗС, составило 96 часов после родов (при норме до 72 часов) [24]. Угнетение секреции молока и ускорение инволюции молочной железы под влиянием препаратов этой группы подтверждаются и результатами экспериментальных исследований [25].
Таким образом, применение антидепрессантов групп ТЦА и СИОЗС в период лактации представляется достаточно безопасным. Женщинам, ранее не принимавшим антидепрессанты, в качестве препаратов первого выбора рекомендуют пароксетин или сертралин, создающие низкие концентрации в молоке матери и сыворотке ребенка и ассоциирующиеся с небольшим количеством побочных эффектов [5]. Флуоксетин не рассматривается в качестве препарата выбора при лактации из-за длительного периода полувыведения (особенно активного метаболита), способствующего кумуляции в сыворотке крови новорожденного. Его рекомендуют применять только женщинам, принимавшим этот препарат во время беременности с хорошим терапевтическим ответом.
Те же предосторожности следует соблюдать в отношении высоких доз циталопрама, создающего высокие концентрации в грудном молоке и плазме крови ребенка. ТЦА могут рассматриваться в качестве препарата выбора для женщин, успешно применявших их для лечения предыдущих эпизодов депрессии в отсутствие противопоказаний, включая суицидальные мысли. В группе ТЦА наиболее хорошо изученными и безопасными препаратами считаются нортриптилин и имипрамин, создающие неопределяемые уровни в сыворотке крови ребенка [26]. В период кормления грудью не рекомендуется применение доксепина из-за его выраженных седативных свойств и наличия метаболита с длительным периодом полувыведения. Его применение ассоциировалось с седацией и угнетением дыхания [21]. Кроме того, при его использовании повышается риск развития гипербилирубинемии у детей [27].
Безопасность антипсихотиков
Сведения о выделении антипсихотиков с грудным молоком и их совместимости с ГВ представлены в табл. 5, распределение по категориям риска при лактации – в табл. 6, побочные эффекты, описанные у детей, получавших их с молоком матери, – в табл. 7.
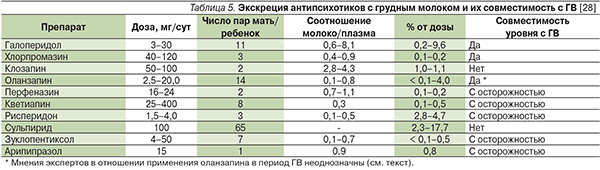
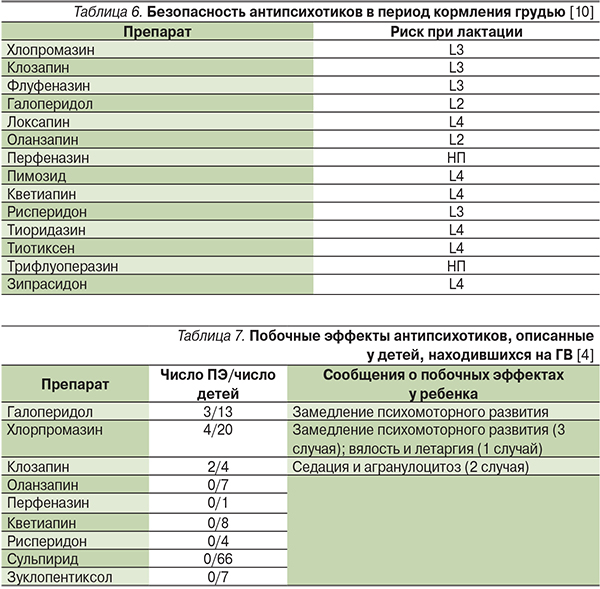
Анализ данных детей, матери которых получали антипсихотики первого поколения в период кормления грудью, в целом свидетельствуют об их хорошей переносимости, хотя описаны отдельные случаи патологической сонливости [4]. При хроническом применении кормящей матерью препаратов с длительным периодом полувыведения (например, хлорпромазина и флуфеназина) возможна их кумуляция в сыворотке крови ребенка, что диктует необходимость тщательного мониторирования симптомов седации и других потенциальных побочных эффектов у детей. В классификации безопасности применения в период кормления грудью хлорпромазин и флуфеназин отнесены к категории L3 (умеренно безопасные), тиоридазин – L4 (возможно опасные), галоперидол – L2 (достаточно безопасные).
Атипичные антипсихотики также выделяются с молоком кормящей матери в небольшом количестве (табл. 10). В частности, доза оланзапина, поступающая в организм ребенка, находящегося на ГВ, составляет менее 1 % от материнской [29, 30]. Однако регулярное поступление препарата с грудным молоком в первые 4 месяца жизни может приводить к его кумуляции в плазме крови ребенка, по-видимому, в связи с незрелостью изоферментов печени, особенно CYP1A2 [31]. В последующие месяцы концентрации оланзапина в плазме ребенка снижаются вплоть до неопределяемого уровня. Имеются единичные сообщения о нежелательных эффектах у детей, матери которых получали оланзапин во время кормления грудью, однако их причинно-следственная связь с применением препарата не установлена. У одного ребенка, подвергшегося воздействию оланзапина внутриутробно и в период ГВ, описаны кардиомегалия, желтуха и седация. В то же время есть данные о хорошей переносимости оланзапина детьми, в т. ч. с высоким уровнем препарата в крови [31]. Тем не менее, согласно результатам систематического обзора, риск от применения оланзапина в период лактации может превышать пользу [32]. Мнения экспертов в отношении безопасности применения оланзапина в период ГВ расходятся. Авторы систематического обзора рекомендуют прекращение кормления грудью в период лечения этим препаратом [32]. В классификации безопасности при лактации он отнесен к категории L2 (достаточно безопасные). Американская академия педиатрии не дает оценку безопасности этого препарата в период ГВ [33].
Есть данные о повышенном риске развития экстрапирамидных расстройств у детей, получавших рисперидон с грудным молоком, в связи с чем авторы систематического обзора не рекомендуют кормление грудью в период его применения [32].
Кветиапин также создает низкие концентрации в молоке, которые слишком малы для того, чтобы оказывать существенный фармакологический эффект [23]. Сообщений о развитии нежелательных эффектов у детей, находящихся на грудном вскармливании при монотероапии этим препаратом не опубликовано. В 6 случаях его применения (от 25 мг дo 400 мг/сут) в комбинации с антидепрессантами из группы СИОЗС у одного ребенка развилось легкое отставание в моторном и психическом развитии и одного – в психическом развитии, однако авторы считают, что эти осложнения не были связаны с применением препарата [23]. Концентрации кветиапина в молоке коррелировали с дозой препарата и колебались от неопределяемых до 264 нг/мл (при приеме матерью 400 мг/сут). Дозы препарата, которые дети получили с молоком, составили от 0,01 до 0,1 мг/кг/сут.
Клозапин способен концентрироваться в молоке матери [34]. Соотношение молоко/плазма для этого препарата составляет 2,8–4/3. Dev и Krupp проследили четырех детей, матери которых принимали клозапин во время кормления грудью [35]. У одного из них наблюдалась повышенная сонливость, у другого развился агранулоцитоз, который саморазрешился после отмены препарата, у двух детей побочные эффекты отсутствовали. Есть одно сообщение об отставании в речевом развитии ребенка, мать которого принимала препарат на протяжении беременности и во время кормления грудью [36]. С учетом способности клозапина накапливаться в молоке при длительном применении, а также риска серьезных побочных эффектов у новорожденных, включая судороги и агранулоцитоз, его применение в период кормления грудью абсолютно противопоказано [3, 32, 37].

Во время ГВ следует также избегать применения практически не изученных в этот период препаратов, таких как зипразидон, амисульприд и арипипразол.
Таким образом, данные о безопасности антипсихотиков, особенно второго поколения, во время лактации ограниченны. Согласно результатам систематического обзора, проанализировавшего все публикации по этому вопросу в базах данных MEDLINE/ PubMed/TOXNET с 1950 по январь 2008 г., оценить соотношение польза/ риск большинства атипичных антипсихотиков на основании имеющихся данных не представляется возможным [38]. Исключение составляет клозапин, риск от применения которого во время кормления грудью может превышать пользу. Авторы систематического обзора пришли к заключению, что оланзпин также имеет неблагоприятное соотношение польза/риск в период лактации [38], однако другие эксперты считают его совместимым с грудным вскармливанием [4].
Безопасность анксиолитиков и снотворных средств
Бензодиазепины и их активные метаболиты выделяются с молоком матери в небольшом количестве (табл. 8). Экскреция с молоком, по-видимому, носит дозозависимый характер [39]. Соотношение концентраций бензодиазепинов молоко/плазма крови матери – самое низкое из всех классов психотропных препаратов [28]. Безопасность разных препаратов бензодиазепинов в период грудного вскармливания в соответствии с американской классификацией представлена в табл. 9. В связи с низкими концентрациями бензодиазепинов в грудном молоке в организм ребенка, находящегося на ГВ, поступают незначительные количества препаратов и вероятность развития нежелательных эффектов у новорожденного низкая. В случае если мать начала прием бензодиазепинов только после родов, их концентрации в плазме ребенка находятся на не определяемом лабораторными методами уровне [40]. Проблемы могут возникать у недоношенных детей с незрелыми ферментами, принимающими участие в метаболизме бензодиазепинов или при применении высоких доз во время беременности или родов [41].
Длительное использование бензодиазепинов в период ГВ не рекомендуется. В этот период следует избегать новых назначений препаратов этой группы, за исключением тех случаев, когда возникают опасения о наличии зависимости у плода, подвергшегося внутриутробному воздействию бензодиазепинов. При необходимости назначения бензодиазепинов в период лактации предпочтение рекомендуется отдавать препаратам с коротким периодом полувыведения, например лоразепаму. Лоразепам создает низкие концентрации в молоке и не оказывает негативного влияния на потребление молока ребенком [42]. Возможно применение мидазолама и оксазепама [54]. Напротив, применение препаратов длительного действия (диазепам, хлордиазепоксид и других) не рекомендуется. При применении диазепама у двух из 14 детей, матери которых принимали препарат в период кормления грудью, наблюдалась седация и связанное с ней нарушение питания [4]. Профиль безопасности хлордиазепоксида в период грудного вскармливания не определен, однако по своим фармакокинетическим свойствам он близок диазепаму, что позволяет предположить возможность развития аналогичных побочных эффектов. Другие нежелательные эффекты, наблюдавшиеся в единичных случаях, при применении бензодизепинов в период лактации указаны в табл. 10. В случае развития побочных эффектов у ребенка необходимо прекратить ГВ или отменить бензодиазепин. Отменять бензодиазепины с целью профилактики синдрома отмены следует постепенно.
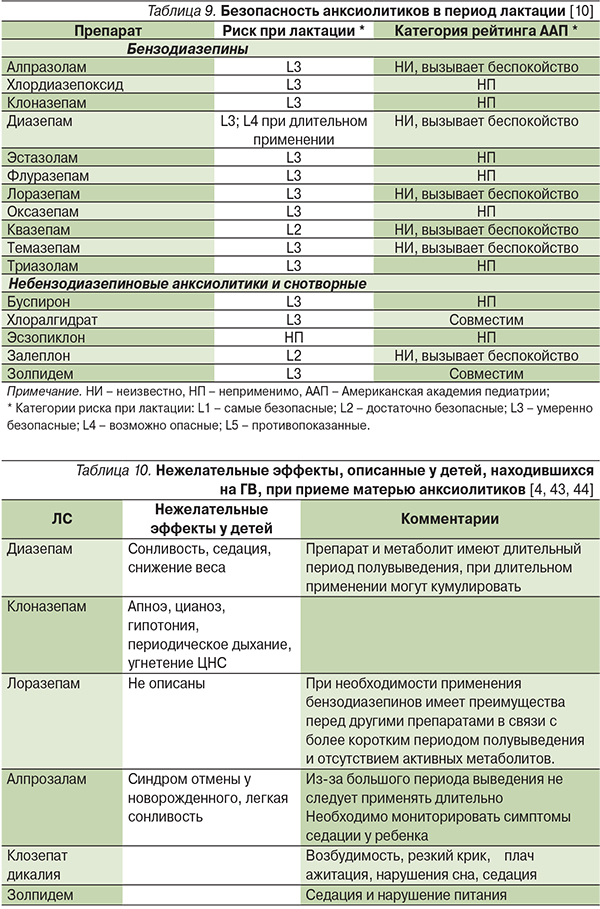
Данные об эффектах небензодиазепиновых анксиолитиков/снотворных средств в период ГВ крайне ограничены. Золпидем выделяется с грудным молоком в небольших количествах. Согласно результатам исследования с участием 5 женщин, концентрации препарата в молоке через 3 часа после введения однократной дозы 20 мг составляли 0,76 – 3,88 мкг, что соответствовало 0,004 – 0,019 % материнской дозы [45]. Через 13–16 часов после введения препарата концентрации в молоке не определялись. Описан один случай седации и нарушение питания у ребенка, получавшего золпидем с молоком матери [4]. Американская академия педиатрии считает его совместимым с ГВ [33]. Рекомендации по применению зопиклона противоречивы. Fortinguerra и соавт., проведшие анализ доказательных данных по использованию ПТП в период лактации, считают возможным его применение короткими курсами при нарушениях сна у кормящих грудью женщин [4], в то же время другие авторы рассматривают зопиклон как препарат, противопоказанный этой категории пациентов, и указывают на возможность его кумуляции в организме новорожденного даже после приема матерью однократной дозы [40]. Аналогичные противоречия в рекомендациях наблюдаются и в отношении залеплона. По данным исследования Darwish и соавт., он быстро исчезает из молока матери [46].
Безопасность нормотимиков
Сведения о выделении нормотимиков с грудным молоком и безопасности применения в период ГВ суммированы в табл. 11.
Концентрации лития в грудном молоке составляют от 30 до 70 % от концентраций в плазме матери, поэтому официально (согласно инструкции по применению) использование препаратов лития в период лактации противопоказано. Однако Американская академия педиатрии считает возможным кормление грудью в период лечения литием при условии мониторинга его концентраций в крови у ребенка, общего анализа крови и клинических симптомов (гипотония, летаргия и цианоз) [33]. Эксперты Великобритании не рекомендуют применение лития в период ГВ [48]. Польза от применения антиконвульсантов в период лактации, по мнению большинства экспертов, перевешивает потенциальные риски. Вальпроевая кислота создает относительно низкие концентрации в грудном молоке (табл. 11), однако в том случае, если мать принимала препарат во время беременности, в первые часы–дни после родов его концентрации у детей, находящихся на ГВ, могут колебаться от 4 до 40 % от уровня в сыворотке крови матери. В послеродовом периоде они быстро снижаются. У детей, матери которых не принимали вальпроат во время беременности, его концентрации в среднем составляли около 6 % от материнского уровня [49]. Побочных эффектов вальпроата у детей при применении во время лактации обычно не наблюдается, хотя описан 1 случай тромбоцитопении и анемии у ребенка [51, 52]. В связи с этим в период ГВ рекомендуется контролировать клиническое состояние детей, уровень ферментов печени и число тромбоцитов [3]. Американские академии неврологии и педиатрии рекомендует женщинам, получающим вальпроат, продолжить кормление грудью.
Концентрации карбамазепина в грудном молоке, как правило, низкие, однако у детей, чьи матери принимали карбамазепин во время беременности, его концентрации в сыворотке крови могут достигать 65 % от уровня в крови матери [52]. При приеме карбамазепина кормящими женщинами с эпилепсией описано два случая нарушения функции печени у новорожденных [53, 54] и один случай транзиторной судорожноподобной активности у детей [55]. Это предполагает необходимость мониторинга концентраций препарата в крови детей, а также уровня печеночных ферментов, билирубина и числа лейкоцитов [3]. Американская академия педиатрии и ВОЗ поддерживают применение карбамазепина во время кормления грудью и рассматривают его как «вероятно безопасный» препарат [33].
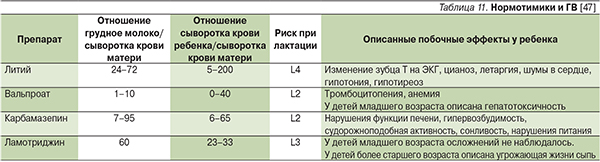
В связи с недостаточным опытом во всех международных руководствах рекомендуется избегать применения в период лактации антиконвульсантов второго поколения, включая ламотриджин, топирамат и габапентин. Ламотриджин достаточно интенсивно выделяется с грудным молоком [56]. Его концентрации в сыворотке крови детей вариабельны, но в целом превышают таковые для других антиконвульсантов. Серьезных побочных реакций ламотриджина у детей, находящихся на грудном вскармливании, не описано. В целенаправленном исследовании с участием 30 женщин, получавших этот нормотимик в период кормления грудью, показана его относительная безопасность и сопоставимость по переносимости с другими антиконвульсантами [57]. Единственным побочным эффектом, зарегистрированным в этом исследовании у детей, был легкий тромбоцитоз. Однако применение ламотриджина в период ГВ потенциально опасно в отношении риска развития сыпи у ребенка [57]. Топирамат, габапентин и леветирацетам, согласно результатам небольших исследований, определяются в молоке примерно в таких же концентрациях, как и в крови матери, однако концентрации в плазме детей, как правило, низкие, что предполагает их быструю элиминацию [57–59].
Таким образом, применение многих психотропных препаратов совместимо с ГВ. Женщины должны быть информированы о потенциальном риске и пользе их приема в период кормления грудью, а также обучены распознаванию ранних признаков токсического воздействия на детей. В случае развития у ребенка каких-либо неблагоприятных симптомов, которые могут быть связаны с приемом ЛС матерью, ГВ следует немедленно прекратить.



