Введение
Проблема острого бактериального риносинусита (ОБР) остается актуальной в оториноларингологии, несмотря на имеющиеся фармакологические возможности. Одну из причин широкой распространенности и роста заболеваемости связывают с нерациональными подходами к лечению [1–4].
На современном этапе развития медицины все назначаемое лечение согласуется с алгоритмами, прописанными в рекомендательных документах. К сожалению, в большинстве российской рекомендательной документации разработанные алгоритмы лечения носят субъективный характер и не основываются на мета-анализах, принятых в зарубежной практике [2]. Часто в этих документах экстраполируются данные зарубежного опыта, что позволяет в лечении больных применять схемы, по сути являющиеся общепринятыми. Основываясь на результатах отечественной и мировой статистики, не подлежит сомнению тот факт, что симптомы бактериального риносинусита (БРС), как субъективные, так и объективные, хорошо устраняются антибиотикотерапией. Основные критерии, лежащие в основе подбора антибиотикотерапии для лечения пациентов с БРС: определение активности воспаления, степени тяжести болезни, этиологически значимые бактериальные возбудители инфекции и их резистентность к антибиотикам, побочные эффекты препаратов, возраст пациента и его аллергологический анамнез [1–4].
В амбулаторных условиях врач подбирает стартовую терапию БРС эмпирическим путем на основании своих предположений либо ранее проведенных исследований о возможной этиологии ОБР и чувствительности предполагаемого возбудителя к назначаемому средству. В отсутствие положительной динамики в течение 3 дней следует принять решение о смене антибиотика [2]. Несмотря на столь очевидную эффективность антибиотиков, не стоит забывать об их побочных эффектах, а также о необходимости грамотной селекции пациентов с исключением таковых с вирусной природой или легким течением РС.
В попытках ускорить выздоровление пациента помимо антибиотиков с большой заслуженной популярностью пользуется местная кортикостероидная терапия, эффективность которой характеризуется высоким уровнем доказательности на протяжении десятилетий [1–4]. Многие дополнительно назначаемые лекарственные средства: препараты муколитического, вазоконстрикторного действий, ирригационные препараты, фито- и физиотерапия обладают более низким уровнем доказательности, но несомненно имеют свои «мишени» в патогенезе ОБР и заслуженно активно используются в практике. Однако часто отмечается одновременное назначение большого числа препаратов, многие из которых характеризуются однотипными эффектами. Подобный нерациональный подход к выбору терапии носит название полипрагмазии. Например, часто необоснованно назначаются антигистаминные средства с целью уменьшения отека, хотя с точки зрения патогенеза с этой задачей призваны справиться либо короткий курс топических деконгестантов, либо более длительное применение топических глюкокортикостероидов, оказывающих менее резкое, но более пролонгированное действие [5].
С целью улучшения оттока слизи используются разноплановые препараты, регулирующие секрецию в виде как спреев для местного применения, так и пероральных форм. И если в EPOS 2012 г. схемы с включением этих препаратов обозначались как «не обладающие достаточной доказательной базой», то в EPOS 2020 г. указывается, что, несмотря на ограниченность совокупных данных (мета-анализов), они активно используются в практике, что косвенно подтверждает их эффективность, следовательно, и востребованность [13, 14].
В течение последних десятилетий прочное место в арсенале лекарственных средств при лечении пациентов с острым риносинуситом (РС) занимает препарат Синуфорте, эффективность которого в качестве монопрепарата и в составе комплексной терапии доказана во многих исследованиях, проведенных более чем в 20 странах Европы [5]. В состав препарата входит лиофилизированный экстракт Цикламена европейского, содержащего тритерпеновые гликозиды (ТГЦЕ). Учитывая происхождение препарата, можно обозначить такого рода лечение как фитотерапию, которая в настоящее время переживает свой ренессанс, поскольку все большее применение лекарственных средств, полученных при помощи самых современных технологий, оказалось неспособно в полной мере справиться с проблемами современной медицины.
В фитотерапии известно воздействие капсаицина и каннабиноидов как агонистов ванилоидного белка-терморецептора 1-го типа (TRPV1 – transient receptor potential vanilloid) слизистой оболочки носа, которые оказывают повреждающее воздействие на эпителий, в результате чего появляется ощущение «полноты носового дыхания», сходное с воздействием нашатырного спирта и переохлаждением. Перспективы местного применения тритерпеновых гликозидов связаны с открытием в биохимии лигандов – химических соединений, образующих комплекс с той или иной биомолекулой (чаще всего белком, например клеточным рецептором). Вследствие такого связывания происходят те или иные биохимические, физиологические или фармакологические эффекты [6].
При попадании на слизистую оболочку полости носа они раздражают холинергические тригеминальные рецепторы, усиливая секреторную активность. Стимулированная гиперсекреция сопровождается изменением реологических свойств секрета и нормализацией его вязкости. Рефлекторная гиперсекреция в комбинации с противоотечным действием препарата приводит к эвакуации секрета из синусов в носоглотку и обеспечивает физиологический дренаж всех синусов одновременно [5–12].
Стоит отметить, что доклинические гистологические исследования показали, что усиление секреторной активности в ответ на интраназальное введение препарата не сопровождается какими-либо видимыми признаками повреждения эпителия слизистой оболочки, наблюдается сохранение ее структуры, соответствующее секреторному циклу, а также отсутствует резорбтивный эффект. Причем в экспериментах использовали сценарий, который был хуже по сравнению с реально возможным: статические модели слизистой оболочки животных были лишены защитного слизистого слоя и в течение значительного времени находились в контакте с препаратом. In vivo в полости носа посредством мукоцилиарного клиренса как в норме, так и в условиях патологического процесса происходит непрерывное движение слизи и постоянная элиминация инородных частиц, в т.ч. молекул лекарственного препарата. Поэтому контакт лекарственного вещества по сравнению с экспериментом был значительно ниже.
Исследования, проведенные в больших группах, показывают высокую клиническую эффективность и экономичность топической фитотерапии ТГЦЕ (в Испании экономия средств составляет 795 евро на одном эпизоде РС и от 700 до 1,400 млн евро на всех больных РС ежегодно) [5]. Однако залог успеха той или иной схемы лечения заключается в рутинном мониторировании ее действия, поэтому они продолжают привлекать внимание клиницистов с точки зрения подтверждения их эффективности и безопасности.
Цель исследования: с учетом вышеизложенного на кафедре оториноларингологии МГМСУ им. А.И. Евдокимова проведено исследование, целью которого стала оценка эффективности и переносимости препарата экстракта Цикламена европейского в составе комплексной терапии пациентов с ОБР средней степени тяжести.
Методы
Под наблюдением находились 114 пациентов (59 женщин, 55 мужчин) в возрасте от 20 до 63 лет (средний возраст – 41,5±6,2 года) с диагнозом ОБР средней степени тяжести, подтвержденным клинико-анамнестическими данными и результатами лабораторно-инструментальных методов исследования. В зависимости от выбранной тактики лечения пациенты были распределены в две группы. В основной (ОГ) схема лечения предусматривала применение антибиотика (амоксициллин/клавуланат 875/125 мг 2 раза в сутки в течение 7 дней перорально в сочетании с экстрактом Цикламена европейского (Синуфорте) по 1 дозе – 1,3 мг/сут в виде интраназального распыления в течение 7 дней), ирригационной терапией 0,9%-ным хлоридом натрия (спрей на основе морской воды) и топическим деконгестантом (ксилометазолин 1% по 1 дозе 2 раза в сутки в течение 3 дней). В группе сравнения (ГС) пациенты использовали аналогичную схему лечения без применения экстракта Цикламена европейского.
Клинико-анамнестическая характеристика пациентов представлена в табл. 1.
Методы исследования пациентов включали оценку лечащим врачом данных клинико-лабораторных показателей, субъективных и объективных критериев заболевания посредством сбора жалоб, анамнеза, проведения эндоскопии полости носа, исследования мукоцилиарного транспорта (сахариновый тест) и интерпретации рентгенографии пациента.
Оценка эффективности проводимой терапии осуществлялась на 3-и и 7-е сутки до, во время и после лечения при помощи 10-балльной шкалы в зависимости от степени уменьшения объективных и субъективных симптомов заболевания. При этом использовалась визуальная аналоговая шкала (ВАШ), представлявшая собой 10-сантиметровую шкалу, на одном из концов которой было обозначено «отсутствие симптома», на другом – «максимальная выраженность симптома» [14]. Восемь промежуточных делений характеризуют плавный переход от одного состояния в другое. Четыре субъективных симптома (заложенность носа, насморк, головная боль, ощущение стекания по задней стенке глотки) оценивал пациент, 3 объективных симптома (отечность, гиперемия слизистой оболочки, наличие отделяемого на задней стенке глотки) оценивал врач. При этом выраженность каждого симптома не должна была превышать 6 баллов, что соответствовало среднетяжелому течению ОРС, согласно критериям EPOS [1]. Итоговая клиническая эффективность лечения была оценена через 7 суток.
При этом выделяли следующие параметры оценки:
1. Отсутствие эффекта: сохранение субъективных и объективных признаков ОБР после лечения.
2. Улучшение: существенное уменьшение субъективных и/или объективных признаков ОБР после лечения.
3. Выздоровление: полное исчезновение субъективных и объективных симптомов ОБР после лечения.
Два объективных метода исследования оценивались отдельно: динамика мукоциллиарного транспорта – до начала и по окончании лечения, рентгенография или компьютерная томография околоносовых пазух – до начала лечения и через 30 дней после него.
Если во время эксперимента выявлялись признаки прогрессирования заболевания или непредвиденное развитие осложнений, пациент исключался из исследования. Это связано с тем, что ему могла потребоваться антибактериальная терапия. Аналогично из исследования удалялись пациенты с непредвиденным развитием аллергической реакции на препарат или его компоненты, за несоблюдение установленного режима приема терапии или если пациент отказывался от участия в эксперименте по собственному желанию.
Результаты и их обсуждение
Согласно полученным результатам, на 3-и сутки лечения выраженность субъективных и объективных симптомов ОБР, представленных в баллах, значительно уменьшилась в обеих группах и статистически достоверные различия между средними показателями отсутствовали (p>0,05). Иная ситуация отмечена после окончания лечения – на 7-е сутки, когда, несмотря на положительную динамику (уменьшение выраженности клинических симптомов ОБР в ГС), в ОГ она была достоверно лучшей (p<0,05) (табл. 2, 3).

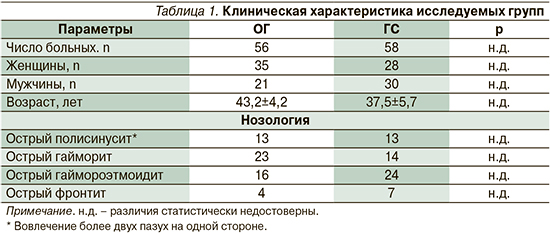
Полученные результаты отразились на итоговой клинической эффективности лечения в обеих группах. При этом в ОГ при сопоставлении с ГС зарегистрировано достоверно большее число случаев выздоровления. Случаи отсутствия эффекта в ОГ в отличие от ГС отсутствовали (рис. 1).
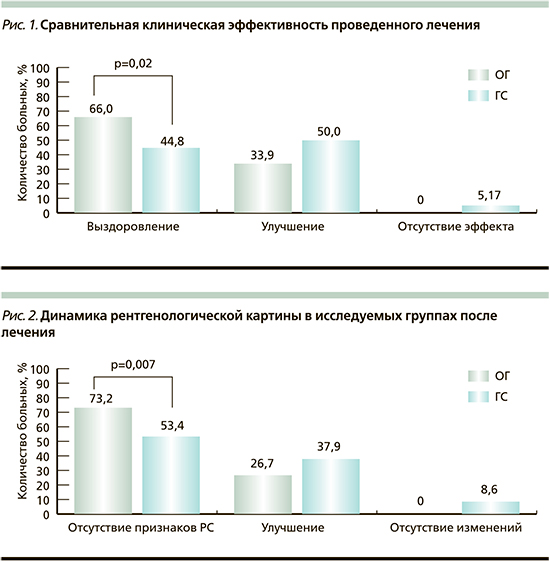
Согласно рекомендательным документам [15], рентгенологическое исследование, «золотым» стандартом которого в отношении околоносовых пазух в настоящее время является компьютерная томография, не обязательно для постановки диагноза, однако для оценки динамики РС с научной точки зрения оно применялось в настоящем исследовании в отношении каждого пациента.
В результате сравнения до- и послеоперационных параметров отмечено, что в ОГ число пациентов с отсутствием признаков РС было достоверно выше по сравнению с группой контроля (p<0,05) (см. рис. 1). Улучшение рентгенологической картины отмечалось в обеих группах и было примерно на одном уровне (рис. 2). Отсутствие изменений отмечено только у 8,6% пациентов ГС и выражалось наличием остаточного выпота в околоносовых пазухах, что потребовало проведения лечебно-диагностической пункции верхнечелюстных пазух и смены группы антибактериальных препаратов на фторхинолоны (левофлоксацин).
Эффективность схемы терапии с экстрактом Цикламена европейского подтверждена и при анализе динамики мукоцилиарного клиренса (рис. 3).
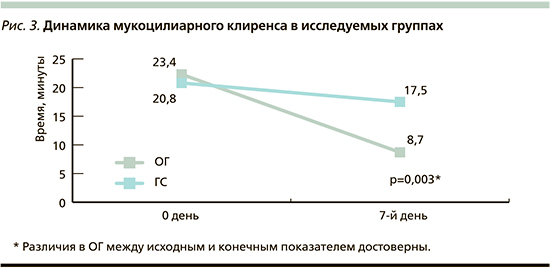
В результате исследования отмечено уменьшение времени мукоциллиарного клиренса в обеих группах, при этом различия показателя к концу терапии были существенными и статистически достоверными в пользу ОГ (p<0,05). Что касается безопасности препаратов, включенных в назначаемые схемы лечения, то на протяжении исследования побочных эффектов от какого-либо из них в обеих группах не выявлено.
Заключение
Проведенное исследование продемонстрировало эффективность комплексной терапии в лечении пациентов с ОБС среднетяжелого течения. Несомненным остается факт необходимости антибиотикотерации в отношении данной нозологии. Что касается мукоактивных средств, в качестве которых в исследовании выступал экстракт Цикламена европейского (Синуфорте), то его включение позволило достоверно улучшить итоговую эффективность лечения, избежать необходимости лечебно-диагностических пункций верхнечелюстных пазух с целью эвакуации остаточного секрета, который присутствовал у ряда больных даже спустя месяц после терапии. Обоснованность применения препарата подтверждена значимым улучшением мукоцилиарного клиренса в ОГ по сравнению с ГС через 7 суток после 3-дневной терапии экстрактом Цикламена европейского. Данная схема лечения характеризуется отсутствием побочных эффектов и позволяет в более короткие сроки достигнуть выздоровления.
Вклад авторов. А.Ю. Овчинников, М.А. Эдже – концепция и дизайн исследования. М.А. Эдже – сбор и обработка материала. М.А. Эдже, Д.О. Семилетова – написание текста. А.Ю. Овчинников, М.А. Эдже – редактирование.



