Артериальная гипертензия (АГ) и дислипидемия (ДЛП) – два фактора кардиоваскулярного риска, которые часто сочетаются и вместе ответственны за повышение риска развития сердечно-сосудистых заболеваний (ССЗ), превосходящее по своим масштабам простую сумму эффектов. По данным исследования NHANES III, у 64 % пациентов с АГ отмечают ДЛП. У 47 % пациентов с ДЛП наблюдается АГ. Сочетание АГ и гиперхолестеринемии на 60 % определяет риск преждевременной смертности от ССЗ [12].
Несмотря на наличие большого арсенала современных антигипертензивных и гиполипидемических препаратов, реальная эффективность лечения этих состояний далека от оптимальной. По данным европейского исследования 16 тыс. больных АГ, только 37 % лечатся эффективно [5]. В России при высокой распространенности АГ, которая встречается среди 40 % лиц старше 18 лет, только 23,2 % мужчин и 18,8 % женщин при лечении АГ достигают целевых уровнией артериального давления – АД [2–4]
По данным исследования DYSIS-RUSSIA, являющегося частью крупного международного исследования, даже у пациентов очень высокого риска достижение целевого уровня холестерина липопротеидов низкой плотности (ЛПНП) в первичном звене здравоохранения в российских городах составляет не более 12 % [1].
К одним из основных причин неадекватного контроля АГ и ДЛП относится низкая приверженность пациентов к проводимой терапии. Особенно это актуально для пациентов с АГ и ДЛП без клинических проявлений атеросклероза, поскольку зачастую ни повышенное АД, ни тем более нарушение липидного обмена ничем себя не проявляют. Поэтому такие пациенты не мотивированы на медикаментозное лечение. Особенно это относится к липидснижающей терапии. В качестве первичной профилактики липидснижающую терапию в реальной клинической практике назначают крайне редко.
В связи с этим на современном этапе активно изучаются пути повышения приверженности к анигипертензивной и липидснижающей терапии.
В настоящее время доказано, что высокая приверженность к лечению коррелирует с повышением выживаемости пациентов в популяции [20].
Важным событием в этой области можно считать создание фиксированной комбинации амлодипина и аторвастатина, позволяющей эффективно воздействовать на оба ключевых фактора кардиоваскулярного риска – АГ и ДЛП. Амлодипин, относящийся к дигидропиридиновым антагонистам кальция III поколения, показан к лечению АГ, вазоспастической и хронической стабильной стенокардии. Аторвастатин, синтетический ингибитор ГМГ-КоА-редуктазы (3-гидрокси-3-метилглутарил коэнзим А-редуктазы), является представителем статинов II поколения. Оба препарата располагают обширной доказательной базой эффективности и безопасности.

Высокие эффективность и безопасность амлодипина как основного антигипертензивного лекарственного средства доказаны во многих крупных исследованиях. Ключевым из них было исследование ALLHAT (Antihypertensive and Lipid Lowering to prevent Heart Attack Trial), в котором более 40 тыс. пациентов рандомизировали для приема хлорталидона, амлодипина, лизиноприла или плацебо. В снижении частоты основной комбинированной конечной точки (фатальная ишемическая болезнь сердца) и нефатального инфаркта миокарда амлодипин по эффективности не уступал хлорталидону, а в отношении снижения риска инсульта был значительно эффективнее лизиноприла [9].
В исследовании VALUE (Valsartan Antihypertensive Long-term Use Evaluation) сравнивали действие валсартана и амлодипина на пациентов с АГ и высоким кардиоваскулярным риском. Первичная конечная точка (кардиоваскулярная заболеваемость и смертность) одинаково снижалась в обеих группах, однако лечение амлодипином ассоциировалось с достоверным уменьшением риска инфаркта миокарда на 16 % и тенденцией к снижению частоты инсульта по сравнению с валсартаном [12].
В исследовании ASCOT BPLA (Anglo-ScandinavianCardiac Outcomes Trial-Blood Pressure-Lowering Arm), в которое были включены пациенты с АГ и сопутствующими факторами риска без клинических проявлений атеросклероза, сравнивали эффективность комбинации амлодипина и периндоприла с атенололом в комбинации с гидрохлоротиазидом. Данное исследование завершилось досрочно в связи с очевидным преимуществом терапии амлодипином и периндоприлом в плане снижения уровня кардиоваскулярной и общей смертности [8, 19].
В исследовании PREVENT лечение амлодипином сопровождалось значительным замедлением прогрессирования атеросклероза сонных артерий и снижением риска инсульта [18].
В исследовании CAMELOT у пациентов с ишемической болезнью сердца (ИБС) амлодипин, по данным внутрисосудистого ультразвукового исследования (УЗИ), останавливал прогрессирование атеросклероза, в то время как у больных группы эналаприла наблюдалась тенденция к его прогрессированию [16].
Не менее широкая доказательная база эффективности имеется у аторвастатина. В упомянутом исследовании ASCOT, касающемся раздела эффективности аторвастатина (LLA), было установлено дополнительное снижение риска нефатального инфаркта миокарда и смерти от ИБС у пациентов, получавших гиполипидемическую терапию аторвастатином и одновременно антигипертензивное лечение амлодипином (на 36 %). При этом исследование было прекращено досрочно в связи со значительным преимуществом добавления аторвастатина к антигипертензивной терапии. В исследовании REVERSAL установлен антиатеросклеротический эффект аторвастатина. В данном исследовании, по данным внутрисососудистого УЗИ, аторвастатин останавливал прогрессирование атеросклероза, чего не наблюдалось при применении правастатина [13]. Среди пациентов с сахарным диабетом 2 типа аторвастатин в дозе 10 мг/сут снижал смертность на 27 % по сравнению с плацебо, эти данные получены в исследовании CARDS [7].
 У пациентов с АГ и гиперхолестеринемией лечение фиксированной комбинацией амлодипина и аторвастатина позволяет снижать уровень холестерина ЛПНП на 41–61%. Фармакокинетические и фармакодинамические свойства амлодипина и аторвастатина практически идеально подходят к созданию их фиксированной комбинации: оба можно принимать 1 раз в сутки независимо от приема пищи, при этом один препарат не оказывает неблагоприятного влияния на эффективность и переносимость другого. Во многих исследованиях, в т.ч. в двух больших когортных ретроспективных исследованиях CAPRE-PBM и CAPRE-M, убедительно доказано преимущество длительного приема фиксированных лекарственных комбинаций по сравнению с длительным приемом тех же препаратов в самостоятельных лекарственных формах как порознь, так и в сочетании. Пациенты, принимавшие фиксированные комбинации амлодипина и статинов, существенно реже самостоятельно прекращали лечение, чем те, кто принимал те же лекарства в отдельных лекарственных формах [17, 21]. Кроме того, одним из главных преимуществ сочетанного использования амлодипина и аторвастатина является их синергичный эффект, направленный на улучшение функции эндотелия сосудов, что повышает органопротекцию и способствует торможению процесса атеросклероза [15]. Сочетанное применение амлодипина и аторвастатина увеличивает эластичность стенок артерий среднего калибра [6, 14], улучшает функцию эндотелия [6], уменьшает выраженность гипертрофии левого желудочка, оказывает антиагрегантный эффект [10], а также снижает активность маркеров воспаления в плазме крови [11] и атеросклеротических бляшках в большей степени, чем при применении каждого из этих препаратов.
У пациентов с АГ и гиперхолестеринемией лечение фиксированной комбинацией амлодипина и аторвастатина позволяет снижать уровень холестерина ЛПНП на 41–61%. Фармакокинетические и фармакодинамические свойства амлодипина и аторвастатина практически идеально подходят к созданию их фиксированной комбинации: оба можно принимать 1 раз в сутки независимо от приема пищи, при этом один препарат не оказывает неблагоприятного влияния на эффективность и переносимость другого. Во многих исследованиях, в т.ч. в двух больших когортных ретроспективных исследованиях CAPRE-PBM и CAPRE-M, убедительно доказано преимущество длительного приема фиксированных лекарственных комбинаций по сравнению с длительным приемом тех же препаратов в самостоятельных лекарственных формах как порознь, так и в сочетании. Пациенты, принимавшие фиксированные комбинации амлодипина и статинов, существенно реже самостоятельно прекращали лечение, чем те, кто принимал те же лекарства в отдельных лекарственных формах [17, 21]. Кроме того, одним из главных преимуществ сочетанного использования амлодипина и аторвастатина является их синергичный эффект, направленный на улучшение функции эндотелия сосудов, что повышает органопротекцию и способствует торможению процесса атеросклероза [15]. Сочетанное применение амлодипина и аторвастатина увеличивает эластичность стенок артерий среднего калибра [6, 14], улучшает функцию эндотелия [6], уменьшает выраженность гипертрофии левого желудочка, оказывает антиагрегантный эффект [10], а также снижает активность маркеров воспаления в плазме крови [11] и атеросклеротических бляшках в большей степени, чем при применении каждого из этих препаратов.
Таким образом, создание фиксированной комбинации, состоящей из амлодипина и аторвастатина, стало логическим и неизбежным для эффективного одновременного контроля АГ и ДЛП.
В связи с вышеизложенным целью нашего собственного исследования явилась оценка эффективности терапии фиксированной комбинацией амлодипина и аторвастатина (Дуплекор, Гедеон Рихтер) по сравнению с лечением отдельными его компонентами пациентов с АГ и ДЛП. Особое внимание уделялось вопросам приверженности лечению.
Материал и методы
В исследование были включены 70 пациентов с АГ и ДЛП, обратившихся к врачу в первичном звене здравоохранения в поликлинику ФГБУ «Клиническая больница № 1».
В исследование включили мужчин и женщин в возрасте от 40 до 65 лет с АГ 1-й и 2-й степеней (АД систолическое – 140–159 и АД диастолическое – 90–104 мм рт.ст.) и ДЛП (общий холестерин >5,0 ммоль/л и/ или ЛПНП >3,0 ммоль/л) без ИБС и других клинических проявлений атеросклероза. Согласно стратификации риска, пациенты с АГ относились к среднему риску. Обязательным условием для включения в исследование стало отсутствие достижения целевого АД (менее 140/90 мм рт.ст.) и коррекции нарушений липидного обмена диетой. Средний возраст всех пациентов в исследовании составил 54,7 года. Среди них были 48 мужчин и 22 женщины. Продолжительность АГ составила в среднем от года до 5 лет. Пациенты, включенные в исследование, ранее не получали антигипертензивного лечения или лечились эпизодически.
Среди включенных в исследование пациентов 46 курили, что составило 65,71 %, 55,6 % имели стаж курения более пяти лет. Пациенты (n = 70) после подписания информированного согласия были распределены методом случайной выборки в две группы – основную и контрольную. Пациенты основной группы (n = 35) получали лечение комбинированным препаратом Дуплекор (амлодипин/ аторвастатин), больные контрольной группы (n=35) получали амлодипин и аторвастатин по отдельности. Исследование продолжалось в течение 6 месяцев. Подбор дозы препаратов проводился методом титрования. Начальные дозы амлодипина составили 5 мг/сут, максимальные –10 мг/сут, стартовая доза аторвастатина составила 10 мг/сут, максимальная – 20 мг в сут. Контрольные визиты назначали через 4 недели, 3 месяца и 6 месяцев от начала лечения. На промежуточных визитах оценивали эффективность (достижение/недостижение целевых значений АД и липидных показателей) и переносимость проводимой терапии. Приверженность к проводимой терапии оценивали через 3 и 6 месяцев от начала исследования. Группы исходно не различались по основным характеристикам (см. таблицу).
В ходе исследования в группах оценивалась приверженность к терапии, динамика АД, липидных показателей через 6 месяцев терапии. Приверженность пациентов к лечению оценивалась с использованием опросника Мориски–Грина.
Шкала приверженности Мориски–Грин – клинико-психологическая тестовая методика, предназначенная для оценки приверженности и скринигового выявления недостаточно приверженных больных в рутинной врачебной практике. Шкала была создана D.E. Morisky, L.W. Green, D.M. Levine в 1985 г. и опубликована в 1986 г. Внутренняя структура Шкалы Мориски–Грина состоит из четырех пунктов, касающихся отношения пациента к приему препаратов. Шкала предназначена для заполнения самим пациентом. Как альтернатива – врач может зачитывать вопросы и помечать ответы на них. В оригинальной шкале каждый пункт оценивается по принципу «да-нет», при этом ответ «да» оценивается в 0 баллов, а ответ «нет» – в 1 балл. Шкала Мориски–Грина используется для включения в программу стандартного медицинского обследования людей с хроническими заболеваниями. Она может быть применена для выделения контингента, нуждающегося в дополнительном внимании как недостаточно приверженного к лечению. Наконец, она часто используется в научных исследованиях как основной инструмент и как эталон сравнения при разработке новых, более подробных и специализированных шкал.
Текст Шкалы (опросника) Мориски–Грина:
- Вы когда-нибудь забывали принять препараты?
- Не относитесь ли Вы иногда невнимательно к часам приема ЛС?
- Не пропускаете ли Вы прием препаратов, если чувствуете себя хорошо?
- Если Вы чувствуете себя плохо после приема ЛС, не пропускаете ли Вы следующий прием?
Интерпретация шкалы: комплаентными (приверженными) считаются больные, набравшие 3 и выше балла. Больные, набравшие 2 балла и менее, считаются неприверженными. Больные, набравшие менее 3 баллов, считаются недостаточно приверженными и находятся в группе риска по развитию неприверженности.
Результаты исследования
Изучая приверженность пациентов двух исследуемых групп, мы получили следующие данные: суммарный балл, оцененный по опроснику Мориски–Грина, который отражает приверженность пациентов, оказался выше у пациентов основной группы, которые получали лечение комбинированным препаратом Дуплекор. В этой группе средний балл по опроснику Мориски–Грина через 3 месяца лечения составил 3,26, а в контрольной группе – 3,03.
К шестому месяцу от начала лечения эти показатели значительно различались: в основной группе балл по опроснику был равен 3,17, в контрольной группе – 2,14, что отражает более высокую приверженность пациентов основной группы по сравнению с пациентами контрольной группы.
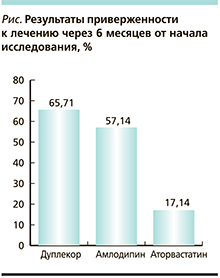
На рисунке представлены результаты приверженности к терапии Дуплекором, амлодипином и аторвастатином. Видно, что к концу исследования пациенты основной группы чаще оставались на лечении Дуплекором, чем на терапии амлодипином и аторвастатином по отдельности. В основной группе из 35 человек через 6 месяцев лечения оставались на терапии Дуплекором 23 (65,71 %) пациента, в контрольной группе на терапии амлодипином – 20 (57,14 %) пациентов, и лишь 6 (17,14 %) пациентов продолжали принимать аторвастатин, что говорит о существенном различии в приверженности к липидснижающей терапии. Однако различия в приверженности к антигипертензивной терапии были недостоверны, тогда как липидснижающей терапии – высокодостоверны (р < 0,00005).
В результате пациенты основной группы добились лучших показателей контроля АД и особенно липидных показателей, чем больные контрольной группы, получавшие аторвастатин и амлодипин по отдельности. В основной группе целевого уровня АД (менее 140/90 мм рт.ст.) достигли 19 (54,28 %) пациентов, в контрольной – 16 (45,7 %). Эти различия были недостоверными. Однако в динамике липидных показателей между группами отмечены выраженные различия. Через 6 месяцев лечения в группе пациентов, получавших Дуплекор, средний уровень общего холестерина снизился с 6,48 до 4,91 ммоль/л, а в контрольной группе – с 6,31 до 5,94 ммоль/л. Различия между достигнутыми средними уровнями общего холестерина в основной и контрольной группах высокодостоверны (р = 0,000001). Аналогично в основной группе отмечено более выраженное снижение уровня ЛПНП. Через 6 месяцев лечения Дуплекором средний уровень ЛПНП снизился от 3,97 до 2,19 ммоль/л, в контрольной группе – от 3,68 до 3,37 ммоль/л. Различия между средними уровнями ЛПНП к концу исследования были высокодостоверными (р < 0,000001).
Результаты данного исследования особенно важны в плане повышения приверженности к лечению статинами. Как уже отмечалось, в целях первичной профилактики статины принимают очень немногие пациенты. В связи с этим пациент, принимая антигипертензивную терапию (приверженность которой по объективным причинам выше, чем статинам) в составе Дуплекора, одновременно повышает приверженность к липидснижающей терапии.
Проводимое лечение в двух исследуемых группах переносилось пациентами удовлетворительно, побочные эффекты лечения встречались в обеих группах не более чем у 1 % (отеки голеней, покраснения лица и т.д.), что не потребовало отмены препарата.
Таким образом, для пациентов с АГ и сопутствующей дислипидемией применение фиксированной комбинации амлодипина/аторвастатина (Дуплекор) является удобным, безопасным и эффективным подходом для одновременного контроля двух важнейших факторов кардиоваскулярного риска. Удобство приема – одна таблетка вместо двух – позволяет значительно упростить лечение АГ и ДЛП, следовательно, улучшить приверженность пациентов к медикаментозной терапии.



